Utilización de la proteína ASC como marcador para cáncer de seno.
Metodo para el diagnostico in vitro de cancer de seno, que comprende las siguientes etapas:
a) preparar una muestra liquida obtenida de un individuo,
b) establecer contacto de dicha muestra con un agente de union especifico para la proteina tipo mancha ("speck-like"), que contiene un dominio de reclutamiento asociado a cas pasa (A SC), bajo condiciones apropiadas para la formacion de un complejo entre dicho agente de union y ASC, y
c) correlacionar la cantidad de complejo formado en (b) con el diagnostico de cancer de seno, de manera que un nivel elevado de ASC en comparacion con controles sanos es indicativo de cancer de seno.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2004/011597.
Solicitante: F. HOFFMANN-LA ROCHE AG.
Nacionalidad solicitante: Suiza.
Dirección: GRENZACHERSTRASSE 124 4070 BASEL SUIZA.
Inventor/es: KARL, JOHANN, BERNDT, PETER, HAGMANN, MARIE-LUISE, LANGEN, HANNO, ZOLG, WERNER, ANDRES, HERBERT, PESTLIN,GABRIELE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N33/574 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para el cáncer.
PDF original: ES-2377407_T3.pdf
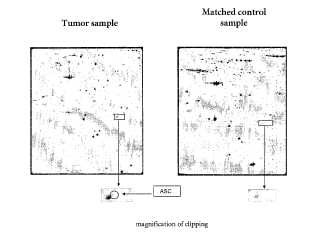
Fragmento de la descripción:
Utilizacion de la proteina ASC como marcador para cancer de seno La presente invencion se refiere al diagnostico de cancer de seno. Da a conocer la utilizacion de una proteina tipo mancha ("speck-like") asociada a apoptosis, que contiene un dominio de reclutamiento asociado a caspasa (= ASC) en el diagnostico de cancer de seno. Ademas, se refiere, en especial, a un metodo para el diagnostico de cancer de seno a partir de una muestra de liquido, derivada de un individuo para la medicion de ASC en dicha muestra. La medicion de ASC puede ser utilizada en la deteccion precoz o diagnostico de cancer de seno. El cancer sigue siendo un importante reto para la salud publica, a pesar de los avances en la deteccion y en la terapia. Entre los diferentes tipos de cancer, el cancer de seno (=BC) es uno de los canceres mas frecuentes entre las mujeres del mundo occidental. Cuando mas pronto se pueda detectar/diagnosticar, mejor es la tasa general de supervivencia. Esto es especialmente cierto para BC. El pronostico en etapas avanzadas del tumor es poco satisfactorio. Mas de un tercio de los pacientes moriran por el avance de la enfermedad dentro de los cinco aros despues del diagnostico, correspondiendo a una tasa de supervivencia de aproximadamente 40% para cinco aros. El tratamiento actual cura solamente una fraccion de l os pacientes y, de manera clara, tiene los mejores efectos en los pacientes diagnosticados en una etapa precoz de la enfermedad. Con respecto a BC como problema de salud publica, es esencial que se desarrollen medidas mas efectivas de deteccion y medidas preventivas, para el cancer de seno. Los procedimientos de dete ccion mas precoces, actualmente disponibles para el cancer de seno comportan la utilizacion de examenes clinicos de los senos y la mamografia. No obstante, debe existir un tamaro significativo del tumor antes de que pueda ser palpable o pueda ser detectado por una mamografia. La densidad de los tejidos del seno y la edad son importantes elementos de prediccion de la exactitud de la mamografia. Las tasas de sensibilidad oscilan entre el 63 % en m ujeres con se nos extremadamente densos hasta 87 % en mujeres con senos casi enteramente grasos. La sensibilidad aumenta con la edad, desde 69% en mujeres de unos 40 aros hasta 83% en mujeres de 80 aros y mas (Carney, P.
A., y otros, Ann. Intern. Med. 138 (3) (2003) 168-175) . Solamente, el 20-25% de las a normalidades detectadas mamograficamente, que son objeto de bi opsia, llegan a ser malignas. La visualizacion de lesiones precancerosas y cancerosas representa el mejor enfoque para la deteccion precoz, pero la mamografia es una prueba costosa que requiere gran cuidado y experiencia, tanto para llevarla a cabo como para la interpretacion de los resultados (WHO, Screening for Breast Cancer, May 10, 2002; Esserman, L., y otros, J. Natl. Cancer Inst. 94 (2002) 369-375) . En estos ultimos aros, se ha informado sobre una gran cantidad de los llamados genes especificos para senos, o incluso llamados especificos para cancer de senos. La inmensa mayoria de los documentos de investigacio n correspondientes o solicitudes de patentes se basan en datos obtenidos por analisis de modelos de expresion de ARN en teji dos de se no (cancer) , en c omparacion con un tejido distinto o a un tejido normal adyacente, respectivamente. Estos enfoques se pueden resumir como tecnicas de visualizacion diferencial de mARN. Como ejemplo de los datos disponibles de las tecnicas de visualizacion de mARN, el documento WO 00/60076 se mencionara y se explicara. Esta solicitud de patente describe y reivindica mas de doscientos polinucleotidos aislados, y los correspondientes polipeptidos asi como, su utilizacion en la deteccion de BC. No obstante, es conocimiento general que las diferencias en el nivel d e mARN no se reflejan po r el nivel de las proteinas correspondientes. Una proteina codificada por un mARN raro puede ser encontrada en cantidades muy grandes, y una proteina codificada por un mARN abundante puede ser, no obstante, dificil de detectar y encontrar en absoluto (Chen, G., y otros, Molecular and Cellular Proteomics, 1.4 (2002) 304-313) . Esta falta de correlacion entre el nivel de mARN y el nivel de la proteina es debido a razones tales como la estabilidad de mARN, la eficacia de la traduccion, la estabilidad de la proteina, etc. El documento WO 01/29235 da a conocer que TMS1 es un nuevo gen regulador apoptotico que es silenciado como resultado de una metilacion anormal. Zhang, H., y otros han analizado la expresion de la proteina de cancer 3 amplificada en un seno (AIB3, conocida tambien como ASC-2, RPA250, PRIP, TRBP y (CNR) en ratones (Zhang, H., y otros, Endocrinology 144 (4) :14351443) . Sus mediciones cuantitativas han rebelado que las concentraciones de AIB3 mARN difieren sustancialmente en diferentes tejidos, en ord en descendente de los siguientes: testiculos, cerebro, timo, grasa blanca, pituitaria, ovario, glandulas adrenales, pulmon, utero, riron, corazon, musculos esqueleticos, higado, y glandulas mamarias virgenes. Han existido tambien enfoques recientes investigando las diferencias de modelos de proteina entre diferentes tejidos o entre tejidos sanos y enfermos, a efectos de identificar moleculas marcadoras candidato que puedan ser utilizadas en el diagnostico de BC. Wulfkuhle y otros. Cancer Research 62 (2002) 6740-6749 han identificado cincuenta y siete proteinas que fueron expresadas de manera diferencial entre tejidos de BC y tejidos normales adyacentes. No se informo de datos sobre muestras de liquidos obtenidas a partir de un individuo.
El documento WO 02/23200 da a c onocer aproximadamente doce puntos asociados con ca ncer de s eno, por desabsorcion laser e ioni zacion con a mpliacion sup erficial (SELDI) . Estos pun tos son apreciados mas frecuentemente en sueros obtenidos a partir de pacientes con BC, en comparacion con los sueros obtenidos a partir de controles sanos. No obstante, la identidad de la molecula o moleculas comprendidas en dicho punto, por ejemplo, su secuencia, no es conocida.
El liquido aspirado de los pezones (NAF) como metodo potencial no invasivo se ha utilizado durante muchos aros, para identificar marcadores especificos para el cancer de seno. Kuerer y otros compararon fluidos aspirados de un par de pezon es, compensa dos bil ateralmente, de muj eres con car cinoma de se no invasiv o u nilateral p or electroforesis de gel 2D (Kuerer, H.M., y otros, Cancer 95 (2002) 2276-2282) . Se detectaron de 30 a 202 puntos de diferentes proteinas en el NAF de senos afectados de carcinoma de seno yno en el NAF equilibrado de senos sanos. Estos puntos fueron detectados por el analisis de una imagen de gel. Sin e mbargo, la identidad de los puntos de proteina no es conocida.
A pesar de la larga y creciente lista de proteinas candidatas a marcadores en el sector del cancer d e seno (BC) , hasta la actualidad, la utilidad clin ica de diagnostico de estas moleculas no es conocida. Para que sea utilidad clinica un nuevo marcador diagnostico, un marcador unico debe ser, como minimo, tan satisfactorio como el mejor marcador individual conocido en la tecnica. Es decir, un nuevo marcad or debe de conducir a un avance en la sensibilidad d el diagnostico y /o a la esp ecificidad utili zado solo o en combinaci on con uno u otros varios marcadores, respectivamente. La sensibilidad al diagnostico y/o especificidad de una prueba es mejor evaluada por sus caracteristicas de receptor-operativas, que se describiran en detalle mas adelante.
En la actualidad, solamente se disponen, pa ra ayudar al diagnostico en el sector BC, pruebas de sang re basadas en la detecci on del antige no del cance r 15-3 (CA 15-3) , una mucina asociada al tumor, y un antigeno carcinoembrionario (CEA) , una glicoproteina asociada al tumor estan disponibles para ayudar al diagnostico de BC. El CA 15-3 tiene valores habitualmente incrementados en pacientes con cancer de seno avanzado. Los niveles de CA 15-3 son dificilmente elevados en mu jeres con etapas precoce s de cancer de seno (Duffy , M.J., Cri tical Reviews in Clinical Laborator y Sciences 38 (2001) 225-262) . Los canceres de ovario, pulmon y prostata pueden aumentar tambien los niveles de CA 15-3. Los niveles elevados de CA 15-3 pueden ser asociados a estados no cancerosas, tales como enfermedades benignas de senos u ovarios, endometriosis, enfermedad inflamatoria de la pelvis y la hepatitis. El embarazo y la lactancia pueden provocar tambien un aumento en los niveles de CA 15-3 (National Cancer Institute, Cancer Facts, Fact Sheet 5.18 (1998) 1-5) . La utilizacion principal de CEA es el control de cancer de colon, especialmente cuando la enfermedad ha producido metastasis. No obstante, una serie de canceres pueden producir niveles elevados de CEA, incluyendo el cancer de seno.
Debido a la falta de esp ecificidad... [Seguir leyendo]
Reivindicaciones:
1. Metodo para el diagnostico in vitro de cancer de seno, que comprende las siguientes etapas:
a) preparar una muestra liquida obtenida de un individuo, b) establecer contacto de dicha muestra con un agente de union especifico para la proteina tipo mancha ("speck-like") , que co ntiene un d ominio de r eclutamiento as ociado a cas pasa (A SC) , ba jo c ondiciones apropiadas para la formacion de un complejo entre dicho agente de union y ASC, y c) correlacionar la cantidad de complejo formado en (b) con el diagnostico de cancer de seno, de manera que un nivel elevado de ASC en comparacion con controles sanos es indicativo de cancer de seno.
2. Metodo, segun la reivindicacion 1, caracterizado, ademas, porque dicha muestra es suero.
3. Metodo, segun la reivindicacion 1, caracterizado, ademas, porque dicha muestra es plasma.
4. Metodo, segun la reivindicacion 1, caracterizado, ademas, porque dicha muestra es sangre entera.
5. Metodo, segun la reivindicacion 1, caracterizado, ademas, porque dicha muestra es liquido aspirado de pezones.
6. Utilizacion in vitro de la proteina ASC en el diagnostico de cancer de seno a partir de una muestra de liquido obtenida de un individuo, en el que un nivel elevado de ASC, en comparacion con controles sanos, es indicativo de cancer de seno.
7. Utilizacion in vitro de la proteina ASC en el diagnostico precoz de cancer de seno a partir de una muestra de liquido obtenida de un individuo, en el que un nivel elevado de ASC, en c omparacion con controles sanos, es indicativo de cancer de seno.
8. Utilizacion in vitro de la proteina ASC en combinacion con una o mas moleculas marcadoras de cancer de seno en el diagnostico de cancer de seno, a partir de una muestra liquida obtenida de un in dividuo, en el que un nivel elevado de ASC, en comparacion con controles sanos, es indicativo de cancer de seno.
9. Utilizacion, segun la reivindicacion 8, en la que, como minimo, otra molecula marcadora es CA 15-3.
10. Utilizacion, segun la reivindicacion 8, en la que, como minimo, otra molecula marcadora es proteina celular II de union a acido retinoico (Swiss-PROT: P29373) .
11. Utilizacion, segun la reivindicacion 8, en la que, como minimo, dos moleculas marcadoras son proteina celular II de union a acido retinoico (Swiss-PROT: P29373) y CA 15-3.
12. Kit inmunologico que comprende, como minimo, un agente de union especifico para ASC, como minimo, u n agente de union especifico para CA 15-3, y reactivos auxiliares para la medicion de ASC y CA 15-3.
13. Kit inmunologico que comprende, como minimo, un agente de union especifico para ASC, como minimo, u n agente de union especifico para la proteina celular II de union a acido retinoico (Swiss-PROT: P29373) y reactivos auxiliares para la medicion de ASC y proteina celular II de union a acido retinoico (Swiss-PROT: P29373) .
14. Kit inmunologico que comprende, como minimo, un agente de union especifico para ASC, como minimo, u n agente de union especifico para la pr oteina celular II de union a acido retinoico (Swiss-PROT: P29373) , como minimo, un agente de union especifico para CA 15-3, y reactivos auxiliares para la medicion de ASC, CA 15-3 y proteina celular II de union a acido retinoico (Swiss-PROT: P29373) .
Patentes similares o relacionadas:
Composiciones para la supresión del cáncer por inhibición de TMCC3, del 29 de Julio de 2020, de Development Center For Biotechnology: Un anticuerpo contra la proteína con dominios de superhélice transmembrana 3 (TMCC3), o un fragmento de unión de la misma, en donde el anticuerpo […]
Métodos para detectar distintivos de enfermedades o afecciones en fluidos corporales, del 15 de Julio de 2020, de PRESIDENT AND FELLOWS OF HARVARD COLLEGE: Un método in vitro para diagnosticar la presencia de un agente infeccioso en un individuo que comprende los pasos de: obtener un primer perfil de expresión […]
Biomarcadores de pronóstico y predictivos y aplicaciones biológicas de los mismos, del 1 de Julio de 2020, de INSTITUT GUSTAVE ROUSSY: Un método para evaluar la sensibilidad o la resistencia de un tumor frente a un agente antitumoral, que comprende evaluar la cantidad de complejo eiF4E-eiF4G (complejo Cap-ON) […]
Métodos para clasificar pacientes con un cáncer sólido, del 24 de Junio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un método in vitro para el pronóstico del tiempo de supervivencia de un paciente que padece un cáncer sólido, cuyo método comprende los siguientes […]
Procedimiento de detección del cáncer, del 24 de Junio de 2020, de Sienna Cancer Diagnostics Ltd: La presente invención proporciona un procedimiento para resolver una evaluación citológica no concluyente de células epiteliales de vejiga en […]
Método para el diagnóstico/pronóstico de cáncer colorrectal, del 17 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención se refiere a un método de obtención de datos útiles para el diagnóstico, el pronóstico o la monitorización de la evolución de cáncer colorrectal (CCR), […]
Criterio de valoración terapéutico equivalente para inmunoterapia de enfermedades basada en antiCTLA-4, del 10 de Junio de 2020, de E. R. Squibb & Sons, L.L.C: Un anticuerpo antiCTLA-4 para su uso en el tratamiento de cáncer en un sujeto, tratamiento que comprende inducir un acontecimiento liminar […]
Método de deducción de un valor de positividad de biomarcador en porcentaje para células seleccionadas presentes en un campo de visión, del 10 de Junio de 2020, de NOVARTIS AG: Método de deducción de un valor para el % de positividad de biomarcador (PBP) para todas las células u, opcionalmente, uno o más subconjuntos de las […]