PROTEINA ALFA DE ACTIVACION DE FIBROBLASTOS DIMERICA AISLADA, Y USOS DE LA MISMA.
LA INVENCION SE REFIERE A FORMAS DIMERAS DE LA PROTEINA CONOCIDA COMO PROTEINA ALFA ACTIVADORA DE FIBROBLASTOS, O FAP AL , Y UTILIZACIONES DE LA MISMA
Tipo: Resumen de patente/invención. Número de Solicitud: W9704215US.
Solicitante: LUDWIG INSTITUTE FOR CANCER RESEARCH
BOEHRINGER INGELHEIM INTERNATIONAL GMBH.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1345 AVENUE OF THE AMERICAS,NEW YORK, NEW YORK 10105.
Inventor/es: OLD, LLOYD, J., ZIMMERMAN, RAINER, PARK,JOHN,E, RETTIG,WOLFGANG.
Fecha de Publicación: .
Fecha Concesión Europea: 18 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- C12P21/06 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
Clasificación PCT:
- A61K38/43 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Enzimas; Proenzimas; Sus derivados.
- C07K14/435 C […] › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de animales; de humanos.
- C07K14/705 C07K 14/00 […] › Receptores; Antígenos celulares de superficie; Determinantes celulares de superficie.
- C12N15/52 C12 […] › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Genes que codifican enzimas o proenzimas.
- C12N9/64 C12N […] › C12N 9/00 Enzimas, p. ej. ligasas (6.); Proenzimas; Composiciones que las contienen (preparaciones para la limpieza de los dientes que contienen enzimas A61K 8/66, A61Q 11/00; preparaciones de uso médico que contienen enzimas A61K 38/43; composiciones detergentes que contienen enzimas C11D ); Procesos para preparar, activar, inhibir, separar o purificar enzimas. › que provienen de tejido animal, p. ej. renina.
- C12P21/06 C12P 21/00 […] › preparados por hidrólisis de un enlace peptídico, p. ej. hidrolizados.
- C12Q1/00 C12 […] › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones.
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
Clasificación antigua:
- A61K38/43 A61K 38/00 […] › Enzimas; Proenzimas; Sus derivados.
- C07K14/435 C07K 14/00 […] › de animales; de humanos.
- C12N15/52 C12N 15/00 […] › Genes que codifican enzimas o proenzimas.
- C12Q1/00 C12Q […] › Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones.
- G01N33/50 G01N 33/00 […] › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
Fragmento de la descripción:
Proteína a de activación de fibroblastos dimérica aislada, y usos de la misma.
Campo de la invención
La presente invención se refiere a determinadas moléculas asociadas a tejidos cancerosos y células estromales tumorales reactivas. Más particularmente, se refiere a moléculas de proteína alfa de activación de los fibroblastos (en lo sucesivo "FAPa") . Con anterioridad ha sido identificada inmunoquímicamente una forma monomérica de la molécula, aunque no han sido aisladas ni clonadas moléculas de ácido nucleico codificantes de la misma ni han sido identificados los dímeros. Éstas son, inter alia, características de la invención. La proteína monomérica presenta un peso molecular comprendido entre aproximadamente 88 y aproximadamente 95 kilodaltons según se determinó mediante SDS-PAGE de muestras sometidas a ebullición. El dímero presentaba un peso molecular de aproximadamente 170 kilodaltons según se determinó mediante SDS-PAGE de muestras no sometidas a ebullición. FAPa se caracteriza por varias características y propiedades que son compartidas y que son características de los enzimas unidos a membrana, sugiriendo muy fuertemente que también es un enzima unido a membrana. Las moléculas de ácido nucleico, que son una parte crucial de la invención, resultan útiles como sondas para células que expresan FAPa y como materiales de partida para la producción recombinante de la proteína. Seguidamente la proteína FAPa puede utilizarse para producir anticuerpos monoclonales específicos de la proteína y de esta manera ellos mismos resultan agentes diagnósticos útiles. También presentan usos adicionales, incluyendo usos relacionados con funciones enzimáticas, tal como se describe en la presente invención.
Antecedentes y antecedentes de la técnica
El crecimiento invasivo de cánceres epiteliales se asocia a cambios celulares y moleculares característicos en el estroma de soporte. Por ejemplo, los cánceres epiteliales inducen la formación de vasos sanguíneos tumorales, el reclutamiento de fibroblastos estromales tumorales reactivos, infiltrados linfoides y fagocíticos, la liberación de péptidos mediadores y enzimas proteolíticos, y la producción de una matriz extracelular alterada (ECM) (ver, por ejemplo, Folkman, Adv. Cancer Res. 43:175-203, 1985; Basset et al., Nature 348:699-704, 1990; Denekamp et al. , Cancer Metastasis Rev. 9:267-282, 1990; Cullen et al., Cancer Res. 51:4978-4985, 1991; Dvorak et al., Cancer Cells 3:77-85, 1991; Liotta et al., Cancer Res. 51:5054s-5059s, 1991; Garin-Chesa et al., J. Histochem. Cytochem. 37:1767-1776, 1989). Una característica molecular altamente consistente del estroma en varios tipos histológicos comunes de los cánceres epiteliales es la inducción de la proteína de activación fibroblástica (FAPa), una glucoproteína de superficie celular con un Mr observado de 95.000 descubierta originalmente con un anticuerpo monoclonal, mAb F19, cultivado contra fibroblastos en proliferación en cultivo (ver Rettig et al., Cancer Res. 46:6046-6412, 1986; Rettig et al., Proc. Natl. Acad. Sci. USA 85:3110-3114, 1988; Garin-Chesa et al., Proc. Natl. Acad. USA 87:7235-7239, 1990; Rettig et al., Cancer Res. 53:3327-3335, 1993).
Algunos estudios inmunohistoquímicos, tales como aquellos citados supra, han demostrado que FAPa se expresa transitoriamente en determinados tejidos mesenquimales fetales normales pero que los tejidos adultos normales son generalmente FAPa-. De manera similar, las células epiteliales, neurales y hematopoyéticas malignas son generalmente FAPa-. Sin embargo, la mayoría de los tipos comunes de cáncer epitelial, incluyendo >90% de los carcinomas de mama, pulmón, piel, páncreas y colorrectal, contienen abundantes fibroblastos estromales reactivos FAPa+ (Garin-Chesa et al., Proc. Natl. Acad. Sci. USA 87:7235-7239, 1990). Los fibroblastos estromales tumorales FAPa+ prácticamente invariablemente acompañan a los vasos sanguíneos tumorales, formando un compartimiento celular diferenciado interpuesto entre el endotelio capilar tumoral y el aspecto basal de los grupos de células epiteliales malignas. Aunque los fibroblastos estromales FAPa+ se encuentran en carcinomas tanto primarios como colorrectales, sólo raramente contienen células estromales FAPa+. En contraste con la localización específica del estroma de FAPa en los neoplasmas epiteliales, FAPa se expresa en las células malignas de una gran proporción de sarcomas óseos y del tejido blando (Rettig et al., Proc. Natl. Acad. Sci. USA 85:3110-3114, 1988). Finalmente, se han detectado fibroblastos FAPa- en el tejido granulado de heridas en cicatrización (Garin-Chesa et al., supra). Basándose en el restringido patrón de distribución de FAPa en los tejidos normales y su expresión uniforme en el estroma de soporte de muchos cánceres epiteliales, se han iniciado ensayos clínicos con mAb F19 marcado con 131I en pacientes con cáncer de colon metastásico (Welt et al., Proc. Am. Assoc. Cancer Res. 33:319, 1992; Welt et al., J. Clin. Oncol. 12:1561-1571, 1994) con el fin de explorar el concepto de "dianización estromal tumoral" para la inmunodetección e inmunoterapia de los cánceres epiteliales.
Rettig et al., Int. J. Cancer 58:385-392, 1994, comentan la molécula FAPa y sus características. Rettig et al. postulan que FAPa se encuentra en complejos de elevado peso molecular, superior a 400 kilodaltons, pero no comentan la posibilidad de moléculas diméricas, ni dicho artículo detalla las propiedades enzimáticas específicas de la molécula.
La inducción de los fibroblastos FAPa+ en tiempos y sitios de remodelado de tejidos durante el desarrollo fetal, la reparación de tejidos y la carcinogénesis, es consistente con que esta molécula presente un papel fundamental en la fisiología del fibroblasto normal. Por lo tanto, resulta interesante y valioso aislar y clonar moléculas de ácido nucleico que codifiquen dicha molécula. Lo anterior constituye un aspecto de la invención, que se describe en detalle, conjuntamente con otras características de la invención, en la exposición siguiente. Entre los aspectos adicionales de la invención se incluyen las moléculas diméricas de FAPa y la explotación de las propiedades de estas moléculas. Estas características también se describen detalladamente a continuación.
Breve descripción de las figuras
La figura 1 compara la secuencia de aminoácidos deducida de FAPa y la secuencia conocida de CD26. La alineación ha sido optimizada.
Las figuras 2A-2H, ambas inclusive, muestran la detección inmunohistoquímica de FAPa y de CD26 en diversos tejidos. En las figuras 2A y 2B, se estudia el cáncer de mama para FAPa (figura 2A) y para CD26 (figura 2B). En las figuras 2C y 2D, se estudia el histiocitoma fibroso maligno para FAPa (figura 2C) y para CD26 (figura 2D) . El tejido cicatrizal dérmico se examina en las figuras 2E (FAPa) y 2F (CD26) . El carcinoma de células renales se estudia en las figuras 2G (FAPa) y 2H (CD26).
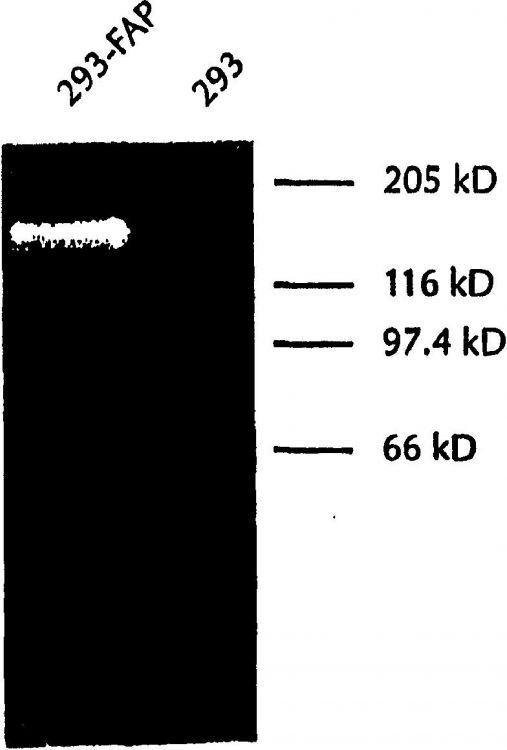
La figura 3 presenta algunos datos generados en experimentos que demostraron que FAPa presentaba actividad degradadora de las proteínas de la matriz extracelular (ECM). Al llevar a cabo la detección zimográfica de extractos en degradación de gelatina de 293-FAB, se encontró que la sustancia activa presentaba un peso molecular de aproximadamente 170 kD mediante SDS-PAGE, utilizando muestras no sometidas a ebullición para conservar la actividad enzimática.
Descripción detallada de las realizaciones preferentes
Ejemplo 1
Previamente se había observado que la línea de células fibroblásticas WI-38 reaccionaba con mAb F19 (Rettig et al., Canc. Res. 46:6406-6412, 1986; Rettig et al., Proc. Natl. Acad. USA 85:3110-3114, 1988; Garin-Chesa et al., Proc. Natl. Acad. Sci. UA 87:7235-7239, 1990; Rettig et al., Canc. Res. 53:3327-3335, 1993). Se utilizó en los experimentos siguientes.
Se preparó una biblioteca de ADNc a partir de WI-38 utilizando técnicas bien conocidas y materiales disponibles comercialmente. Específicamente, la biblioteca se construyó en el vector de expresión pCDNAI utilizando el kit de aislamiento de ARNm Fast Track y un sistema fagémido de biblioteca de ADNc. Tras preparar la biblioteca, los vectores se introdujeron mediante electroporación en la línea celular E. coli MC 1061/P3. El vector de expresión pCDNAI contiene un gen de resistencia a antibiótico, de manera que se seleccionaron...
Reivindicaciones:
1. Molécula de FAPa dimérica aislada, que presenta un peso molecular de 170 kilodaltons, determinado mediante SDS PAGE, en la que dicha molécula FAPa dimérica es capaz de degradar las proteínas de la matriz extracelular.
2. Molécula FAPa dimérica según la reivindicación 1, en la que cada monómero de dicha molécula FAPa dimérica consiste de la secuencia de aminoácidos SEC ID nº 2.
3. Molécula FAPa dimérica según la reivindicación 1, producida recombinantemente.
4. Molécula FAPa dimérica según la reivindicación 3, producida por una célula eucariótica.
5. Método para cortar un dipéptido terminal de fórmula Xaa Pro separándolo de una molécula, que comprende poner en contacto dicha molécula con una segunda molécula, siendo dicha segunda molécula la molécula PAPa dimérica según la reivindicación 1 y presentando FAPa actividad enzimática.
6. Método para identificar una sustancia que interacciona con la molécula FAPa dimérica según la reivindicación 1 que presenta actividad de FAPa, que comprende combinar dicha molécula con una muestra que debe someterse a ensayo, y determinar cualquier interacción con dicha molécula a modo de indicación de la presencia de una molécula que interacciona con una molécula que presenta actividad de FAPa.
7. Método según la reivindicación 6, en el que dicha sustancia es un antagonista de la actividad de FAPa.
8. Método según la reivindicación 6, en el que dicha sustancia es un agonista de la actividad de FAPa.
9. Método según la reivindicación 6, en el que dicha sustancia es un inhibidor de la actividad de FAPa.
10. Método según la reivindicación 6, que comprende combinar dicha sustancia con un extracto celular que presenta actividad de FAPa.
11. Método según la reivindicación 10, en el que dicho extracto celular es un extracto de una célula que ha sido transformado o transfectado con una molécula de ácido nucleico que codifica una molécula con actividad de FAPa.
12. Método según la reivindicación 11, en el que dicha célula es un procariota.
13. Método según la reivindicación 11, en el que dicha célula es un eucariota.
14. Método para determinar si una sustancia interacciona con la molécula FAPa dimérica según la reivindicación 1 que presenta actividad de FAPa, que comprende combinar dicha sustancia y dicha molécula con Ala-Pro-AFC, determinar la interacción de dicha molécula con Ala-Pro-AFG y comparar dicha interacción con la interacción de dicha molécula con Ala-Pro-AFC en ausencia de dicha sustancia, en el que una diferencia entre los mismos indica que dicha sustancia interacciona con dicha molécula.
Patentes similares o relacionadas:
 Quitina, hidrolizado y procedimiento para la producción de uno o más productos de interés a partir de insectos mediante
hidrólisis enzimática, del 29 de Julio de 2020, de Ynsect: Hidrolizado preparado a partir de insectos, que comprende al menos 40 % en peso de proteínas sobre el peso total de materia seca, un contenido […]
Quitina, hidrolizado y procedimiento para la producción de uno o más productos de interés a partir de insectos mediante
hidrólisis enzimática, del 29 de Julio de 2020, de Ynsect: Hidrolizado preparado a partir de insectos, que comprende al menos 40 % en peso de proteínas sobre el peso total de materia seca, un contenido […]
 Procedimiento de fermentación de alimentación discontinua de alta densidad celular para producir proteínas recombinantes, del 25 de Marzo de 2020, de WYETH LLC: Un procedimiento de producción de una proteína recombinante que comprende:
cultivar una célula bacteriana recombinante para expresar una proteína recombinante […]
Procedimiento de fermentación de alimentación discontinua de alta densidad celular para producir proteínas recombinantes, del 25 de Marzo de 2020, de WYETH LLC: Un procedimiento de producción de una proteína recombinante que comprende:
cultivar una célula bacteriana recombinante para expresar una proteína recombinante […]
Uso de tripeptidil peptidasas tolerantes a la prolina en composiciones de aditivo para piensos, del 26 de Febrero de 2020, de Dupont Nutrition Biosciences ApS: Un método para preparar una composición de aditivo para piensos que comprende: mezclar al menos una tripeptidil peptidasa tolerante a la prolina que tiene […]
Enzimas específicas de sitio y métodos de uso, del 19 de Febrero de 2020, de Poseida Therapeutics, Inc: Un polipéptido que comprende al menos una secuencia de aminoácidos que tiene la secuencia de LSTEQVVAIASX1X2GGKQALEAVKAQLLVLRAAPYE (SEQ ID NO: 1), en donde […]
Composiciones para unir módulos de dedos de cinc, del 15 de Enero de 2020, de Sangamo Therapeutics, Inc: Una proteína de dedos de cinc de múltiples dedos que se une específicamente a un sitio diana, comprendiendo la proteína de dedos de cinc de […]
Concentrado de proteínas de granos que contienen almidón: composición, método de fabricación y usos del mismo, del 1 de Enero de 2020, de THE UNITED STATES OF AMERICA AS REPRESENTED BY THE SECRETARY OF AGRICULTURE: Un proceso para producir un concentrado de proteinas a partir de un grano o semilla oleaginosa que contiene almidon, el proceso comprende: (i) moler el […]
 Terapia de ARNm para el tratamiento de enfermedades oculares, del 25 de Diciembre de 2019, de Translate Bio, Inc: Una composición que comprende un ARNm que codifica un péptido o polipéptido terapéutico para su uso en el tratamiento de una enfermedad, trastorno o afección ocular en un […]
Terapia de ARNm para el tratamiento de enfermedades oculares, del 25 de Diciembre de 2019, de Translate Bio, Inc: Una composición que comprende un ARNm que codifica un péptido o polipéptido terapéutico para su uso en el tratamiento de una enfermedad, trastorno o afección ocular en un […]
 Purificación de proteínas con prefiltrado, del 27 de Noviembre de 2019, de EMD Millipore Corporation: Un método para eliminar constituyentes de unión no específica de una corriente que contiene proteínas que comprende:
hacer fluir la corriente que contiene proteínas […]
Purificación de proteínas con prefiltrado, del 27 de Noviembre de 2019, de EMD Millipore Corporation: Un método para eliminar constituyentes de unión no específica de una corriente que contiene proteínas que comprende:
hacer fluir la corriente que contiene proteínas […]