METODO Y APARATO PARA SEPARAR MOLECULAS BIOLOGICAS.
Un método para separar moléculas biológicas, que comprende:
(a) aplicar un primer campo eléctrico a las moléculas para hacer que éstas migren,
en un canal de enfoque lineal común, hacia sus respectivos puntos de equilibrio isoeléctrico, para producir una separación isoeléctrica lineal;
(b) cambiar el estado electroforético de las moléculas; y
(c) aplicar un segundo campo eléctrico a la separación isoeléctrica en una dirección a lo largo de la separación isoeléctrica, para hacer que las moléculas migren y se separen en un canal de separación lineal común
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB01/04696.
Solicitante: DELTADOT LTD.
Nacionalidad solicitante: Reino Unido.
Dirección: ROOM 504, HIGH ENERGY PHYSICS, DEPARTMENT OF PHYSI,IMPERIAL COLLEGE, LONDON SW7 B.
Inventor/es: SIDERIS, DIMITRIOS, HASSARD, STUART, SANDERS,GILES,HUGO,WILLIAM, HASSARD,JOHN.
Fecha de Publicación: .
Fecha Concesión Europea: 20 de Enero de 2010.
Clasificación Internacional de Patentes:
- C07K1/24 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › por medios electroquímicos.
- C07K1/28 C07K 1/00 […] › Focalización isoeléctrica.
- G01N27/447C4
- G01N27/447C7
Clasificación PCT:
- C07K1/28 C07K 1/00 […] › Focalización isoeléctrica.
- G01N27/447 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 27/00 Investigación o análisis de materiales mediante el empleo de medios eléctricos, electroquímicos o magnéticos (G01N 3/00 - G01N 25/00 tienen prioridad; medida o ensayo de variables eléctricas o magnéticas o de las propiedades eléctricas o magnéticas de los materiales G01R). › utilizando la electroforesis.
Clasificación antigua:
- C07K1/28 C07K 1/00 […] › Focalización isoeléctrica.
- G01N27/447 G01N 27/00 […] › utilizando la electroforesis.
Fragmento de la descripción:
Método y aparato para separar moléculas biológicas.
El presente invento se refiere a un método y un aparato para separar moléculas biológicas. Es de aplicación en particular, aunque no exclusivamente, para la separación para fines de identificación de proteínas y moléculas similares.
En la separación convencional en grupos de proteínas, de la que es un ejemplo la técnica del SDS-PAGE (Sulfato dodecil sódico-Electroforesis de Gel de Poliacrilamida), se usan diferentes propiedades de las proteínas para separarlas según un mapa bidimensional. Típicamente, las proteínas adquiridas de una muestra son primero separadas de acuerdo con sus puntos de equilibrio isoeléctrico, depositadas para ello sobre un gel en tira de pH graduado. Bajo un campo eléctrico moderado, se permite que las proteínas establezcan sus puntos de equilibrio isoeléctrico dentro de ese gel. El gel en la tira se coloca después sobre el borde de una placa de separación por electroforesis bidimensional convencional, en un sistema de SDS-PAGE. Un intenso campo eléctrico ortogonal hace entonces que las proteínas migren en la segunda dimensión, a través de la placa, de acuerdo con su relación de carga/masa. El SDS (Sulfato dodecil sódico) cambia el estado electroforético e las moléculas de modo que, cuando éstas están sobre la placa, se mueven a una velocidad proporcional a su relación de carga/masa. Las proteínas más pequeñas se mueven más rápidamente que las mayores (por ser mayor su movilidad en el campo constante) y, eventualmente, se llega a una separación bidimensional u ortogonal de las proteínas a través de la superficie de la placa. Al final del procedimiento de separación, cada proteína aparece como una mancha separada sobre el gel.
Para someter a nuevas pruebas las proteínas separadas, las manchas individuales pueden ser "excavadas" del gel, o extraídas de otro modo, e investigadas, por ejemplo en un espectrómetro de masas.
Hay una serie de problemas que se plantean con esta técnica conocida, incluyendo el de la lentitud de la separación, lo engorroso de los procedimientos más bien ad hoc requeridos, el hecho de que se precisen muchas manipulaciones, con la consiguiente susceptibilidad a errores sistemáticos, y la imposibilidad de realizar análisis paralelos para comparación.
Un objeto del presente invento es suavizar al menos esas dificultades de la técnica anterior.
De acuerdo con un primer aspecto del invento, se proporciona un método para separar moléculas biológicas, que comprende:
(a) aplicar un primer campo eléctrico a las moléculas para hacer que éstas migren, en un canal de enfoque lineal común, hacia sus respectivos puntos de equilibrio isoeléctrico, para producir una separación isoeléctrica lineal;
(b) cambiar el estado electroforético de las moléculas; y
(c) aplicar un segundo campo eléctrico a la separación isoeléctrica en una dirección a lo largo de la separación isoeléctrica para hacer que las moléculas migren y se separen en un canal de separación lineal común.
De acuerdo con un segundo aspecto, se proporciona un aparato para separar moléculas biológicas, que comprende:
(a) un canal de enfoque lineal dispuesto, cuando se aplica un primer campo eléctrico a lo largo de la longitud del canal, para hacer que las moléculas migren hacia sus respetivos puntos de equilibrio isoeléctrico, para producir una separación isoeléctrica lineal; y
(b) un canal de separación lineal común en el cual las moléculas migran cuando se aplica un segundo campo eléctrico a la separación isoeléctrica en una dirección a lo largo de la separación isoeléctrica.
Con el aparato y el método del presente invento, se pueden llevar a cabo separaciones precisas y rápidas, esencialmente en una dimensión, sin que para ello se requiera el uso de geles bidimensionales como en la técnica anterior. Esto proporciona una serie de ventajas, concretamente la posibilidad de reconocimiento de un patrón mejorado y más simple, que puede ser efectuado en tiempo real. Esto, a su vez, permite la posibilidad, en ciertas realizaciones, de recoger colectivamente las proteínas u otras moléculas de interés usando un conmutador rápido de alto voltaje, por ejemplo aplicado en una bifurcación o en una polifurcación en el canal de separación. Esto permite el fácil aislamiento de una molécula dada después de que haya sido reconocida por el software.
El uso de un sistema se separación esencialmente unidimensional, que permita en algunas realizaciones la medición simultánea tanto de la relación de carga/masa molecular como también el punto de equilibro isoeléctrico, permite la posibilidad de usar múltiples canales en paralelo. Esto proporciona la capacidad para llevar a cabo estudios comparativos en tiempo real, algo que ha sido difícil o imposible con las técnicas anteriores.
El canal de enfoque primero o isoeléctrico puede ser realizado en una serie de formas. Es esencialmente un canal lineal, que puede ser recto o curvado. Como posibles realizaciones se incluyen una tira o longitud alargada de material de enfoque isoeléctrico, por ejemplo de un gel que tenga un gradiente del pH previamente definido. Como alternativa, el canal puede ser definido por un canal, estría o túnel que haya sido cortado, desarrollado o formado de otro modo en un chip. El canal incluirá, típicamente, algún gel de enfoque isoeléctrico que tenga un gradiente del pH previamente definido.
El canal de separación es también, esencialmente, un canal lineal que puede ser curvado o recto. Puede estar definido, por ejemplo, por un capilar o por un canal, estría o túnel cortado, desarrollado o formado de otro modo en un chip. Típicamente, el canal contendrá un gel de electroforesis, normalmente sin gradiente del pH.
El invento se extiende a cualquier combinación compatible de diferentes características descritas o representadas en relación con las diferentes realizaciones. Se extiende, además, a cualquier combinación compatible de características o conceptos establecidos en la introducción o a los que se haga referencia en cualquiera de las reivindicaciones.
El presente invento puede ser puesto en práctica de una serie de formas y se describirán a continuación varias realizaciones específicas, a modo de ejemplos, con referencia a los dibujos que se acompañan, en los cuales:
La Figura 1 representa una primera realización del invento;
La Figura 2 representa una segunda realización;
La Figura 3 ilustra la forma en que pueden moverse las proteínas desde el canal de enfoque al canal de separación;
La Figura 4 representa el mecanismo de transferencia en un sistema de un solo chip;
La Figura 5(a) representa la topología del chip en una realización con múltiples canales;
La Figura 5(b) representa la fase de separación isoeléctrica;
La Figura 5(c) representa la fase de inserción electroforética;
La Figura 5(d) representa la fase de separación electroforética;
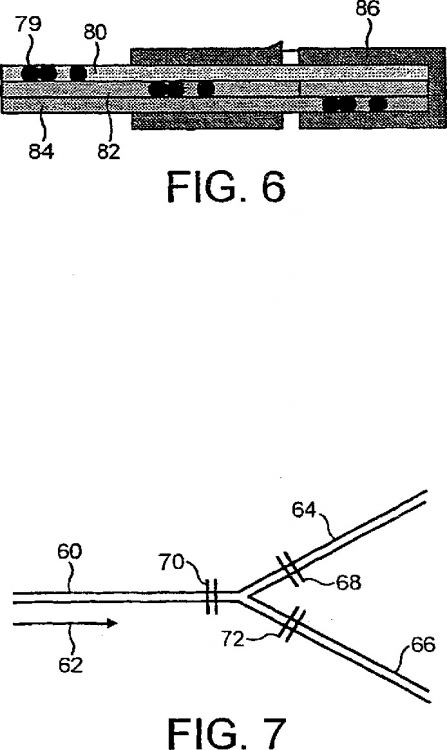
La Figura 6 representa todavía otra realización, en la que se hace uso de tres canales; y
La Figura 7 representa el sistema de recogida molecular preferido.
Pasando en primer lugar a la Figura 1, se ha representado en ella una primera realización del invento, en la cual, como en todas las realizaciones, se consigue la separación molecular esencialmente en una dimensión, en vez en las dos de la técnica anterior. El dispositivo representado comprende un chip 10 de PDMS (polidimetil siloxano), silicio, zafiro, diamante, o alguna combinación de éstos. Sobre o dentro del chip hay un microcanal indicado en general como 12. La anchura del canal puede ser desde una fracción de micrómetro hasta cientos de micrómetros, y su profundidad desde una fracción de micrómetro hasta miles de micrómetros. En la realización preferida, sin embargo, el microcanal tiene aproximadamente 50 micrómetros de anchura, y aproximadamente 500 micrómetros de profundidad.
El canal está dividido en dos partes, a saber: la sección de enfoque, indicada en general en 14, y una sección de separación indicada en general en 16. El canal 12 contiene un gel electroforético. Éste tiene, preferiblemente, un pH uniforme en toda la sección de separación 16, y un pH variable en la sección de enfoque. Es preferible que no haya discontinuidad en el límite entre la sección de enfoque y la sección de separación. Para facilidad de funcionamiento, se prefiere...
Reivindicaciones:
1. Un método para separar moléculas biológicas, que comprende:
(a) aplicar un primer campo eléctrico a las moléculas para hacer que éstas migren, en un canal de enfoque lineal común, hacia sus respectivos puntos de equilibrio isoeléctrico, para producir una separación isoeléctrica lineal;
(b) cambiar el estado electroforético de las moléculas; y
(c) aplicar un segundo campo eléctrico a la separación isoeléctrica en una dirección a lo largo de la separación isoeléctrica, para hacer que las moléculas migren y se separen en un canal de separación lineal común.
2. Un método según la reivindicación 1, en el cual el canal de enfoque es adyacente a por lo menos una parte inicial del canal de separación.
3. Un método según la reivindicación 1, en el cual el canal de enfoque es contiguo, extremo con extremo, al canal de separación, de modo que las moléculas que salen por el extremo del canal de enfoque se mueven entrando por el comienzo del canal de separación.
4. Un método según una cualquiera de las reivindicaciones precedentes, en el cual se cambia el estado electroforético de las moléculas por desnaturalización.
5. Un método según una cualquiera de las reivindicaciones 1 a 3, en el cual se cambia el estado elfito de las moléculas por exposición de las mismas a un detergente.
6. Un método según una cualquiera de las reivindicaciones 1 a 3, en el que se cambia el estado electroforético de las moléculas por calentamiento.
7. Un método según una cualquiera de las reivindicaciones precedentes, que incluye medir o determinar la velocidad de las moléculas al migrar éstas en el canal de separación.
8. Un método según una cualquiera de las reivindicaciones 1 a 6, que incluye determinar, a partir del movimiento de las moléculas dentro del canal de separación, sus respectivas relaciones de carga/masa y puntos de equilibrio isoeléctrico.
9. Un método según una cualquiera de las reivindicaciones 1 a 6, que incluye analizar el movimiento de las moléculas en el canal de separación y recoger automáticamente una muestra de las moléculas de interés, dependiendo del resultado del análisis.
10. Un método según una cualquiera de las reivindicaciones precedentes, en el cual las moléculas son proteínas.
11. Aparato para separar moléculas biológicas, que comprende:
(a) un canal de enfoque lineal (14, 30, 38, 80) dispuesto para, cuando se aplica un primer campo eléctrico a lo largo de la longitud del canal, hacer que las moléculas migren hacia sus respectivos puntos de equilibrio isoeléctrico, para producir una separación isoeléctrica lineal; y
(b) un canal de separación lineal común (16, 26, 36, 82), en el cual migran las moléculas cuando se aplica un segundo campo eléctrico a la separación isoeléctrica en una dirección a lo largo de la separación isoeléctrica.
12. Aparato según la reivindicación 11, en el cual el canal de enfoque (30, 38, 80) está dispuesto adyacente a por lo menos una parte inicial (28, 34) del canal de separación (26, 36, 82).
13. Aparato según la reivindicación 12, que incluye medios de transferencia para transferir las moléculas lateralmente desde el canal de enfoque al canal de separación.
14. Aparato según la reivindicación 13, en el cual los medios de transferencia comprenden electrodos (44, 46) para crear un campo eléctrico.
15. Aparato según la reivindicación 13, en el cual los medios de transferencia comprenden medios de secador.
16. Aparato según la reivindicación 11, en el cual el canal de enfoque (14) es contiguo, extremo con extremo, al canal de separación (16), de modo que las moléculas que salen por el extremo del canal de enfoque se mueven entrando por el comienzo del canal de separación.
17. Aparato según una cualquiera de las reivindicaciones 11 a 16, en el cual el aparato incluye un chip (10), estando definido el canal de separación por un canal en el chip.
18. Aparato según la reivindicación 17, en el cual el canal de enfoque está también definido por un canal en el chips (10).
19. Aparato según la reivindicación 17, en el cual el canal de enfoque está definido por una tira de enfoque isoeléctrico (30).
20. Aparato según una cualquiera de las reivindicaciones 11 a 19, que incluye medios (23) para medir o determinar la velocidad de las moléculas al migrar éstas a lo largo del canal de separación.
21. Aparato según una cualquiera de las reivindicaciones 11 a 19, que incluye medios para determinar, a partir del movimiento de las moléculas dentro del canal de separación, sus respectivas relaciones de carga/masa y puntos de equilibrio isoeléctrico.
22. Aparato según una cualquiera de las reivindicaciones 11 a 19, que incluye medios para analizar el movimiento de las moléculas a lo largo del canal de separación, y medios (66, 68, 70) para recoger automáticamente una muestra de las moléculas de interés.
23. Aparato según una cualquiera de las reivindicaciones 11 a 22, que incluye una pluralidad de canales de separación lineal adyacentes (34).
24. Aparato según la reivindicación 23, que incluye una pluralidad correspondiente de canales de enfoque lineal adyacentes (38).
25. Aparato según la reivindicación 11, que incluye una pluralidad de canales de enfoque (38) y una pluralidad correspondiente de canales de separación adyacentes (34), contenidos todos en un solo chip.
26. Aparato según la reivindicación 25, que incluye electrodos laterales primero y segundo (44, 46) para generar un campo eléctrico para transferir simultáneamente las moléculas en cada canal de enfoque lateralmente adentro de un canal de separación adyacente correspondiente.
27. Aparato según la reivindicación 12, que incluye un canal de separación más (84) adyacente al citado canal de separación (82).
28. Aparato según la reivindicación 12, en el cual el canal de enfoque y el canal de separación están dispuestos sobre un gel común.
29. Un método según una cualquiera de las reivindicaciones 1 a 10, en el cual el segundo campo eléctrico se extiende en toda la longitud de la separación isoeléctrica.
30. Aparato según una cualquiera de las reivindicaciones 11 a 28, en el cual el segundo campo eléctrico se extiende en toda la longitud de la separación isoeléctrica.
Patentes similares o relacionadas:
MEDIO PARA ELECTROFORESIS ANALITICA Y PREPARATIVA., del 16 de Julio de 2006, de WEBER, GERHARD: Medio para enfoque isoeléctrico analítico y preparativo con un contenido en ácidos y bases de diversos valores de pKs, con un contenido en por lo menos tres ácidos, […]
DISPOSITIVO PARA SEPARAR Y/O ANALIZAR VARIAS DIANAS MOLECULARES DISUELTAS EN UNA MEZCLA COMPLEJA, del 11 de Julio de 2011, de COMMISSARIAT A L'ENERGIE ATOMIQUE ET AUX ENERGIES ALTERNATIVES: Dispositivo para separar y/o detectar varias dianas moleculares disueltas en una mezcla compleja, dicho dispositivo comprendiendo una red de capilares (D) que permiten […]
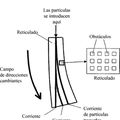 PROCEDIMIENTO DE SEPARACION CONTINUA DE PARTICULAS USANDO RETICULADOS DE OBSTACULOS ALINEADOS ASIMETRICAMENTE RESPECTO A CAMPOS, del 15 de Junio de 2010, de THE TRUSTEES OF PRINCETON UNIVERSITY: Un dispositivo microfluídico para separar partículas según su tamaño que comprende:
un canal microfluídico y
un reticulado que comprende una red […]
PROCEDIMIENTO DE SEPARACION CONTINUA DE PARTICULAS USANDO RETICULADOS DE OBSTACULOS ALINEADOS ASIMETRICAMENTE RESPECTO A CAMPOS, del 15 de Junio de 2010, de THE TRUSTEES OF PRINCETON UNIVERSITY: Un dispositivo microfluídico para separar partículas según su tamaño que comprende:
un canal microfluídico y
un reticulado que comprende una red […]
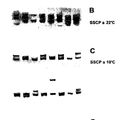 POLIMORFISMO DE CONFORMACION DE HEBRA UNICA MULTITEMPERATURA (MSSCP), del 5 de Abril de 2010, de KUCHARCZYK, KRZYSZTOF: Método para detectar una variación en una molécula de ácido nucleico comprendiendo dicho método los pasos de:
(a) prever ácidos nucleicos; (b) transformar los ácidos […]
POLIMORFISMO DE CONFORMACION DE HEBRA UNICA MULTITEMPERATURA (MSSCP), del 5 de Abril de 2010, de KUCHARCZYK, KRZYSZTOF: Método para detectar una variación en una molécula de ácido nucleico comprendiendo dicho método los pasos de:
(a) prever ácidos nucleicos; (b) transformar los ácidos […]
 CAMARAS DE ELECTROFORESIS DE CAMPOS PULSANTES, ACCESORIOS Y PROCEDIMIENTO DE EMPLEO PARA LA SEPARACION DE MOLECULAS DE ADN, del 18 de Marzo de 2010, de CENTRO NACIONAL DE INVESTIGACIONES CIENTIFICAS (CNIC): Se brindan métodos de empleo, accesorios y cámaras óptimos para realizar electroforesis de campos pulsantes (ECP) a moléculas de ADN en los sistemas "Contour Clamped Homogeneous […]
CAMARAS DE ELECTROFORESIS DE CAMPOS PULSANTES, ACCESORIOS Y PROCEDIMIENTO DE EMPLEO PARA LA SEPARACION DE MOLECULAS DE ADN, del 18 de Marzo de 2010, de CENTRO NACIONAL DE INVESTIGACIONES CIENTIFICAS (CNIC): Se brindan métodos de empleo, accesorios y cámaras óptimos para realizar electroforesis de campos pulsantes (ECP) a moléculas de ADN en los sistemas "Contour Clamped Homogeneous […]
MICROCHIPS DE ELECTROFORESIS CAPILAR DE RESINA EPON SU-8 CON DETECCION ELECTROQUIMICA INTEGRADA, del 18 de Marzo de 2010, de UNIVERSIDAD DE OVIEDO: Microchips de electroforesis capilar de resina EPON SU-8 con detección electroquímica integrada, preferentemente amperométrica, totalmente integrada […]
Casetes para su uso en ensayos electroforéticos paralelos automatizados y procedimientos para su fabricación y uso, del 17 de Junio de 2020, de Coastal Genomics Inc: Un casete para su uso en ensayos electroforéticos paralelos, comprendiendo el casete: - una bandeja, teniendo la bandeja una base y dos pares […]
Aparato para detección de biomoléculas y su fabricación, del 3 de Junio de 2020, de HAI KANG LIFE CORPORATION LIMITED: Un biochip para detectar o secuenciar biomoléculas que comprende: un miembro base; una capa dieléctrica depositada sobre el miembro base y que tiene […]