CAMARAS DE ELECTROFORESIS DE CAMPOS PULSANTES, ACCESORIOS Y PROCEDIMIENTO DE EMPLEO PARA LA SEPARACION DE MOLECULAS DE ADN.
Se brindan métodos de empleo, accesorios y cámaras óptimos para realizar electroforesis de campos pulsantes (ECP) a moléculas de ADN en los sistemas "Contour Clamped Homogeneous Electri Field" (CHEF) y "Transversal Alternating Field Electrophoresis" (TAFE).
Las cámaras separan rápidamente a moléculas de ADN en minigeles. Las distancias entre los electrodos de polaridades opuestas están comprendidas entre 6,2 y 15 cm y determinan las dimensions de las cámaras y accesorios. Las moléculas son separadas reproduciblemente porque los accesorios garantizan resistencia eléctrica homgénea en el tampón y minigel. Las cámaras admiten alto formato de muestras usando eficientemente los reactivos. Esto se logra excluynedo las zonas no útiles de electroforesis. Par mayor optimización, las cámaras TAFE poseen varias zonas útiles de electroforesis (ZUE) con un minigel cada una. Una o varias ZUE pueden ser activadas a voluntad en la electroforesis para variar entre los experimentos la cantidad de minigeles,muestras y tampón. Se presentan cámaras en "configuración TAFE invertida" con los cátodos en su parte inferior
Tipo: Resumen de patente/invención. Número de Solicitud: W0100003CU.
Solicitante: CENTRO NACIONAL DE INVESTIGACIONES CIENTIFICAS (CNIC).
Nacionalidad solicitante: Cuba.
Dirección: AVENIDA 25, NO. 15202,ESQ. A 158 CUBANACAN, PLAYA,CIUDAD DE LA HABANA 12100.
Inventor/es: RIVERON ROJAS,ANA MARIA, OROZCO OROZCO,ESTHER, ARENCIBIA DIAZ,OSCAR, LOPEZ CANOVA,LILIA, HERRERA ISIDRON,JOSE ALFREDO, PEREZ PEREZ,GABRIEL, CANINO RAMOS,CARLOS ALBERTO CLLE 192, BATISTA SANTILER,LUIS MARIANO, GIGATO P REZ,REGNAR, RUIZ ESQUIVEL,LEONARDO, NOA BLANCO,MARIA DOLORES, JAVERT HIGGINSON,ELISA.
Fecha de Publicación: .
Fecha Concesión Europea: 14 de Octubre de 2009.
Clasificación Internacional de Patentes:
- G01N27/447B
- G01N27/447C4
Clasificación PCT:
- G01N27/447 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 27/00 Investigación o análisis de materiales mediante el empleo de medios eléctricos, electroquímicos o magnéticos (G01N 3/00 - G01N 25/00 tienen prioridad; medida o ensayo de variables eléctricas o magnéticas o de las propiedades eléctricas o magnéticas de los materiales G01R). › utilizando la electroforesis.
Clasificación antigua:
- C12Q1/68 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12Q PROCESOS DE MEDIDA, INVESTIGACION O ANALISIS EN LOS QUE INTERVIENEN ENZIMAS, ÁCIDOS NUCLEICOS O MICROORGANISMOS (ensayos inmunológicos G01N 33/53 ); COMPOSICIONES O PAPELES REACTIVOS PARA ESTE FIN; PROCESOS PARA PREPARAR ESTAS COMPOSICIONES; PROCESOS DE CONTROL SENSIBLES A LAS CONDICIONES DEL MEDIO EN LOS PROCESOS MICROBIOLOGICOS O ENZIMOLOGICOS. › C12Q 1/00 Procesos de medida, investigación o análisis en los que intervienen enzimas, ácidos nucleicos o microorganismos (aparatos de medida, investigación o análisis con medios de medida o detección de las condiciones del medio, p. ej. contadores de colonias, C12M 1/34 ); Composiciones para este fin; Procesos para preparar estas composiciones. › en los que intervienen ácidos nucleicos.
- G01N27/47
Fragmento de la descripción:
Cámaras de electroforesis de campos pulsantes, accesorios y procedimiento de empleo para la separación de moléculas de ADN.
Campo técnico
La presente invención se refiere al campo de la Biología Molecular y, en particular, se refiere a cámaras de electroforesis de campos pulsantes de los sistemas Campo Eléctrico Homogéneo con Contornos Fijados (Contour Clamped Homogeneous Electric Field) (CHEF) y Electroforesis de Campo Alternativo Transversal (Transversal Alternating Field Electrophoresis) (TAFE). La presente invención se refiere también al uso de estas cámaras para la separación de moléculas de ADN y a un procedimiento para la selección de las condiciones de electroforesis empleando dichas cámaras.
Antecedentes de la invención
La electroforesis de campos pulsantes (ECP) data de 1984, cuando Schwartz D. C. y Cantor C. (Cell, 37, 67-75, 1984; Patente de Estados Unidos Nº 4.473.452) observaron que las grandes moléculas intactas de ADN se resolvían en los geles de agarosa en patrones de bandas mediante la aplicación de pulsos eléctricos que alternaban periódicamente su dirección de aplicación, la que formaba un cierto ángulo en relación con el gel. Los autores también determinaron que la separación de las moléculas dependía esencialmente de la duración de los pulsos eléctricos. Con posterioridad, se determinó que la geometría de las líneas de fuerza de los campos eléctricos alternantes, la intensidad de los mismos, la temperatura experimental, la fuerza iónica de la solución tampón y la concentración del gel de agarosa eran factores importantes que influían en la resolución que podía alcanzarse entre las moléculas de ADN (Birren B. y Lai E. Academic Press. Nueva York, 1993, pp 107, 111, 129, 131, 135; López-Cánovas L. y cols., J. of Chromatogr. A, 1998, 806, 123-139; López-Cánovas L. y cols., J. of Chromatogr. A, 1998, 806, 187-197).
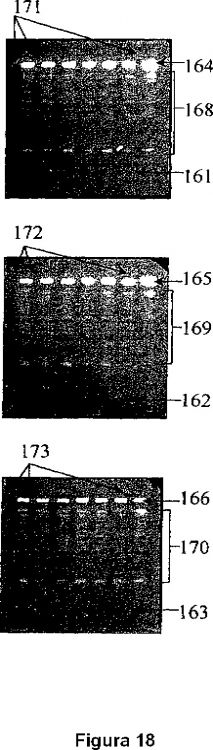
La electroforesis de campos pulsantes brinda la separación de las moléculas de ADN en forma de patrones de bandas. Es decir, cada patrón se forma después de la electroforesis en las carrileras de los geles de separación. A su vez, en cada pocillo del gel se cargan bloques de agarosa que contienen las moléculas inmovilizadas de ADN, las que durante la electroforesis migran a lo largo de dichas carrileras y forman los patrones de bandas. Por tanto, este tipo de electroforesis tiene asociado un procedimiento para preparar moléculas de ADN intactas e inmovilizadas en bloques de gel. Esas moléculas pueden ser, o no, digeridas con endonucleasas de restricción antes de sufrir el procedimiento de electroforesis.
Se han desarrollado varios sistemas para realizar la ECP, los que se caracterizan por poseer cámaras en las cuales se colocan los electrodos en ordenamientos diferentes. Entre esas cámaras se encuentran las cámaras con ordenamiento de electrodos OFAGE ("Orthogonal Field Alternating Gel Electrophoresis", Carle C. F. y Olson M. V. Nucleic Acids Res. 1984, 12, 5647-5664), CHEF ("Contour Clamped Homogeneous Electric Field", Chu G. Science 234, 1986, 1582-1585), TAFE ("Transversal Alternating Field Electrophoresis", Patente de Estados Unidos Nº 4.740.283), FIGE ("Field Inversión Gel Electrophoresis", Patente de Estados Unidos Nº 4.737.251 de Carle G. F. y Olson M. V) y las mini-cámaras MiniTAFE y MiniCHEF (Riverón, A. M. y cols., Anal. Lett, 1995, 28, 1973-1991; Solicitud de Patente Europea EP 0 745 844).
Todos estos sistemas se caracterizan por poseer circuitos electrónicos para alternar los campos eléctricos y por poseer accesorios para preparar el gel. También existen accesorios para preparar las muestras. Ellos se diferencian entre sí por la complejidad de la electrónica para energizar los electrodos y cambiar la orientación del campo eléctrico. También se diferencian por su capacidad, o incapacidad, de brindar trayectorias rectas de migración en los patrones de bandas. La posibilidad de obtener trayectorias rectas de migración es esencial cuando se desean comparar los patrones que brindan numerosas muestras, mientras que la sencillez en la electrónica facilita y abarata la producción de los sistemas. De los sistemas mencionados, existen tres que brindan trayectorias rectas de migración de las moléculas:
Estos sistemas tienen en común que en sus cámaras se coloca un gel que es atravesado simétricamente por las líneas de fuerza de los campos eléctricos que se generan en los electrodos que tienen polaridad opuesta en el ordenamiento de electrodos. En ese gel se cargan las muestras que contienen las moléculas intactas de ADN que son separadas. En todas esas cámaras también existen zonas por donde pasan líneas de fuerza del campo eléctrico que no atraviesan el gel y por tanto no actúan sobre las moléculas. La zona de la cámara que contiene el gel y por la cual pasan las líneas de fuerza del campo eléctrico que actúan directamente sobre las moléculas se denominará aquí zona útil de electroforesis (ZUE), mientras que las zonas de la cámara por donde pasan líneas de fuerza del campo eléctrico que no actúan sobre las moléculas la denominaremos zonas no útiles de electroforesis (ZNU). Todas las cámaras existentes para realizar ECP poseen una región ZUE y regiones ZNU.
La cámara y la electrónica del sistema FIGE son sencillas y existen cámaras que permiten analizar simultáneamente numerosas muestras (hasta 96 muestras, empleando dos peines de 48 dientes en la Cubeta OnePhorAll Submarine Gel System de la Jordan Scientific, Catálogo BDH, 1997, Sección E pp 4-371), pero en las cámaras FIGE se observan fenómenos de inversión de la movilidad de las moléculas (Carle G. F., Frank M. y Olson M. V. Science, vol. 232, pp 65-68, 1986). Debido a la ausencia de teoría que prediga si estas moléculas de ADN invertirán su movilidad bajo determinadas condiciones experimentales en el FIGE, dicha inversión limita la utilización de dichas cámaras para analizar el tamaño de las moléculas de ADN que son separadas y comparar sus patrones de bandas. Por ejemplo, ese fenómeno puede provocar que dos moléculas de ADN de tamaños diferentes migren la misma distancia en el gel, lo que impide identificarlas, salvo que se recurra a procedimientos de hibridación con sondas. Hasta el momento, las dos únicas formas de estimar el tamaño de grandes moléculas específicas de ADN separadas en experimentos de ECP son:
En el FIGE los marcadores de talla también pueden sufrir fenómenos de inversión de la movilidad y como se mencionó no existe teoría capaz de predecir el momento y las condiciones en que una molécula invertirá su movilidad. Estas son limitaciones serias para emplear cámaras FIGE en estudios comparativos de numerosas muestras, como ocurre, por ejemplo, en la epidemiología molecular. Por esa razón, los sistemas más utilizados en la actualidad para comparar los patrones de bandas de múltiples muestras son el CHEF y el TAFE.
El sistema TAFE fue propuesto por Gardiner K. y cols. en su publicación en Somatic Cell Mol. Genet. 1986, 12, 185-195, lo denominaron...
Reivindicaciones:
1. Cámaras de electroforesis de campo pulsado con conjuntos de electrodos tipo TAFE (Electroforesis de Campo Alternativo Transversal, "Transversal Alternating Field Electrophoresis") o CHEF (Campo Eléctrico Homogéneo con Contornos Fijados, "Contour Clamped Homogeneous Electric Field") para la separación de moléculas de ADN cargadas en geles empleando un sistema para energizar sus electrodos y alternar la dirección de aplicación de los campos eléctricos generados por el conjunto de electrodos, así como un sistema para hacer circular el tampón, en donde dichas cámaras comprenden,
estando dichas cámaras CHEF y TAFE y sus conjuntos de accesorios completamente ensamblados y se utilizan de acuerdo con procedimientos específicos de utilización, cámaras en las que la separación de moléculas de ADN se realiza de acuerdo a los procedimientos para realizar la electroforesis en dichas cámaras, comprendiendo los procedimientos de uso varios pasos.
2. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que las cámaras CHEF poseen una ZUE única que puede soportar un minigel con forma rectangular o cuadrada.
3. Cámaras de electroforesis de acuerdo con la reivindicación 2 en las que las dimensiones del minigel rectangular que se emplea en las cámaras CHEF son d/3 centímetros de longitud y d/1,732 centímetros de ancho (a), siendo el ancho de 3,6 a aproximadamente 8,7 cm y la longitud de 2,1 a aproximadamente 5 cm.
4. Cámaras de electroforesis de acuerdo con la reivindicación 2 en las que la longitud y el ancho "a" del minigel con forma cuadrada de las cámaras CHEF es de d/3 centímetros, siendo "a" de 2,1 a aproximadamente 5 cm.
5. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que las bases de las cámaras CHEF que comprenden la ZUE poseen un área igual a [2+ (d/0,87)] [6+d], siendo dicha área de aproximadamente 111,3 a aproximadamente 404,1 cm2, mientras que las partes restantes de la base de dicha cámara están cubiertas con bloques de materiales de elevada constante dieléctrica.
6. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que las cámaras con un conjunto de electrodos TAFE tienen una pared frontal rectangular con el lado más largo paralelo a cualquier electrodo del conjunto y hasta 50 cm de longitud ("L"), cámara que soporta un minigel en una ZUE única o más minigeles en las ZUE formadas dividiendo la longitud del lado más largo de dicha pared de la cámara y los electrodos del conjunto.
7. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que la longitud de los minigeles de las cámaras TAFE es d 0,515 centímetros, longitud que es de 3,2 a aproximadamente 7,7 cm.
8. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que un minigel de las cámaras CHEF o TAFE tiene "N" pocillos que soportan "N" como el número máximo de minibloques, siendo N igual a (a-0,2)/0,25, y "a" el ancho de minigel, que es de 1,7 a 50 cm en TAFE.
9. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que el área correspondiente a la ZUE en las paredes laterales de la cámara TAFE, o las paredes que soportan el gel y los electrodos, es igual a [2+1,4 d] [2+0, 54 d] - 1,02 [1+0,54 d]2, donde los valores de las áreas están comprendidos entre 37,8 y 149,5 cm2, mientras que las partes de dichas paredes laterales que corresponden a la ZNU están bloqueadas con piezas de elevada constante dieléctrica.
10. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que las cámaras TAFE se subdividen uniformemente en varias ZUE con un minigel en cada una, minigeles que se colocan a lo ancho en tándem, secuencialmente uno al lado del otro, con sus caras paralelas a los electrodos.
11. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que las cámaras TAFE poseen una plataforma de electrodos fija o desmontable única que contiene el conjunto de electrodos (cámara TAFE de tipo I) siendo "L" la longitud de dichos electrodos hasta 50 cm.
12. Cámaras de electroforesis de acuerdo con las reivindicaciones 1 u 11 en las que la cámara TAFE de la plataforma de electrodo único de tipo I está subdividida uniformemente y forma varias ZUE con todos los minigeles soportados en un solo marco.
13. Cámaras de electroforesis de acuerdo con las reivindicaciones 1 u 11 en las que la cámara TAFE de la plataforma de electrodo único de tipo I está subdividida uniformemente y forma varias ZUE colocándose cada minigel independientemente en una ZUE, para lo cual la dichas cámaras deben poseer piezas ranuradas lateralmente por donde se deslizan dichos minigeles.
14. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que una cámara TAFE posee diversas miniplataformas independientes fijas o desmontables de un conjunto de electrodos con un minigel cada una, plataformas en las que la zona útil para electroforesis (ZUE) está limitada y que comprenden electrodos físicamente separados de los electrodos de las restantes plataformas de dicha cámara, pero que pueden conectarse en paralelo con ellos para adquirir continuidad, de manera que cuando la cámara se energiza con una sola fuente de potencia, todas las muestras cargadas en todos los minigeles de las plataformas estén sometidas a las mismas condiciones de electroforesis (cámara TAFE de tipo II).
15. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que una cámara TAFE tiene piezas de la forma apropiada hechas de cualquier material con elevada constante dieléctrica, piezas que ocupan y ocluyen totalmente las regiones de la cámara que corresponden a las zonas útiles para electroforesis (ZUE) y que son tantas como las necesarias para analizar el número de muestras deseado en la cantidad mínima de ZUE.
16. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que las cámaras TAFE poseen de 1 a 30 ZUE y soportan de 1 a 30 minigeles.
17. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que dichas cámaras TAFE pueden tener configuración TAFE invertida, configuración en la que los cátodos de las miniplataformas están en el fondo de la cámara de electroforesis y los ánodos en su parte superior, cargándose por tanto las muestras en la parte inferior del minigel, de manera que las muestras migran en el sentido contrario al de la fuerza de gravedad.
18. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que las cámaras TAFE poseen paredes externas paralelas al plano imaginario que contiene el cátodo de un campo eléctrico y el ánodo del otro campo eléctrico, siendo estas paredes las que no soportan los electrodos, y colocándolas como máximo a 2 cm de dicho plano imaginario, o bloques hechos de materiales con elevada constante dieléctrica que ocupan las partes de la cámara que corresponden las zonas no útiles para electroforesis (ZNU).
19. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que los electrodos que se mantienen fijos por la acción de un sistema de fijación en las cámaras CHEF y TAFE, entran dentro de la cámara desde el exterior, se energizan con una sola fuente de potencia durante la electroforesis y entran en contacto con el tampón que pasa a través de las perforaciones de los tapones elásticos insertados en los orificios perforados en la base de las cámaras CHEF o en las paredes de las cámaras TAFE que soportan el gel, usándose dichos tapones para fijar los electrodos a la cámara.
20. Cámaras de electroforesis de acuerdo con las reivindicaciones 1 ó 19 en las que los tapones elásticos a través de los que pasan los electrodos pueden ser de silicona, goma u otro material elástico cualquiera.
21. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que las cámaras TAFE poseen un sistema de tensión de los electrodos que atraviesan las paredes de dicha cámara, sistema que se coloca en la salida de cada electrodo, estando comprendido dicho sistema por:
22. Empleo de las cámaras de electroforesis de acuerdo con las reivindicaciones 1 ó 21 en el que el procedimiento de empleo del sistema de fijación y tensión de los electrodos de las cámaras TAFE comprende los siguientes pasos:
23. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que el conjunto de láminas rectangulares extraíbles de las cámaras CHEF tiene dos tipos de láminas rectangulares: los tipos "A" y "B", hechas ambas de un material de elevada constante dieléctrica, láminas cuyos lados más largos son tan anchos como el ancho de la cámara, y los otros lados son de al menos 2 cm de altura en la lámina de tipo "A" y de 0,5 cm en el tipo "B".
24. Cámaras de electroforesis de acuerdo con las reivindicaciones 1 ó 23 en las que las láminas de tipo "A" se colocan sobre la base de la cámara sobresaliendo desde la superficie de la solución tampón, las láminas sobre la base están separadas de la misma de 0,02 a aproximadamente 0,05 cm y forman un hueco entre sus bordes inferiores y la base, hueco a través del cual sólo puede circular la solución tampón.
25. Cámaras de electroforesis de acuerdo con las reivindicaciones 1 ó 23 en las que las láminas de tipo B están pegadas a la base de la cámara y sumergidas totalmente en la solución tampón de tal forma que al circular el tampón en la cámara este fluye solamente por encima de las láminas de tipo "B".
26. Cámaras de electroforesis de acuerdo con las reivindicaciones 1 ó 23 en las que las ambos tipos de láminas (A y B) se ubican alternativamente en la entrada y en la salida de la solución tampón hacia el conjunto de electrodos, colocación hecha en el siguiente orden: una lámina de tipo A seguida de una lámina de tipo B, repitiendo "n" veces ese par de láminas, donde "n" es un número entero entre 1 y 4 y colocando la última lámina aproximadamente a 1 cm de los electrodos y siendo dicha última lámina de tipo A.
27. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que el conjunto de láminas rectangulares extraíbles de las cámaras TAFE son dos láminas idénticas hechas de un material de elevada constante dieléctrica, láminas similares a las paredes de la cámara y colocadas en paralelo con el plano que contiene los electrodos del mismo lado que el gel, estando dichas láminas ranuradas horizontalmente hasta 0,5 cm en su tercio inferior, y siendo la ranura tan grande como el ancho de la cámara o el minigel.
28. Cámaras de electroforesis de acuerdo con las reivindicaciones 1 ó 27 en las que las dos láminas extraíbles de las cámaras TAFE están colocadas de la siguiente manera: una cerca de la entrada de tampón y la otra cerca de la salida, láminas que dividen la cámara en tres compartimentos: el central, que contiene la ZUE, y dos laterales a través de los cuales se suministra el tampón a la cámara o se extrae de la misma.
29. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que el conjunto de dispositivos desmontables para moldear minigeles, dispositivos formados por marcos, placas base, tapas y diversas piezas con forma de peine con dientes de idéntico ancho e idéntico espesor cada uno, que están comprendidos por:
30. Cámaras de electroforesis de acuerdo con la reivindicación 29 en las que el peine de dientes largos en su parte anterior es liso mientras que en su parte posterior y por encima de los dientes está engrosado formándose un escalón, siendo dichos dientes de tamaños idénticos, que son de: espesor de 0,03 a aproximadamente 0,1 cm, ancho de 0,15 cm al ancho del minigel "a" menos 0,3 cm (a - 0,3), y longitud igual al espesor (e) del minigel menos 0,1 cm (e - 0,1).
31. Cámaras de electroforesis de acuerdo con la reivindicación 29 en las que el peine de dientes cortos posee la misma forma y dimensiones que el de dientes largos excepto que la longitud de los dientes es aproximadamente 0,2 cm menor.
32. Cámaras de electroforesis de acuerdo con la reivindicación 29 en las que la tapa 2, o tapa que encaja en la parte trasera del peine, posee dos caras planas y en un borde sobresaliente, mientras que la tapa 1, que encaja en la parte delantera del peine, tiene dos caras planas pero uno de sus bordes está rebajado en forma de cuña.
33. Cámaras de electroforesis de acuerdo con la reivindicación 1 en las que el conjunto del sistema desarmable de bloques, tapas y cortadores para formar los minibloques de muestras de dichos minigeles está comprendido por:
34. Uso de las cámaras de electroforesis de acuerdo con la reivindicación 1 en el que el procedimiento de uso del sistema desarmable de tapas y cortadores de bloques para preparar minibloques de muestras con tamaños (profundidad, ancho y espesor) similares a los tamaños de los pocillos del minigel, comprende los siguientes pasos:
35. Uso de las cámaras de electroforesis de acuerdo con la reivindicación 1 en el que el procedimiento de uso del dispositivo desarmable formado por marcos, placas base, tapas y peines con el que los minigeles de la ZUE de dicha cámara se moldean con un área transversal homogénea comprende las siguientes etapas:
36. Uso de las cámaras de electroforesis de acuerdo con la reivindicación 1 en el que el procedimiento para realizar la electroforesis en las cámaras TAFE que tienen varias ZUE para analizar un número "x" de muestras, comprende los siguientes pasos:
37. Uso de las cámaras de electroforesis de acuerdo con la reivindicación 1 en el que es necesario llenar dichas cámaras TAFE con solución tampón hasta un nivel que sobrepase el espesor del gel en al menos 0,3 cm para realizar la electroforesis, consiguiéndose por adición del tampón a la cámara, volumen de tampón que se calcula a partir del conocimiento de "d", o separación entre los electrodos de polaridades opuestas en el conjunto, de acuerdo con la fórmula {[2 + (d/cos (30º))] [6 + d]} (0,3 + espesor del gel), siendo el volumen añadido a la cámara de aproximadamente 72,3 a aproximadamente 323,3 ml de la misma si los geles son de 0,35 a 0,5 cm de espesor.
38. Uso de las cámaras de electroforesis de acuerdo con la reivindicación 1 en el que es necesario llenar dichas cámaras TAFE con solución tampón hasta un nivel que sobrepase la altura del gel en al menos 0,3 cm para realizar la electroforesis, consiguiéndose por adición del tampón a la cámara, volumen que puede conocerse a partir del conocimiento de "d", o separación entre los electrodos de polaridades opuestas en el conjunto, y el número de ZUE activas ("NZUEactivas") en la cámara de acuerdo con la fórmula [(2+1,4 d) (2+0,54 d)-1,02 (1+0,54 d)2] L NZUEactivas/NZUEtotal, estando esos valores comprendidos entre 63,2 y 7390 ml.
39. Uso de las cámaras de electroforesis de acuerdo con la reivindicación 1 en el que las cámaras CHEF y TAFE de ZUE activa única admiten activación a potencias de campo eléctrico de hasta 16 o 25 V/cm respectivamente, siempre que las cámaras se activen usando fuentes de potencia con una salida de potencia máxima de 300 vatios, y que la solución de tampón se mantenga a una temperatura constante, que puede ser de aproximadamente 4 a aproximadamente 30ºC.
40. Uso de las cámaras de electroforesis de acuerdo con las reivindicación 1 ó 36 en el que las cámaras TAFE de varias ZUE activas admiten activación a potencias de campo eléctrico de 8 a 25 V/cm, campo eléctrico que depende del número de ZUE activadas, siempre que el tampón se mantenga a una temperatura constante que puede ser de 4 a 30ºC.
Patentes similares o relacionadas:
 DISPOSITIVO PARCIALMENTE DESECHABLE PARA ELECTROFORESIS, del 3 de Agosto de 2010, de UNIVERSIDAD DEL PAIS VASCO- EUSKAL HERRIKO UNIBERSITATEA (80%)
LABORATORIOS AIDELOS, SRL (20%): Dispositivo parcialmente desechable para electroforesis.
La invención se refiere a un dispositivo para electroforesis, parcialmente desechable, con […]
DISPOSITIVO PARCIALMENTE DESECHABLE PARA ELECTROFORESIS, del 3 de Agosto de 2010, de UNIVERSIDAD DEL PAIS VASCO- EUSKAL HERRIKO UNIBERSITATEA (80%)
LABORATORIOS AIDELOS, SRL (20%): Dispositivo parcialmente desechable para electroforesis.
La invención se refiere a un dispositivo para electroforesis, parcialmente desechable, con […]
 PROCEDIMIENTO DE SEPARACION CONTINUA DE PARTICULAS USANDO RETICULADOS DE OBSTACULOS ALINEADOS ASIMETRICAMENTE RESPECTO A CAMPOS, del 15 de Junio de 2010, de THE TRUSTEES OF PRINCETON UNIVERSITY: Un dispositivo microfluídico para separar partículas según su tamaño que comprende:
un canal microfluídico y
un reticulado que comprende una red […]
PROCEDIMIENTO DE SEPARACION CONTINUA DE PARTICULAS USANDO RETICULADOS DE OBSTACULOS ALINEADOS ASIMETRICAMENTE RESPECTO A CAMPOS, del 15 de Junio de 2010, de THE TRUSTEES OF PRINCETON UNIVERSITY: Un dispositivo microfluídico para separar partículas según su tamaño que comprende:
un canal microfluídico y
un reticulado que comprende una red […]
DISPOSITIVO PARA SEPARAR Y/O ANALIZAR VARIAS DIANAS MOLECULARES DISUELTAS EN UNA MEZCLA COMPLEJA, del 11 de Julio de 2011, de COMMISSARIAT A L'ENERGIE ATOMIQUE ET AUX ENERGIES ALTERNATIVES: Dispositivo para separar y/o detectar varias dianas moleculares disueltas en una mezcla compleja, dicho dispositivo comprendiendo una red de capilares (D) que permiten […]
 METODO Y APARATO PARA SEPARAR MOLECULAS BIOLOGICAS, del 25 de Mayo de 2010, de DELTADOT LTD: Un método para separar moléculas biológicas, que comprende:
(a) aplicar un primer campo eléctrico a las moléculas para hacer que éstas migren, […]
METODO Y APARATO PARA SEPARAR MOLECULAS BIOLOGICAS, del 25 de Mayo de 2010, de DELTADOT LTD: Un método para separar moléculas biológicas, que comprende:
(a) aplicar un primer campo eléctrico a las moléculas para hacer que éstas migren, […]
 POLIMORFISMO DE CONFORMACION DE HEBRA UNICA MULTITEMPERATURA (MSSCP), del 5 de Abril de 2010, de KUCHARCZYK, KRZYSZTOF: Método para detectar una variación en una molécula de ácido nucleico comprendiendo dicho método los pasos de:
(a) prever ácidos nucleicos; (b) transformar los ácidos […]
POLIMORFISMO DE CONFORMACION DE HEBRA UNICA MULTITEMPERATURA (MSSCP), del 5 de Abril de 2010, de KUCHARCZYK, KRZYSZTOF: Método para detectar una variación en una molécula de ácido nucleico comprendiendo dicho método los pasos de:
(a) prever ácidos nucleicos; (b) transformar los ácidos […]
Casetes para su uso en ensayos electroforéticos paralelos automatizados y procedimientos para su fabricación y uso, del 17 de Junio de 2020, de Coastal Genomics Inc: Un casete para su uso en ensayos electroforéticos paralelos, comprendiendo el casete: - una bandeja, teniendo la bandeja una base y dos pares […]
Aparato para detección de biomoléculas y su fabricación, del 3 de Junio de 2020, de HAI KANG LIFE CORPORATION LIMITED: Un biochip para detectar o secuenciar biomoléculas que comprende: un miembro base; una capa dieléctrica depositada sobre el miembro base y que tiene […]
Un canal catiónico no selectivo en células neurales y compuestos que bloquean el canal para su uso en el tratamiento de la inflamación del cerebro, del 6 de Mayo de 2020, de UNIVERSITY OF MARYLAND, BALTIMORE: Un antagonista de SUR1 que bloquea el canal de NCCa-ATP para su uso en (a) la prevención o el tratamiento de la inflamación de las células neurales […]