Aparato para prolongar la supervivencia de plaquetas.
Un aparato para procesar una muestra de plaquetas, que comprende:
un primer recipiente estéril que tiene uno o más puertos y que contiene una preparación de células sanguíneas que comprende plaquetas, un segundo recipiente estéril que tiene uno o más puertos y que contiene un azúcar nucleosídico que es ácido citidin-5'- monofosfo-N-acetilneuramínico, estando adaptado el primer recipiente al segundo recipiente a través de un conducto estéril fijable de forma reversible al puerto del primer recipiente y al puerto del segundo recipiente, comprendiendo además el conducto una válvula, en el que el azúcar nucleosídico presente en el segundo recipiente estéril se introduce en el primer recipiente estéril y las plaquetas en la preparación de células sanguíneas allí se hacen competentes para el almacenamiento en frío después de que las plaquetas se ponen en contacto con el azúcar nucleosídico.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/031921.
Solicitante: VELICO MEDICAL, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 100 CUMMINGS CENTER, SUITE 436 H BEVERLY MA 01915-6122 ESTADOS UNIDOS DE AMERICA.
Inventor/es: ROSIELLO,KEITH, CLAUSEN,Henrik.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A01N1/02 NECESIDADES CORRIENTES DE LA VIDA. › A01 AGRICULTURA; SILVICULTURA; CRIA; CAZA; CAPTURA; PESCA. › A01N CONSERVACION DE CUERPOS HUMANOS O ANIMALES O DE VEGETALES O DE PARTES DE ELLOS (conservación de alimentos o productos alimenticios A23 ); BIOCIDAS, p. ej. EN TANTO QUE SEAN DESINFECTANTES, PESTICIDAS O HERBICIDAS (preparaciones de uso médico, dental o para el aseo que eliminan o previenen el crecimiento o la proliferación de organismos no deseados A61K ); PRODUCTOS QUE ATRAEN O REPELEN A LOS ANIMALES; REGULADORES DEL CRECIMIENTO DE LOS VEGETALES. › A01N 1/00 Conservación de cuerpos humanos o animales, o partes de ellos. › Conservación de partes vivas.
PDF original: ES-2376777_T3.pdf
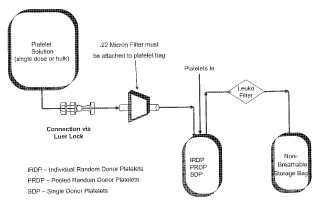
Fragmento de la descripción:
Aparato para prolongar la supervivencia de plaquetas Campo de la invención La invención se refiere a composiciones y métodos para reducir la eliminación de plaquetas, y prolongar la supervivencia de las plaquetas.
Antecedentes de la invención Las plaquetas son células sanguíneas anucleadas derivadas de la médula ósea que protegen a mamíferos heridos de la pérdida de sangre adhiriéndose a sitios de daño vascular y promoviendo la formación de coágulos de fibrina en el plasma. Los seres humanos carentes de plaquetas circulantes por fallo de la médula ósea padecen sangrados espontáneos potencialmente mortales, y las deficiencias menos graves de plaquetas contribuyen a complicaciones de sangrado después de un traumatismo o una cirugía.
Una reducción en el número de plaquetas circulantes hasta por debajo de ∼70.000 por μl supuestamente da como resultado una prolongación de una prueba de tiempo de sangrado cutáneo estandarizada, y el intervalo de sangrado se prolonga, extrapolándose hasta casi el infinito, a medida que el recuento de plaquetas cae hasta cero. Se piensa que los pacientes con recuento de plaquetas de menos de 20.000 por μl son muy susceptibles a hemorragia espontánea de superficies mucosas, especialmente cuando la trombocitopenia está causada por fallo de la médula ósea y cuando los pacientes afectados sufren complicaciones con septicemia u otras agresiones. Las deficiencias plaquetarias asociadas con trastornos de la médula ósea tales como anemia aplásica, leucemias agudas y crónicas, cáncer metastático, pero que resultan especialmente de tratamientos para el cáncer con radiación ionizante y quimioterapia, representan un importante problema de salud pública. La trombocitopenia asociada a cirugía mayor, daño y septicemia también deriva en administración de cantidades significativas de transfusiones de plaquetas.
Un avance principal en cuidados médicos hace medio siglo fue el desarrollo de transfusiones de plaquetas para corregir tales deficiencias plaquetarias, y más de 9 millones de transfusiones de plaquetas tuvieron lugar sólo en EE.UU. en 1999 (Jacobs et al., 2001) . Las plaquetas, sin embargo, a diferencia de todos los demás tejidos trasplantables, no toleran la refrigeración, debido a que desaparecen rápidamente de la circulación de los receptores si se someten a periodos de enfriamiento incluso muy cortos, y el efecto de refrigeración que acorta la supervivencia plaquetaria es irreversible (Becker et al., 1973; Berger et al., 1998) .
La necesidad resultante de mantener estas células a temperatura ambiente antes de una transfusión ha impuesto un conjunto único de requisitos logísticos costosos y complejos para el almacenamiento de plaquetas. Debido a que las plaquetas son metabólicamente activas a temperatura ambiente, se requiere una agitación constante en recipientes porosos para permitir la liberación del CO2 desprendido, para evitar las consecuencias tóxicas de la acidosis metabólica. Las condiciones de almacenamiento a temperatura ambiente dan como resultado degradación macromolecular y funciones hemostáticas reducidas de las plaquetas, un conjunto de defectos conocido como "la lesión del almacenamiento" (Chemoff y Sny der, 1992) . Pero el problema principal con el almacenamiento a temperatura ambiente, que conduce a su limitación corta (5 días) , es el mayor riesgo de infección bacteriana. Actualmente, la contaminación bacteriana de los componentes de la sangre es la complicación infecciosa del uso de componentes de la sangre más frecuente, superando con mucho la producida por agentes virales (Engelfriet et al., 2000) . En EE.UU. se dan anualmente 3000-4500 casos de septicemia bacteriana debido a componentes sanguíneos contaminados por bacterias (Yomtovian et al., 1993) .
El mecanismo que subyace a la intolerancia única e irreversible al frío de plaquetas ha sido un misterio, como lo ha sido su significancia fisiológica. Las plaquetas circulantes son discos de superficie lisa que se convierten en formas complejas al reaccionar ante un daño vascular. Alrededor de 40 años atrás, los investigadores observaron que las plaquetas discoidales también cambian de forma a temperaturas de refrigeración (Zucker y Borrelli, 1954) . La prueba subsiguiente de que una forma discoidal era el mejor vaticinador de la viabilidad para plaquetas almacenadas a temperatura ambiente (Schlichter y Harker, 1976) condujo a la conclusión de que el cambio de forma inducido por frío per se era responsable de la eliminación rápida de las plaquetas enfriadas. Presumiblemente, las plaquetas con forma irregular deformadas por enfriamiento quedaban atrapadas en la microcirculación.
Basándose en nuestros estudios que relacionaban la señalización con los mecanismos que conducen a los cambios en la forma de las plaquetas inducidos por ligandos (Hartwig et al., 1995) , predijimos que el enfriamiento, inhibiendo la extrusión de calcio, podría elevar los niveles de calcio hasta un grado consistente con la activación de la proteína gelsolina, que corta los filamentos de actina y recubre los extremos positivos de los filamentos de actina. También argumentamos que una transición de la fase lipídica de membrana a temperaturas bajas agruparía los fosfoinosítidos. El agrupamiento de fosfoinosítidos destapa los extremos positivos de los filamentos de actina (Janmey y Stossel, 1989) para crear sitios de nucleación para el alargamiento de los filamentos. Aportamos pruebas experimentales para ambos mecanismos, documentando la activación de la gelsolina, el destape de los extremos positivos de los filamentos de actina, y el ensamblaje de la actina en plaquetas enfriadas (Hoffmeister et al., 2001; y
Winokur y Hartwig, 1995) . Otros han dado a conocer cambios espectroscópicos en plaquetas enfriadas consistentes con una transición de fase de membrana (Tablin et al., 1996) . Esta información sugirió un método para mantener la forma discoidal de las plaquetas enfriadas, usando un quelante de calcio permeable a las células para inhibir el aumento de calcio y citocalasina B para evitar el ensamblaje de la actina en extremos positivos. Aunque la adición de estos agentes conservó la forma discoidal de las plaquetas a 4º C (Winokur y Hartwig, 1995) , tales plaquetas también se eliminan rápidamente de la circulación, como damos a conocer aquí. Por lo tanto, continúa existiendo el problema de la eliminación rápida de las plaquetas enfriadas, y son necesarios métodos para aumentar el tiempo de circulación así como el tiempo de almacenamiento para plaquetas.
SUMARIO DE LA INVENCIÓN
Se ha descubierto ahora que el enfriamiento de plaquetas humanas causa el agrupamiento de los complejos de la subunidad α (GP1bα) del complejo del receptor del factor von Willebrand (vWf) en la superficie de las plaquetas. El agrupamiento de complejos de GP1bα en la superficie de las plaquetas provoca el reconocimiento por receptores del complemento de macrófagos tipo tres (αMβ2, CR3) in vitro e in vivo. Los receptores CR3 reconocen azúcares enlazados mediante N con βGlcNAc terminales en la superficie de las plaquetas, que han formado complejos GP1bα, y fagocitan las plaquetas, eliminándolas de la circulación y dando como resultado una pérdida concomitante de la función hemostática.
Los solicitantes han descubierto que el tratamiento de plaquetas con una cantidad efectiva de un azúcar nucleotídico, ácido citidin-5'-monofosfo-N-acetilneuramínico (CMP-ácido siálico) , que es un agente modificador de glucano, conduce a la sialilación en GP1bα de los restos de βGlcNAc expuestos. Las cantidades efectivas de un agente modificador de glucano varían de aproximadamente 1 micromolar a aproximadamente 10 milimolares, aproximadamente 1 micromolar a aproximadamente 1 milimolar y, lo más preferentemente, aproximadamente 200 micromolares a aproximadamente 600 micromolares del agente modificador de glucano. Esto tiene el efecto funcional de reducir la eliminación de plaquetas, bloquear la fagocitosis plaquetaria, aumentar el tiempo de circulación de las plaquetas, y aumentar tanto el tiempo de almacenamiento de las plaquetas como la tolerancia a los cambios en la temperatura. Adicionalmente, las plaquetas tomadas de un mamífero se pueden almacenar en frío durante periodos prolongados, es decir, a 4 grados C durante 24 horas, 2 días, 3 días, 5 días, 7 días, 12 días o 20 días o más, sin pérdida significativa de la función hemostática después del trasplante. El almacenamiento en frío proporciona una ventaja que inhibe el crecimiento de microorganismos contaminantes en la preparación... [Seguir leyendo]
Reivindicaciones:
1. Un aparato para procesar una muestra de plaquetas, que comprende: un primer recipiente estéril que tiene uno o más puertos y que contiene una preparación de células sanguíneas que comprende plaquetas, un segundo recipiente estéril que tiene uno o más puertos y que contiene un azúcar nucleosídico que es ácido citidin-5'monofosfo-N-acetilneuramínico, estando adaptado el primer recipiente al segundo recipiente a través de un conducto estéril fijable de forma reversible al puerto del primer recipiente y al puerto del segundo recipiente, comprendiendo además el conducto una válvula, en el que el azúcar nucleosídico presente en el segundo recipiente estéril se introduce en el primer recipiente estéril y las plaquetas en la preparación de células sanguíneas allí se hacen competentes para el almacenamiento en frío después de que las plaquetas se ponen en contacto con el azúcar nucleosídico.
2. El aparato de la reivindicación 1, que comprende además un tercer recipiente estéril que tiene uno o más puertos adaptados al primer recipiente a través de un segundo conducto estéril fijable de forma reversible al puerto del primer recipiente y al puerto del tercer recipiente, comprendiendo además el conducto una válvula.
3. El aparato de la reivindicación 1 ó 2, en el que el conducto comprende además un filtro para leucocitos.
4. El aparato de la reivindicación 1 ó 2, en el que el primer recipiente, el segundo recipiente o el tercer recipiente son bolsas de sangre.
5. El aparato de la reivindicación 1 ó 2, en el que el segundo recipiente es una jeringuilla.
6. El aparato de la reivindicación 1, en el que el conducto está adaptado a un filtro en línea que tiene un diámetro medio de poros suficientemente pequeño para evitar sustancialmente el flujo de bacterias a través del filtro en línea.
7. El aparato de la reivindicación 6, en el que el filtro en línea tiene un diámetro medio de poros menor que alrededor de 0, 50 micrómetros.
8. El aparato de las reivindicaciones 1 ó 2, en el que el puerto del segundo recipiente tiene una barrera frangible.
9. El aparato de la reivindicación 1 ó 2, en el que el primer conducto o el segundo conducto se fija reversiblemente al puerto del primer recipiente, al puerto del segundo recipiente o al puerto del tercer recipiente a través de un alojamiento estéril.
10. Un aparato para procesar una muestra de plaquetas, que comprende: un primer recipiente estéril que contiene un azúcar nucleosídico que es ácido citidin-5'-monofosfo-N-acetilneuramínico y que tiene uno o más puertos, y un conjunto que comprende un conducto y una pluralidad de alojamientos estériles, en el que cada uno de los alojamientos estériles es adaptable de forma reversible a los recipientes de almacenamiento de sangre, teniendo los recipientes de almacenamiento de sangre una muestra de células sanguíneas que comprende plaquetas, y comprendiendo además al menos un puerto para conectar los alojamientos estériles del conjunto, en el que las plaquetas se introducen en el primer recipiente estéril a través del conducto y se hacen competentes para el almacenamiento en frío al poner en contacto las plaquetas con el azúcar nucleosídico presente en el primer recipiente estéril.
11. El aparato de la reivindicación 10, en el que el conjunto comprende además un filtro para leucocitos próximo al primer recipiente.
12. El aparato de la reivindicación 10, en el que el azúcar nucleosídico está contenido en el primer recipiente.
13. El aparato de la reivindicación 10, que comprende además un segundo recipiente que tiene uno o más puertos y que contiene un azúcar nucleosídico que modifica la superficie celular de las plaquetas, el primer recipiente adaptado al segundo recipiente a través de un conducto estéril fijable de forma reversible al puerto del primer recipiente y al puerto del segundo recipiente.
14. El aparato de la reivindicación 13, en el que el segundo recipiente es una jeringuilla.
15. El aparato de la reivindicación 13, en el que el conducto se adapta a un filtro en línea que tiene un diámetro medio de poros suficientemente pequeño para evitar sustancialmente el flujo de bacterias a través del filtro en línea.
16. El aparato de la reivindicación 15, en el que el filtro en línea tiene un diámetro medio de poros menor que alrededor de 0, 50 micrómetros.
17. El aparato de la reivindicación 15, en el que el puerto del segundo recipiente tiene una barrera frangible.
18. Un aparato para procesar una muestra de plaquetas, que comprende: un primer recipiente estéril que tiene uno o más puertos, comprendiendo además el primer recipiente un subrecipiente colocado en él, teniendo el subrrecipiente
un puerto y una barrera frangible y conteniendo un azúcar nucleosídico que es ácido citidin-5'-monofosfo-Nacetilneuramínico, y un conjunto que comprende un conducto y una pluralidad de alojamientos estériles, en el que las plaquetas se introducen en el primer recipiente estéril a través del conducto y se hacen competentes para el almacenamiento en frío después de que las plaquetas se ponen en contacto con el azúcar nucleosídico presente en el primer recipiente.
19. El aparato de la reivindicación 18, en el que el conjunto comprende además un filtro para leucocitos próximo al primer recipiente.
20. Un método para tratar una plaqueta, que comprende obtener un aparato de las reivindicaciones 1, 10 ó 18, obtener una muestra de células sanguíneas, que incluye una subpoblación de plaquetas, y exponer las plaquetas al
azúcar nucleosídico, que es ácido citidin-5'-monofosfo-N-acetilneuramínico, en el aparato, haciendo de ese modo a la subpoblación de plaquetas competentes para el almacenamiento en frío.
21. El método de la reivindicación 20, que comprende además separar los leucocitos de las células sanguíneas antes de exponer las plaquetas al azúcar nucleosídico.
22. El método de la reivindicación 20, en el que las plaquetas se ponen en contacto con el azúcar nucleosídico antes 15 de la infusión de las plaquetas tratadas a un paciente.
23. El método de la reivindicación 20, en el que las plaquetas se ponen en contacto con el azúcar nucleosídico antes del almacenamiento en frío de las plaquetas.
24. El método de la reivindicación 20, en el que las plaquetas se ponen en contacto con el azúcar nucleosídico en el momento de la recogida de la sangre de un donante de sangre.
25. El método de la reivindicación 20, que comprende además separar las células sanguíneas en subpoblaciones de plaquetas, plasma, glóbulos rojos y glóbulos blancos.
26. El método de la reivindicación 25, en el que las plaquetas se ponen en contacto con el azúcar nucleosídico después de que las células de sanguíneas se han separado mediante aféresis.
27. Una plaqueta tratada obtenida mediante el método de la reivindicación 20.
28. La plaqueta tratada de la reivindicación 27, en la que las plaquetas, después del almacenamiento en frío, son adecuadas para la transfusión a un paciente.
Patentes similares o relacionadas:
Uso de un sistema de banco de células de crioconservación cerrado de alta capacidad y procedimiento para descongelar y dispensar células almacenadas, del 22 de Julio de 2020, de Boehringer Ingelheim Animal Health USA Inc: Uso de un sistema de banco de células de crioconservación de fase cerrada y alta capacidad para almacenar grandes volúmenes de células, en el que el uso comprende las siguientes […]
Un dispositivo y método para calentar o enfriar una muestra, del 22 de Julio de 2020, de Cell Therapy Catapult Limited: Un dispositivo para calentar o enfriar una o más muestras, comprendiendo el dispositivo una pluralidad de miembros que pueden funcionar en uso para calentar […]
Sistema y aparato para la auditoría de muestras biológicas en almacenamiento en frío, del 15 de Julio de 2020, de Kustodian Ltd: Un sistema para la auditoría remota en vivo de muestras biológicas mientras están contenidas en una vasija llena de fluido refrigerante , comprendiendo el sistema: […]
APARATO PARA CONTENER Y TRANSPORTAR UN ÓRGANO EX-VIVO CONECTADO A UNA MÁQUINA DE PERFUSIÓN, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: Aparato para contener y transportar un órgano ex-vivo conectado a una máquina de perfusión por medio de al menos dos conductos de perfusión (A), que permite poner o sacar […]
Procedimiento de conservación de células, tejidos u órganos en hipotermia, del 24 de Junio de 2020, de Etablissement Français du Sang: Procedimiento in vitro o ex vivo de conservación de las células animales, preferiblemente de células humanas, en hipotermia intensa, que comprende una etapa que consiste en […]
Kit para acondicionamiento y purificación ex-vivo de un órgano explantado, del 17 de Junio de 2020, de Aferetica S.r.l: Un kit para acondicionamiento y purificación ex vivo de un órgano explantado, comprendiendo: - medios de conexión a y de dicho órgano ; […]
Sistemas de conservación y procesamiento de espermatozoides, del 17 de Junio de 2020, de XY, LLC: Un procedimiento para producir una muestra de esperma de mamífero no humano adecuada para la fertilización in vitro, que incluye la etapa de: […]
Sorbente polimérico para la eliminación de impurezas de sangre completa y productos sanguíneos, del 17 de Junio de 2020, de Cytosorbents Corporation: Un método para tratar la sangre y los productos sanguíneos almacenados que maximiza la vida útil y/o minimiza una complicación relacionada con la transfusión […]