Oligonucleótidos para su uso en la modulación de lipoproteínas y en los niveles de colesterol en humanos.
Un oligonucleótido que consiste en la secuencia de base con ID DE SECUENCIA Nº:
2, donde el oligonucleótido es un oligonucleótido quimérico de 20 nucleótidos de longitud compuesto de una región de hueco central que consiste en diez 2'-desoxinucleótidos flanqueados por los dos lados por cinco alas de nucleótidos compuestos por nucleótidos de 2'-metoxietilo (2'MOE), donde los enlaces de internucleósido son fosforotioato a lo largo del oligonucleótido y todos los residuos de citidina son 5-metilcitidinas, para su uso en el tratamiento de un humano que padece, o tiene un riesgo elevado de padecer hipercolesterolemia, donde:
(a) dicho oligonucleótido se administra durante un período de carga y un período de mantenimiento, o se administra durante un período de mantenimiento, sin un período de carga precedente;
(b) una dosis de 200 mg de dicho oligonucleótido se administra una vez por semana durante el período de mantenimiento; y
(c) dicha dosis de 200 mg se administra por inyección subcutánea.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E11171206.
Solicitante: GENZYME CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 500 KENDALL STREET CAMBRIDGE, MA 02142 ESTADOS UNIDOS DE AMERICA.
Inventor/es: GEARY,Richard S, CROOKE,Rosanne,M, YU,ZHENGRONG.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K48/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen material genético que se introduce en las células del cuerpo vivo para tratar enfermedades genéticas; Terapia génica.
- A61P3/06 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 3/00 Medicamentos para el tratamiento de trastornos del metabolismo (de la sangre o de fluido extracelular A61P 7/00). › Antihiperlipidémicos.
- C12N15/11 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Fragmentos de ADN o de ARN; sus formas modificadas (ADN o ARN no empleado en tecnología de recombinación C07H 21/00).
PDF original: ES-2550824_T3.pdf
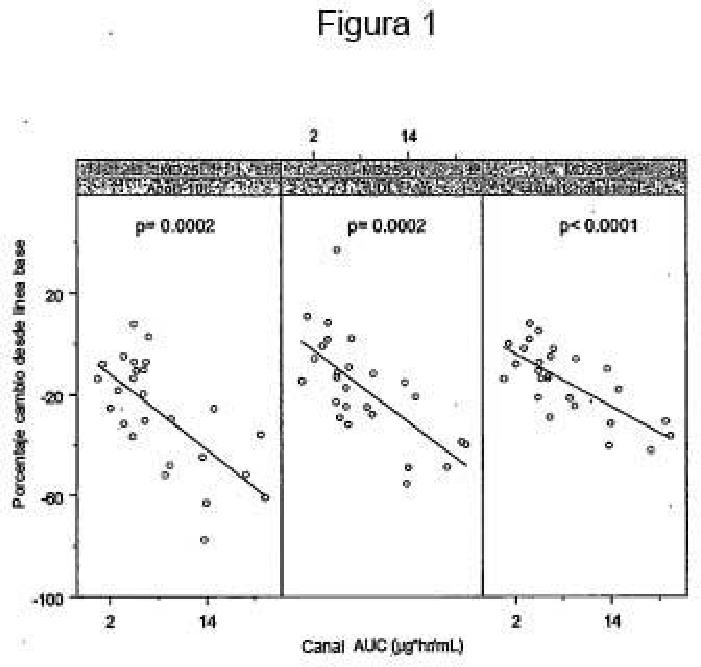
Fragmento de la descripción:
Oligonucleótidos para su uso en la modulación de lipoproteínas y en los niveles de colesterol en humanos.
CONTEXTO DEL INVENTO
Ámbito del Invento 10
El presente invento trata del oligonucleótido del ID DE SEC. Nº:2 para su uso en el tratamiento de hipercolesterolemia de acuerdo con las reivindicaciones. En este documento se presentan compuestos y métodos para reducir el colesterol LDL y el tratamiento de afecciones asociadas con niveles de colesterol elevados. Más específicamente, se presentan compuestos y métodos para inhibir la expresión de apolipoproteína B en el hígado.
Descripción de las técnicas relacionadas
La cardiopatía coronaria (CHD, por sus siglas en inglés) ha sido la causa principal de muertes en los Estados Unidos durante un siglo y las causas de muertes más habituales en las sociedades occidentales son complicaciones derivadas de la ateroesclerosis (Knopp, New Engl. J. Medicine, 1999, 341, 498-511; Davis y Hui, 20 Arterioscler. Thromb. Vasc. Biol., 2001, 21, 887-898; Bonow, Circulation, 2002, 106, 3140-3141) . Un nivel alto de colesterol de lipoproteína de baja densidad (colesterol LDL) está ampliamente reconocido como factor de riesgo de CHD. De todas formas, a pesar de la intervención farmacológica, muchos individuos no consiguen reducir los niveles de colesterol LDL.
Las directrices para la terapia de reducción de lípidos las estableció el Panel de Tratamiento de Adultos III del Programa Nacional de Educación sobre el Colesterol (NCEP, por sus siglas en inglés) en 2001. El Comité Coordinador del NCEP recomendó modificaciones a estas directrices en 2004 e incluyó objetivos de tratamientos más agresivos (Grundy et al., Circulation, 2004, 110, 227-239) . Estas directrices definen 3 categorías de riesgo de accidentes coronarios graves y proporcionan unos objetivos de niveles aceptables de colesterol LDL. Los que tienen 30 un riesgo mayor son los pacientes con riesgo de CHD o equivalentes a CHD y deberían mantener el colesterol LDL por debajo de 100 mg/dL. Las directrices de NCEP más recientes recomiendan que los pacientes con alto riesgo de CHD usen terapia con medicamentos para conseguir niveles de colesterol LDL de menos de 70 mg/dL. El CHD equivalente se define como sujetos con diabetes, enfermedad vascular periférica, aneurisma aórtico abdominal, enfermedad de las arterias carótidas sintomáticas y los que tienen factores de riesgo múltiples que confieren un 35 riesgo para 10 años de CHD de más del 20 %. Para la segunda categoría, los pacientes que tienen riesgo moderadamente alto para CHD con factores de riesgo múltiples (2 o más) en los cuales el riesgo para 10 años de CHD del 20 %, el objetivo es un colesterol LDL de menos de 130 mg/dL. Las recomendaciones más recientes incluyen una opción terapéutica para reducir los niveles de colesterol LDL a menos de 100 mg/dL en la categoría de riesgo moderadamente alto. La tercera categoría incluye individuos con 0-1 factores de riesgo y el colesterol LDL 40 objetivo es de menos de 160mg/dL. Los factores de riesgo incluyen la edad, fumar, hipertensión, colesterol HDL bajo e historial familiar de CHD. La terapia con medicamentos debería iniciarse cuando el colesterol LDL en suero se mantenga por encima de 130, 160 y 190 mg/dL en los 3 grupos de riesgo, respectivamente, independientemente de cambios en los hábitos terapéuticos (Grundy et al., Circulation, 2004, 110, 227-239) .
Las lipoproteínas de baja densidad son una de las cinco grandes clases de lipoproteínas, que incluyen las siguientes: quilomicrones, responsables del transporte de lípidos de la dieta del intestino a los tejidos; lipoproteínas de muy baja densidad (VLDL) ; lipoproteínas de densidad intermedia (IDL) ; lipoproteínas de baja densidad (LDL) ; todas ellas transportan triacilgliceroles y colesterol desde el hígado a los tejidos; y lipoproteínas de alta densidad (HDL) , que transportan colesterol endógeno a partir de tejidos al hígado. Las partículas de las lipoproteínas pasan 50 por un procesamiento metabólico continuo y tienen propiedades y composiciones variadas. Los componentes de proteína de las lipoproteínas son conocidos como apolipoproteínas. Por lo menos nueve apolipoproteínas, una de las cuales es la apolipoproteína B, se distribuyen en cantidades significativas entre las diversas lipoproteínas humanas.
La apolipoproteína B (también conocida como ApoB, apolipoproteína B-100; ApoB-100, apolipoproteína B-55 48; ApoB-48 y antígeno Ag (x) ) , es una gran glicoproteína implicada en el ensamblaje y secreción de lípidos y en el transporte y absorción mediada por receptores y la administración de distintas clases de lipoproteínas. La apolipoproteína B lleva a cabo varias funciones, incluida la absorción y procesamiento de lípidos de la dieta, así como la regulación de los niveles de lipoproteína circulante (Davidson and Shelness, Annu. Rev. Nutr., 2000, 20, 169-193) . 60
En los mamíferos existen dos formas de apolipoproteína B. ApoB-100 representa la proteína de largo completo que contiene 4536 residuos de aminoácidos, sintetizados primariamente en el hígado humano (Davidson y Shelness, Annu. Rev. Nutr., 2000, 20, 169-193) . Una forma truncada conocida como apoB-48 es colineal con los residuos de amino terminal 2152 y se sintetiza en el intestino delgado de todos los mamíferos (Davidson y Shelness, 65 Annu. Rev. Nutr., 2000, 20, 169-193) . En humanos, apoB-48 circula en asociación con quilomicrones y restos y esas partículas se despejan por un receptor independiente conocido como proteína relacionada con receptor de LDL (Davidson y Shelness, Annu. Rev. Nutr., 2000, 20, 169-193) . ApoB-48 puede entenderse como una adaptación en la que el lípido de la dieta se suministra a partir del intestino delgado al hígado, mientras que apoB-100 participa en el transporte y suministro de colesterol (Davidson y Shelness, Annu. Rev. Nutr., 2000, 20, 169-193) . ApoB-100 es el principal componente proteico del LDL y contiene el dominio necesario para la interacción de esta especie de 5 lipoproteína con el receptor de LDL. Además, apoB-100 contiene un residuo de cisteína no apareado que media una interacción con apolipoproteína (a) y genera lipoproteína (a) o Lp (a) , otra lipoproteína independiente con potencial aterogénico (Davidson y Shelness, Annu. Rev. Nutr., 2000, 20, 169-193) . Los niveles elevados de plasma de apoB-100 que contenga lipoproteína Lp (a) se asocian con un alto riesgo de ateroesclerosis y sus manifestaciones, que podrían incluir hipercolesterolemia (Seed et al., N. Engl. J. Med., 1990, 322, 1494-1499) , infarto de miocardio 10 (Sandkamp et al., Clin. Chem., 1990, 36, 20-23) y trombosis (Nowak-Gottl et al., Pediatrics, 1997, 99, E11) .
La apolipoproteína B implica homeostasis de colesterol y su sobreproducción se ha asociado con varias enfermedades, incluida la hipercolesterolemia familiar, apoB-100 defectuoso familiar e hipercolesterolemia familiar combinada (Kane y Havel, The Metabolic and Molecular Bases of Inherited Diseases [Bases metabólica y molecular 15 de enfermedades hereditarias], 2001, 8ª edición, 2717-2751) . También se observan perturbaciones del metabolismo de apoB-100 que se corresponden con un alto riesgo de CHD en diabetes y obesidad (Grundy, Am. J. Cardiol., 1998, 81, 18B-25B; Chan et al., Diabetes, 2002, 51, 2377-2386; Chan et al., Metabolism, 2002, 51, 1041-1046) . Además, se ha demostrado por medio de estudios genéticos en modelos de ratón que existe una correlación entre la apolipoproteína B elevada, niveles elevados de colesterol y ateroesclerosis (Kim y Young, J. Lipid Res., 1998, 39, 20 703-723; Nishina et al., J. Lipid Res., 1990, 31, 859-869) .
En estudios de pacientes con hipobetalipoproteínaemia familiar (FHBL) , estos pacientes mostraron una reducción de los niveles de apolipoproteína B en suero, niveles reducidos de colesterol LDL en suero y una reducción de la incidencia de enfermedad de la arteria coronaria (Schonfeld et al., J. Lipid Res., 2003, 44, 878-883) . 25 Los estudios en murinos han demostrado que los ratones que tienen deficiencias heterocigóticas en la apolipoproteína B muestran una reducción del colesterol LDL en suero y de la apolipoproteína B y, además, están protegidos contra la hipercolesterolemia inducida por la dieta. (Farese et al., Proc. Natl. Acad. Sci. U. S. A., 1995, 92, 1774-1778) .
WO 2004/044181, WO 03/097662 y WO 03/011887 presentan oligonucleótidos antisentido dirigidos a la apolipoproteína B.
RESUMEN DEL INVENTO
El presente invento proporciona un oligonucleótido que consiste en la secuencia de la base del núcleo del ID de la SEC. Nº:2, donde el oligonucleótido es un oligonucleótido quimérico de 20 nucleótidos de longitud compuesto por una región de hueco central... [Seguir leyendo]
Reivindicaciones:
1. Un oligonucleótido que consiste en la secuencia de base con ID DE SECUENCIA Nº:2, donde el oligonucleótido es un oligonucleótido quimérico de 20 nucleótidos de longitud compuesto de una región de hueco central que 5 consiste en die.
2. desoxinucleótidos flanqueados por los dos lados por cinco alas de nucleótidos compuestos por nucleótidos d.
2. metoxietilo (2MOE) , donde los enlaces de internucleósido son fosforotioato a lo largo del oligonucleótido y todos los residuos de citidina son 5-metilcitidinas, para su uso en el tratamiento de un humano que padece, o tiene un riesgo elevado de padecer hipercolesterolemia, donde:
(a) dicho oligonucleótido se administra durante un período de carga y un período de mantenimiento, o se administra durante un período de mantenimiento, sin un período de carga precedente;
(b) una dosis de 200 mg de dicho oligonucleótido se administra una vez por semana durante el período de mantenimiento; y
(c) dicha dosis de 200 mg se administra por inyección subcutánea. 15
2. El oligonucleótido para su uso de acuerdo con la reivindicación 1, donde el período de carga dura 3, 4, 5, 6, 7, 8, 9 o 10 días, y donde una única administración o múltiples administraciones se realizan todos los días, cada 2 días, cada 3 días, cada 4 días, cada 5 días, cada 6 días o todas las semanas.
3. El oligonucleótido para su uso de acuerdo con la reivindicación 1, donde el período de carga dura 11, 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34 o 35 días, y se hace una única administración todos los días, cada 2 días, cada 3 días, cada 4 días, cada 5 días, cada 6 días o cada 7 días.
4. El oligonucleótido para su uso de acuerdo con cualquiera de las reivindicaciones 1-3, donde las dosis 25 administradas durante el período de mantenimiento son iguales a las dosis administradas durante el período de carga.
5. El oligonucleótido para su uso de acuerdo con cualquiera de las reivindicaciones 1-3, donde las dosis administradas durante el período de mantenimiento son más bajas que las dosis administradas durante el 30 período de carga.
6. El oligonucleótido para su uso de acuerdo con cualquiera de las reivindicaciones 1-3, donde las dosis administradas durante el período de mantenimiento son menos frecuentes que la dosis administrada durante el período de carga. 35
7. El oligonucleótido para su uso de acuerdo con cualquiera de las reivindicaciones 1-6, donde dicho humano muestra por lo menos una indicación seleccionada a partir del grupo que consta de: nivel alto de colesterol total en suero, nivel alto de Colesterol LDL en suero, proporción alta de colesterol total:HDL y proporción alta de LDL:HDL. 40
8. El oligonucleótido para su uso de acuerdo con cualquiera de las reivindicaciones 1-6, donde dicho humano ha padecido o padece hipercolesterolemia homocigótica familiar o heterocigótica familiar.
9. El oligonucleótido para su uso de acuerdo con cualquiera de las reivindicaciones 1-6, donde dicho humano ha 45 padecido, padece o tiene un alto riesgo de hipercolesterolemia no familiar.
10. El oligonucleótido para su uso de acuerdo con cualquiera de las reivindicaciones 1-6, donde dicho humano tiene niveles de Colesterol LDL en suero por encima de aproximadamente 70 mg/dL, por encima de aproximadamente 100 mg/dL o por encima de aproximadamente 130 mg/dL, antes de la administración de dicho oligonucleótido. 50
Patentes similares o relacionadas:
Composiciones útiles en el tratamiento de la deficiencia de ornitina transcarbamilasa (OTC), del 8 de Julio de 2020, de THE TRUSTEES OF THE UNIVERSITY OF PENNSYLVANIA: Un vector vírico recombinante que comprende una secuencia de ácido nucleico que codifica la proteína ornitina transcarbamilasa humana (hOTC) y secuencias […]
Terapia génica para la diabetes, del 8 de Julio de 2020, de UCL Business Ltd: Una molécula de ácido nucleico que comprende una secuencia de nucleótidos que codifica una proteína preproinsulina funcional en donde la secuencia de nucleótidos tiene al menos […]
Vacuna de ADN que contiene un epítopo específico de VEGF y/o un epítopo específico de angiopoyetina-2, del 1 de Julio de 2020, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno del núcleo del virus de la hepatitis B quimérico con una inserción para uso en el tratamiento o la profilaxis […]
Ácido nucleico antisentido, del 24 de Junio de 2020, de NIPPON SHINYAKU CO., LTD.: Un oligómero antisentido de 14 a 32 bases de longitud, que comprende dos unidades de oligómeros conectadas seleccionadas del grupo que consiste […]
Composiciones para modular la expresión de SOD-1, del 24 de Junio de 2020, de Biogen MA Inc: Un compuesto antisentido según la siguiente fórmula: mCes Aeo Ges Geo Aes Tds Ads mCds Ads Tds Tds Tds mCds Tds Ads mCeo Aes Geo mCes Te (secuencia […]
Plekhg5 como diana farmacéutica para trastornos neurológicos, del 15 de Junio de 2020, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): Plekhg5 como diana farmacéutica para trastornos neurológicos. La invención hace referencia al uso del gen Plekhg5 como diana farmacológica para el cribado, […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Método para activar células T auxiliares, del 10 de Junio de 2020, de OTSUKA PHARMACEUTICAL CO., LTD.: Una composición para su uso en el tratamiento o prevención del cáncer mediante la activación de células T auxiliares en un sujeto, en donde dicha composición […]