7-Hidroxicumarinas sustituidas con heterociclo reactivas y sus conjugados.
Un compuesto que tiene la estructura de fórmula 3:**Fórmula**
en la que
X es O o S;
R1, R2, R3 y R4 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino, hidroxilo, sulfonilo, fosfonilo o ácido borónico; o alquilo o alcoxilo que están sustituidos opcionalmente a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo o ácido borónico;
R10, R11 y R12 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino, hidroxilo, sulfonilo, fosfonilo, ácido borónico L-RG o WSG; o alquilo o alcoxilo que están sustituidos opcionalmente a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo, ácido borónico, L-RG o WSG; RG es un grupo químicamente reactivo que es acrilamida, amina, ácido carboxílico, éster activado de ácido carboxílico, acilazida, acilnitrilo, aldehído, haluro de alquilo, anhídrido, haluro de arilo, azida, aziridina, boronato, diazoalcano, halogenoacetamida, halogenotriazina, hidrazina, hidroxilamina, imidoéster, isotiocianato, maleimida, complejo de platino reactivo, haluro de sulfonilo o derivado de psoraleno;
L es un ligador opcional que es nulo, alquilo, alcoxilo, tioalquilo, aminoácido, sulfoaminoácido, poliamina, polietilenglicol, arilo o heteroarilo;
WSG es un grupo hidrosoluble que es sulfonato, tiosulfato, fosfonato, boronato, amonio, piridio, quinolio o acridio;
al menos uno de R10, R11 y R12 contiene L-RG; y
al menos uno de R10, R11 y R12 es WSG.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E10158457.
Solicitante: BECTON, DICKINSON AND COMPANY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: ONE BECTON DRIVE FRANKLIN LAKES, NJ 07417 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DIWU,ZHENJUN, DUBROVSKY,TIMOTHY, ABRAMS,BARNABY, LIAO,JINFANG, MENG,QINGLIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K49/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones para examen in vivo.
- C07D405/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 405/00 Compuestos heterocíclicos que contienen a la vez uno o más heterociclos que tienen átomos de oxígeno como únicos heteroátomos del ciclo y uno o más heterociclos que tienen átomos de nitrógeno como único heteroátomo del ciclo. › unidos directamente por un enlace entre dos miembros cíclicos.
- C07D405/14 C07D 405/00 […] › que contienen tres o más heterociclos.
- C07D409/04 C07D […] › C07D 409/00 Compuestos heterocíclicos que contienen dos o más heterociclos, teniendo al menos un ciclo átomos de azufre como únicos heteroátomos del ciclo. › unidos directamente por un enlace entre dos miembros cíclicos.
- C07D409/14 C07D 409/00 […] › que contienen tres o más heterociclos.
- C07D417/04 C07D […] › C07D 417/00 Compuestos heterocíclicos que contienen dos o más heterociclos, teniendo al menos un ciclo átomos de nitrógeno y azufre como únicos heteroátomos del ciclo, no previstos por el C07D 415/00. › unidos directamente por un enlace entre dos miembros cíclicos.
- C07D417/14 C07D 417/00 […] › que contiene tres o más heterociclos.
PDF original: ES-2548380_T3.pdf


Fragmento de la descripción:
7. Hidroxicumarinas sustituidas con heterociclo reactivas y sus conjugados Antecedentes de la invención Campo de la invención La invención se refiere a productos químicos fluorescentes, incluyendo tintes reactivos, a conjugados de tinte y a sus usos.
Descripción de la técnica relacionada Las sondas fluorescentes específicas de analito son reactivos útiles para el análisis de analitos en una muestra. Los analitos se marcan mediante unión específica a las sondas, y el marcaje facilita la detección del analito. Las aplicaciones de sondas fluorescentes para el análisis de analitos en una muestra incluyen inmunoensayos de fluorescencia, incluyendo la identificación y/o separación de subpoblaciones de células en una mezcla de células por citometría de flujo, microscopía de fluorescencia y visualización de analitos separados en gel por tinción de fluorescencia. Estas técnicas se describen por Herzenberg et al., “CELLULAR IMMUNOLOGY" 3ª ed., capítulo 22; Blackwell Scientific Publications (1978) ; por Goldman, "FLUORESCENCE ANTIBODY METHODS" Academic Press, Nueva York, (1968) y por Taylor et aI., “APPLICATIONS OF FLUORESCENCE IN THE BIOMEDICAL SCIENCES”, Alan Liss Inc., (1986) .
Cuando se emplean tintes fluorescentes con los fines anteriores, hay muchas consideraciones que afectan a la elección del tinte fluorescente. Una consideración es las características de absorción y emisión del tinte fluorescente, puesto que muchos ligandos, receptores y materiales de la muestra bajo ensayo, p.ej. sangre, orina y líquido cerebroespinal, tendrán fluorescencia e interferirán con una determinación exacta de la fluorescencia del marcador fluorescente. Este fenómeno se llama autofluorescencia o fluorescencia de fondo. Una segunda consideración es la capacidad de conjugar el tinte fluorescente con ligandos, receptores y otros materiales biológicos y no biológicos, y el efecto de dicha conjugación sobre el tinte fluorescente. En muchas situaciones, la conjugación con otra molécula puede dar como resultado un cambio sustancial en las características fluorescentes del tinte fluorescente y, en algunos casos, destruir sustancialmente o reducir la eficacia cuántica del tinte fluorescente. También es posible que la conjugación con el tinte fluorescente inactive la función de la molécula que está marcada. Una tercera consideración es la eficacia cuántica del tinte fluorescente, que es preferiblemente alta para una detección sensible. Una cuarta consideración es la capacidad de absorción de luz, o coeficiente de extinción, de los tintes fluorescentes, que es preferiblemente lo mayor posible. Una consideración adicional es si las moléculas fluorescentes interaccionarán entre sí cuando estén en estrecha proximidad, dando como resultado un autoapagamiento. Otra consideración es si hay unión no específica del tinte fluorescente a otros compuestos o las paredes del envase, por sí mismos o junto con el compuesto con el que está conjugado el tinte fluorescente.
La aplicabilidad y valor de los métodos indicados anteriormente están estrechamente ligados a la disponibilidad de compuestos fluorescentes adecuados. En particular, existe la necesidad de sustancias fluorescentes que puedan excitarse por fuentes de láser viables comerciales tales como láser violeta (405 nm) , láser de argón (488 nm) y láser de He-Ne (633 nm) . Hay muchos tintes fluorescentes desarrollados para láser de argón (excitación a 488 nm) y láser de He-Ne (excitación a 633 nm) . Por ejemplo, la fluoresceína, que se excita bien por el láser de argón a 488 nm, es un emisor útil en la región verde. Sin embargo, hay pocos tintes fluorescentes disponibles para el láser violeta a 405 nm.
Ciertos tintes de cumarina han demostrado utilidad para una variedad de aplicaciones de detección biológica. Véanse, por ejemplo, la patente de EE.UU. nº 6.207.404 de Miller et al.; la patente de EE.UU. nº 5.830.912 de Gee et al. y la patente de EE.UU. nº 4.956.480 de Robinson. En comparación con otros tintes fluorescentes tales como fluoresceínas, rodaminas y cianinas, muchos tintes de cumarina tienen ciertas propiedades ventajosas. El menor tamaño de los tintes de cumarina minimiza el efecto del tinte sobre la afinidad y especificidad de un reactivo específico de antígeno marcado con tinte. Además, las cumarinas menores tienen mayor eficacia de marcaje que fluoresceínas, rodaminas y cianinas. No obstante, muchos tintes de cumarina son conocidos por compartir ciertas desventajas, tales como un fuerte apagamiento de la fluorescencia de los tintes de hidroxicumarina conjugados con proteínas, debido a su fuerte hidrofobicidad y alto pKa. El apagamiento de fluorescencia de la cumarina es el resultado del autoapagamiento (distancia estrecha entre marcajes de cumarina) y/o por el apagamiento por residuos aminoacídicos ricos en electrones (tales como histidina triptófano y tirosina, etc.) . Además, la absorción típicamente débil a 405 nm de las cumarinas limita seriamente sus aplicaciones para analizar células usando un láser de excitación violeta, tal como el usado en algunos citómetros de flujo.
Se han usado cumarinas cloradas para marcar moléculas orgánicas pequeñas (p.ej., Zlokarnik et al., 1998, Science 279: 84 y patente de EE.UU. nº 5.955.604) . Para marcar moléculas orgánicas pequeñas, ni el autoapagamiento ni el apagamiento por el sustrato son un problema grave, porque solo está presente una sola molécula de cumarina en cada conjugado. En contraposición, para marcar anticuerpos, tanto el autoapagamiento como el apagamiento por el sustrato son un problema significativo, porque es deseable conjugar múltiples moléculas de tinte con cada anticuerpo. Se considera generalmente que la cloración de cumarinas o fluoresceínas daría como resultado un 2 10
marcaje inferior de los anticuerpos debido al denominado “efecto del átomo pesado” y la hidrofobicidad aumentada (patente de EE.UU. nº 5.516.629 de Park et al.; patente de EE.UU. nº 5830912 de Gee et al.; patente de EE.UU. nº
6.472.205 de Tsien y Zlokarnik; Haugland, “Handbook of Fluorescent Probes and Research Chemicals, Molecular Probes”, 9ª ed., pág. 7-74, 2002) .
La solicitud de patente de EE.UU. en tramitación junto con la presente de nº de serie 12/220.939, presentada el 29/07/2008 (publicada como US 2010-0029017) , describe anticuerpos conjugados con una pluralidad de tintes de 7hidroxicumarina monoclorada y su uso en ensayos biológicos. Estos tintes de hidroxicumarina monoclorada exhiben inesperadamente un autoapagamiento reducido cuando se usan como marcadores de anticuerpo con múltiples tintes por anticuerpo. Estos anticuerpos marcados con tinte exhiben típicamente máximos de absorbancia cercanos a 405 nm y exhiben una emisión máxima en el azul.
El documento US 5.830.912 da a conocer 6, 8-difluoro-7-hidroxicumarinas y derivados de 6, 8-difluoro-7hidroxicumarinas, incluyendo tintes reactivos, conjugados de tinte y sustratos enzimáticos. Estos tintes fluorescentes sustituidos con flúor poseen típicamente mayor fotoestabilidad y menor sensibilidad al pH en el intervalo de pH fisiológico que sus análogos no fluorados, exhiben menos apagamiento de fluorescencia cuando se conjugan con una sustancia, poseen espectros de absorción y emisión que coinciden estrechamente con los de sus análogos no fluorados y exhiben también mayores rendimientos cuánticos que sus análogos no fluorados.
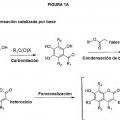
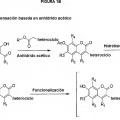
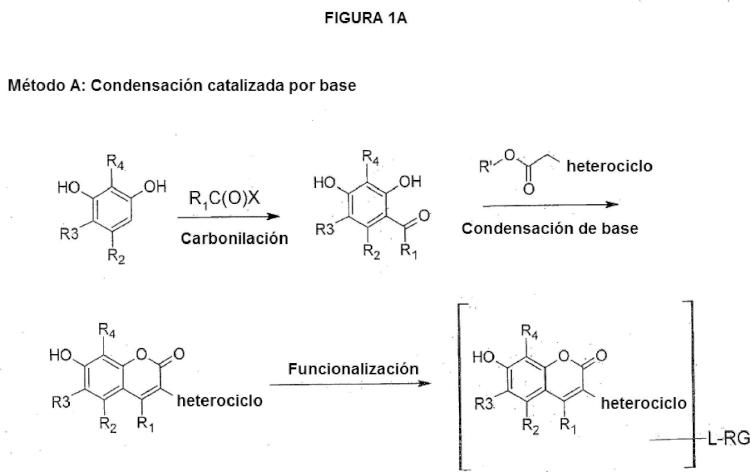
Sumario de la invención La presente invención proporciona tintes de 7-hidroxicumarina sustituida con heterociclo hidrosolubles y derivados de tintes de 7-hidroxicumarina sustituida con heterociclo hidrosolubles, incluyendo tintes reactivos y conjugados de tinte.
Los tintes de 7-hidroxicumarina sustituida con heterociclo hidrosolubles de la presente invención exhiben combinaciones novedosas de propiedades que hacen a estos tintes fluorescentes particularmente adecuados para uso en ensayos biológicos, incluyendo para uso como marcadores de biopolímeros. Se ha descubierto que la sustitución con heterociclo y la adición de grupos hidrosolubles a 7-hidroxicumarinas da como resultado inesperadamente una nueva clase de cumarinas fluorescentes útiles en ensayos biológicos y para preparar conjugados biológicos que tienen una fuerte absorción de 405 nm y son altamente fluorescentes. Además, la halogenación de 7-hidroxicumarinas sustituidas con heterociclo reduce significativamente el pKa de los tintes de cumarina, de modo que los conjugados de cumarina resultantes tienen su fluorescencia máxima en el intervalo de pH fisiológico. Estos tintes de 7-hidroxicumarina sustituida con heterociclo son fuertemente fluorescentes, y la intensidad de fluorescencia potenciada de los conjugados de tinte de 7-hidroxicumarina sustituida... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto que tiene la estructura de fórmula 3:
en la que X es O o S;
R1, R2, R3 y R4 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino, hidroxilo, sulfonilo, fosfonilo o ácido borónico; o alquilo o alcoxilo que están sustituidos opcionalmente a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo o ácido borónico;
R10, R11 y R12 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino, hidroxilo, sulfonilo, fosfonilo, ácido borónico L-RG o WSG; o alquilo o alcoxilo que están sustituidos opcionalmente a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo, ácido borónico, L-RG o WSG;
RG es un grupo químicamente reactivo que es acrilamida, amina, ácido carboxílico, éster activado de ácido carboxílico, acilazida, acilnitrilo, aldehído, haluro de alquilo, anhídrido, haluro de arilo, azida, aziridina, boronato, diazoalcano, halogenoacetamida, halogenotriazina, hidrazina, hidroxilamina, imidoéster, isotiocianato, maleimida, complejo de platino reactivo, haluro de sulfonilo o derivado de psoraleno;
L es un ligador opcional que es nulo, alquilo, alcoxilo, tioalquilo, aminoácido, sulfoaminoácido, poliamina, polietilenglicol, arilo o heteroarilo;
WSG es un grupo hidrosoluble que es sulfonato, tiosulfato, fosfonato, boronato, amonio, piridio, quinolio o acridio;
al menos uno de R10, R11 y R12 contiene L-RG; y
al menos uno de R10, R11 y R12 es WSG.
2. El compuesto de la reivindicación 1, que tiene la estructura de fórmula 4:
en la que X es O o S; R1, R2, R3 y R4 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino,
hidroxilo, sulfonilo, fosfonilo o ácido borónico; o alquilo o alcoxilo que están sustituidos opcionalmente a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo o ácido borónico; R10, y R11 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino, hidroxilo, sulfonilo, fosfonilo, ácido borónico L-RG o WSG; o alquilo o alcoxilo que están sustituidos opcionalmente a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo, ácido borónico, L-RG o WSG;
RG es un grupo químicamente reactivo como se define en la reivindicación 1; L es un ligador opcional como se define en la reivindicación 1; WSG es un grupo hidrosoluble como se define en la reivindicación 1; al menos uno de R10 y R11 contiene L-RG;
al menos uno de R10 y R11 es WSG; y al menos uno de R10 y R11 contiene un sulfonato.
3. El compuesto de la reivindicación 1, que tiene la estructura de fórmula 5:
en la que X es O o S; R1, R2, R3 y R4 son independientemente hidrógeno, cloro o fluoro; R10 y R11 son independientemente hidrógeno, cloro, fluoro o sulfonato; RG es un grupo químico reactivo como se define en la reivindicación 1;
L es un ligador opcional como se define en la reivindicación 1, y en la que al menos uno de R10 y R11 es un sulfonato.
4. El compuesto de la reivindicación 3, en el que RG es un éster activado de ácido carboxílico, acilazida, acilnitrilo, aldehído, haluro de alquilo, anhídrido, haluro de arilo, azida, aziridina, halogenoacetamida, halogenotriazina, amina, hidrazina, hidroxilamina, imidoéster, isotiocianato o maleimida.
5. El compuesto de cualquiera de las reivindicaciones 3 o 4, en el que L es nulo, alquilo, alcoxilo, tioalquilo, aminoácido, sulfonaminoácido, poliamina o polietilenglicol que tiene 3-20 átomos de carbono.
6. El compuesto de la reivindicación 1, que tiene la estructura de fórmula 6:
en la que 20 R1, R2, R3 y R4 son independientemente hidrogeno, cloro o fluoro;
R10 y R11 son independientemente hidrógeno, cloro, fluoro o sulfonato;
RG es un grupo químico reactivo como se define en la reivindicación 1;
L es un ligador opcional que es nulo, alquilo, alcoxilo, tioalquilo, aminoácido, sulfoaminoácido, poliamina,
polietilenglicol, arilo, arilalquilo o heteroarilo, y 25 en la que al menos uno de R10 y R11 es un sulfonato.
7. El compuesto de la reivindicación 6, en el que RG es un éster activado de ácido carboxílico, acilazida, acilnitrilo, aldehído, haluro de alquilo, anhídrido, haluro de arilo, azida, aziridina, halogenoacetamida, halogenotriazina, amina, hidrazina, hidroxilamina, imidoéster, isotiocianato o maleimida.
8. El compuesto de la reivindicación 1, que tiene la estructura de fórmula 7:
en la que R3 y R4 son independientemente hidrógeno, cloro o fluoro; R10 y R11 son independientemente hidrógeno, cloro, fluoro o sulfonato; n es un entero de 1 a 10; y en la que al menos uno de R10 y R11 es un sulfonato.
9. Un conjugado de tinte que tiene la estructura de fórmula 11:
en la que X es O o S; R1, R2, R3 y R4 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, azido, amino, hidroxilo,
sulfonilo, fosfonilo o ácido borónico; o alquilo o alcoxilo que están opcionalmente sustituidos a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo o ácido borónico;
R10, R11 y R12 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino, hidroxilo, sulfonilo, fosfonilo, ácido borónico o WSG; o alquilo o alcoxilo que están opcionalmente sustituidos a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo, ácido borónico o WSG;
WSG es un grupo hidrosoluble que es un sulfonato, tiosulfato, fosfonato, boronato, amonio, piridio, quinolio o acridio; n es un entero de 1 a 35; 20 SUB es un sustrato que es un biopolímero o un anticuerpo;
al menos uno de R10, R11 y R12 está unido covalentemente a SUB a través de un ligador opcional L, en el que L es nulo, alquilo, alcoxilo, tioalquilo, aminoácido, sulfoaminoácido, poliamina, polietilenglicol, arilo o heteroarilo; y al menos uno de R10, R11 y R12 es WSG.
10. El conjugado de tinte de la reivindicación 9, que tiene la estructura de fórmula 12:
en la que X es O o S; 5 R1, R2, R3 y R4 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino,
hidroxilo, sulfonilo, fosfonilo o ácido borónico; o alquilo o alcoxilo que están opcionalmente sustituidos a su vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo o ácido borónico; R10 y R11 son independientemente H, halógeno, alquilo, alcoxilo, ariloxilo, tiol, alquiltiol, ariltiol, azido, amino,
hidroxilo, sulfonilo, fosfonilo, ácido borónico o WSG; o alquilo o alcoxilo que están opcionalmente sustituidos a su 10 vez una o más veces con halógeno, amino, hidroxilo, sulfonilo, fosfonilo, carbonilo, ácido borónico o WSG;
WSG es un grupo hidrosoluble como se define en la reivindicación 9;
n es un entero de 1 a 35;
SUB es un sustrato como se define en la reivindicación 9;
al menos uno de R10 y R11 está unido covalentemente a SUB a través de un ligador L opcional como se define en la 15 reivindicación 9;
al menos uno de R10 y R11 es WSG; y
al menos uno de R10 y R11 contiene un sulfonato.
11. El conjugado de tinte de la reivindicación 9, que tiene la estructura de fórmula 13:
en la que X es O o S; R1, R2, R3 y R4 son independientemente hidrógeno, cloro o fluoro; R10 y R11 son independientemente hidrógeno, cloro, fluoro o sulfonato; L es un ligador opcional como se define en la reivindicación 9;
SUB es un sustrato como se define en la reivindicación 9; y en la que al menos uno de R10 y R11 es un sulfonato.
12. El conjugado de tinte de la reivindicación 11, en el que L es nulo, alquilo, alcoxilo, tioalquilo, aminoácido, sulfoaminoácido, poliamina o polietilenglicol que tiene 3-20 átomos de carbono.
13. Un método de detección de un analito en una muestra que comprende a) combinar dicha muestra con un reactivo de detección que comprende un conjugado de tinte de cualquiera de las reivindicaciones 9 a 12 en condiciones en que dicho reactivo de detección forme un complejo con dicho analito;
b) detectar dichos complejos.
14. Un kit que comprende al menos un compuesto de tinte reactivo que tiene la estructura de fórmula 3, fórmula 4, fórmula 5, fórmula 6 o fórmula 7.
15. Un kit que comprende al menos un conjugado de tinte que tiene la estructura de fórmula 11, fórmula 12 o fórmula 13.
16. El compuesto de la reivindicación 1, que tiene la estructura:
Patentes similares o relacionadas:
Derivados de piperidina 1,4 sustituidos, del 29 de Julio de 2020, de 89Bio Ltd: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: A se selecciona de […]
Compuestos y procedimientos de uso, del 29 de Julio de 2020, de Medivation Technologies LLC: Un compuesto de fórmula (Aa-1): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en la que: A representa H, halógeno, amino, […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Ureas asimétricas p-sustituidas y usos médicos de las mismas, del 22 de Julio de 2020, de Helsinn Healthcare SA: Un compuesto de Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde: una línea discontinua indica un enlace opcional; X es CH; […]
N-acil-N''-(piridin-2-il) ureas y análogos que presentan actividades anticancerosas y antiproliferativas, del 24 de Junio de 2020, de Deciphera Pharmaceuticals, LLC: Un compuesto de fórmula I, **(Ver fórmula)** o una sal, un enantiómero, un estereoisómero o un tautómero farmacéuticamente aceptables del mismo, en donde […]
Derivados de lactama, urea cíclica y carbamato y de triazolona como inhibidores potentes y selectivos de ROCK, del 24 de Junio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Fórmula (I): **(Ver fórmula)** o un estereoisómero, un tautómero, una sal farmacéuticamente aceptable del mismo, en donde: […]
Nuevos derivados de dihidroisoquinolin-1-ona bicíclicos, del 17 de Junio de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto seleccionado de 6-cloro-2-piridin-3-il-3,4-dihidro-2H-isoquinolin-1-ona; 5-(6-cloro-1-oxo-3,4-dihidro-1H-isoquinolin-2-il)-nicotinonitrilo; […]
Compuestos de diaminopirimidilo sustituidos, composiciones de los mismos y procedimientos de tratamiento con ellos, del 17 de Junio de 2020, de SIGNAL PHARMACEUTICALS LLC: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal, un tautómero, un isotopólogo o un estereoisómero farmacéuticamente aceptable […]