Sistemas de cultivo de células madre.
Un procedimiento para mantener células madre en un estado indiferenciado,
comprendiendo el procedimiento incubar dichas células con un sistema de cultivo que comprende células alimentadoras, en el que las células alimentadoras en el sistema de cultivo consisten esencialmente en células alimentadoras de fibroblastos expandidas de células del cordón umbilical humano y en el que dicho sistema de cultivo no tiene agentes antibacterianos ni agentes antifúngicos, en el que:
(a) las células madre no son células madre embrionarias humanas;
(b) las células madre son células madre hematopoyéticas obtenidas de tejido de médula ósea de un individuo de cualquier edad o de sangre del cordón de un individuo neonato; o
(c) las células madre son células germinales embrionarias obtenidas del tejido genital de un feto en cualquier momento durante la gestación.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/IL2005/001397.
Solicitante: HADASIT MEDICAL RESEARCH SERVICES AND DEVELOPMENT LTD.
Nacionalidad solicitante: Israel.
Dirección: KIRYAT HADASSAH, P.O. BOX 12000 91120 JERUSALEM ISRAEL.
Inventor/es: Banin,Eyal, BEN SHUSHAN,ETTI, TANNENBAUM,SHELLY, ITSYKSON,PAVEL, REUBINOFF,BENJAMIN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N5/071 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células o tejidos de vertebrados, p.ej. células o tejidos humanos.
- C12N5/0735 C12N 5/00 […] › Células madre embrionarias; Células germinales embrionarias.
PDF original: ES-2525684_T3.pdf
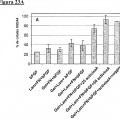
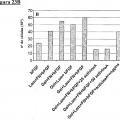
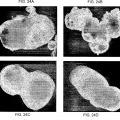
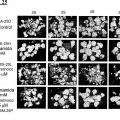
Fragmento de la descripción:
Sistemas de cultivo de células madre Campo de la invención
La divulgación se refiere a células madre (SC) en particular a procedimientos y sistemas para manipular células madre embrionarias humanas (hESC).
Lista de la técnica anterior
La siguiente es una lista de la técnica anterior, que se considera pertinente para describir el estado de la técnica en el campo de la invención.
(1) Thomson, J.A. y col. Embryonic stem cell lines derived from human blastocysts. Science 282, 1145-1147 (1998).
(2) Reubinoff, B.E., Pera, M.F., Fong, C.Y., Trounson, A. y Bongso, A. Embryonic stem cell lines from human blastocysts: somatic differentiation in vitro. Nat Biotechnol 18, 399-44 (2)
(3) Amit, M. y col. Clonally derived human embryonic stem cell lines maintain pluripotency and proliferative potential for prolonged periods of culture. Dev Biol 227, 271-278 (2).
(4) Xu, C. y col. Feeder-free growth of undifferentiated human embryonic stem cells. Nat Biotechnol 19, 971-974 (21).
(5) Amit, M. y col. Human feeder layers for human embryonic stem cells. Biol Reprod 68, 215-2156 (23).
(6) Richards, M., Fong, C.Y., Chan, W.K., Wong, P.C. y Bongso, A. Human feeders support prolonged undifferentiated growth of human inner cell masses and embryonic stem cells. Nat Biotechnol 2, 933-936 (22).
(7) Cowan, C.A. y col. Derivation of embryonic stem-cell lines from human blastocysts. N Engl J Med 35, 1353- 1356 (24).
(8) Amit, M., Shariki, C., Margulets, V. y Itskovitz-Eldor, J. Feeder layer- and Serum-Free Culture of Human Embryonic Stem Cells. Biol Reprod 7(3): 837-45 (24).
(9) Pera, M.F. y col. Regulation of human embryonic stem cell differentiation by BMP-2 and its antagonist noggin.
J Cell Sci 117, 1269-128 (24).
(1) Documento GB24928.
(11) Documento WO 4/31343
(12) Xu, R.H., y col. Basic FGF and suppression of BMP signaling sustain undifferentiated proliferation of human ES cells. Nat Methods. 3, 164-5 (25)
(13) Vallier L, y col. Activin/Nodal and FGF pathways cooperate to maintain pluripotency of human embryonic stem cells. J Cell Sci. 118, 4495-59 (25)
Antecedentes de la invención
Las células madre son células inmaduras, no especializadas, que se renuevan durante periodos largos mediante división celular. En ciertas condiciones, se pueden diferenciar en células maduras, funcionales. Las células madre embrionarias humanas (hESC) derivan de blastocistos humanos sobrantes tempranos1,2. Las células ES humanas son células madre únicas porque pueden auto-renovarse infinitamente en cultivo, y ya que tienen un potencial notable para desarrollarse en linajes extraembrionarios así como todas las células somáticas y tejidos del cuerpo humano.
Dadas las propiedades únicas de las hESC, se espera que tengan aplicaciones de largo alcance en las áreas de la investigación científica básica, farmacología y medicina regenerativa. Las líneas celulares ES humanas pueden proporcionar un potente modelo in vitro para el estudio de la biología molecular y celular del desarrollo humano temprano, para la genómica funcional, exploración y descubrimiento de fármacos. Pueden servir para exploración de alto rendimiento de toxicología y teratogenicidad. Dado que las hESC pueden auto-renovarse indefinidamente y pueden diferenciarse en cualquier tipo celular, pueden servir como una fuente donante renovable, ilimitada, de células o tejidos diferenciados funcionalmente maduros para terapias de trasplante. Además, las hESC modificadas genéticamente trasplantadas pueden actuar como vectores para transportar y expresar genes en órganos diana en el transcurso de la terapia génica.
Aunque la promesa de las hESC para la investigación científica básica, farmacología y medicina regenerativa es notable, el aprovechamiento de las hESC para la mayoría de las aplicaciones depende de un desarrollo adicional. Se requiere un control mejorado del crecimiento de las hESC indiferenciadas, el desarrollo de cultivos sin alimentadores a granel de células indiferenciadas, el desarrollo de sistemas de cultivo sin animales, y el desarrollo de procedimientos y herramientas que dirijan la diferenciación y generen cultivos puros de células funcionales maduras de un tipo específico.
En la actualidad, pocos sistemas de cultivo se usan más habitualmente para propagar hESC indiferenciadas1'4 En el sistema de cultivo inicial que se ha desarrollado, se cultivan hESC indiferenciadas en medio que contiene suero como colonias, sobre una capa de células alimentadoras de fibroblastos (de origen de ratón1,2 o humano5,11). Es posible retirar todos los productos animales de este sistema de cultivo y reemplazarlos con los de una fuente
humana6. Se ha descubierto que en este sistema las células se propagan como grupos a una escala baja que no permite clonación2
Un sistema de cultivo alternativo que se ha desarrollado y se usa extensivamente es un sistema sin suero que incluye el medio de anulación (KO) complementado con reemplazo de suero de anulación (KOSR) y FGF2. Este sistema permite la clonación de hESC indiferenciadas, aunque con una baja eficacia3. Se cultivan células indlferencladas como colonias planas y pueden propagarse como grupos pequeños o células individuales (usando tripsina7).
Otro sistema de cultivo alternativo para su uso en la proliferación de crecimiento indiferenciado de hESC comprende una matriz de cultivo que comprende matriz extracelular (ECM) preparada a partir de células alimentadoras y un medio acondicionado que se pre-acondiciona por células alimentadoras. Las células principales sugeridas en las células alimentadoras incluyen fibroblastos embrionarios de ratón primarios (PMEF), una línea celular de fibroblastos embrionarios de ratón (MEF), fibroblastos fetales murinos (MFF), fibroblastos embrionarios humanos (HEF), músculo fetal humano (HFM), células cutáneas fetales humanas (HFS), células cutáneas adultas humanas, fibroblastos de prepucio humano (HFF)1, células epiteliales de trompas de Falopio adultas humanas (HAFT) o células del estroma de la médula ósea humana (HMSC).
Puede conseguirse propagación ¡ndiferenciada con el sistema de cultivo sin suero KO sin el uso de alimentadores sembrando en placas y cultivando colonias con matrices extracelulares (ECM) dentro de un medio KO acondicionado con alimentador complementado con KOSR y FGF24. Además se ha sugerido que el acondicionamiento de alimentador puede reemplazarse sustituyendo el medio con altas concentraciones de FGF2 y noggina12. Como alternativa, se reemplazó el acondicionamiento de alimentador por el factor de crecimiento transformante pi y UF humano (además de FGF2) y cultivando las células en fibronectina humana8 En una publicación reciente, se ha presentado la propagación ¡ndiferenciada de colonias de hESC, en ausencia de alimentadores con un medio químicamente definido sin reemplazo de suero, complementado con activina o nodal más FGF213.
Una limitación clave de los sistemas de cultivo del hESC es que no permite la propagación de poblaciones puras de células madre indiferenciadas y su uso siempre implica algún nivel de diferenciación de fondo. Las células madre más habitualmente siguen una ruta de diferenciación por defecto a un tipo celular epitelial que crece como una monocapa de células escamosas planas o forma estructuras quístlcas. Más probablemente, esta forma de diferenciación representa la diferenciación de hESC en endodermo extraembrionario6
La diferenciación espontánea de hESC en linajes supuestamente extraembrionarios también interfiere con la derivación de células diferenciadas somáticas. En diversas condiciones inductoras de diferenciación, tales como en cultivos en suspensión de cuerpos embrioides (EB), la diferenciación en estructuras extraembrionarias quísticas puede ser común o puede predominar y limitar la diferenciación en linajes somáticos. El control y la eliminación de la diferenciación en linajes extraembrionarios pueden, por lo tanto, ser de valor incalculable en la derivación de linajes somáticos, además de su importancia en el mantenimiento de las células madre en un estado indiferenciado. Se ha demostrado recientemente que en condiciones de cultivo inductoras de diferenciación, el antagonista de la proteína morfogenética del hueso (BMP) noggina puede prevenir la diferenciación extraembrionaria de hESC y promover su diferenciación en el linaje neural9
Sumario de la invención
De acuerdo con un primer aspecto, la presente invención proporciona un cultivo celular que comprende células obtenidas de tejido del cordón umbilical humano, siendo las células derivadas del cordón umbilical humano capaces de mantener células madre (SC) en un estado indiferenciado... [Seguir leyendo]
Reivindicaciones:
1. Un procedimiento para mantener células madre en un estado indiferenciado, comprendiendo el procedimiento incubar dichas células con un sistema de cultivo que comprende células alimentadoras, en el que las células alimentadoras en el sistema de cultivo consisten esencialmente en células alimentadoras de fibroblastos expandidas de células del cordón umbilical humano y en el que dicho sistema de cultivo no tiene agentes antibacterianos ni agentes antifúngicos, en el que:
(a) las células madre no son células madre embrionarias humanas;
(b) las células madre son células madre hematopoyéticas obtenidas de tejido de médula ósea de un individuo de cualquier edad o de sangre del cordón de un individuo neonato; o
(c) las células madre son células germinales embrionarias obtenidas del tejido genital de un feto en cualquier momento durante la gestación.
2. El procedimiento de la reivindicación 1, en el que todas las células alimentadoras en el sistema de cultivo son células de fibroblastos.
3. El procedimiento de la reivindicación 1 o 2, en el que dichas células madre son células madre humanas.
4. El procedimiento de una cualquiera de las reivindicaciones 1 a 3, para propagar dichas células madre en un estado indiferenciado.
5. El procedimiento de una cualquiera de las reivindicaciones 1 a 4, que comprende incubar dichas células madre con un sustituto de reemplazo de suero humanizado.
6. El procedimiento de la reivindicación 5, en el que dicho sustituto de reemplazo de suero humanizado es seleccionado de TCH, Nutridoma-CS, N2 y una combinación de los mismos.
7. El procedimiento de una cualquiera de las reivindicaciones 1 a 6, en el que el sistema de cultivo es un sistema de cultivo sin suero.
8. El procedimiento de la reivindicación 7, en el que el sistema de cultivo comprende un medio básico seleccionado de medio de cultivo de células madre Cellgro, KO DMEM, Neurobasal y X-Vivo 1.
9. El procedimiento de la reivindicación 8, en el que cuando dicho medio básico es Neurobasal, el sistema comprende además un complemento de N2 o una modificación de complemento de N2.
1. Un procedimiento para obtener un cultivo celular que comprende células alimentadoras obtenidas de tejido del cordón umbilical humano, comprendiendo el procedimiento:
(a) aislar células del cordón umbilical de tejido del cordón umbilical; y
(b) cultivar dichas células del cordón umbilical en un medio de cultivo que incluye suero que no tiene agentes antibióticos ni agentes antifúngicos,
en el que dichas células del cordón umbilical se obtienen triturando dicho tejido del cordón umbilical en trozos pequeños, y en el que los trozos de tejido del cordón umbilical triturados se fijan a las paredes de un recipiente en presencia de medio de cultivo, y se permite que se incuben sin perturbación durante varias semanas hasta que las células de fibroblastos comienzan a migrar fuera de los trozos del cordón umbilical,
para obtener dicho cultivo celular en el que las células derivadas del cordón umbilical humano son capaces de mantener células madre en un estado indiferenciado cuando se co-cultivan con las mismas, y en el que las células alimentadoras consisten esencialmente en células de fibroblastos.
11. El procedimiento de la reivindicación 1, en el que dicho tejido del cordón umbilical es obtenido de mujeres embarazadas sanas que se someten a cesáreas opcionales a término.
12. Un procedimiento para mantener células madre en un estado indiferenciado de acuerdo con una cualquiera de las reivindicaciones 1 a 9, en el que dicho sistema de cultivo comprende un cultivo celular obtenido acuerdo con el procedimiento de la reivindicación 1 u 11.
13. Un sistema de cultivo que comprende células alimentadoras para el mantenimiento de células madre en un estado indiferenciado, en el que las células alimentadoras en el sistema de cultivo consisten esencialmente en células alimentadoras de fibroblastos expandidas de células del cordón umbilical humano, estando dicho sistema de cultivo sin agentes antibacterianos y agentes antifúngicos.
14. El sistema de cultivo de la reivindicación 13 que es adecuado para el mantenimiento de células madre embrionarias en un estado indiferenciado.
15. El sistema de cultivo de la reivindicación 13 o 14, en el que dichas células madre son células madre humanas.
16. El sistema de cultivo de una cualquiera de las reivindicaciones 13 a 15, para la propagación de células madre ¡ndiferencladas.
17. El sistema de cultivo de una cualquiera de las reivindicaciones 13 a 16, que es un sistema de cultivo sin animales.
18. El sistema de cultivo de una cualquiera de las reivindicaciones 13 a 17, que comprende un sustituto de
reemplazo de suero humanizado.
Patentes similares o relacionadas:
DISPOSITIVO PARA LA SELECCIÓN DE ESPERMATOZOIDES, del 23 de Julio de 2020, de INSTITUTO NACIONAL DE INVESTIGACION Y TECNOLOGIA AGRARIA Y ALIMENTARIA (INIA): Dispositivo para la selección de espermatozoides que comprende una unidad de selección que comprende a su vez un compartimento de carga (1b) […]
Método para preparar una disolución acuosa que contiene medio de cultivo y agente quelante, del 22 de Julio de 2020, de Kyowa Kirin Co., Ltd: Método para preparar una disolución acuosa que presenta una filtrabilidad de membrana mejorada que comprende un medio de cultivo, en el que el medio de […]
Células madre multipotentes del árbol biliar extrahepático y métodos para su aislamiento, del 1 de Julio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Metodo de obtencion de celulas madre/progenitoras multipotentes de mamifero capaces de diferenciarse en linajes endodermicos multiples, donde las celulas […]
Procedimientos y composiciones para el tratamiento de una afección genética, del 24 de Junio de 2020, de Sangamo Therapeutics, Inc: Una célula precursora de glóbulos rojos genomanipulada caracterizada por una modificación genómica dentro del exón 2 o el exón 4 de BCL11A o dentro de BCL11A-XL […]
Métodos y dispositivos para trasplante celular, del 10 de Junio de 2020, de Sernova Corporation: Un dispositivo para implantar células en un cuerpo huésped, que comprende: un andamio poroso que comprende al menos una cámara que tiene un extremo proximal y un extremo […]
Composiciones, usos y preparación de lisados de plaquetas, del 27 de Mayo de 2020, de EMORY UNIVERSITY: Una composición que comprende componentes de lisado de plaquetas con una concentración de fibrinógeno de menos de 20 μg/ml.
Métodos y composiciones para el tratamiento de enfermedades autoinmunes e inflamatorias, del 29 de Abril de 2020, de Lankenau Institute for Medical Research: Un anticuerpo anti-RhoB o fragmento del mismo para uso en la inhibición de una enfermedad inflamatoria o autoinmune en un sujeto que lo necesita, en el que […]
Células virales resistentes y sus usos, del 22 de Abril de 2020, de Sigma-Aldrich Co. LLC: Una línea celular de ovario de hámster chino (CHO) modificada genéticamente en la que la entrada y/o propagación del virus diminuto del ratón (MVM) […]