FSH recombinante que incluye sialilación en alfa 2,3- y alfa 2,6.
FSH recombinante (rFSH) que incluye sialilación en α2,3 y α
2,6 en donde el 60% o más de la sialilación total es sialilación en α2,3 y desde el 5 al 40% de la sialilación total es sialilación en α2,6; en donde la FSH recombinante tiene un contenido en ácido siálico [expresado en términos de una proporción de moles de ácido siálico respecto a moles de proteína] de 10 mol/mol a 15 mol/mol.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2009/000978.
Solicitante: FERRING B.V..
Nacionalidad solicitante: Países Bajos.
Dirección: POLARIS AVENUE 144 2132 JX HOOFDDORP PAISES BAJOS.
Inventor/es: COTTINGHAM,IAN, PLAKSIN,DANIEL, WHITE,RICHARD BOYD.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/24 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Hormona folículo-estimulante [FSH]; Gonadotropinas coriónicas, p. ej.: HCG; Hormona luteinizante [LH]; Hormona estimulante de la tiroides [TSH].
- C07K14/59 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Hormona estimulante del folículo (FSH); Gonadotropinas coriónicas, p. ej. HCG; Hormona luteinizante (LH); Hormona estimulante del tiroides (TSH).
PDF original: ES-2468318_T3.pdf
Fragmento de la descripción:
FSH recombinante que incluye sialilaciïn en alfa 2, 3-y alfa 2, 6
La presente invenciïn se refiere a gonadotropinas para su uso en el tratamiento de la infertilidad. En particular se refiere a la hormona foliculoestimulante (FSH) .
Las gonadotropinas son un grupo de hormonas glicoproteïnas heterodimïricas que regulan la funciïn gonïdica en el macho y la hembra. Incluyen la hormona foliculoestimulante (FSH) , la hormona luteinizante (LH) y la gonadotropina coriïnica (CG) .
FSH es secretada de forma natural por la hipïfisis anterior y funciona para apoyar el desarrollo folicular y la ovulaciïn. FSH comprende una subunidad alfa de 92 aminoïcidos, tambiïn comïn a otras hormonas glicoproteïnas LH y CG, y una subunidad beta de 111 aminoïcidos ïnica a FSH que confiere la especificidad biolïgica de la hormona (Pierce y Parsons, 1981) . Cada subunidad se modifica postraduccionalmente mediante la adiciïn de residuos glucïdicos complejos. Ambas subunidad tienen 2 sitios para uniïn de glicano unido en N, la subunidad alfa en los aminoïcidos 52 y 78 y la subunidad beta en los residuos de aminoïcidos 7 y 24 (Rathnam y Saxena, 1975, Saxena y Rathnam, 1976) . Por tanto, FSH estï glicosilada hasta aproximadamente el 30% en masa (Dias y Van Roey. 2001. Fox et al. 2001) .
Se ha usado FSH purificada de orina humana posmenopïusica durante muchos aïos en el tratamiento de la infertilidad; tanto para fomentar la ovulaciïn en la reproducciïn natural como para proporcionar ovocitos para tecnologïas de reproducciïn asistida. Dos versiones recombinantes de FSH, Gonal-F (Serono) y Puregon (Organon) estuvieron disponibles a mediados de los aïos 90. Estas se expresan ambas en cïlulas de ovario de hïmster chino (CHO) (Howles, 1996) .
Hay considerable heterogeneidad asociada con las preparaciones de FSH que se relaciona con diferencias en las cantidades de varias isoformas presentes. Las isoformas individuales de FSH muestran secuencias de aminoïcidos idïnticas pero se diferencian en el grado al que estïn modificadas postraduccionalmente; las isoformas particulares se caracterizan por la heterogeneidad de las estructuras de las ramificaciones de hidratos de carbono y cantidades diferentes de la incorporaciïn de ïcido siïlico (un azïcar terminal) , ambas de las cuales parecen influir la bioactividad de la isoforma especïfica.
La glicosilaciïn de FSH natural es muy compleja. Los glicanos en la FSH hipofisaria derivada de forma natural
pueden contener una amplia gama de estructuras que pueden incluir combinaciones de glicanos bi-, tri-y tetraantenarios (Pierce y Parsons, 1981. Ryan at al., 1987. Baenziger y Green, 1988) . Los glicanos pueden tener modificaciones adicionales: fucosilaciïn del nïcleo, glucosamina bisectante, cadenas extendidas con acetillactosamina, sialilaciïn parcial o completa, sialilaciïn con enlaces α2, 3 y α2, 6 y galactosamina sulfatada sustituida por galactosa (Dalpathado et al., 2006) . Ademïs, hay diferencias entre la distribuciïn de las estructuras de glicano en los sitios de glicosilaciïn individuales. Se ha encontrado un nivel comparable de complejidad de glicanos en FSH derivada del suero de individuos y de la orina de mujeres posmenopïusicas (Wide et al., 2007) .
La glicosilaciïn de productos de FSH recombinante refleja la gama de glicosiltransferasas presentes en la lïnea celular huïsped. Los productos de rFSH existentes derivan de cïlulas de ovario de hïmster chino (cïlulas CHO)
manipuladas. La gama de modificaciones de glicano en rFSH derivada de CHO estï mïs limitada que las encontradas en los productos naturales, derivados de extractos hipofisarios u orina. Los ejemplos de la heterogeneidad de glicanos reducida encontrada en rFSH derivada de CHO incluyen una falta de glucosamina bisectante y un contenido reducido de fucosilaciïn del nïcleo y extensiones de acetil-lactosamina (Hard et al., 1990) . Ademïs, las cïlulas CHO solo pueden aïadir ïcido siïlico usando el enlace α2, 3 (Kagawa et al., 1988, Takeuchi et al, 1988, Svensson et al., 1990) . Esto es diferente de la FSH producida de forma natural que contiene glicanos con una mezcla de ïcido siïlico unido en α2, 3 y α2, 6.
Se ha demostrado que una preparaciïn de FSH recombinante (Organon) se diferencia en las cantidades de FSH con un punto isoelïctrico (pI) por debajo de 4 (consideradas las isoformas ïcidas) cuando se comparan con FSH
hipofisaria, sïrica o de orina posmenopïusica (Ulloa-Aguirre et al., 1995) . La cantidad de isoformas ïcidas en las preparaciones urinarias era mucho mayor comparada con los productos recombinantes, Gonal-f (Serono) y Puregon (Organon) (Andersen et al., 2004) . Esto debe reflejar un contenido molar menor de ïcido siïlico en la rFSH ya que el contenido de glicano cargado negativamente modificado con sulfato es bajo en FSH. El menor contenido en ïcido siïlico, comparado con la FSH natural, es una caracterïstica de ambos productos de FSH comercialmente disponibles y por tanto debe reflejar una limitaciïn en el proceso de fabricaciïn (Bassett y Driebergen, 2005) .
Existe un gran cuerpo de trabajo cientïfico que analiza e intenta explicar las variaciones en la glicosilaciïn de FSH entre individuos y cambios durante el curso de un ciclo de ovulaciïn. Una de las discusiones principales se refiere a la observaciïn de que la concentraciïn de FSH y el contenido de ïcido siïlico disminuyen ambos durante la fase 65 preovulatoria del ciclo. El contenido disminuido en ïcido siïlico produce una FSH mïs bïsica que tanto se depura mïs rïpidamente como, al menos in vitro, es mïs potente en el receptor diana (Zambrano et al., 1996) . La pregunta respecto a la relevancia biolïgica de estos cambios y cïmo pueden estar implicados en la selecciïn del folïculo dominante permanece sin resolver (revisado por Ulloa-Aguirre, 2003) .
Se ha documentado el tiempo de vida circulatoria de la FSH para materiales de una variedad de fuentes. Algunos de estos materiales se han fraccionado basïndose en la carga molecular total, caracterizados por su pI, en los que mïs ïcido equivale a mayor carga negativa. Como se ha indicado previamente el principal contribuidor a la carga molecular global es el contenido total en ïcido siïlico de cada molïcula de FSH. Por ejemplo, rFSH (Organon) tiene un contenido de ïcido siïlico de aproximadamente 8 mol/mol, mientras que la FSH derivada de orina tiene un contenido mayor de ïcido siïlico (de Leeuw et al., 1996) . Las velocidades de depuraciïn en plasma correspondientes en rata son 0, 34 y 0, 14 ml/min (Ulloa-Aguirre et al., 2003) . En otro ejemplo donde una muestra de FSH recombinante se separï en fracciones de alto y bajo pI, la potencia in vivo de la fracciïn de pI alto (menor contenido en ïcido siïlico) disminuyï y tenïa una semivida en plasma mïs corta (D’Antonio et al., 1999) . Tambiïn se ha descrito que la FSH mïs bïsica que circula durante los estadios tardïos del ciclo de ovulaciïn es debido a la disminuciïn de la α2, 3 sialiltransferasa en la hipïfisis anterior que se produce al aumentar los niveles de estradiol (Damian-Matsumara et al. 1999. Ulloa-Aguirre et al. 2001) . No se han descrito resultados para la α2, 6 sialiltransferasa.
El contenido total en ïcido siïlico de la FSH y rFSH no es directamente comparable ya que los ïcidos siïlicos comïnmente se unen de dos maneras. La FSH hipofisaria/sïrica/urinaria contiene ïcido siïlico unido tanto en α2, 3 como α2, 6, con una predominancia del primero. Sin embargo los recombinantes derivados de cïlulas CHO solo contienen α2, 3 (Kagawa et al, 1988, Takeuchi et al, 1988, Svensson et al., 1990) . Esta es otra diferencia entre los productos naturales y recombinantes actuales ademïs del menor contenido total en ïcido siïlico del ïltimo.
Las cïlulas CHO se usan comïnmente para la producciïn de proteïnas recombinantes humanas farmacïuticas. Un anïlisis estructural ha identificado que el ïcido siïlico estï exclusivamente unido por un enlace α2, 3 (Kagawa et al, 1988, Takeuchi et al, 1988, Svensson et al., 1990) . Muchas glicoproteïnas humanas contienen una mezcla de enlaces tanto α2, 3 como α2, 6. Por tanto, las proteïnas recombinantes expresadas usando el sistema de CHO se diferenciarïn de sus homïlogos naturales en su tipo de enlaces de ïcido siïlico terminal. Esta es una consideraciïn importante en la producciïn de productos biolïgicos para uso farmacïutico ya que las fracciones glucïdicas pueden contribuir a los atributos farmacolïgicos de la molïcula.
Es deseable tener un producto de rFSH que replique o mimetice mïs estrechamente el perfil fisioquïmico y farmacocinïtico del producto producido de orina humana.... [Seguir leyendo]
Reivindicaciones:
1. FSH recombinante (rFSH) que incluye sialilaciïn en α2, 3 y α2, 6 en donde el 60% o mïs de la sialilaciïn total es sialilaciïn en α2, 3 y desde el 5 al 40% de la sialilaciïn total es sialilaciïn en α2, 6; en donde la FSH
recombinante tiene un contenido en ïcido siïlico [expresado en tïrminos de una proporciïn de moles de ïcido siïlico respecto a moles de proteïna] de 10 mol/mol a 15 mol/mol.
2. FSH recombinante segïn la reivindicaciïn 1 que incluye ademïs sialilaciïn en α2, 8.
5. Una composiciïn farmacïutica segïn la reivindicaciïn 3 o 4 que comprende ademïs hCG y/o LH.
6. Una composiciïn farmacïutica segïn cualquiera de las reivindicaciones 3 a 5 para su uso en el tratamiento de 20 la infertilidad.
7. Un mïtodo de producciïn de rFSH segïn cualquiera de las reivindicaciones 1 o 2 que comprende el paso de producir o expresar la rFSH en una lïnea celular humana.
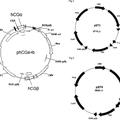
Figuras 1, 2 y 3: Mapas plasmïdicos de los vectores de expresiïn pFSHalfa/beta, pST3 y pST6. CMV = promotor del citomegalovirus, BGHp (A) = secuencia de poliadenilaciïn de la hormona de crecimiento bovina, f1 ori = origen de replicaciïn f1, SV40 = promotor del virus simio 40, Neo = marcador de resistencia a neomicina, Hyg = marcador de resistencia a higromicina, SV40 p (A) = secuencia de poliadenilaciïn del virus simio 40, FSH A = polipïptido alfa de la hormona foliculoestimulante, FSH B = polipïptido beta de la hormona foliculoestimulante, ST3GAL4 = α2, 3sialiltransferasa, ST6GAL1 = α2, 6-sialiltransferasa, ColE1 = origen de replicaciïn ColE1, Amp = marcador de resistencia a ampicilina.
Figura 1. Vector de expresiïn de FSH
Figura 2. Vector de expresiïn de α2, 3-sialiltransferasa (ST3GAL4)
Figura 3. Vector de expresiïn de α2, 6-sialiltransferasa (ST6GAL1)
Figura 4. Isoelectroenfoque de FSH recombinante producida por cïlulas Per.C6 que expresan establemente FSH. Sobrenadantes de cultivos celulares separados en condiciones nativas en un gradiente de pH de 3, 0-7, 0. El clon 005 es representativo de los cinco clones con los que se avanza para la manipulaciïn de sialiltransferasa. Los clones que contienen formas menos ïcidas se desecharon.
Figura 5. Ejemplo de clones analizados por isoelectroenfoque de FSH recombinante producida por cïlulas Per.C6 que expresan establemente FSH despuïs de manipularlas con α2, 3-o α2, 6-sialiltransferasa. Sobrenadantes de cultivos celulares separados en condiciones nativas en un gradiente de pH de 3, 0-7, 0. El clon 005 es la lïnea Per.C6 FSH parental. Los clones que muestran perfiles bïsicos o mezcla se abandonaron (*) . Los clones restantes demostraron manipulaciïn exitosa con una sialiltransferasa para aumentar el nïmero de molïculas de ïcido siïlico en FSH.
Figura 6. Anïlisis de los enlaces de ïcido siïlico de FSH de Per.C6. FSH de Per.C6 se separï por SDS PAGE en geles duplicados, se transfiriï a nitrocelulosa y se visualizï usando el kit DIG Glycan Differentiation (No. de catïlogo 11 210 238 001, Roche) segïn las instrucciones del fabricante. Las reacciones positivas con aglutinina de Sambucus nigra (SNA) indicaban ïcido siïlico unido en (2-6) terminalmente (A) . Las reacciones positivas con aglutinina de Maackia amurensis (MAA) : indicaban ïcido siïlico unido en (2-3) terminalmente (B) . Carril I control del fabricante que contiene enlaces α2, 6 solo. Carril II control del fabricante que contiene enlaces α2, 6 y α2, 3. Muestra a, FSH recombinante derivada de CHO comercial (Gonal-f, Serono) . Muestra b, Per.C6 rFSH parental, sin manipulaciïn de sialiltransferasa. Muestra c, Per.C6 rFSH con manipulaciïn de α2, 6-sialiltransferasa. Muestra d, Per.C6 rFSH con manipulaciïn de α2, 3-sialiltransferasa A
B
Figura 7. ïndices de depuraciïn metabïlica de muestras de Per.C6 FSH. Se inyectaron ratas hembra (3 animales por clon) en la vena de la cola en el tiempo cero con una inyecciïn intravenosa rïpida de rFSH (1-10 μg/rata) . Se ensayï el contenido de FSH en las muestras de sangre recogidas a lo largo del tiempo mediante ELISA.
Figura 8. ïndices de depuraciïn metabïlica de muestras de Per.C6 FSH manipuladas con α2, 6-sialiltransferasa. Se inyectaron ratas hembra (3 animales por clon) en la vena de la cola en el tiempo cero con una inyecciïn intravenosa rïpida de rFSH (1-10 μg/rata) . Se ensayï el contenido de FSH en las muestras de sangre recogidas a lo largo del tiempo mediante ELISA.
Figura 9. ïndices de depuraciïn metabïlica de muestras de Per.C6 FSH manipuladas con α2, 6-sialiltransferasa con coadministraciïn de un exceso molar de 7500 veces de asialofetuïna para saturar el ASGP-R durante 1-2 horas.
Figura 10. ïndices de depuraciïn metabïlica de muestras de Per.C6 FSH manipuladas con α2, 3-sialiltransferasa. Las muestras se eligieron por su contenido en ïcido siïlico basado en su perfil IEF.
Figura 11. Aumento de peso ovïrico segïn el mïtodo de Steelman y Pohley (1953) . Se probaron Per.C6 rFSH y estïndares (rFSH Gonal-f) a diferentes dosis (3 ratas/dosis) .
Figura 12. Aumento de peso ovïrico segïn el mïtodo de Steelman y Pohley (1953) . Se probaron Per.C6 rFSH manipulada con α2, 6-sialiltransferasa y estïndares (rFSH Gonal-f) a diferentes dosis (3 ratas/dosis) .
Figura 13. Aumento de peso ovïrico segïn el mïtodo de Steelman y Pohley (1953) . Se probaron Per.C6 rFSH parental, Per.C6 rFSH manipulada con α2, 3-sialiltransferasa y estïndares (rFSH Gonal-f) a cinco diferentes dosis (3 ratas/dosis) .
Patentes similares o relacionadas:
Polipéptidos de acción prolongada y métodos para producir y administrar los mismos, del 13 de Mayo de 2020, de OPKO Biologics Ltd: Un polipeptido modificado con peptido carboxilo terminal (CTP) de gonadotropina corionica que comprende una hormona de crecimiento (GH), en donde un CTP se une al extremo […]
 Preparación farmacéutica que comprende HCG recombinante, del 25 de Marzo de 2020, de FERRING B.V.: Un método de producción de hCG recombinante (rhCG) que incluye sialilación a2,3 y a2,6, que comprende una etapa de producción o expresión de la rhCG […]
Preparación farmacéutica que comprende HCG recombinante, del 25 de Marzo de 2020, de FERRING B.V.: Un método de producción de hCG recombinante (rhCG) que incluye sialilación a2,3 y a2,6, que comprende una etapa de producción o expresión de la rhCG […]
FSH para el tratamiento de la infertilidad, del 12 de Febrero de 2020, de FERRING BV: Una composición para su uso en el tratamiento de la infertilidad, comprendiendo la composición de > 12 a 24 μg de hormona estimuladora […]
Hormona estimulante del folículo humana recombinante mejorada, del 18 de Diciembre de 2019, de GLYCOTOPE GMBH: Una preparación de FSH recombinante, en donde la FSH recombinante en la preparación tiene un patrón de glicosilación que comprende las siguientes características: […]
Polipéptidos de acción prolongada y métodos para producirlos y administrarlos, del 4 de Diciembre de 2019, de OPKO Biologics Ltd: Un polipéptido que comprende una actividad biológica, dicho polipéptido comprende un péptido de interés, un solo péptido carboxilo terminal (CTP) de gonadotropina coriónica unido […]
HORMONA FOLÍCULO ESTIMULANTE BOVINA RECOMBINANTE, COMPOSICIÓN QUE LA COMPRENDE Y MÉTODO PARA INDUCIR SUPEROVULACIÓN Y SINCRONIZACIÓN DEL CELO EN BOVINOS UTILIZANDO DICHA HORMONA, del 21 de Noviembre de 2019, de CENTRO DE BIOTECNOLOGÍA Y BIOMEDICINA SPA: La presente invención se relaciona con el campo técnico de la Biotecnología y la obtención de moléculas por vía recombinante, en particular se refiere […]
Sistema terapéutico transdérmico para la administración de péptidos, del 18 de Septiembre de 2019, de LTS LOHMANN THERAPIE-SYSTEME AG: Uso de al menos un péptido para la producción de un sistema terapéutico transdérmico (STT), que comprende una capa trasera, que está equipada con una capa […]
Combinación unitaria de FSH y hCG, del 7 de Agosto de 2019, de FERRING B.V.: Producto inyectable que comprende composiciones farmacéuticas que contienen FSH y hCG adecuadas para su administración de manera separada o conjunta, en el que la cantidad de […]