Procedimiento para la preparación de fenilalcanoles m- ó p-substituidos mediante alquilación.
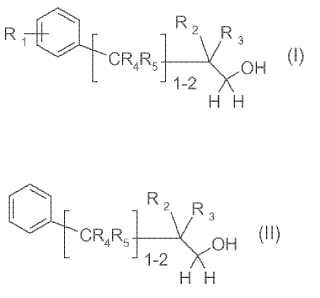
Procedimiento para la preparación de fenilalcanoles m- ó p-substituidos de fórmula (I)**Fórmula**
en la que R1 está unido al anillo de fenilo en la posición m ó p y significa alquilo C1-C5,
y R2, R3, R4 y R5 significanindependientemente entre sí hidrógeno o metilo, caracterizado porque se alquila un fenilalcanol no substituido defórmula (II)**Fórmula**
en la que R2, R3, R4 y R5 tienen los significados indicados debajo de la fórmula (I) junto con un halogenuro dealquilo C1-C5 de fórmula (III)**Fórmula**
R1-Hal (III),en la que R1 tiene el significado indicado debajo de la fórmula (I) y Hal significa halógeno, en presencia de uncatalizador de Friedel-Crafts dando una mezcla de fenilalcanoles m- y p-alquilsubstituidos de fórmula (I), acontinuación la mezcla de reacción se procesa y se separa el fenilalcanol m-alquilsubstituido de fórmula (I) deseadoo el fenilalcanol p-alquilsubstituido de fórmula (I) deseado, los demás productos formados se reconducen a lamezcla de reacción y estos en presencia de un catalizador de Friedel-Crafts se isomerizan al fenilalcanol m- ó palquilsubstituidodeseado.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/065466.
Solicitante: BASF SE.
Nacionalidad solicitante: Alemania.
Dirección: 67056 LUDWIGSHAFEN ALEMANIA.
Inventor/es: EBEL, KLAUS, BECK, KARL, PELZER, RALF, DR., GRIESBACH,Ulrich, BOTZEM,JÖRG, LANVER,ANDREAS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C29/32 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 29/00 Preparación de compuestos que tienen grupos hidroxilo o grupos O-metal unidos a un átomo de carbono que no forma parte de un ciclo aromático de seis miembros. › por reacciones que aumentan el número de átomos de carbono sin formación de grupos hidroxilo.
- C07C29/56 C07C 29/00 […] › por isomerización.
- C07C33/20 C07C […] › C07C 33/00 Compuestos insaturados que tienen grupos hidroxilo o grupos O-metal unidos a átomos de carbono acíclicos. › monocíclicos.
- C07C45/29 C07C […] › C07C 45/00 Preparación de compuestos que tienen grupos C=O unidos únicamente a átomos de carbono o hidrógeno; Preparación de los quelatos de estos compuestos. › de grupos hidroxilo.
- C07C47/228 C07C […] › C07C 47/00 Compuestos que tienen grupos —CHO. › conteniendo ciclos aromáticos de seis miembros, p. ej. fenilacetaldehído.
PDF original: ES-2451010_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de fenilalcanoles m- ó p-substituidos mediante alquilación Es objeto de la presente invención un procedimiento para la preparación de fenilalcanoles m- ó p-alquilsubstituidos mediante alquilación de Friedel-Crafts de fenilalcoholes y subsiguiente isomerización de los subproductos no deseados al fenilalcanol m- ó p-alquilsubstituido buscado. Los fenilalcanoles m- ó p-alquilsubstituidos así como los fenilalcanales m- ó p-alquilsubstituidos preparados a partir de estos, por ejemplo derivados de la substancia odorífera 3-fenil-1-propanol, son de interés como compuestos químicos aromáticos.
Para la preparación de fenilalcanoles alquilsubstituidos y sus derivados son conocidas distintas síntesis.
En el documento WO 2008/053148 está descrita una síntesis en 3 etapas para la preparación de 3- (3-tecbutilfenil) propanal a partir de 1-terc-butil-3-etilbenceno. A este respecto el compuesto de partida primeramente se broma dando el 1-terc-butil-3- (1-bromo-etil) benceno y a continuación se elimina dando el correspondiente estireno substituido. Mediante hidroformilación se obtiene a continuación el 3- (3-terc-butilfenil) propanal. Para un proceso industrial esta síntesis resulta poco adecuada debido a sus bajos rendimientos.
La preparación de 2-metil-3- (3-terc-butilfenil) propanal y de 2-metil-3- (3-isobutilfenil) propanal la consigue Ishii y col.
(J. Org. Chem. 2005, 70, 5471-5474) por acoplamiento oxidativo catalizado con paladio de terc-butilbenceno o isopropilbenceno con metacroleína seguido de una hidrogenación catalizada con paladio. En el paso de acoplamiento se utiliza un sistema catalizador constituido por Pd (OAc) 2 y H4PMO11VO40 x 26 H2O. Se necesita una elevada cantidad de catalizador de aprox. el 7% en moles. Con un rendimiento de aprox. el 65% la relación m/p asciende a 56/44 (para 2-metil-3- (3-terc-butilfenil) propanal) o a 51/40 (para 2-metil-3- (3-isobutilfenil) propanal) . También este procedimiento resulta poco adecuado para un proceso industrial.
En el documento EP 0 045 571 está descrita la alquilación de Friedel-Crafts de 2-metil-3-fenilpropanol a 2-metil-3- (3terc-butilfenil) propanol y 2-metil-3- (4-terc-butilfenil) propanol. Como reactivos de alquilación se utilizan isobutileno, diisobutileno y cloruro de terc-butilo. Como catalizadores se usan cloruro de hierro y ácido fosfórico y como disolvente cloruro de metileno o ácido fosfórico. Dependiendo de las condiciones de reacción y del catalizador se obtienen relaciones m/p de 1/13 a 1/5. Los rendimientos globales (isómero m e isómero p) ascienden a hasta el 52%.
En el documento DE 29 52 712 se describe igualmente la alquilación de Friedel-Crafts catalizada con cloruro de hierro de 2-metil-3-fenilpropanol. En ciclohexano o dicloroetano como disolvente se obtuvo un rendimento del 84-86% de 2-metil-3- (4-terc-butilfenil) propanol. La formación del compuesto isómero m, (2-metil-3- (3-terc-butilfenil) propanol) , no se comprobó. Es un inconveniente de las alquilaciones de Friedel-Crafts descritas la cantidad no identificada del compuesto isómero m fornado (la relación m : p es como máx. de 1:5) .
Frente a estos procedimientos conocidos el procedimiento conforme a la invención permite preparar los fenilalcanoles m-substituidos o los fenilalcanoles p-substituidos, que sirven como precursores de los muy interesantes fenilalcanales correspondientemente substituidos (fenilalquilaldehídos) , económicamente y con buen rendimiento y de la forma más sencilla.
La presente invención se refiere a un procedimiento para la preparación de fenilalcanoles substituidos en posición m ó p que pueden obtenerse mediante alquilación de Friedel-Crafts de fenilalcanoles no substituidos junto con haloogenuros de alquilo. La alquilación se realiza en determinados catalizadores de Friedel Krafts. Es por consiguiente objeto de la invención un procedimiento para la preparación de fenilalcanoles m- ó p-alquilsubstituidos de fórmula (I)
en la que R1 está unido al anillo de fenilo en la posición m ó p y significa alquilo C1-C5 y R2, R3, R4 y R5 significan independientemente entre sí hidrógeno o metilo, que está caracterizado porque se alquila un fenilalcanol no substituido de fórmula (II)
en la que R2, R3, R4 y R5 tienen los mismos significados indicados debajo de la fórmula (I) junto con un halogenuro de alquilo C1-C5 de fórmula (III)
R1-Hal (III) ,
en la que R1 tiene el significado indicado debajo de la fórmula (I) y Hal significa halógeno, en presencia de un catalizador de Friedel-Crafts dando una mezcla de fenilalcanoles m- y p-alquilsubstituidos de fórmula (I) y a continuación la mezcla de reacción, preferentemente en presencia de agua a un valor del pH alcalino, se procesa y se separa, preferentemente por destilación, el fenilalcanol m-alquilsubstituido de fórmula (I) deseado o el fenilalcanol p-alquilsubstituido de fórmula (I) deseado, y los demás subproductos formados se reconducen a la mezcla de reacción y estos en presencia de un catalizador de Friedel-Crafts se isomerizan al fenilalcanol m- ó palquilsubstituido deseado.
Para influir en la relación m y p de la reacción de alquilación en la dirección adecuada, se realiza después de la alquilación y después de la separación del producto deseado, es decir o del fenilalcanol m-alquilsubstituido o del fenilalcanol p-alquilsubstituido, todavía una isomerización de los componentes no deseados al componente deseado. El paso de reacción denominado como isomerización designa el ajuste de un equilibrio de los distintos componentes de la reacción en las condiciones presentes en presencia de un catalizador de Friedel-Crafts. A continuación del paso de la isomerización se realiza un procesamiento, preferentemente un procesamiento acuoso, preferentemente a un valor del pH alcalino, siendo con muy especial preferencia un procesamiento acuoso en presencia de lejía alcalina, como p.ej. lejía de sosa y/o lejía de potasa, entonces se separa el producto deseado, preferentemente por destilación y el producto no deseado se somete de nuevo a una isomerización. El paso de isomerización puede realizarse de forma cuasi continua, realizándose después de cada paso de isomerización un procesamiento acuoso, preferentemente en condiciones alcalinas como se ha indicado anteriormente, con subsiguiente separación, preferentemente separación por destilación, para aumentar el rendimiento del producto deseado.
El procesamiento acuoso de la masa de reacción conforme al presente procedimiento se realiza después de la alquilación y también después del paso de la isomerización mezclando la masa de reacción a temperatura ambiente con agua, preferentemente a un valor del pH alcalino, con especial preferencia en presencia de lejía alcalina, en especial lejía de sosa o lejía de potasa. Seguidamente se separa el producto de reacción deseado, preferentemente por destilación,
Se ha encontrado que en la alquilación de fenilalcanoles no substituidos a fenilalcanoles alquilsubstituidos bajo determinadas condiciones pueden obtenerse relaciones de isómeros m/p de > 1, 5/1. De este modo apenas pueden obtenerse fenilalcanoles m- ó p-substituidos de fórmula (I) puros, de modo que a la alquilación se le conectó una isomerización de los subproductos no deseados a uno de los productos de reacción deseados.
Naturalmente es igualmente posible separar, p.ej. por destilación fraccionada, el componente m-alquilsubstituido y el componente p-alquilsubstituido de fórmula (I) y llevar de nuevo los demás subproductos a la masa de reacción para aumentar por isomerización el rendimiento de ambos componentes.
Como halogenuros de alquilo C1-C5 se consideran en el procedimiento conforme a la invención p.ej. bromuro de metilo, yoduro de metilo, bromuro de etilo, yoduro de etilo, cloruro de n-propilo, bromuro de n-propilo, yoduro de npropilo, cloruro de isopropilo, bromuro de isopropilo, cloruro de sec-butilo, bromuro de sec-butilo, cloruro de tercbutilo, bromuro de terc-butilo, cloruro de n-pentilo, bromuro de n-pentilo.
Son halogenuros de alquilo C1-C5 de fórmula (III) preferidos halogenuro de etilo, en especial bromuro de etilo y yoduro de etilo, halogenuro de isopropilo, en especial cloruro de isopropilo y bromuro de isopropilo, halogenuro de isobutilo, en especial cloruro de isobutilo y bromuro de isobutilo, halogenuro de terc-butilo, en especial cloruro de terc-butilo.
Es preferido un procedimiento para la preparación de fenilpropanoles m- ó p-substituidos de fórmula (IV) 5 en la que R1, R2, R3, R4 y R5 tienen los significados indicados debajo de la fórmula (I) , que está caracterizado porque se alquila un fenilpropanol no substituido de fórmula (V)
en la... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de fenilalcanoles m- ó p-substituidos de fórmula (I)
en la que R1 está unido al anillo de fenilo en la posición m ó p y significa alquilo C1-C5, y R2, R3, R4 y R5 significan independientemente entre sí hidrógeno o metilo, caracterizado porque se alquila un fenilalcanol no substituido de fórmula (II)
en la que R2, R3, R4 y R5 tienen los significados indicados debajo de la fórmula (I) junto con un halogenuro de 15 alquilo C1-C5 de fórmula (III)
R1-Hal (III) ,
en la que R1 tiene el significado indicado debajo de la fórmula (I) y Hal significa halógeno, en presencia de un catalizador de Friedel-Crafts dando una mezcla de fenilalcanoles m-y p-alquilsubstituidos de fórmula (I) , a continuación la mezcla de reacción se procesa y se separa el fenilalcanol m-alquilsubstituido de fórmula (I) deseado o el fenilalcanol p-alquilsubstituido de fórmula (I) deseado, los demás productos formados se reconducen a la mezcla de reacción y estos en presencia de un catalizador de Friedel-Crafts se isomerizan al fenilalcanol m- ó palquilsubstituido deseado.
2. Procedimiento conforme a la reivindicación 1 para la preparación de fenilalcanoles m- ó p-substituidos de fórmula (IV)
en la que R1, R2, R3, R4 y R5 tienen los significados indicados en la reivindicación 1, caracterizado porque se 30 alquila un fenilpropanol no substituido de fórmula (V)
en la que R2, R3, R4 y R5 tienen los significados indicados debajo de la fórmula (IV) junto con un halogenuro de alquilo C1-C5 de fórmula (III)
R1-Hal (III) ,
en la que R1 y Hal tienen los significados indicados en la reivindicación 1, en presencia de un catalizador de Friedel40 Crafts dando una mezcla de fenilpropanoles m- y p-alquilsubstituidos de fórmula (IV) , y a continuación la mezcla de
reacción se procesa y se separa el fenilpropanol m- ó p-alquilsubstituido de fórmula (IV) deseado, preferentemente por destilación, y los demás subproductos formados se reconducen a la mezcla de reacción y estos en presencia de un catalizador de Friedel-Crafts se isomerizan al fenilalcanol m- ó p-alquilsubstituido deseado.
3. Procedimiento conforme a una de las reivindicaciones 1 ó 2, caracterizado porque se parte de un fenilpropanol no substituido de fórmula (VI)
en la que R2 tiene el significado indicado en la reivindicación 1, este junto con un halogenuro de alquilo C1-C5 de fórmula (III)
R1-Hal (III) ,
en la que R1 y Hal tienen los significados indicados en la reivindicación 1, se hace reaccionar en presencia de un catalizador de Friedel-Crafts dando un fenilpropanol m- ó p-alquilsubstituido de fórmula (VII)
en la que R1 y R2 tienen los significados indicado debajo de las fórmulas (VI) y (III) , y a continuación la mezcla de reacción se procesa y se separa el fenilpropanol m- ó p-alquilsubstituido de fórmula (VII) deseado, preferentemente por destilación, y los demás subproductos formados se reconducen a la mezcla de reacción y estos en presencia de un catalizador de Friedel-Crafts se isomerizan al fenilpropanol m- ó p-alquilsubstituido deseado.
4. Procedimiento conforme a una de las reivindicaciones 1 a 3, caracterizado porque como halogenuro de alquilo C1-C5 se utiliza halogenuro de etilo, en especial bromuro de etilo y yoduro de etilo, halogenuro de isopropilo, en especial cloruro de isopropilo y bromuro de isopropilo, halogenuro de isobutilo, en especial cloruro de isobutilo y bromuro de isobutilo, o halogenuro de terc-butilo, en especial cloruro de terc-butilo.
5. Procedimiento conforme a una de las reivindicaciones 1 a 4, caracterizado porque como catalizador de Friedel-Crafts se usa AlCl3, AlBr3, TiCl4, ZrCl4, VCl3, ZnCl2, FeBr3, FeCl3.
6. Procedimiento conforme a la reivindicación 5, caracterizado porque como catalizador de Friedel-Crafts se usa AlCl3 o AlBr3.
7. Procedimiento conforme a una de las reivindicaciones 1 a 6, caracterizado porque el catalizador de Friedel-Crafts se utiliza en una cantidad de 1 a 200% en moles, en especial entre 33% y 110% en moles, referida a la cantidad en moles del fenilalcanol utilizado.
8. Procedimiento conforme a una de las reivindicaciones 1 a 6, caracterizado porque la alquilación se lleva a cabo a una temperatura entre 0 ºC y 100 ºC.
9. Procedimiento conforme a una de las reivindicaciones 1 a 8, caracterizado porque se hace reaccionar 2-metil-3fenilpropanol junto con halogenuro de terc-butilo, en especial cloruro de terc-butilo, en presencia de un catalizador de Friedel-Crafts, en especial en presencia de tricloruro de aluminio o tribromuro de aluminio, para obtener 2-metil-3 (3- ó 4-terc-butilfenil) propanol, y a continuación la mezcla de reacción se procesa y se separa el 2-metil-3- (3- ó 4terc-butilfenil) propanol deseado, preferentemente por destilación, y los demás subproductos formados se reconducen a la mezcla de reacción y estos en presencia de un catalizador de Friedel-Crafts se isomerizan al 2metil-3- (3- ó 4-terc-butilfenil) propanol deseado.
10. Procedimiento conforme a una de las reivindicaciones 1 a 9, caracterizado porque después del procesamiento de la mezcla de reacción se separa el producto de reacción m-substituido deseado.
11. Procedimiento para la preparación de substancias odoríferas de fórmula (VIII)
en la que R1 está unido al anillo de fenilo en la posición m ó p y significa alquilo C1-C5 y R2, R3, R4 y R5 significan independientemente entre sí hidrógeno o metilo, caracterizado porque se alquila un fenilalcanol no substituido de fórmula (II)
en la que R2, R3, R4 y R5 tienen los significados indicados debajo de la fórmula (VIII) junto con un halogenuro de alquilo C1-C5 de fórmula (III)
R1-Hal (III) ,
en la que R1 tiene el significado indicado debajo de la fórmula (VIII) y Hal significa halógeno, en presencia de un catalizador de Friedel-Crafts dando un fenilalcanol m- ó p-alquilsubstituido de fórmula (I)
en la que R1, R2, R3, R4 y R5 tienen los significados indicados debajo de la fórmula (VIII) , y a continuación la mezcla de reacción se procesa y se separa el fenilalcanol m- ó p-alquilsubstituido de fórmula (I) obtenido, preferentemente por destilación, y los demás subproductos formados se reconducen a la mezcla de reacción y estos en presencia de un catalizador de Friedel-Crafts se isomerizan al fenilalcanol m- ó p-alquilsubstituido deseado, y a continuación se transforma por oxidación o deshidrogenación en el fenilalcanal m- ó p-alquilsubstituido de fórmula (VIII) .
Patentes similares o relacionadas:
Proceso, del 7 de Agosto de 2019, de GIVAUDAN SA: Un proceso para formar un compuesto según la fórmula (I)**Fórmula** que comprende la etapa de funcionalizar regio-selectivamente un compuesto de dialquilbenceno**Fórmula** […]
Procedimientos de preparación de compuestos, tales como 3-arilbutanales, útiles en la síntesis de medetomidina, del 14 de Junio de 2019, de I-TECH AB: Procedimiento de preparación de un compuesto de fórmula I**Fórmula** en la que dicho procedimiento comprende hacer reaccionar un compuesto de fórmula II**Fórmula** […]
Compuestos capaces de liberar compuestos fragantes, del 30 de Noviembre de 2018, de GIVAUDAN SA: Utilización de un compuesto de fórmula (I)**Fórmula** como precursor para generar, por oxidación espontánea en aire, una cetona o aldehído de la […]
3-(4-isobutil-2-metilfenil)propanal como ingrediente de perfume, del 16 de Marzo de 2016, de GIVAUDAN SA: Compuesto según la fórmula (I)**Fórmula**
Método para la preparación de 2-(2,3-dimetilfenil)-1-propanal, del 27 de Enero de 2016, de LONZA LTD.: Un método para la preparación del compuesto de fórmula (XXI),**Fórmula** el método comprende una etapa (N); la etapa (N) comprende una reacción (N-reac); la reacción […]
Método para la preparación de 2-(2,3-dimetilfenil)-1-propanal con cloroacetona, del 30 de Diciembre de 2015, de LONZA LTD.: Método para la preparación de un compuesto de fórmula (XXI);**Fórmula** el método comprende dos etapas, los dos etapas que son una etapa (Q1) y una etapa (Q2); la etapa […]
Método de preparación de medetomidina, del 30 de Diciembre de 2015, de LONZA LTD.: Un método de preparación de medetomidina, el método comprende una etapa (N) y un etapa (M1); la etapa (M1) comprende una reacción (M1-reac); la reacción […]
Procedimiento para la obtención de alquiltoluenos m-substituidos mediante isomerización con líquidos iónicos como catalizadores, del 24 de Septiembre de 2014, de BASF SE: Procedimiento para la obtención de alquiltoluenos m-substituidos de la fórmula (I)**Fórmula** donde R1 significa alquilo con 1 a 5 átomos de carbono, […]