Compuesto de triazolopiridina, y acción del mismo como inhibidor de prolil-hidroxilasa e inductor de la producción de eritropoyetina.
Un compuesto representado por la siguiente fórmula [I], o una sal farmacéuticamente aceptable del mismo,
o un solvato del mismo:**fórmula**
en la que
la fórmula estructural parcial:**Fórmula**
es un grupo representado por cualquiera de las siguientes fórmulas:**Fórmula**
R1 es
(1) un átomo de hidrógeno,
(2) un grupo alquilo C1-6,
(3) un grupo arilo C6-14,
(4) un grupo cicloalquilo C3-8,
(5) un grupo aril C6-14-alquilo C1-6, o
(6) un grupo cicloalquil C3-8-alquilo C1-6;
R2 es
(1) un átomo de hidrógeno,
(2) un grupo alquilo C1-10,
(3) un grupo arilo C6-14 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B,
(4) un grupo cicloalquilo C3-8 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B,
(5) un grupo cicloalquenilo C3-8 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B,
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/JP2010/062037.
Solicitante: JAPAN TOBACCO INC..
Nacionalidad solicitante: Japón.
Dirección: 2-1, TORANOMON 2-CHOME, MINATO-KU TOKYO 105-8422 JAPON.
Inventor/es: ITO, TAKASHI, YOKOTA, MASAHIRO, ABE,HIROYUKI, MITANI,IKUO, OGOSHI,YOSUKE, MATSUI,TAKUYA, TERASHITA,MASAKAZU, MOTODA,DAI, UEYAMA,KAZUHITO, HOTTA,TAKAHIRO.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/437 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › conteniendo el sistema heterocíclico un ciclo de cinco eslabones teniendo el nitrógeno como heteroátomo del ciclo, p. ej. indolicina, beta-carbolina.
- A61P43/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
- A61P7/06 A61P […] › A61P 7/00 Medicamentos para el tratamiento de trastornos de la sangre o del fluido extracelular. › Antianémicos.
- C07D471/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 471/00 Compuestos heterocíclicos que contienen átomos de nitrógeno como únicos heteroátomos del sistema condensado, teniendo al menos un ciclo de seis miembros con un átomo de nitrógeno, no previstos en los grupos C07D 451/00 - C07D 463/00. › Sistemas condensados en orto.
PDF original: ES-2477968_T3.pdf
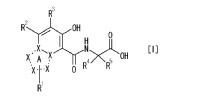
Fragmento de la descripción:
Compuesto de triazolopiridina, y acción del mismo como inhibidor de prolil-hidroxilasa e inductor de la producción de eritropoyetina
La presente invención se refiere a un novedoso compuesto de triazolopiridina que tiene una acción inhibidora de prolil-hidroxilasa (en lo sucesivo también se denomina PHD) y una capacidad inductora de la producción de eritropoyetina (en lo sucesivo también se denomina EPO). La presente invención también se refiere a un inhibidor de prolil-hidroxilasa (en lo sucesivo también se denomina inhibidor de PHD) y un agente inductor de la producción de eritropoyetina (en lo sucesivo también se denomina agente inductor de la producción de EPO), conteniendo cada uno el compuesto de triazolopiridina.
Técnica anterior
La EPO es una hormona que promueve el crecimiento de glóbulos rojos que consiste en 165 aminoácidos. La EPO se produce principalmente en el riñón y en parte en el hígado, y la producción de la misma aumenta bajo condiciones de bajo oxígeno.
La anemia se refiere a una afección que muestra bajos niveles de glóbulos rojos y hemoglobina en la sangre. Los síntomas de la misma se derivan de la deficiencia de oxígeno debida al reducido número de glóbulos rojos, o cambios de la circulación dinámica debido a la elevada frecuencia respiratoria y frecuencia cardíaca para compensar la deficiencia de oxígeno, e incluyen malestar general, fácilmente fatigado, respiración corta, palpitación, pesadez de la cabeza, mareo, mala cara, rigidez del hombro, dificultad para despertarse por la mañana y similares.
La causa de la anemia se divide ampliamente en baja producción, destrucción promovida y pérdida promovida de glóbulos rojos, y la anemia incluye anemia debida a anomalía de la hematopoyesis en la médula ósea, anemia debida a falta de hierro, vitamina B12 o ácido fólico, hemorragia durante accidente u operación, anemia asociada a inflamación crónica (enfermedades autoinmunitarias, tumor maligno, enfermedades crónicamente transmitidas, discrasia de células plasmáticas, etc.), anemia asociada a enfermedades endocrinas (hipotiroidismo, síndrome poliglandular autoinmune, diabetes tipo IA, hemorragia uterina disfuncional, etc.), anemia asociada a insuficiencia cardíaca crónica, anemia asociada a úlcera, anemia asociada a enfermedades hepáticas, anemia senil, anemia inducida por fármacos, anemia renal (anemia asociada a insuficiencia renal), anemia asociada a quimioterapia y similares.
En 1989, una preparación de EPO humana recombinante génica fue autorizada por la Agencia Estadounidense del medicamento (FDA) para aplicación a anemia renal, anemia asociada a tratamiento con AZT de pacientes con VIH, anemia asociada a quimioterapia de pacientes con cáncer, o para la reducción del volumen de transfusión de sangre para pacientes que se someten a una operación. Además, su aplicación se ha extendido a anemia del prematuro y similares.
La anemia renal se trata con un agente estimulante de la eritropoyesis (ESA). La anemia renal se produce principalmente por la disminución de la producción de EPO en las células intersticiales en la periferia de túbulos renales del riñón. Es una aplicación en la que la eritropoyetina humana recombinante génica se usa muy frecuentemente para suplemento de EPO. La eritropoyetina humana recombinante génica ha reducido impresionantemente el número de pacientes en necesidad de transfusión periódica de sangre, mejoró diversos síntomas asociados a la anemia y contribuyó enormemente a la mejora de ADL (actividades de la vida diaria) y QOL (calidad de vida). Por otra parte, siendo una preparación biológica, es cara y requiere altos gastos médicos. Además, tiene una semivida corta en la sangre y requiere administración intravenosa de 2 - 3 veces por semana del circuito de diálisis en pacientes en hemodiálisis. Así, se desea disminuir la frecuencia de inyección para prevenir accidentes médicos, y también desde el punto de vista de la cantidad de práctica médica y residuos. Además, para pacientes en diálisis peritoneal y pacientes con insuficiencia renal en periodo de prediálisis, para los que se ha empleado la administración subcutánea que proporciona un mayor periodo de duración, todavía es necesaria una vez cada una o dos semanas de administración. En este caso, los pacientes frecuentemente necesitan ir al hospital solo para la administración de la eritropoyetina humana recombinante génica, causando una carga a los pacientes.
Además, se ha desarrollado un medicamento de EPO de acción prolongada que tiene una semivida prolongada en sangre mediante inyección intravenosa o inyección subcutánea modificando EPO añadiendo una nueva cadena de azúcar o cadena de PEG. Sin embargo, como solo se han desarrollado preparaciones para inyección, se desea una ESA administrable por vía oral para prevenir accidentes médicos y reducir la carga a los pacientes.
Además, se espera que un ESA administrable por vía oral se administre a un intervalo más amplio de tratamientos para no solo anemia renal, sino también anemia producida por diversas causas.
Como molécula representativa que promueve la transcripción de EPO puede mencionarse el factor inducible de hipoxia (en lo sucesivo también se denomina HIF). El HIF es una proteína que consiste en un heterodímero que tiene una subunidad a reguladora del oxígeno y una subunidad (5 constitucionalmente expresada, en la que la prolina en la subunidad a se hidroxila por prolil-hidroxilasa (PHD) en presencia de oxígeno y la subunidad a resultante está
unida a protema von Hippel-Lindau (VHL) y ubiquitinada. Sin embargo, como la subunidad a no se somete a hidroxilación por PHD bajo condiciones de bajo oxigeno, no está ubiquitinada pero sí unida a un elemento de respuesta a hipoxia intranuclear (HRE) para promover la transcripción de EPO presente aguas debajo de HIF. Por tanto, la inhibición de la actividad de PHD produce la prevención de la ubiquitinación de HIF y estabilización de la misma. Por consiguiente, aumenta la producción de EPO.
Ejemplos de las enfermedades que se espera mejoren Inhibiendo PHD para estabilizar HIF Incluyen enfermedades cardiacas Isquémicas (angina de pecho, Infarto de miocardio, etc.), trastornos cerebrovasculares isquémicos (Infarto cerebral, embolia cerebral, ataque isquémico cerebral transitorio, etc.), insuficiencias renales crónicas (nefropatla isquémica, trastorno intersticial de los tribuios renales, etc.), complicaciones diabéticas (herida diabética, etc.), deterioros cognltlvos (demencia, enfermedad de Alzhelmer, enfermedad de Parkinson, enfermedad de Huntlngton etc.) y similares.
Resumen de la invención
Problemas a resolver por la invención
De los hallazgos obtenidos de los estudios hasta ahora se ha dilucidado que un medicamento que inhibe prolil- hidroxllasa (PHD) promueve la producción de erltropoyetina (EPO) y es eficaz para la profilaxis o tratamiento de diversas enfermedades y patologías (trastornos) producidas por la disminución de la producción de EPO, particularmente para el tratamiento de anemia.
Por consiguiente, la presente invención tiene como objetivo proporcionar un medicamento que tiene una acción inhibidora de prolil-hidroxilasa (PHD). Además, la presente invención tiene como objetivo proporcionar un medicamento que tiene capacidad inductora de la producción de EPO.
Se han desvelado inhibidores de prolil-hidroxilasa en los documentos JP1132257, W27/1395, W27/13699, W27/1511, W28/8952, W28/136, W29/73497.
Medios para solucionar los problemas
Los presentes inventores han encontrado un compuesto que tiene una acción inhibidora de prolil-hidroxilasa (PHD) y capacidad inductora de la producción de EPO, y completado la presente invención.
Más particularmente, la presente invención proporciona lo siguiente.
[1 ] Un compuesto representado por la siguiente fórmula [I] (en lo sucesivo también se denomina el compuesto de la presente Invención) o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo:
R
en la que
la fórmula estructural parcial:
R1 es
(1) un átomo de hidrógeno,
(2) un grupo alquilo Ci_6,
(3) un grupo arilo Ce-14,
(4) un grupo cicloalquilo C3-8,
(5) un grupo aril C6-i4-alquilo C1.6, o
(6) un grupo cicloalquil C3-8-alquilo C1-6;
R2 es
(1) un átomo de hidrógeno,
(2) un grupo alquilo C-mo,
(3) un grupo arilo C6-14 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B,
(4) un grupo cicloalquilo C3-8 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto representado por la siguiente fórmula [I], o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo:
R3
en la que
la fórmula estructural parcial:
R1
es un grupo representado por cualquiera de las siguientes fórmulas:
(1) un átomo de hidrógeno,
(2) un grupo alquilo C-ue,
(3) un grupo arilo Ce-14,
(4) un grupo cicloalquilo C3-8,
(5) un grupo aril C6-i4-alquilo C-ue, o
(6) un grupo cicloalquil C3-8-alquilo Ci_e;
R2 es
(1) un átomo de hidrógeno,
(2) un grupo alquilo C-mo,
(3) un grupo arilo Ce-14 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyeles diferentes seleccionados del siguiente grupo B,
(4) un grupo cicloalquilo C3.8 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyeles diferentes seleccionados del siguiente grupo B,
(5) un grupo cicloalquenllo C3.8 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B,
(6) un grupo heteroarilo opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B (en el que el heteroarilo tiene, además de átomos de carbono, 1 a 6 heteroátomos seleccionados de átomo de nitrógeno, átomo de oxígeno y átomo de azufre),
(7) un grupo aril C6-i4-alquilo Ci.6 (en el que arilo C6-14 está opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B), o
(8) un grupo cicloalquil C3-8-alquilo Ci.6 (en el que cicloalquilo C3-8 está opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B);
(1) un átomo de hidrógeno,
(2) un átomo de halógeno,
(3) un grupo alquilo C-ue,
(4) un grupo arilo Ce-14,
(5) un grupo cicloalquilo C3_8, o
(6) un grupo aril C6-i4-alquilo Ci_6; y
R4 y R5 son cada uno independientemente
(1) un átomo de hidrógeno, o
(2) un grupo alquilo C-ue, grupo B:
(a) un átomo de halógeno,
(b) un grupo alquilo Ci.e,
(c) un grupo cicloalquilo C3.8,
(d) un grupo clano, y
(e) un grupo halo-alquilo Ci.6.
2. El compuesto según la reivindicación 1, en el que la fórmula estructural parcial:
es un grupo representado por la siguiente fórmula
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
3. El compuesto según la reivindicación 1, en el que la fórmula estructural parcial:
es un grupo representado por la siguiente fórmula
N
\
N
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
4. El compuesto según la reivindicación 1, en el que la fórmula estructural parcial:
\ A ,x X+*X
R1
es un grupo representado por la siguiente fórmula
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
5. El compuesto según la reivindicación 1, en el que la fórmula estructural parcial:
,'X'Y
\ A ,X
'-X
Y N=N
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
6. El compuesto según una cualquiera de las reivindicaciones 1 a 5, en el que tanto R4 como R5 son átomos de hidrógeno, o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
7. El compuesto según una cualquiera de las reivindicaciones 1 a 5, en el que R3 es un átomo de sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
8. El compuesto según una cualquiera de las reivindicaciones 1 a 5, en el que R1 es un átomo de sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
9. El compuesto según una cualquiera de las reivindicaciones 1 a 5, en el que R2es
(1) un grupo alquilo C-mo,
(2) un grupo arilo Ce-14 opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del grupo B anteriormente mencionado,
(3) un grupo aril C6-i4-alquilo Ci_6 (en el que arilo Ce-14 está opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del grupo B anteriormente mencionado), o
(4) un grupo cicloalquil C3-8-alquilo Ci_6 (en el que cicloalquilo C3-8 está opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del grupo B anteriormente mencionado),
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
1. El compuesto según la reivindicación 2, en el que tanto R4 como R5 son átomos de hidrógeno, o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
11. El compuesto según la reivindicación 1, en el que R3 es un átomo aceptable del mismo, o un solvato del mismo.
12. El compuesto según la reivindicación 11, en el que R1 es un átomo aceptable del mismo, o un solvato del mismo.
13. El compuesto según la reivindicación 12, en el que R2 es
(1) un grupo alquilo C-mo, o
(2) un grupo aril C6-i4-alquilo Ci_6 (en el que arilo Ce-14 está opclonalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del grupo B anteriormente mencionado),
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
14. Un compuesto según la reivindicación 1 representado por la siguiente fórmula [1-1] o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo:
de hidrógeno, o una sal farmacéuticamente de hidrógeno, o una sal farmacéuticamente
hidrógeno, o una hidrógeno, o una
[M]
en la que la fórmula estructural parcial:
-y1
es un grupo representado por cualquiera de las siguientes fórmulas:
R11 es
(1) un átomo de hidrógeno,
(2) un grupo alquilo C-ue,
(3) un grupo fenilo,
(4) un grupo clcloalqullo C3-8,
(5) un grupo fenll-alqullo Ci.e, o
(6) un grupo cicloalqull C3-s-alqu¡lo C-i-e;
R21 es
(1) un átomo de hidrógeno,
(2) un grupo alquilo C-mo,
(3) un grupo fenilo opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B,
(4) un grupo cicloalquilo C3-8,
(5) un grupo cicloalquenilo C3-8,
(6) un grupo tienilo opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B,
(7) un grupo fenil-alquilo Cve (en el que fenilo está opcionalmente sustituido con el mismo sustituyente o 1 a 5 sustituyentes diferentes seleccionados del siguiente grupo B), o
(8) un grupo cicloalqull C3-s-alquilo Cve;
R31 es
(1) un átomo de hidrógeno,
(2) un átomo de halógeno,
(3) un grupo alquilo C1.6,
(4) un grupo fenilo,
(5) un grupo cicloalquilo C3-8, o
(6) un grupo fenil-alquilo Ci-6¡ y R41 y R51 son cada uno independientemente
(1) un átomo de hidrógeno, o
(2) un grupo alquilo C1.6,
grupo B:
(a) un átomo de halógeno,
(b) un grupo alquilo C1.6,
(c) un grupo cicloalquilo C3-8,
(d) un grupo ciano, y
(e) un grupo halo-alquilo Ci-6.
15. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
16. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
17. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
18. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
F
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
2. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
21. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
22. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
24. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
25. Un compuesto según la reivindicación 1 representado por la siguiente fórmula:
o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
26. Una composición farmacéutica que comprende el compuesto según una cualquiera de las reivindicaciones 1 a
25, o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo, y un vehículo farmacéuticamente aceptable.
27. Un agente terapéutico para su uso en el tratamiento de anemia que comprende el compuesto según una cualquiera de las reivindicaciones 1 a 25, o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
28. Un agente terapéutico para su uso en el tratamiento de anemia renal que comprende el compuesto según una
cualquiera de las reivindicaciones 1 a 25, o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo.
29. Use del compuesto según una cualquiera de las reivindicaciones 1 a 25, o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo, para la producción de un agente terapéutico para anemia.
3. Use del compuesto según una cualquiera de las reivindicaciones 1 a 25, o una sal farmacéuticamente aceptable 2 del mismo, o un solvato del mismo, para la producción de un agente terapéutico para anemia renal.
31. Un compuesto según una cualquiera de las reivindicaciones 1 a 25, o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo, para su uso en el tratamiento de anemia.
32. Un compuesto según una cualquiera de las reivindicaciones 1 a 25, o una sal farmacéuticamente aceptable del mismo, o un solvato del mismo, para su uso en el tratamiento de anemia renal.
33. Un envase comercial que comprende la composición farmacéutica según la reivindicación 26 y un material escrito asociado al mismo, material escrito que establece que la composición farmacéutica puede o debe usarse para el tratamiento o profilaxis de una enfermedad seleccionada de anemia y anemia renal.
34. Un kit que comprende la composición farmacéutica según la reivindicación 26 y un material escrito asociado al 5 mismo, material escrito que establece que la composición farmacéutica puede o debe usarse para el tratamiento o
profilaxis de una enfermedad seleccionada de anemia y anemia renal.
Patentes similares o relacionadas:
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
 Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]
Compuestos utilizados como inhibidores de la quinasa reordenada durante la transfección (RET), del 1 de Julio de 2020, de GlaxoSmithKline Intellectual Property Development Limited: Un compuesto de acuerdo con la Fórmula (I), o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en donde: X es N o CR5; Y es un enlace; […]
Derivado de dihidroindolizinona, del 1 de Julio de 2020, de ONO PHARMACEUTICAL CO., LTD.: (3S)-3-[2-(6-amino-2-fluoro-3-piridinil)-4-fluoro-1H-imidazol-5-il]-7-[5-cloro-2-(1H-tetrazol-1-il)fenil]-2,3-dihidro- (1H)-indolizinona, una…
Inhibidor de fibrosis, del 1 de Julio de 2020, de NIPPON SHINYAKU CO., LTD.: Composición farmacéutica que comprende un derivado heterocíclico seleccionado de ácido 2-{4-[N-(5,6-difenilpirazin-2-il)-N-isopropilamino]butiloxi}acético […]
Métodos de monitorización terapéutica de profármacos de ácido fenilacético, del 24 de Junio de 2020, de Immedica Pharma AB: Glicerilo tri-[4-fenilbutirato] (HPN-100) para su uso en un método para tratar un trastorno del ciclo de la urea en un sujeto que tiene discapacidad […]