Composiciones farmacéuticas que comprenden un profármaco inhibidor de la polimerasa del VHC.
Composición farmacéutica que comprende el compuesto 1 proporcionado a continuación:
**Fórmula**
presente en una cantidad comprendida entre aproximadamente 50% p/p y 95% p/p, hidroxipropilcelulosa presente en una cantidad comprendida entre 1% p/p y 4% p/p, y por lo menos un excipiente presente en una cantidad de, como máximo, 49% p/p.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/050182.
Solicitante: F. HOFFMANN-LA ROCHE AG.
Inventor/es: SHAH, NAVNIT, HARGOVINDAS, SANDHU, HARPREET K., CHATTERJI,ASHISH, DESAI,DIPEN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/513 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo grupos oxo unidos directamente al heterociclo, p. ej. citosina.
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
PDF original: ES-2513415_T3.pdf




Fragmento de la descripción:
Composiciones farmacéuticas que comprenden un profármaco inhibidor de la polimerasa del VHC
La presente invención proporciona nuevas formulaciones de (2R, 3R, 4R, 5R) -5- (4-amino-2-oxo-2H-pirimidín-1-il) -4fluoro-2-isobutiriloximetil-4-metil-tetrahidro-furán-3-il éster de ácido isobutírico e hidroxipropilcelulosa que proporcionan una elevada densidad aparente y un tamaño de gránulo reducido más adecuados para una compresión y flujo mejorados y para perfiles de disolución rápida.
El (2R, 3R, 4R, 5R) -5- (4-amino-2-oxo-2H-pirimidín-1-il) -4-fluoro-2-isobutiriloximetil-4-metil-tetrahidro-furán-3-il éster de ácido isobutírico (compuesto 1) es un profármaco inhibidor de la polimerasa del virus de la hepatitis C (VHC) . El compuesto 1 puede prepararse tal como se describe en la patente WO nº 2007/065829. El virus de la hepatitis C es una enfermedad infecciosa transmitida por la sangre que afecta al hígado. La infección con frecuencia es asintomática, aunque, tras establecerse, la infección crónica puede provocar la inflamación del hígado (hepatitis crónica) . No se encuentra disponible ninguna vacuna contra el virus de la hepatitis C.
NH2 O O
ON
N
O
O
F
O
Compuesto 1
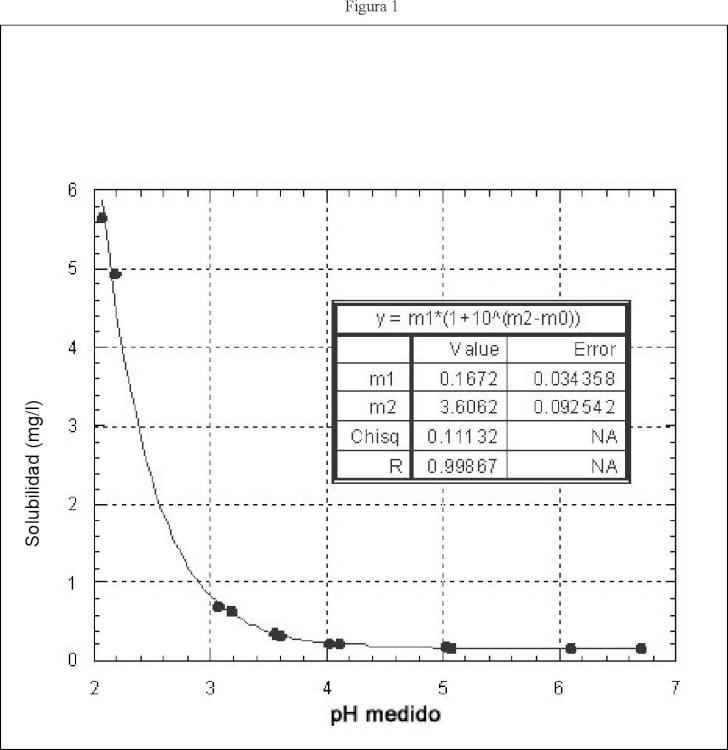
Se está evaluando clínicamente el compuesto 1 para el tratamiento de la infección hepática causada por el virus de la hepatitis C. La dosis diaria estimada es de 1 a 2 g, requiriendo que el producto farmacéutico presente una carga de fármaco elevada para conseguir el mejor régimen de tratamiento para el paciente. El compuesto 1 es una base débil con una pKa de 3, 5, requiriendo de esta manera que el producto farmacéutico presente un perfil de liberación inmediata (IR) para superar las limitaciones de solubilidad dependiente del pH (ver la figura 1) . Tal como se muestra en la figura 1, la solubilidad del fármaco cae drásticamente a pH>4, sugiriendo que la absorción del fármaco podría encontrarse limitada por la tasa de disolución a pHs fisiológicamente relevantes. La dosis elevada y la necesidad de un perfil de liberación inmediata se complican adicionalmente por la reducida densidad aparente de la sustancia farmacológica (0, 04 a 0, 3 g/cm3) . Las tecnologías convencionales de fabricación que hacen uso de excipientes de utilización común requieren la utilización de múltiples etapas de densificación, así como de cantidades elevadas de excipientes, tales como ligantes. Además del procedimiento multietapa de fabricación, la elevada utilización de ligante presenta un impacto negativo sobre la disolución del producto, resultando en una biodisponibilidad más baja.
La disponibilidad de productos farmacéuticos que puedan fabricarse comercialmente y que proporcionen el mejor modo de tratamiento para el paciente es un componente crucial del proceso de desarrollo de un fármaco. La seguridad, eficacia y aceptabilidad del fármaco pueden resultar significativamente influidas por la selección de la forma de dosificación, que depende de la dosis y de las propiedades fisicoquímicas y biofarmacéuticas del agente terapéuticamente activo. La utilización de las tecnologías de fabricación apropiadas y de excipientes farmacéuticamente aceptables puede resolver muchos problemas comunes en dichos compuestos. Por ejemplo, entre los enfoques utilizados con frecuencia para resolver los problemas biofarmacéuticos se incluyen tecnologías tales como la reducción del tamaño de partícula, la disolución en lípidos, la conversión a dispersiones sólidas o la utilización de formas amorías. De manera similar, existen enfoques bien establecidos para controlar las malas propiedades de los particulados, por ejemplo las propiedades de flujo y de compactación, mediante la mezcla con excipientes y su procesamiento, por ejemplo mediante granulación y mediante la separación por tamaño de las partículas. Algunas tecnologías de fabricación tales como la granulación (seca/húmeda) , la granulación en lecho fluido y la granulación de alto cizallamiento son enfoques utilizados comúnmente para resolver las dificultades de fabricación relacionadas con el flujo, la uniformidad del contenido y la compresión. De manera similar, se dispone de muchas tecnologías para resolver propiedades biofarmacéuticas pobres de los compuestos. Aunque se encuentran disponibles muchas tecnologías para resolver dichos problemas, la combinación de estos retos, tales como la dosis, la solubilidad y las propiedades fisicoquímicas pobres, puede comportar dificultades insuperables durante el desarrollo de productos adecuados. Por consiguiente, con frecuencia se utilizan nuevos enfoques para formular dichos productos, para conseguir resultados óptimos con respecto a la fabricabilidad, estabilidad, biodisponibilidad y comodidad para el paciente.
La presente invención proporciona una composición que comprende el compuesto 1, proporcionado a continuación:
presente en una cantidad comprendida entre aproximadamente 50% p/p y aproximadamente 95% p/p, hidroxipropilcelulosa presente en una cantidad comprendida entre aproximadamente 1% p/p y aproximadamente 4% p/p, y por lo menos un excipiente presente en una cantidad de, como máximo, aproximadamente 49% p/p. El excipiente puede seleccionarse de entre el grupo que consiste de adyuvantes de compresión, desintegrantes, glidantes, lubricantes, agentes de recubrimiento con película y mezclas de los mismos.
La figura 1 proporciona un gráfico que ilustra el perfil de solubilidad según el pH del compuesto 1 a temperatura ambiente.
La figura 2 proporciona un gráfico que ilustra el efecto del tipo de ligante y de su concentración sobre la densidad aparente de gránulos de compuesto 1.
La figura 3 proporciona un gráfico que ilustra el efecto del tipo de ligante y de su concentración sobre los perfiles de compresión de compuesto 1.
La figura 4 proporciona un gráfico que ilustra el efecto del tipo de ligante y de su concentración sobre el perfil de disolución in vitro (aparato USP II, 37º C, 50 rpm en 1.000 ml de HCl 0, 005 N) de compuesto 1.
La figura 5 proporciona un gráfico que ilustra el efecto del grado de la hidroxipropilcelulosa sobre el tamaño acumulativo de gránulo, medido utilizando un tamiz acústico ATM con la amplitud fijada a 6 durante 7 minutos, del compuesto 1.
La figura 6 proporciona un gráfico que ilustra el efecto de diferentes grados de hidroxipropilcelulosa sobre los perfiles de compresión, medidos utilizando un simulador de compactación Presstor® que simulaba Fette 2090 a 50 rpm, de compuesto 1.
La figura 7 proporciona un gráfico que ilustra el efecto de diferentes grados de hidroxipropilcelulosa sobre los perfiles de disolución de compuesto 1.
La figura 8 proporciona un gráfico que ilustra el efecto del método de adición de ligante sobre los perfiles de disolución de compuesto 1.
La presente invención proporciona formulaciones de compuesto 1 con hidroxipropilcelulosa (HPC) como ligante que resuelven muchos problemas no deseables asociados al procesamiento y comportamiento del compuesto 1 y permiten la fabricación de formas de dosificación cómodas para el paciente. Las características clave de la presente invención son: (a) la utilización de hidroxipropilcelulosa como ligante al nivel de entre 1% y 4% p/p, (b) la carga de compuesto 1 al nivel de entre 50% y 95% p/p en el producto final, (c) la utilización de hidroxipropilcelulosa como agente activo en superficie, (d) una composición global y un procedimiento de preparación de la forma de dosificación final, (e) un perfil de disolución que proporciona un 80% de liberación de la unidad de dosificación del compuesto 1 en menos de 45 minutos, y (f) una biodisponibilidad mejorada del compuesto 1 en comparación con formulaciones preparadas utilizando métodos alternativos. El desarrollo de formas de dosificación adecuadas de compuesto 1 requiere la utilización de excipientes altamente funcionales que puedan proporcionar los atributos anteriormente indicados del compuesto 1 a niveles bajos de utilización. Se requieren ligantes convencionales al nivel de entre 5% y 10% p/p con el fin de proporcionar una densificación adecuada del compuesto 1, reduciendo de esta manera la carga farmacológica de compuesto 1 en el producto final. Inesperadamente, para el compuesto 1, se encontró que la hidroxipropilcelulosa proporcionaba la densidad de gránulos requerida con un nivel de ligante de tan sólo 1% a 4% p/p.
Tal como se utiliza en la presente invención, los términos y expresiones siguientes presentan los significados proporcionados a continuación.
El término “API” se refiere al ingrediente farmacéutico activo.
El término “excipientes” se... [Seguir leyendo]
Reivindicaciones:
1. Composición farmacéutica que comprende el compuesto 1 proporcionado a continuación:
NH2 O
O
N
NO
O
O
F
O
presente en una cantidad comprendida entre aproximadamente 50% p/p y 95% p/p, hidroxipropilcelulosa presente en una cantidad comprendida entre 1% p/p y 4% p/p, y por lo menos un excipiente presente en una cantidad de, como máximo, 49% p/p.
2. Composición farmacéutica según la reivindicación 1, en la que el compuesto 1 se encuentra presente en una cantidad comprendida entre 60% p/p y 90% p/p.
3. Composición farmacéutica según la reivindicación 2, en la que el compuesto 1 se encuentra presente en una cantidad comprendida entre 70% p/p y 85% p/p. 15
4. Composición farmacéutica según las reivindicaciones 1 a 3, en la que hidroxipropilcelulosa se encuentra presente en una cantidad comprendida entre 1, 5% p/p y 4% p/p.
5. Composición farmacéutica según la reivindicación 4, en la que hidroxipropilcelulosa se encuentra presente en una 20 cantidad comprendida entre 2% p/p y 3% p/p.
6. Composición farmacéutica según cualquiera de las reivindicaciones 1 a 5, en la que el excipiente se selecciona de entre el grupo que consiste de adyuvantes de compresión, desintegrantes, glidantes, lubricantes, agentes de recubrimiento con película y mezclas de los mismos.
7. Composición farmacéutica según la reivindicación 6, en la que el adyuvante de compresión se selecciona de entre el grupo que consiste de lactosa monohidrato, celulosa microcristalina, almidón 1500 y lactosa anhidra.
8. Composición farmacéutica según la reivindicación 7, en la que el adyuvante de compresión se encuentra presente 30 en una cantidad de, como máximo, 49% p/p.
9. Composición farmacéutica según la reivindicación 6, en la que el desintegrante se selecciona de entre el grupo que consiste de croscarmelosa sódica, crospovidona, almidón, celulosa e hidroxipropilcelulosa de baja sustitución.
10. Composición farmacéutica según la reivindicación 9, en la que el desintegrante se encuentra presente en una cantidad de, como máximo, 10% p/p.
11. Composición farmacéutica según la reivindicación 6, en la que el glidante se selecciona de entre el grupo que consiste de talco, dióxido de silicio coloidal y almidón de maíz. 40
12. Composición farmacéutica según la reivindicación 11, en la que el glidante se encuentra presente en una cantidad de, como máximo, aproximadamente 5% p/p.
13. Composición farmacéutica según la reivindicación 6, en la que el lubricante se selecciona de entre el grupo que
consiste de estearato de magnesio, ácido esteárico, aceite hidrogenado, polietilenglicol, estearil-fumarato sódico y behenato de glicerilo.
14. Composición farmacéutica según la reivindicación 13, en la que el lubricante se encuentra presente en una cantidad de, como máximo, 2% p/p. 50
15. Composición farmacéutica según la reivindicación 6, en la que el agente de recubrimiento con película se selecciona de entre el grupo que consiste de recubrimiento basado en hipromelosa o alcohol polivinílico de dióxido de titanio y talco.
16. Composición farmacéutica según la reivindicación 15, en la que el recubrimiento se encuentra presente en una cantidad de, como máximo, 5% p/p.
17. Composición farmacéutica según cualquiera de las reivindicaciones 1 a 16, en la que la composición se
encuentra en forma granular y presenta una densidad aparente de aproximadamente 0, 35 g/cm3 o superior.
18. Composición farmacéutica según cualquiera de las reivindicaciones 1 a 17, en la que la hidroxipropilcelulosa presenta una viscosidad comprendida en el intervalo de entre 5 y 1.500 mPa·s a una concentración de entre 1% y 5 5% p/p en agua a 25º C con un peso molecular comprendido en el intervalo de entre 80.000 y 1.150.000 daltons.
19. Composición farmacéutica según cualquiera de las reivindicaciones 1 a 18, en la que la composición se presenta en forma de tableta.
20. Utilización de una composición según cualquiera de las reivindicaciones 1 a 19 para uso en el tratamiento de una enfermedad mediada por el virus de la hepatitis C (VHC) .
21. Composiciones farmacéuticas según cualquiera de las reivindicaciones 1 a 19 para la utilización en terapia.
Figura 1
Solubilidad (mg/l)
Figura 2
Figura 3
4/
Figura 4
Figura 5
Figura 6
Figura 7 Efecto de diferentes grados de hidroxipropilcelulosa sobre los perfiles de disolución
Figura 8
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Formulación de vitamina D de liberación modificada estabilizada y método de administración de la misma, del 22 de Julio de 2020, de EirGen Pharma Ltd: Una formulacion oral de liberacion controlada de un compuesto de vitamina D que comprende uno o ambos de 25- hidroxivitamina D2 y 25-hidroxivitamina D3, la formulacion […]
Métodos y composiciones para la administración oral de proteínas, del 22 de Julio de 2020, de Entera Bio Ltd: Una única composición farmacéutica oral que comprende una proteína que tiene un peso molecular de hasta 100.000 Daltons, siendo dicha proteína PTH; […]
Composición farmacéutica que comprende un agente antipsicótico atípico y método para su preparación, del 15 de Julio de 2020, de PHARMATHEN S.A.: Comprimido de liberación controlada de Paliperidona en forma de comprimido de varias capas que comprende: a) un núcleo de matriz que comprende […]
Composiciones y métodos para tratar el virus de la hepatitis C, del 15 de Julio de 2020, de Gilead Pharmasset LLC: Una composición farmacéutica que comprende: a) de aproximadamente el 25% a aproximadamente el 35% p/p de GS-7977 cristalino que tiene la estructura **(Ver […]
Macrogols para aplicación a la mucosa, y sus usos terapéuticos, del 15 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Composición farmacéutica en forma sólida que comprende, por unidad de dosificación, entre 5 y 400 mg de un PEG con un grado de 3000 o más, para uso en el tratamiento […]
Composición farmacéutica novedosa, del 1 de Julio de 2020, de NOVARTIS AG: Un comprimido farmaceutico que comprende: a) un farmaco que es el solvato con sulfoxido de dimetilo de N-{3-[3-ciclopropil-5-(2-fluoro-4-5 yodofenilamino)-6,8- dimetil-2,4,7-trioxo-3,4,6,7-tetrahidro-2H-pirido[4,3-d]pirimidin-1-il]fenil}acetamida […]
Preparación para el control del peso corporal a base de quitosano y celulosa, del 1 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Una composición oral sólida que contiene una combinación de quitosano de hongos o levaduras, celulosa amorfa en polvo y opcionalmente excipientes.