Combinación de ADNasa I y glucosaminoglucanos para su uso en limpieza de ADN extracelular.
Uso de un glucosaminoglucano o una sal fisiológicamente aceptable del mismo en la fabricación de un medicamento destinado al tratamiento de un sujeto con un trastorno caracterizado por la presencia de ADN extracelular endógeno,
en el que el sujeto es sometido 5 también a tratamiento con una ADNasa I, tal que el glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 8 a 40 kd y el glucosaminoglucano o la sal del mismo incrementa la actividad de la ADNasa I, en el que el trastorno es:
(a) Un trastorno respiratorio caracterizado por la presencia de ADN extracelular endógeno en el pulmón;
(b) Seleccionado entre fibrosis quística, enfermedad pulmonar obstructiva crónica y neumonía;
(c) Lupus eritematoso sistémico (LES); o
(d) Un trastorno caracterizado por la presencia de ADN extracelular endógeno en un sitio inflamatorio.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2003/000668.
Solicitante: OCKHAM BIOTECH LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: Manor Farm, 98 Swanwick Lane Swanwick Hampshire SO31 7HA REINO UNIDO.
Inventor/es: SHUTE,JANIS KAY, HOCKEY,PETER MOREY, CARROLL,MARY PATRICIA, DR. CONWAY,JOY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/726 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Glicosaminoglicanos, es decir mucopolisacáridos (sulfato de condroitina, sulfato de dermatano A61K 31/737).
- A61K31/727 A61K 31/00 […] › Heparina; Heparano.
- A61K31/728 A61K 31/00 […] › Acido hialurónico.
- A61K31/737 A61K 31/00 […] › Polisacáridos sulfatados, p. ej. sulfato de condroitina, sulfato de dermatano (A61K 31/727 tiene prioridad).
- A61K38/46 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Hidrolasas (3).
- A61K47/36 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Polisacáridos; Sus derivados, p. ej. gomas o resinas, almidón, alginato, dextrina, ácido hialurónico, quitosano, inulina, agar o pectina.
- A61K9/00 A61K […] › Preparaciones medicinales caracterizadas por un aspecto particular.
- A61P11/12 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 11/00 Medicamentos para el tratamiento de trastornos del aparato respiratorio. › Mucolíticos.
- A61P43/00 A61P […] › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
PDF original: ES-2527096_T3.pdf

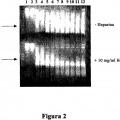


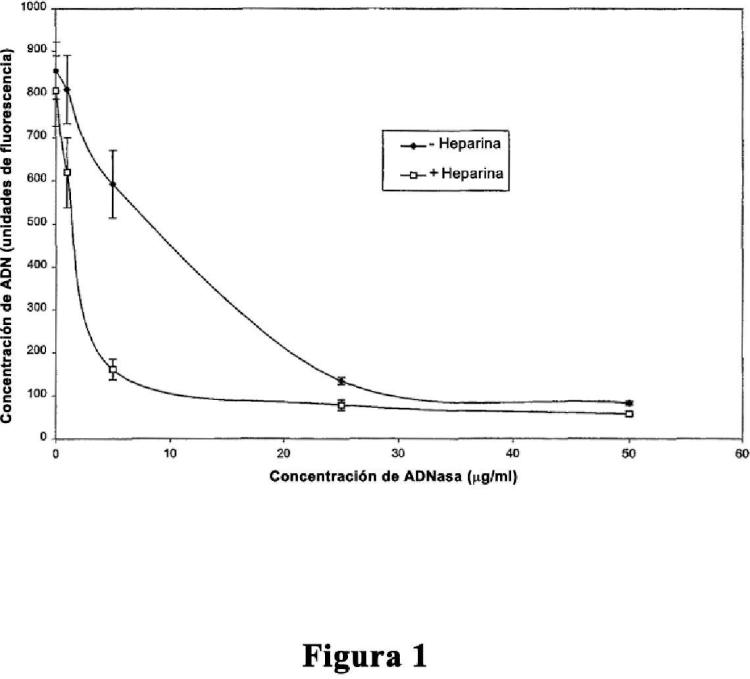
Fragmento de la descripción:
Combinación de ADNasa I y glucosaminoglucanos para su uso en limpieza de ADN extracelular
Campo de la invención La presente invención se describe en las reivindicaciones 1 a 21 y se refiere a ADNasa I y en particular al uso de ADNasa I en el tratamiento de trastornos caracterizados por la presencia de ADN extracelular endógeno.
Antecedentes de la invención Las ADNasas son un grupo de enzimas de fosfodiesterasa capaces de hidrolizar el ADN. Actúan de una forma inespecífica, ya que no necesitan la presencia de una secuencia específica en la molécula diana y son capaces de degradar extensamente moléculas de ADN escindiéndolas múltiples veces. Los dos tipos principales de ADNasas son las enzimas de tipo ADNasa I y ADNasa II. Existen también enzimas de tipo ADNasa tipo III. La ADNasa I necesita cationes para estar activa y tiene un pH óptimo casi neutro. Hidroliza el ADN para producir nucleótidos de fosfato en 5’. La ADNasa II puede activarse mediante cationes divalentes y tiene un pH ácido óptimo. Hidroliza el ADN para producir nucleótidos de fosfato en 3’.
Clínicamente se piensa sobre todo que las ADNasas, y en particular la ADNasa I, son útiles en el tratamiento de trastornos respiratorios y en la actualidad se usan para tratar la fibrosis quística. Se ha sugerido que las ADNasas también pueden ser útiles en el tratamiento de una serie de otras dolencias que incluyen las que implican sitios inflamatorios y trastornos autoinmunitarios como lupus eritematoso sistémico (LES) . Los trastornos respiratorios en cuyo tratamiento, según se cree, la ADNasa tiene utilidad se caracterizan por un aumento en la viscosidad del moco debido a la presencia de ADN genómico humano y bacteriano.
El moco es una mezcla compleja de sales, agua, glucoproteínas, proteoglucanos y proteínas que limpia, lubrica y protege numerosos pasos en el organismo, incluidos los de los pulmones. Sin embargo, la presencia de ADN genómico y en particular de largas cadenas de ADN genómico, aumenta la viscosidad del moco hasta el punto en que se ve comprometido el aclaramiento mucociliar. El moco viscoso no se limpia adecuadamente mediante los mecanismos normales y bloquea u obstruye las vías respiratorias del pulmón, limitando de este modo el flujo en las vías respiratorias. También puede promover la aparición de infecciones. En conjunto el efecto puede ser fatal o discapacitante.
Según se piensa el ADN genómico viscoso en estas dolencias respiratorias se origina principalmente en células inflamatorias infiltrantes como los neutrófilos. Estas células, según se cree, experimentan necrosis, en lugar del proceso más controlado de la apoptosis, para liberar grandes cantidades de ADN genómico gelatinoso en el moco. La liberación de otros polímeros, tales como actina, a partir de las células necrosantes puede incrementar aún más la viscosidad del moco.
La fibrosis quística es uno de los principales trastornos respiratorios en los que el incremento anómalo de producción de mucosidad y la presencia de ADN en el moco desempeñan un papel importante. La fibrosis quística es un trastorno heredado autosómico recesivo causado por mutación del gen regulador de la conductancia de transmembrana de la fibrosis quística (CFTR) . Es el trastorno heredado más común en personas de ascendencia 45 europea y aparece también en otras poblaciones, aunque normalmente con una menor incidencia. Los pacientes con fibrosis quística muestran normalmente dificultad en la respiración, una pérdida excesiva de sales durante la sudoración y una digestión y absorción incompletas del alimento. La enfermedad puede afectar también a la fertilidad masculina.
El CFTR es un canal de cloruros y está presente en células secretoras de mucosidad. Los iones cloruro son liberados en el moco a través del canal de CFTR. Así se eleva la osmolaridad del moco y se produce el paso de agua desde las células al moco, diluyéndolo y ayudando a garantizar que tiene la viscosidad correcta. En pacientes con fibrosis quística, debido al defecto en CFTR, los iones cloruro no son transportados eficazmente en el moco y de este modo el moco es más viscoso. La captación de sodio, normalmente limitada por la actividad del CTFR, se 55 incrementa y, con ello, la captación de agua que conduce a secreciones condensadas deshidratadas que promueven la infección bacteriana y con ello la inflamación. El número de glóbulos blancos, y en particular neutrófilos, en el moco en el pulmón de pacientes con fibrosis quística también se incrementa enormemente y la necrosis de estas células libera ADN genómico que aumenta adicionalmente la viscosidad del moco.
La fibrosis quística es normalmente fatal, aunque la esperanza de vida para las personas afectadas está en aumento debido a la mejora en los tratamientos. En la década de 1960 en promedio las personas aquejadas de fibrosis quística tenían una esperanza de vida de menos de diez años, mientras que actualmente la esperanza de vida media se aproxima a treinta años.
Las ADNasas, y en particular la ADNasa I humana recombinante usada comúnmente en el tratamiento de fibrosis quística, son costosas. Además, aunque las ADNasas se usan en la actualidad para tratar a pacientes con fibrosis quística, aproximadamente del 50 al 70% de los pacientes con fibrosis quística muestran sólo un beneficio mínimo o inexistente después del tratamiento.
Resumen de la invención La presente invención se basa en el hallazgo de que los glucosaminoglucanos que tienen un peso molecular medio de 8 a 40 kd pueden reforzar la actividad de la ADNasa I. El glucosaminoglucano en sí no escinde el ADN, sino que aumenta la capacidad de hacerlo de la ADNasa I. Este efecto sinérgico inesperado significa que se necesita menos ADNasa I para conseguir el mismo efecto y también que pueden alcanzarse niveles superiores de actividad total en un sistema usando la misma cantidad de ADNasa I.
El mayor nivel de actividad que puede conseguirse con la misma cantidad de enzima puede significar que las dolencias o las personas previamente refractarias al tratamiento con ADNasas, o que obtuvieron un beneficio mínimo del tratamiento, pueden ahora ser tratables. También puede significar que debe usarse menos ADNasa I lo que es importante en particular en aplicaciones en las que se emplean ADNasas I recombinantes ya que estas enzimas son costosas.
En consecuencia, la presente invención proporciona el uso de un glucosaminoglucano o una sal fisiológicamente aceptable del mismo en la fabricación de un medicamento destinado al tratamiento de un sujeto con un trastorno caracterizado por la presencia de ADN extracelular endógeno, en el que el sujeto es sometido también a tratamiento con una ADNasa I, el glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 8 a 40 kd y el glucosaminoglucano o la sal del mismo incrementa la actividad de la ADNasa I, en el que el trastorno es: (a) un trastorno respiratorio caracterizado por la presencia de ADN extracelular endógeno en el pulmón; (b) seleccionado entre fibrosis quística, enfermedad pulmonar obstructiva crónica y neumonía; (c) lupus eritematoso sistémico (LES) ;
o (d) un trastorno caracterizado por la presencia de ADN extracelular endógeno en un sitio inflamatorio.
La presente invención también proporciona el uso de una ADNasa I en la fabricación de un medicamento destinado al tratamiento de un sujeto con un trastorno caracterizado por la presencia de ADN extracelular endógeno, en el que el sujeto es sometido también a tratamiento con un glucosaminoglucano o una sal fisiológicamente aceptable del mismo, el glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 8 a 40 kd y el glucosaminoglucano o la sal del mismo incrementa la actividad de la ADNasa I, en el que el trastorno es: (a) un trastorno respiratorio caracterizado por la presencia de ADN extracelular endógeno en el pulmón; (b) seleccionado entre fibrosis quística, enfermedad pulmonar obstructiva crónica y neumonía; (c) lupus eritematoso sistémico (LES) ;
o (d) un trastorno caracterizado por la presencia de ADN extracelular endógeno en un sitio inflamatorio.
La presente invención proporciona además una composición farmacéutica que comprende:
- Un glucosaminoglucano o una sal fisiológicamente aceptable del mismo que tiene un peso molecular medio de 8 a 40 kd;
- Una ADNasa I; y
- Un excipiente, vehículo o diluyente farmacéuticamente aceptable.
La presente invención también proporciona:
- Productos que comprenden un glucosaminoglucano o una sal fisiológicamente aceptable del mismo, tales que el
glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 8 a 40 kd, y una... [Seguir leyendo]
Reivindicaciones:
1. Uso de un glucosaminoglucano o una sal fisiológicamente aceptable del mismo en la fabricación de un medicamento destinado al tratamiento de un sujeto con un trastorno caracterizado por la presencia de ADN
extracelular endógeno, en el que el sujeto es sometido también a tratamiento con una ADNasa I, tal que el glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 8 a 40 kd y el glucosaminoglucano o la sal del mismo incrementa la actividad de la ADNasa I, en el que el trastorno es:
(a) Un trastorno respiratorio caracterizado por la presencia de ADN extracelular endógeno en el pulmón; 10
(b) Seleccionado entre fibrosis quística, enfermedad pulmonar obstructiva crónica y neumonía;
(c) Lupus eritematoso sistémico (LES) ; o 15 (d) Un trastorno caracterizado por la presencia de ADN extracelular endógeno en un sitio inflamatorio.
2. Uso de una ADNasa I en la fabricación de un medicamento destinado al tratamiento de un sujeto con un trastorno caracterizado por la presencia de ADN extracelular endógeno, en el que el sujeto es sometido también a tratamiento con un glucosaminoglucano o una sal fisiológicamente aceptable del mismo, tal que el
glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 8 a 40 kd y el glucosaminoglucano o la sal del mismo incrementa la actividad de la ADNasa I, en el que el trastorno es:
(a) Un trastorno respiratorio caracterizado por la presencia de ADN extracelular endógeno en el pulmón; 25 (b) Seleccionado entre fibrosis quística, enfermedad pulmonar obstructiva crónica y neumonía;
(c) Lupus eritematoso sistémico (LES) ; o
(d) Un trastorno caracterizado por la presencia de ADN extracelular endógeno en un sitio inflamatorio. 30
3. Uso de acuerdo con la reivindicación 1 ó 2, en el que el glucosaminoglucano o la sal fisiológicamente aceptable comprende unidades de disacáridos de repetición de fórmula general (1)
-[A-B]- (1) 35 donde:
cada A es el mismo o diferente y representa una fracción de fórmula (i) o (ii)
donde:
-Uno entre R1 y R2 es hidrógeno, y el otro es -C2H, -SO3H o -CH2OR;
- En el que R es hidrógeno o -SO3H;
-Uno entre R3 y R4 es hidrógeno, y el otro es -OR en el que R es hidrógeno o -SO3H.
50. Uno entre R5 y R6 es hidrógeno, y el otro es -OH;
- * representa un enlace directo con un átomo de hidrógeno o una fracción B adyacente; y - ** representa un enlace directo con una fracción B adyacente; cada B es el mismo o diferente y representa una fracción de fórmula (iii) o (iv)
donde:
-Uno entre R7 y R8 es hidrógeno y el otro es -CH2OH o -CH2OSO3H;
-Uno entre R9 y R10 es hidrógeno y el otro es -NHAc, -NH2 o -NHSO3H; 15
-Uno entre R11 y R12 es hidrógeno y el otro es -OH o -OSO3H;
indica un enlace en cualquier orientación estereoquímica.
20. * representa un enlace directo con un átomo de hidrógeno o una fracción A adyacente; - ** representa un enlace directo con una fracción A adyacente,
4. Uso de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que el glucosaminoglucano es:
(a) Una heparina; o 30
(b) Condroitín sulfato A, condroitín sulfato C, condroitín sulfato D, condroitín sulfato E, ácido hialurónico, queratán sulfato o heparán sulfato.
5. Uso de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que se usa la sal sódica 35 de heparina o de sulfato de heparina.
6. Uso de acuerdo con una cualquiera de las reivindicaciones precedentes en el que la ADNasa I:
(a) Tiene la secuencia de aminoácidos de SEQ ID NO: 2 o es una ADNasa I con más del 65% de identidad de 40 secuencia de aminoácidos con la secuencia de aminoácidos de SEQ ID NO: 2 y que conserva actividad hidrolítica;
(b) Es una ADNasa I de tipo humano; y/o
(c) Es una ADNasa I recombinante. 45
7. Uso de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que el glucosaminoglucano o la sal tiene:
(a) un peso molecular medio de 12 a 18 kd;
(b) una actividad anticoagulante; y/o
(c) no ha sido sometido a fragmentación y/o despolimerización. 5
8. Uso de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que la proporción entre la cantidad de glucosaminoglucano o sal del mismo y la cantidad de ADNasa I administrada es de 5.000:1 a 1:50 unidad por unidad.
10. Uso de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que:
(a) El glucosaminoglucano o la sal del mismo y la ADNasa I se administran al mismo tiempo; 15
(b) El glucosaminoglucano o la sal del mismo se administra antes o después de la ADNasa I; y/o
(c) El glucosaminoglucano o la sal del mismo y la ADNasa I se administran como medicamentos separados.
11. Uso de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que el sujeto tiene un VEF1 de menos del 75% del valor esperado para un sujeto equivalente que no tiene el trastorno.
12. Uso de acuerdo con una cualquiera de las reivindicaciones precedentes, en el que el
glucosaminoglucano, o la sal y/o la ADNasa I se administran por inhalación, por vía intranasal y/o por instilación. 25
13. Una composición farmacéutica que comprende:
- Un glucosaminoglucano o una sal fisiológicamente aceptable del mismo que tiene un peso molecular medio de 8 a
kd; 30
- Una ADNasa I; y
- Un excipiente, vehículo o diluyente farmacéuticamente aceptable.
14. Una composición farmacéutica de acuerdo con la reivindicación 13 que está en la forma de un polvo seco.
15. Productos que comprenden un glucosaminoglucano o una sal fisiológicamente aceptable del mismo, teniendo el glucosaminoglucano o la sal del mismo un peso molecular medio de 8 a 40 kd, y una ADNasa I para su uso en el tratamiento de un trastorno caracterizado por la presencia de ADN extracelular endógeno en el sujeto destinado a tratamiento, donde el glucosaminoglucano o la sal del mismo incrementa la actividad de la ADNasa I y donde los productos están destinados a administrarse de una forma simultánea, separada o en secuencia, en los que el trastorno es:
(a) Un trastorno respiratorio caracterizado por la presencia de ADN extracelular endógeno en el pulmón;
(b) Seleccionado entre fibrosis quística, enfermedad pulmonar obstructiva crónica y neumonía;
(c) Lupus eritematoso sistémico (LES) ; o 50
(d) Un trastorno caracterizado por la presencia de ADN extracelular endógeno en un sitio inflamatorio.
16. Productos para su uso de acuerdo con la reivindicación 15, en los que:
(A) el glucosaminoglucano o la sal fisiológicamente aceptable del mismo comprende unidades de disacáridos de repetición de fórmula general (1)
-[A-B]- (1)
donde: cada A es el mismo o diferente y representa una fracción de fórmula (i) o (ii)
donde:
-Uno entre R1 y R2 es hidrógeno, y el otro es -C2H, -SO3H o -CH2OR;
- En el que R es hidrógeno o -SO3H;
-Uno entre R3 y R4 es hidrógeno, y el otro es -OR en el que R es hidrógeno o -SO3H;
- Uno entre R5 y R6 es hidrógeno, y el otro es -OH; - * representa un enlace directo con un átomo de hidrógeno o una fracción B adyacente; y - ** representa un enlace directo con una fracción B adyacente;
cada B es el mismo o diferente y representa una fracción de fórmula (iii) o (iv)
donde:
-Uno entre R7 y R8 es hidrógeno y el otro es -CH2OH o -CH2OSO3H;
-Uno entre R9 y R10 es hidrógeno y el otro es -NHAc, -NH2 o -NHSO3H;
- Uno entre R11 y R12 es hidrógeno y el otro es -OH o -OSO3H;
indica un enlace en cualquier orientación estereoquímica; - * representa un enlace directo con un átomo de hidrógeno o una fracción A adyacente;
- ** representa un enlace directo con una fracción A adyacente, o una sal fisiológicamente aceptable del mismo; o
(B) El glucosaminoglucano o la sal del mismo es una heparina; o
(C) El glucosaminoglucano o la sal del mismo es condroitín sulfato A, condroitín sulfato C, condroitín sulfato D,
condroitín sulfato E, ácido hialurónico, queratán sulfato o heparán sulfato; o 5
(D) Se usa la sal sódica de heparina o de sulfato de heparina; o
(E) El glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 12 a 18 kd; o 10 (F) El glucosaminoglucano o la sal del mismo tiene actividad anticoagulante; o
(G) El glucosaminoglucano o la sal del mismo no ha sido sometido a fragmentación y/o despolimerización; o
(H) La ADNasa I tiene la secuencia de aminoácidos de SEQ ID NO: 2 o es una ADNasa I con más del 65% de 15 identidad de secuencia de aminoácidos con la secuencia de aminoácidos de SEQ ID NO: 2;
(I) La ADNasa I es una ADNasa I de tipo humano; o
(J) La ADNasa I es una ADNasa I recombinante; o 20
(K) La proporción entre la cantidad de glucosaminoglucano o sal del mismo y la cantidad de ADNasa I administrada es de 5.000:1 a 1:50 unidad por unidad; o
(L) la proporción entre la cantidad de glucosaminoglucano o sal del mismo y la cantidad de ADNasa I que se 25 administrará es de 25:1 a 1:25.
17. Un agente para su uso en el tratamiento de un sujeto que tiene un trastorno caracterizado por la presencia de ADN extracelular endógeno, comprendiendo el agente un glucosaminoglucano o una sal fisiológicamente aceptable del mismo, tal que el glucosaminoglucano o la sal del mismo tiene un peso molecular
medio de 8 a 40 kd, en el que dicho sujeto es sometido a tratamiento con una ADNasa I y el glucosaminoglucano o la sal del mismo incrementa la actividad de la ADNasa I, en el que el trastorno es:
(a) Un trastorno respiratorio caracterizado por la presencia de ADN extracelular endógeno en el pulmón; 35 (b) Seleccionado entre fibrosis quística, enfermedad pulmonar obstructiva crónica y neumonía;
(c) Lupus eritematoso sistémico (LES) ; o
(d) Un trastorno caracterizado por la presencia de ADN extracelular endógeno en un sitio inflamatorio. 40
18. Un agente para su uso en el tratamiento de un sujeto que tiene un trastorno caracterizado por la presencia de ADN extracelular endógeno, comprendiendo el agente una ADNasa I, en el que dicho sujeto es sometido a tratamiento con un glucosaminoglucano o una sal fisiológicamente aceptable del mismo, tal que el glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 8 a 40 kd y el glucosaminoglucano o la sal
del mismo incrementa la actividad de la ADNasa I, en el que el trastorno es:
(a) Un trastorno respiratorio caracterizado por la presencia de ADN extracelular endógeno en el pulmón;
(b) Seleccionado entre fibrosis quística, enfermedad pulmonar obstructiva crónica y neumonía; 50
(c) Lupus eritematoso sistémico (LES) ; o
(d) Un trastorno caracterizado por la presencia de ADN extracelular endógeno en un sitio inflamatorio.
19. Una composición farmacéutica de acuerdo con la reivindicación 13 ó 14 o un agente para su uso de acuerdo con la reivindicación 17 ó 18, donde:
(A) El glucosaminoglucano o la sal fisiológicamente aceptable del mismo comprende unidades de disacáridos de repetición de fórmula general (1)
-[A-B]- (1) donde: cada A es el mismo o diferente y representa una fracción de fórmula (i) o (ii)
donde:
-Uno entre R1 y R2 es hidrógeno, y el otro es -C2H, -SO3H o -CH2OR;
- En el que R es hidrógeno o -SO3H;
-Uno entre R3 y R4 es hidrógeno, y el otro es -OR en el que R es hidrógeno o -SO3H;
-Uno entre R5 y R6 es hidrógeno, y el otro es -OH;
- * representa un enlace directo con un átomo de hidrógeno o una fracción B adyacente; y - ** representa un enlace directo con una fracción B adyacente; cada B es el mismo o diferente y representa una fracción de fórmula (iii) o (iv) :
donde.
30. Uno entre R7 y R8 es hidrógeno y el otro es -CH2OH o -CH2OSO3H;
-Uno entre R9 y R10 es hidrógeno y el otro es -NHAc, -NH2 o -NHSO3H;
- Uno entre R11 y R12 es hidrógeno y el otro es -OH o -OSO3H;
indica un enlace en cualquier orientación estereoquímica; - * representa un enlace directo con un átomo de hidrógeno o una fracción A adyacente;
- ** representa un enlace directo con una fracción A adyacente, o una sal fisiológicamente aceptable del mismo; o
(B) El glucosaminoglucano o la sal del mismo es una heparina; o (C) El glucosaminoglucano o la sal del mismo es condroitín sulfato A, condroitín sulfato C, condroitín sulfato D, condroitín sulfato E, ácido hialurónico, queratán sulfato o heparán sulfato; o (D) Se usa la sal sódica de heparina o de sulfato de heparina; o (E) El glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 12 a 18 kd; o (F) El glucosaminoglucano o la sal del mismo tiene actividad anticoagulante; o 15
(G) El glucosaminoglucano o la sal del mismo no ha sido sometido a fragmentación y/o despolimerización; o
(H) La ADNasa I tiene la secuencia de aminoácidos de SEQ ID NO: 2 o es una ADNasa I con más del 65% de
identidad de secuencia de aminoácidos con la secuencia de aminoácidos de SEQ ID NO: 2; 20
(I) La ADNasa I es una ADNasa I de tipo humano; o
(J) La ADNasa I es una ADNasa I recombinante; o
(K) La proporción entre la cantidad de glucosaminoglucano o sal del mismo y la cantidad de ADNasa I administrada es de 5000:1 a 1:50 unidad por unidad; o (L) La proporción entre la cantidad de glucosaminoglucano o sal del mismo y la cantidad de ADNasa I que se administrará es de 25:1 a 1:25. 30
20. Un nebulizador u otro dispositivo de aerosol líquido, inhalador de polvo seco o inhalador dosificador que contiene una composición que comprende:
- Un glucosaminoglucano o una sal fisiológicamente aceptable del mismo que tiene un peso molecular medio de 8 a 35 40 kd;
- Una ADNasa I; y
- Un excipiente, vehículo o diluyente farmacéuticamente aceptable. 40
21. Uso de un glucosaminoglucano o una sal fisiológicamente aceptable del mismo, tal que el glucosaminoglucano o la sal del mismo tiene un peso molecular medio de 8 a 40 kd para incrementar la actividad de una ADNasa I in vitro.
Patentes similares o relacionadas:
 Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]
Derivado de dihidroindolizinona, del 1 de Julio de 2020, de ONO PHARMACEUTICAL CO., LTD.: (3S)-3-[2-(6-amino-2-fluoro-3-piridinil)-4-fluoro-1H-imidazol-5-il]-7-[5-cloro-2-(1H-tetrazol-1-il)fenil]-2,3-dihidro- (1H)-indolizinona, una…
Inhibidor de fibrosis, del 1 de Julio de 2020, de NIPPON SHINYAKU CO., LTD.: Composición farmacéutica que comprende un derivado heterocíclico seleccionado de ácido 2-{4-[N-(5,6-difenilpirazin-2-il)-N-isopropilamino]butiloxi}acético […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]
Compuestos utilizados como inhibidores de la quinasa reordenada durante la transfección (RET), del 1 de Julio de 2020, de GlaxoSmithKline Intellectual Property Development Limited: Un compuesto de acuerdo con la Fórmula (I), o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en donde: X es N o CR5; Y es un enlace; […]
Métodos de monitorización terapéutica de profármacos de ácido fenilacético, del 24 de Junio de 2020, de Immedica Pharma AB: Glicerilo tri-[4-fenilbutirato] (HPN-100) para su uso en un método para tratar un trastorno del ciclo de la urea en un sujeto que tiene discapacidad […]