Anticuerpos humanizados específicos a Fc gamma RIIB y sus métodos de uso.
Un anticuerpo humanizado que comprende una región Fc humana y un dominio variable,
en donde dicho anticuerpo se une específicamente al dominio extracelular de FcγRIIB humano a través de dicho dominio variable, en donde dicho dominio variable comprende un dominio variable de cadena pesada que comprende la secuencia de aminoácidos de sec. con núm. de ident.:68 y un dominio variable de cadena ligera que comprende la secuencia de aminoácidos de sec. con núm. de ident.:62, o un fragmento de dicho anticuerpo que comprende dicho dominio variable y se une específicamente al dominio extracelular de FcγRIIB humano a través de dicho dominio variable.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/069767.
Solicitante: MACROGENICS, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 9640 Medical Center Drive Rockville, MD 20850 ESTADOS UNIDOS DE AMERICA.
Inventor/es: JOHNSON,LESLIE,S, HUANG,Ling.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- A61P43/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
- C07H21/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con desoxirribosilo como radical sacárido.
- C07K16/18 C07 […] › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- C12N15/00 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K).
- C12N5/06
- C12P21/04 C12 […] › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Péptidos o polipéptidos cíclicos o puenteados, p. ej. bacitracina.
- G01N33/564 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › para complejos inmunológicos preexistentes o enfermedades autoinmunes.
PDF original: ES-2489646_T3.pdf
Fragmento de la descripción:
Anticuerpos humanizados específicos a Fe gamma RIIB y sus métodos de uso.
2. Campo de la invención
La presente invención se relaciona con anticuerpos humanizados de FcyRIIB, fragmentos y variantes de estos que se unen a FcyRIIB humano con una afinidad mayor que con la que dicho anticuerpo se une a FcyRIIA. Además la invención incluye los anticuerpos humanizados de la invención para uso en el tratamiento de cualquier enfermedad relacionada con la pérdida del equilibrio de la señalización mediada por el receptor Fe, tal como cáncer (preferentemente una malignidad de célula B, particularmente, leucemia linfocítica crónica de células B o linfoma de no Hodgkin), enfermedad autoinmunitaria, enfermedad inflamatoria o trastorno alérgico mediado por IgE. La presente invención abarca además los anticuerpos humanizados de FcyRIIB de la invención o un fragmento de unión a antigeno de este, para el uso en conjunto con otras terapias contra el cáncer. Los anticuerpos humanizados de la invención se pueden usar en métodos para mejorar el efecto terapéutico de los anticuerpos terapéuticos administrando los anticuerpos humanizados de la invención para mejorar la función efectora de los anticuerpos terapéuticos. Los anticuerpos humanizados de la invención se pueden usar en métodos para mejorar la eficacia de una composición de vacuna administrando los anticuerpos humanizados de la invención con una composición de vacuna.
3. Antecedentes de la invención
3.1 Receptores Fe y su papel en el sistema inmunológico
La interacción de los complejos anticuerpo-antígeno con las células del sistema inmunológico resulta en una amplia matriz de respuestas, que van desde funciones efectoras tales como la citotoxicidad dependiente de anticuerpos, desgranulación de mastocitos, y fagocitosis a señales inmunomoduladoras tales como la regulación de la proliferación de linfocitos y secreción de anticuerpos. Todas estas interacciones se inician a través de la unión del dominio Fe de los anticuerpos o complejos inmunológicos a receptores especializados de superficie celular en las células hematopoyéticas. La diversidad de respuestas celulares desencadenadas por anticuerpos y complejos inmunológicos resulta de la heterogeneidad estructural de los receptores Fe. Los receptores Fe comparten dominios de unión de ligando estructuralmente relacionados que median presumiblemente la señalización intracelular.
Los receptores de Fe, miembros de la superfamilia de proteínas de genes de inmunoglobulina, son glicoproteínas de superficie que pueden unir la porción Fe de las moléculas de inmunoglobulina. Cada miembro de la familia reconoce inmunoglobulinas de uno o más isotipos a través de un dominio de reconocimiento en una cadena del receptor Fe. Los receptores Fe se definen por su especificidad para los subtipos de inmunoglobulinas. Los receptores Fe para IgG se denominan como FcyR, para IgE como FcsR, y para IgAcomo FcaR. Diferentes células accesorias portan receptores Fe para anticuerpos de isotipo diferente, y el isotipo del anticuerpo determina qué células accesorias participarán en una respuesta determinada (revisado por Ravetch J.V. y otros 1991, Annu. Rev. Immunol. 9: 457-92; Gerber J.S. y otros 21 Microbes and Infection, 3: 131-139; Billadeau D.D. y otros 22, The Journal of Clinical Investigaron, 2(19): 161- 168; Ravetch J.V. y otros 2, Science, 29: 84-89; Ravetch J. V. y otros, 21 Annu. Rev. Immunol. 19:275-9; Ravetch J.V. 1994, Cell, 78(4): 553-6). Los diferentes receptores Fe, las células que los expresan, y su especificidad de isotipo se resumen en la Tabla 1 (adaptado de Immunobiology: The Immune System in Health and Disease, 4ta edición 1999, Elsevier Science Ltd/Garland Publishing, Nueva York).
Otra técnica anterior relativa a tal materia objeto incluye WO 26113665 la cual se dirige a moléculas de diacuerpo y sus usos en el tratamiento de una variedad de enfermedades y trastornos, que incluyen trastornos inmunológicos, enfermedades infecciosas, intoxicación y cáncer. Las moléculas de diacuerpo descritas en la misma comprenden dos cadenas de polipéptidos que se asocian para formar al menos dos sitios de unión al epítopo, que pueden reconocer epítopos iguales o diferentes en antígenos iguales o distintos. Además, los antígenos pueden ser de moléculas iguales o diferentes. Las cadenas individuales de polipéptido de la molécula de diacuerpo pueden estar unidas covalentemente a través de enlaces covalentes de enlace no peptídico, tales como, pero sin limitarse a, puente disulfuro de residuos de cisteína situados dentro de cada cadena de polipéptido. En modalidades particulares, las moléculas de diacuerpo de la presente invención comprenden además una región Fe, que permite la funcionalidad similar al anticuerpo para modificar en la molécula.
WO 2721841 se relaciona con moléculas, particularmente polipéptidos, más particularmente inmunoglobulinas (por ejemplo, anticuerpos), que comprenden una variante de región Fe, en donde dicha variante de región Fe comprende al menos una modificación de aminoácidos respecto a una región Fe silvestre, cuya variante de región Fe se une a FcyRIIIA y/o FcyRIIA con una afinidad mayor, respecto a una molécula comparable que comprende la región Fe silvestre. Las moléculas descritas en las mismas son particularmente útiles al impedir, tratar, o mejorar uno o más síntomas asociados con una enfermedad, trastorno, o infección. Las moléculas descritas en las mismas son particularmente útiles para el tratamiento o prevención de una enfermedad o trastorno donde se desea una eficacia mejorada de la función celular efectora (por ejemplo, ADCC) mediada por FcyR, por ejemplo, cáncer, enfermedad infecciosa, y para mejorar la eficacia terapéutica de los anticuerpos terapéuticos cuyo efecto se media por ADCC.
WO 25115452 se relaciona con anticuerpos o fragmentos de estos que se unen específicamente a FcyRIIB, particularmente FcyRIIB humano, con afinidad mayor que con la que dichos anticuerpos o fragmentos de estos se unen a FcyRIIA, particularmente FcyRIIA humano. Se proporciona además el uso de un anticuerpo anti-FcyRIIB o un fragmento de unión al antígeno de este, como una terapia de agente único para el tratamiento, prevención, manejo, o mejora de un cáncer, preferentemente una malignidad de célula B, particularmente, leucemia linfocítica crónica de células B o linfoma de no Hodgkin, un trastorno autoinmunitario, un trastorno inflamatorio, un trastorno alérgico mediado por IgE, o uno o más de sus síntomas. Además, se proporcionan métodos para mejorar el efecto terapéutico de los anticuerpos terapéuticos administrando los anticuerpos descritos en la misma para mejorar la función efectora de los anticuerpos terapéuticos. Se describen además los métodos para mejorar la eficacia de una composición de vacuna administrando dichos anticuerpos.
Receptores Fcy
Cada miembro de esta familia es una glicoproteína de membrana integral, que posee los dominios extracelulares relacionados a un conjunto C2 de dominios relacionados con la inmunoglobulina, un único dominio de inmunoadsorción de membrana y un dominio intracitoplasmático de longitud variable. Existen tres FcyRs conocidos, designados FcyRI(CD64), FcyRII(CD32), y FcyRIM(CD16). Los tres receptores se codifican por genes distintos; sin embargo, la extensa homología entre los tres miembros de la familia sugiere que provinieron de un progenitor común quizás por la duplicación de genes. Esta invención se centra específicamente en FcyRIl(CD32).
FcyRII(CD32)
Las proteínas FcyRII son glicoproteínas integrales de membrana de 4 kDa que unen sólo la IgG acomplejada debido a una baja afinidad por el Ig monomérico (1® M'1). Este receptor FcyR es el más ampliamente expresado, presente en todas las células hematopoyéticas, que incluyen monocitos, macrófagos, células B, células NK, neutrófilos, mastocitos y plaquetas. FcyRII tiene sólo dos regiones similar a inmunoglobulina en su cadena de unión a inmunoglobulina y de ahí una afinidad mucho menor por IgG que FcyRI. Existen tres genes FcyRIl humanos (FcyRII-A, FcyRII-B, FcyRII-C), todos los cuales unen IgG en agregados o complejos inmunológicos.
Las diferencias distintas dentro de los dominios citoplasmáticos de FcyRII-A (CD32A) y FcyRII-B (CD32B) crean dos respuestas funcionalmente heterogéneas para la ligación de los receptores. La diferencia fundamental es que la isoforma A inicia la señalización intracelular que conduce a la activación celular tales como fagocitosis y estallido respiratorio, mientras que la ¡soforma B inicia las señales inhibidoras, por ejemplo, inhibición de la activación de células B.
Señalización a través de FcyRs
Tanto las señales de activación como... [Seguir leyendo]
Reivindicaciones:
Un anticuerpo humanizado que comprende una región Fe humana y un dominio variable, en donde dicho anticuerpo se une específicamente al dominio extracelular de FcyRIIB humano a través de dicho dominio variable, en donde dicho dominio variable comprende un dominio variable de cadena pesada que comprende la secuencia de aminoácidos de sec. con núm. de ident.:68 y un dominio variable de cadena ligera que comprende la secuencia de aminoácidos de sec. con núm. de ident.:62, o un fragmento de dicho anticuerpo que comprende dicho dominio variable y se une específicamente al dominio extracelular de FcyRIIB humano a través de dicho dominio variable.
El anticuerpo humanizado de la reivindicación 1, en donde el dominio Fe comprende al menos una modificación de aminoácidos en el dominio de Fe.
El anticuerpo humanizado de la reivindicación 2, en donde al menos dicha una modificación de aminoácidos comprende una sustitución en la posición 243, una sustitución en la posición 292, una sustitución en la posición 3, una sustitución en la posición 35, y una sustitución en la posición 396 y en donde dichas posiciones están de acuerdo con Kabat.
El anticuerpo humanizado de la reivindicación 3, en donde la sustitución en la posición 243 es una sustitución con leucina, la sustitución en la posición 292 es una sustitución con prolina, la sustitución en la posición 3 es una sustitución con leucina, la sustitución en la posición 35 es una sustitución con isoleucina, y la sustitución en la posición 396 es una sustitución con leucina y en donde dichas posiciones están de acuerdo con Kabat.
El anticuerpo humanizado de la reivindicación 1, en donde dicho anticuerpo o fragmento de este es un fragmento F(ab')2 o un fragmento F(ab).
El anticuerpo humanizado de la reivindicación 1, en donde dicho anticuerpo o fragmento de este es un anticuerpo de cadena sencilla.
El anticuerpo humanizado de la reivindicación 1, en donde dicho anticuerpo está operativamente enlazado a un polipéptido heterólogo.
El anticuerpo humanizado de la reivindicación 1, en donde dicho anticuerpo está conjugado a un agente terapéutico.
El anticuerpo humanizado de la reivindicación 8, en donde dicho agente terapéutico es una citotoxina.
Un ácido nucleico aislado que comprende uan secuencia de nucleótidos que codifica el dominio variable de la cadena pesada o dominio variable de la cadena ligera del anticuerpo de la reivindicación 1.
El uso del anticuerpo humanizado de la reivindicación 1 en la preparación de una medicamento para el tratamiento del cáncer, en donde dicho medicamento es para el uso en conjunto con un anticuerpo secundario que se une específicamente a un antígeno de cáncer y es citotóxico y en donde dicho cáncer está caracterizado por dicho antígeno de cáncer.
Una composición farmacéutica que comprende (i) una cantidad terapéuticamente eficaz del anticuerpo humanizado de la reivindicación 1; (¡i) un anticuerpo citotóxico que une específicamente un antígeno de cáncer; y (iii) un portador farmacéuticamente aceptable.
La composición farmacéutica de la reivindicación 12 para uso en el tratamiento del cáncer.
El uso de acuerdo con la reivindicación 11, o la composición de acuerdo con la reivindicación 12 o composición para uso de acuerdo con la 13, en donde dicho antígeno de cáncer es el antígeno pancarcinoma KS %, antígeno del carcinoma ovárico (CA125), fosfato de ácido prostático, antígeno específico de próstata, antígeno asociado a melanoma p97, antígeno de melanoma gp75, antígeno de melanoma de alto peso molecular (FIMWMAA), antígeno de membrana específico de próstata, antígeno carcinoembrionario (CEA), TAG-72, GICA 19-9, CTA-1, LEA, antígeno 38.13 de linfoma de Burkitt, CD19, CD2, CD33, GD2, GD3, GM2, GM3, un antígeno de superficie celular de tipo trasplante específico de tumor (TSTA), L6 humano, L2 humano, EGFR, o FIER2/neu.
El uso de acuerdo con la reivindicación 11, o la composición de acuerdo con la reivindicación 12 o composición para el uso de acuerdo con la 13, en donde dicho antígeno de cáncer es un antígeno de carcinoma de mama, ovario, próstata, cervical, o pancreático.
17.
18.
19.
2.
21.
22.
El uso del anticuerpo humanizado de la reivindicación 1 en la preparación de una medicamento para el tratamiento de un trastorno autoinmunitario.
El uso del anticuerpo humanizado de la reivindicación 1 en la preparación de una medicamento para el tratamiento o prevención de un trastorno alérgico mediado por IgE, en donde dicho trastorno es asma, rinitis alérgica, una alergia gastrointestinal, eosinofilia, conjuntivitis, dermatitis atópica, urticaria, anafilaxis, o nefritis glomerular.
El anticuerpo humanizado de la reivindicación 1 para usar en (i) el tratamiento de un trastorno autoinmunitario;
(¡i) el tratamiento o prevención de un trastorno alérgico mediado por IgE, en donde dicho trastorno es asma, rinitis alérgica, una alergia gastrointestinal, eosinofilia, conjuntivitis, dermatitis atópica, urticaria, anafilaxis, o nefritis glomerular;
Un método para el diagnóstico de una enfermedad autoinmunitario en un sujeto que comprende:
(a) contactar una muestra biológica de dicho sujeto con una cantidad eficaz del anticuerpo humanizado de la reivindicación 1, y
(b) detectar la unión de dicho anticuerpo,
en donde dicha detección por encima de un nivel de base o estándar indica que dicho sujeto tiene una enfermedad autoinmunitaria.
El uso del anticuerpo humanizado de la reivindicación 1 en la preparación de un medicamento para mejorar la presentación de antígeno o procesamiento de antigeno de un antigeno, de ese modo mejorar una respuesta inmune a la composición vacunal en un sujeto.
El uso del anticuerpo humanizado de la reivindicación 1 en la preparación de un medicamento para el tratamiento del cáncer y la reducción en la población de células cancerosas que expresan FcyRIIB en un paciente, en donde dicho cáncer está caracterizado por un antigeno de cáncer.
El uso del anticuerpo humanizado de la reivindicación 21 en la preparación de un medicamento para el tratamiento del cáncer y la eliminación de las células cancerosas que expresan FcyRIIB en un paciente, en el que dicho cáncer está caracterizado por un antigeno de cáncer, que es el antígeno pancarcinoma KS %, antígeno del carcinoma ovárico (CA125), fosfato de ácido prostático, antígeno específico de próstata, antígeno asociado a melanoma p97, antígeno de melanoma gp75, antígeno de melanoma de alto peso molecular (HMWMAA), antígeno de membrana específico de próstata, antígeno carcinoembrionario (CEA), TAG-72, GICA 19-9, CTA-1, LEA, antígeno 38.13 de linfoma de Burkitt, CD19, CD2, CD33, GD2, GD3, GM2, GM3, un antígeno de superficie celular de tipo trasplante específico de tumor (TSTA), L6, L2, EGFR, o HER2/neu.
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
CD33 soluble para tratar síndromes mielodisplásicos (MDS), del 8 de Enero de 2020, de H. Lee Moffitt Cancer Center And Research Institute, Inc: Una proteína de fusión recombinante quimérica, que comprende: (a) una combinación de al menos dos fracciones de unión a S100A9 seleccionados de entre el grupo que […]
Métodos para la diferenciación y transducción in vitro de células b de memoria con vectores virales pseudotipados vsv-g, del 1 de Enero de 2020, de Immusoft Corporation: Un método in vitro para expresar un ácido nucleico de interés en una célula B, que comprende (a) poner en contacto células B de memoria con una composición que comprende […]
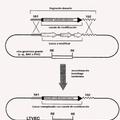 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Intercambio de casetes de la región variable de la inmunoglobulina, del 12 de Junio de 2019, de Humanigen, Inc: Un método de modificación genética de un anticuerpo que retiene la especificidad de unión de un anticuerpo de referencia con un antígeno diana, comprendiendo el método: […]
Procedimiento de modificar células eucariotas, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento de reemplazar in situ, en parte, en una célula madre embrionaria (ES) de ratón, un locus génico endógeno de región variable de […]
Diacuerpos covalentes y usos de los mismos, del 2 de Abril de 2019, de MACROGENICS, INC: Una molécula de diacuerpo que comprende una primera cadena polipeptídica y una segunda cadena polipeptídica, en la que: (a) dicha primera cadena […]