Uso de un inhibidor de psd-95 tratamiento para la epilepsia.
Un inhibidor de PSD-95 que bloquea la unión de un ligando de unión con PDZ a un dominio PDZ de PSD-95 para su uso en el tratamiento de la epilepsia,
en donde el inhibidor es administrado al menos aproximadamenteuna hora después de la terminación de un episodio de epilepsia.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/043831.
Solicitante: NoNO Inc.
Nacionalidad solicitante: Canadá.
Dirección: 88 Strath Avenue Toronto ON M8X 1R5 CANADA.
Inventor/es: GURD,JAMES, DYKSTRA,CRYSTAL, TYMIANSKI,MICHAEL.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/16 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
PDF original: ES-2446306_T3.pdf
Fragmento de la descripción:
Uso de un inhibidor de psd-95 tratamiento para la epilepsia FUNDAMENTO DE LA INVENCIÓN.
La epilepsia es un trastorno neurológico caracterizado por las convulsiones recurrentes, no provocadas (Blume et al., Epilepsia 2001; 42:1212 - 1218) . Estas convulsiones son los signos y/o síntomas transitorios debidos a la actividad neuronal anómala, excesiva o sincrónica en el cerebro (Fisher et al., Epilepsia 46 (4) : 470-2) . La epilepsia no ha de entenderse como un trastorno individual, sino más bien como un grupo de síndromes con síntomas ampliamente divergentes, pero todos ellos implicando episodios de actividad eléctrica anómala en el cerebro. Es uno de los trastornos neurológicos graves más comunes en los Estados Unidos y con frecuencia requiere tratamiento a largo plazo. Cada año 150.000 personas en los Estados Unidos han sido diagnosticadas de epilepsia, con una incidencia acumulada durante toda la vida próxima al 3 % (Hauser et al., Epilepsia 1991; 32: 429 - 445; Begley et al., Epilepsia 1994; 35: 1230 - 1243) . La incidencia es máxima durante el primer año de vida y en las personas de edad avanzada. Id. Del 30 % a 40 % de los pacientes siguen teniendo convulsiones a pesar de usar medicamentos antiepilépticos existentes, bien sea solos o en combinación (Kwan et al., N. Engl. J. Med. 2000; 342: 314 - 319) . Los pacientes con convulsiones no controladas experimentan una morbilidad y una mortalidad significativas y también se enfrentan al estigma y la discriminación sociales.
Los fármacos antiepilépticos conocidos incluyen medicamentos "tradicionales" tales como el fenobarbital, primidona, fenitoína, carbamazepina y valproato, así como nuevos fármacos antiepilépticos que inducen bloqueo de los canales de iones dependiente del voltaje, la mejora de la neurotransmisión inhibidora, y/o la reducción de la neurotransmisión excitadora. Los ejemplos incluyen el antagonismo de glutamato en los receptores de N-metil-Daspartato (NMDA) (por ejemplo felbamato) y receptores de ácido α-amino-3-hidroxi-5-metil-4-isoxazol propiónico (AMPA) (p. ej. felbamato, topiramato) y la inhibición de la reabsorción de ácido γ-aminobutírico (GABA) en neuronas y astrocitos (p. ej. tiagabina) .
La proteína de densidad postsináptica 95 (PSD- 95) acopla NMDARs a las rutas que median la excitotoxicidad y el daño cerebral isquémico (Aarts et al., Science 298, 846 - 850 (2002) ) . Este acoplamiento se interrumpió por la transducción de las neuronas con péptidos que se unen a dominios modulares en cualquier lado del complejo de interacción PSD-95/NMDAR. Este tratamiento atenuó la señalización aguas abajo de NMDAR sin bloquear la actividad de NMDAR, protegió las neuronas corticales cultivadas de las agresiones excitotóxicas y redujo el volumen del infarto cerebral en ratas sometidas a isquemia cerebral focal transitoria. Este resultado ha dado lugar a la propuesta de usar antagonistas peptídicos de PSD-95/NMDAR para tratar la apoplejía y otras enfermedades mediadas por la excitotoxicidad. No se han observado efectos secundarios significativos en ensayos de fase I de tal antagonista.
El documento US 20060148711 discute polipéptidos de fusión en los cuales varios péptidos PL, uno de los cuales es el 9 aminoácidos C-terminal de Tax, están unidos a un resto transportador tat para la inhibición de interacciones PDZ:PL en el tratamiento de varios trastornos neurológicos, uno de los cuales es la epilepsia.
El documento EP1884521 A1 discute proteínas de fusión que incluyen TAT-NR2B9c para el tratamiento de varios trastornos asociados con el daño a las neuronas, uno de los cuales es la epilepsia.
BREVE RESUMEN DE LA INVENCIÓN
La presente invención proporciona un inhibidor de PSD-95 que bloquea la unión de un ligando de unión de PDZ a un dominio PDZ de PSD-95 para ser usado en el tratamiento de la epilepsia, en donde el inhibidor es administrado al menos aproximadamente una hora después de la terminación de un episodio de epilepsia. La memoria descriptiva también describe métodos de tratamiento o de profilaxis de un paciente que tiene epilepsia, o está en riesgo de desarrollar sus síntomas, que comprende administrar al paciente un régimen efectivo de un agente que inhibe la unión específica de dominios PDZ de PSD - 95 a un ligando de unión de PDZ (también llamado "PL") , p. ej. un receptor de NMDA. Opcionalmente, el agente es un péptido quimérico que comprende un péptido activo que tiene una secuencia de aminoácidos que consiste en 3 a 25 aminoácidos a partir del término C de un receptor de NMDA o un dominio PDZ 1 y/o 2 de un receptor de PSD-95 enlazado a un péptido de internalización. Opcionalmente, el péptido activo tiene una secuencia de aminoácidos que comprende [E/D/N/Q] - [S/T] - [D/E/Q/N] - [V/L]. Opcionalmente, el péptido activo comprende una secuencia de aminoácidos carboxilo terminal elegida del grupo que consiste en ESDV (SEQ ID NO: 1) , ESEV (SEQ ID NO: 2) , ETDV (SEQ ID NO: 3) , TEVE (SEQ ID NO: 4) , DTDV (SEQ ID NO: 5) , DTEV (SEQ ID NO: 6) . Opcionalmente, el péptido activo tiene una secuencia de aminoácidos que comprende KLSSIETDV (SEQ ID NO: 7) . Opcionalmente, el péptido quimérico tiene una secuencia de aminoácidos que comprende YGRKKRRQRRRKLSSIETDV (SEC ID NO: 8) . Opcionalmente, el péptido quimérico tiene una secuencia de aminoácidos que consiste en YGRKKRRQRRRKLSSIETDV (SEC ID NO: 8) . Opcionalmente, el péptido activo tiene una secuencia de aminoácidos que comprende KLSSIESDV (SEQ ID NO: 9) . Opcionalmente, el péptido quimérico tiene una secuencia de aminoácidos que comprende YGRKKRRQRRRKLSSIESDV (SEQ ID NO: 10) . Opcionalmente, la secuencia de aminoácidos consiste en YGRKKRRQRRRKLSSIESDV (SEQ ID NO: 10) .
La memoria describe también un método de tratamiento de la epilepsia que comprende la administración de un régimen efectivo de un inhibidor de PSD-95 que bloquea la unión de un ligando de unión de PDZ a un dominio PDZ 5 de PSD-95. Opcionalmente, el dominio PDZ de PSD-95 es dominio PDZ 2 de PSD-95. Como se describe en el presente texto, el inhibidor puede ser administrado al menos aproximadamente una hora después del inicio de un episodio de epilepsia, por ejemplo al menos aproximadamente tres horas después de iniciarse un episodio de epilepsia. Esto puede ser especialmente adecuado cuando el episodio tiene una duración de menos de aproximadamente 10 minutos. De acuerdo con la presente invención, y como se especifica en las reivindicaciones,
el inhibidor es administrado al menos aproximadamente una hora después de la finalización de un episodio de epilepsia. Por ejemplo, el inhibidor se administra al menos aproximadamente tres horas después de la finalización de un episodio de epilepsia. Si se desea, el inhibidor se administra no después de aproximadamente 1 semana, p. ej. no después de 1 día, después de la finalización de un episodio de epilepsia. Opcionalmente, el inhibidor es Tat-NR2B9c. Opcionalmente, el inhibidor es F-Tat-NR2B9c. Opcionalmente, el inhibidor tiene la estructura:
Por ejemplo, el inhibidor es 0625-0057. El inicio, la finalización y/o la duración del episodio de epilepsia pueden determinarse usando la electroencefalografía, p. ej. mediante monitorización electroencefalográfica por video (V -EEG) .
De acuerdo con la presente invención como se especifica en las reivindicaciones, el agente puede ser administrado al menos una hora después de un episodio de epilepsia (p. ej. una convulsión) . El agente puede ser administrado, por ejemplo, al menos aproximadamente tres, cuatro, cinco, seis, ocho, diez, doce, dieciséis o veinticuatro horas después de un episodio de epilepsia. El agente puede también administrarse días después del episodio de epilepsia, por ejemplo, al menos aproximadamente 1, 2, 3, 4, 5, 7, 8, 9, 10 o 12 días después de la iniciación. El agente puede también administrarse al menos una semana después del episodio de epilepsia, por ejemplo, al menos aproximadamente 1, 2 o 3 semanas después del episodio. El inhibidor puede ser administrado después del episodio de epilepsia pero no más tarde de una o más horas, p. ej. no más tarde de aproximadamente 1, 2, 3, 4, 5, 6, 7, 8, 10, 12, 18 o 24 horas después del episodio. El inhibidor puede ser administrado después del episodio de epilepsia pero no después de uno o más días, p. ej. no después de aproximadamente 1, 2, 3, 4, 5, 6, 7, 8, 9, 10, 11, 12, o 14 días después del episodio. El inhibidor puede ser administrado después del episodio de epilepsia, pero no más tarde de una o más semanas, p. ej. no después de aproximadamente 1, 1, 5, 2, 2, 5 o 3 semanas después del episodio.
El momento de la administración después de un episodio de epilepsia puede ser medido a partir del momento del inicio del episodio (p. ej.... [Seguir leyendo]
Reivindicaciones:
1. Un inhibidor de PSD-95 que bloquea la unión de un ligando de unión con PDZ a un dominio PDZ de PSD95 para su uso en el tratamiento de la epilepsia, en donde el inhibidor es administrado al menos aproximadamente una hora después de la terminación de un episodio de epilepsia.
3. El inhibidor para ser usado en la reivindicación 2ª, en donde el péptido es KLSSIESDV (SEC ID NO: 9) o KLSSIETDV (SEC ID NO: 7) , opcionalmente en donde el péptido está enlazado a un péptido de internalización.
5. El inhibidor para ser usado en cualquiera de las reivindicaciones precedentes, en donde la actividad 15 epiléptica se observa en la región CA1 del cerebro.
6. El inhibidor para ser usado en cualquiera de las reivindicaciones precedentes, en donde el episodio de epilepsia tiene una duración de menos de aproximadamente 10 minutos.
7. El inhibidor para ser usado en cualquiera de las reivindicaciones precedentes, en donde la duración del episodio de epilepsia se determina usando electroencefalografía.
8. El inhibidor para ser usado en cualquiera de las reivindicaciones precedentes, en donde el inhibidor se administra al menos aproximadamente tres horas después de la terminación de un episodio de epilepsia.
9. El inhibidor para ser usado en cualquiera de las reivindicaciones precedentes, en donde el inhibidor se administra no más tarde de aproximadamente una semana después de la terminación de un episodio de epilepsia.
10. El inhibidor para ser usado en cualquiera de las reivindicaciones precedentes, en donde el inhibidor se 25 administra no más tarde de aproximadamente un día después de la terminación de un episodio de epilepsia.
11. El inhibidor para ser usado en cualquiera de las reivindicaciones precedentes, en donde el inhibidor es Tat-NR2B9c (SEC ID NO: 10) .
12. El inhibidor para ser usado en cualquiera de las reivindicaciones precedentes, en donde el inhibidor es F-Tat-NR2B9C (SEC ID NO: 46) .
13. El inhibidor para ser usado según cualquiera de las reivindicaciones precedentes, en donde el inhibidor es 0625-0057.
14. El inhibidor para ser usado según cualquiera de las reivindicaciones precedentes, que tiene la estructura:
en donde R1 es un miembro elegido entre el grupo que consiste en ciclohexilo sustituido con 0-4 R7, fenilo sustituido 35 con 0-4 R7, - (CH2) u- (CHR8R9) , un alquilo C1-6 ramificado (isopropilo, isobutilo, 1-isopropil-2-metil-butilo, 1-etil-propilo) , y -NH-C (O) - (CR10R11) vH;
cada R7 es independientemente un miembro elegido entre el grupo que consiste en alquilo C1-6, alcoxi C1-6, -C (O) R12, OH, COOH, -NO, indolina N-sustituida y un péptido de translocación de la membrana celular
cada R8 y R9 se elige independientemente entre el grupo que consiste en H, OH, ciclohexano, ciclopentano, fenilo,
fenilo sustituido (p. ej. sustituido con grupos halo, alquilo y/o hidroxilo) y ciclopentadieno; cada R10 y R11 se elige independientemente entre el grupo que consiste en H, ciclohexano, fenilo y un péptido de translocación de la membrana celular;
R12 es un miembro elegido entre el grupo que consiste en alquilo C1-6 y arilo; y
cada uno de los valores u y v son independientemente de 0 a 20;
en donde uno de los grupos R2, R3, R4, R5 y R6 es -COOH, y en donde el resto de los grupos R2, R3, R4, R5 y R6 son elegidos cada uno de ellos independientemente entre el grupo que consiste en F, H, OCH3 y CH3.
Figura 1
Figura 2
Figura 3
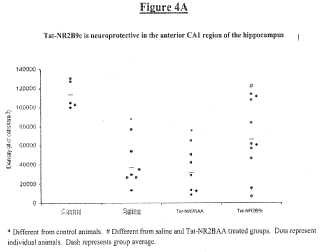
Figura 4A
Figura 5
Patentes similares o relacionadas:
Inmunoterapia novedosa contra diversos tumores, entre ellos tumores cerebrales y neuronales, del 22 de Julio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido que comprende una secuencia de aminoácidos acorde con la SEQ ID N.º 19, en que dicho péptido tiene una longitud total de entre 9 y 16 aminoácidos.
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Métodos de tratamiento y prevención de infecciones por staphylococcus aureus y afecciones asociadas, del 15 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición para uso en un método de inmunización de un sujeto contra la infección por S. aureus, comprendiendo dicha composición: (i) un fragmento de polipéptido […]
Administración de agentes terapéuticos mediante una proteína de unión a colágeno, del 15 de Julio de 2020, de THE BOARD OF TRUSTEES OF THE UNIVERSITY OF ARKANSAS: Una composición que comprende un segmento polipeptídico de unión a colágeno de origen bacteriano unido a un agente terapéutico, para su uso en el tratamiento […]
Polipéptidos de unión específica novedosos y usos de los mismos, del 15 de Julio de 2020, de Pieris Pharmaceuticals GmbH: Muteína de lipocalina lagrimal humana que tiene especificidad de unión para IL-17A, en la que la muteína se une a IL-17A con una KD de aproximadamente 1 nM o menos, en la que […]
Composiciones farmacéuticas para el tratamiento de superinfecciones bacterianas post-influenza, del 24 de Junio de 2020, de INSERM (INSTITUT NATIONAL DE LA SANTE ET DE LA RECHERCHE MEDICALE): Un polipéptido de flagelina en combinación con al menos un antibiótico para su uso en el tratamiento de una superinfección bacteriana post-influenza […]
Reactivos SIRP-alfa de alta afinidad, del 24 de Junio de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un polipéptido SIRPα de alta afinidad que comprende al menos una y no más de 15 modificaciones de aminoácidos dentro del dominio d1 de una secuencia SIRPα de tipo […]
Péptidos de unión beta amiloide y sus usos para el tratamiento y el diagnóstico de la demencia de Alzheimer, del 17 de Junio de 2020, de Priavoid GmbH: Péptido que contiene al menos una secuencia de aminoácidos que se une a especies beta amiloides y en el que la carga negativa del grupo carboxilo presente […]