Selección de fármacos para terapia del cáncer de mama utilizando matrices de anticuerpos.
Método que comprende:
(a) lisar células de un tumor mamario aislado tras la administración de un fármaco anticáncer,
o previamente a laincubación con un fármaco anticáncer, para producir un extracto celular,
(b) detectar un estado de activación de uno o más analitos en el extracto celular utilizando un ensayo quecomprende una pluralidad de series de dilución de anticuerpos de captura específicos de uno o más analitos, enel que los anticuerpos de captura se inmovilizan sobre un soporte sólido, y en el que el ensayo comprende:
(i) incubar el extracto celular con una pluralidad de series de dilución de anticuerpos de captura para formaruna pluralidad de analitos capturados,
(ii) incubar la pluralidad de analitos capturados con anticuerpos de detección que comprenden una pluralidadde anticuerpos independientes del estado de activación y una pluralidad de anticuerpos dependientes delestado de activación específicos para los analitos correspondientes con el fin de formar una pluralidad deanalitos capturados detectables, en el que los anticuerpos independientes de estado de activación se marcancon glucosidasa oxidasa, en el que la glucosa oxidasa y los anticuerpos independientes del estado deactivación se conjugan con una molécula de dextrano activada por sulfhidrilo, en el que los anticuerposdependientes del estado de activación se marcan con un primer miembro de una pareja de amplificación deseñales y en el que la glucosa oxidasa genera un agente oxidante que se canaliza y reacciona con el primermiembro de la pareja de amplificación de señales,
(iii) incubar la pluralidad de analitos capturados detectables con un segundo miembro de la pareja deamplificación de señal para generar una señal amplificada, y
(iv) detectar la señal amplificada generada a partir del primer y segundo miembros de la pareja deamplificación de señales, y
(c) determinar si el fármaco anticáncer resulta adecuado o inadecuado para el tratamiento del tumor de mamamediante comparación del estado de activación detectado para uno o más analitos con un perfil de activación dereferencia generado en ausencia del fármaco anticáncer, en el que el método está destinado a la selección de unfármaco anticáncer adecuado para el tratamiento de un tumor de mama.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/035013.
Solicitante: NESTEC S.A..
Nacionalidad solicitante: Suiza.
Dirección: AVENUE NESTLE 55 1800 VEVEY SUIZA.
Inventor/es: SINGH, SHARAT, HARVEY,JEANNE, KIM,PHILLIP, LIU,XINJUN, LIU,LIMIN, BARHAM,ROBERT, NERI,BRUCE.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
PDF original: ES-2398618_T3.pdf
Fragmento de la descripción:
Selección de fármacos para terapia del cáncer de mama utilizando matrices de anticuerpos ANTECEDENTES DE LA INVENCIÓN
El proceso de transducción de señales en las células es responsable de una diversidad de funciones biológicas, entre ellas la división y muerte celular, el metabolismo, la activación de las células inmunológicas, la neurotransmisión y la percepción sensorial, entre otras muchas. De acuerdo con lo anteriormente expuesto, los trastornos en la transducción normal de señales en las células pueden conducir a varios estados patológicos, tales como la diabetes, las enfermedades cardiovasculares, la autoinmunidad y el cáncer.
Una ruta de transducción de señales bien caracterizada es la ruta de la MAP quinasa, que es responsable de la transducción de la señal del factor de crecimiento epidérmico (EGF) de estimulación de la proliferación celular en las células (ver la figura 1) . El EGF se une a una tirosina quinasa unida a receptor transmembranal, el receptor del factor de crecimiento epidérmico (EGFR) , que resulta activado por la unión del EGF. La unión de EGF al EGFR activa la actividad de tirosina quinasa del dominio citoplasmático del receptor. Una consecuencia de esta activación de quinasa es la autofosforilación del EGFR en los residuos de tirosina. Los residuos de tirosina fosforilada en el EGFR activado proporcionan un sitio de anclaje para la unión de proteínas adaptadoras que contienen dominio SH2, tales como GRB2. En su función de adaptador, GRB2 se une además a un factor de intercambio de nucleótidos guanina, SOS, mediante un dominio SH3 en GRB2. La formación del complejo EGFR-GRB2-SOS conduce a la activación de SOS del factor de intercambio de nucleótidos de guanina, que estimula la eliminación de GDP de Ras. Tras la eliminación de GDP, Ras se une a GTP y resulta activado.
Tras la activación, Ras se une y activa la actividad de proteína quinasa de la RAF quinasa, una proteína quinasa específica de serina/treonina. A continuación se activa una cascada de proteínas quinasas que conduce a la proliferación celular. En líneas generales, la RAF quinasa fosforila y activa la MEK, otra serina/treonina quinasa. La MEK activada fosforila y activa la proteína quinasa activada por mitógeno (MAPK) . Entre las dianas para la fosforilación adicional por la MAPK se encuentran la proteína ribosómica 40S quinasa S6 (RSK) . La fosforilación de la RSK por la MAPK resulta en la activación de RSK, que a su vez fosforila la proteína ribosómica S6. Otra diana conocida de la MAPK es el protooncogén c-Myc, un gen importante para la proliferación celular que se encuentra mutado en una diversidad de cánceres. MAPK también fosforila y activa otra proteína quinasa, MNK, que a su vez fosforila el factor de transcripción CREB. Indirectamente, MAPK regula además la transcripción del gen Fos, que codifica todavía otro factor de transcripción que participa en la proliferación celular. Mediante la alteración de los niveles y actividades de dichos factores de transcripción, MAPK transduce la señal extracelular originaria del EGF llevando a una transcripción alterada de genes que resultan importantes para la progresión del ciclo celular.
Dada la función crucial que desempeñan las rutas de transducción de señales en el crecimiento celular, no sorprende que muchos cánceres aparezcan como resultado de mutaciones y otras alteraciones en componentes de la transducción de señales que resultan en la activación aberrante de las rutas de proliferación celular. Por ejemplo, la sobreexpresión o hiperactividad de EGFR se ha asociado a varios cánceres, incluyendo el glioblastoma multiforme, el cáncer de colon y el cáncer de pulmón. Esto ha impulsado el desarrollo de terapéuticas anticáncer dirigidas contra EGFR, incluyendo el gefitinib y el erlotinib para el cáncer de pulmón, y el cetuximab para el cáncer de colon.
El cetuximab es un ejemplo de un inhibidor de anticuerpos monoclonales, el cual se une al dominio del EGFR de unión a ligandos extracelulares, impidiendo de esta manera la unión de ligandos que activan la EGFR tirosina quinasa. En contraste, el gefitinib y el erlotinib son moléculas pequeñas que inhiben la EGFR tirosina quinasa de localización intracelular. En ausencia de actividad de quinasa, el EGFR no puede autofosforilarse en los residuos de tirosina, lo que es un requisito previo para la unión de proteínas adaptadoras posteriores, tales como GRB2. Al detener la cascada de señalización en las células basadas en esta ruta para el crecimiento, se reducen la proliferación y migración tumorales.
Además, otros estudios han demostrado que aproximadamente 70% de los melanomas humanos y una fracción menor de otros tumores presentan una mutación puntual (V599E) en el gen Raf que conduce a la activación persistente de la ruta de MPAK (ver, por ejemplo, Davies et al., Nature 417:949-954, 2002) . Estos resultados sugieren que las mutaciones, en particular en las rutas de transducción de señales, pueden ser características de tipos particulares de tumor y que dichas rutas específicas alteradas de transducción de señales podrían ser una diana prometedora para la intervención quimioterapéutica.
Dado que diferentes tratamiento del cáncer, particularmente la quimioterapia del cáncer, pueden funcionar directa o indirectamente mediante el bloqueo o la activación de las rutas celulares de transducción de señales implicadas en la proliferación o muerte celulares, respectivamente, la actividad de una ruta dada de transducción de señales en una forma particular de cáncer podría servir como un buen indicador de la eficacia de diversos tratamientos del cáncer. De acuerdo con lo anteriormente expuesto, además de satisfacer otras necesidades, la presente invención proporciona un método para evaluar la efectividad de las potenciales terapias anticáncer en un paciente individual.
De esta manera, la presente invención proporciona métodos para ayudar al médico a seleccionar una terapia del cáncer adecuada, a la dosis correcta y en el momento correcto para cada paciente.
BREVE DESCRIPCIÓN RESUMIDA DE LA INVENCIÓN
La presente invención proporciona métodos según las reivindicaciones para detectar los estados de activación de los componentes de las rutas de transducción de señales en las células tumorales (por ejemplo células circulantes de un tumor mamario) . La información sobre los estados de activación de los componentes de las rutas de transducción de señales derivadas de la práctica de la presente invención puede utilizarse para el diagnóstico del cáncer, para el pronóstico y para el diseño de tratamientos del cáncer.
En un aspecto, la presente invención proporciona un método según la reivindicación 1 para seleccionar un fármaco anticáncer adecuado para el tratamiento de un tumor mamario, comprendiendo el método:
(a) lisar células de un tumor mamario aislado tras la administración de un fármaco anticáncer, o previamente a la incubación con un fármaco anticáncer, para producir un extracto celular, (b) detectar un estado de activación de uno o más analitos en el extracto celular utilizando un ensayo que comprende una pluralidad de series de dilución de anticuerpos de captura específicos de uno o más analitos, en el que los anticuerpos de captura se inmovilizan sobre un soporte sólido, y
(c) determinar si el fármaco anticáncer resulta adecuado o inadecuado para el tratamiento del tumor de mama mediante comparación del estado de activación detectado para uno o más analitos con un perfil de activación de referencia generado en ausencia del fármaco anticáncer.
En una realización preferente, el método según, la presente invención proporciona un método según la reivindicación 1 para la selección de un fármaco anticáncer adecuado para el tratamiento de un tumor mamario, comprendiendo el método:
(a) lisar células de un tumor mamario aislado tras la administración de un fármaco anticáncer, o previamente a la incubación con un fármaco anticáncer, para producir un extracto celular,
(b) detectar un estado de activación de uno o más analitos en el extracto celular utilizando un ensayo que comprende una pluralidad de series de dilución de anticuerpos de captura específicos de uno o más analitos, en el que los anticuerpos de captura se inmovilizan sobre un soporte sólido,
(c) comparar el estado de activación detectado para el analito o analitos con un perfil de activación de referencia generado en ausencia del fármaco anticáncer, e
(d) indicación de que el fármaco anticáncer resulta adecuado para el tratamiento del tumor mamario en el caso de que el estado de activación detectado para el analito... [Seguir leyendo]
Reivindicaciones:
1. Método que comprende:
(a) lisar células de un tumor mamario aislado tras la administración de un fármaco anticáncer, o previamente a la incubación con un fármaco anticáncer, para producir un extracto celular,
(b) detectar un estado de activación de uno o más analitos en el extracto celular utilizando un ensayo que comprende una pluralidad de series de dilución de anticuerpos de captura específicos de uno o más analitos, en el que los anticuerpos de captura se inmovilizan sobre un soporte sólido, y en el que el ensayo comprende:
(i) incubar el extracto celular con una pluralidad de series de dilución de anticuerpos de captura para formar una pluralidad de analitos capturados,
(ii) incubar la pluralidad de analitos capturados con anticuerpos de detección que comprenden una pluralidad de anticuerpos independientes del estado de activación y una pluralidad de anticuerpos dependientes del estado de activación específicos para los analitos correspondientes con el fin de formar una pluralidad de analitos capturados detectables, en el que los anticuerpos independientes de estado de activación se marcan con glucosidasa oxidasa, en el que la glucosa oxidasa y los anticuerpos independientes del estado de activación se conjugan con una molécula de dextrano activada por sulfhidrilo, en el que los anticuerpos dependientes del estado de activación se marcan con un primer miembro de una pareja de amplificación de señales y en el que la glucosa oxidasa genera un agente oxidante que se canaliza y reacciona con el primer miembro de la pareja de amplificación de señales,
(iii) incubar la pluralidad de analitos capturados detectables con un segundo miembro de la pareja de amplificación de señal para generar una señal amplificada, y
(iv) detectar la señal amplificada generada a partir del primer y segundo miembros de la pareja de amplificación de señales, y
(c) determinar si el fármaco anticáncer resulta adecuado o inadecuado para el tratamiento del tumor de mama mediante comparación del estado de activación detectado para uno o más analitos con un perfil de activación de referencia generado en ausencia del fármaco anticáncer, en el que el método está destinado a la selección de un fármaco anticáncer adecuado para el tratamiento de un tumor de mama.
2. Método según la reivindicación 1, en el que la etapa (c) comprende identificar el tumor de mama como sensible o no sensible al tratamiento con el fármaco anticáncer mediante comparación del estado de activación detectado para el analito o analitos con un perfil de activación de referencia generado en ausencia del fármaco anticáncer, en el que el método está destinado a la identificación de la respuesta de un tumor de mama al tratamiento con un fármaco anticáncer.
3. Método según la reivindicación 1, en el que la etapa (c) comprende predecir la probabilidad de que el sujeto responderá al tratamiento al tratamiento con el fármaco anticáncer mediante comparación del estado de activación detectado para el analito o analitos con un perfil de activación de referencia generado en ausencia del fármaco anticáncer, en el que el método está destinado a la predicción de la respuesta de un sujeto que presenta un tumor de mama al tratamiento con un fármaco anticáncer.
4. Método según cualquiera de las reivindicaciones 1 a 3, en el que el tumor de mama se deriva de un sujeto con carcinoma ductal, en el que el carcinoma ductal es preferentemente carcinoma ductal invasiva o carcinoma ductal in situ, o en el que el tumor de mama se deriva de un sujeto con carcinoma lobular, en el que el carcinoma lobular es preferentemente carcinoma lobular invasivo o carcinoma lobular in situ.
5. Método según cualquiera de las reivindicaciones 1 a 3, en el que las células comprenden células circulantes del tumor de mama, en el que las células circulantes preferentemente han sido aisladas de una muestra mediante separación inmunomagnética, en el que la muestra preferentemente se selecciona de entre el grupo que consiste de sangre completa, suero, plasma, lavado ductal, líquido aspirado del pezón, linfa, aspirado de médula ósea, orina, saliva, aspirado con aguja fina y combinaciones de los mismos, en el que las células circulantes preferentemente se seleccionan de entre el grupo que consiste de células tumorales circulantes, células endoteliales circulantes, células progenitoras endoteliales circulantes, células madre cancerosas, células tumorales diseminadas y combinaciones de las mismas.
6. Método según cualquiera de las reivindicaciones 1 a 3, en el que las células han sido aisladas a partir de tejido tumoral, en el que el tejido tumoral preferentemente es tejido tumoral primario o tejido tumoral metastásico, en el que las células preferentemente han sido aisladas de tejido tumoral en forma de una muestra de aspirado con aguja fina.
7. Método según cualquiera de las reivindicaciones 1 a 3, en el que las células aisladas se estimulan in vitro con factores de crecimiento.
8. Método según cualquiera de las reivindicaciones 1 a 3, en el que el fármaco anticáncer se selecciona de
entre el grupo que consiste de un anticuerpo monoclonal, inhibidor de tirosina quinasa, agente quimioterapéutico, agente terapéutico hormonal, agente radioterapéutico, vacuna, y combinaciones de los mismos, en el que el anticuerpo monoclnoal preferentemente se selecciona de entre el grupo que consiste de trastuzumab (Herceptina®) , alemtuzumab (Campath®) , bevacizumab (Avastin®) , cetuximab (Erbitux®) , gemtuzumab (Mylotarg®) , panitumumab (VectibixTM) , rituximab (Rituxan®) , tositumomab (BEXXAR®) y combinaciones de los mismos, en el que el inhibidor de tirosina quinasa preferentemente se selecciona de entre el grupo que consiste de gefitinib (Iressa®) , sunitinib (Sutent®) , erlotinib (Tarceva®) , lapatinib (Tykerb®) , canertinib (CI 1033) , semaxinib (SU5416) , vatalanib (PTK787/ZK222584) , sorafenib (BA.
4. 9006) , mesilato de imatinib (Gleevec®) , leflunómido (SU101) , vandetanib (ZACTIMA TM, ZD6474) y combinaciones de los mismos, en el que el agente quimioterapéutico se selecciona preferentemente de entre el grupo que consiste de pemetrexed (ALIMTA®) , gemcitabina (Gemzar®) , sirolimus (rapamicina) , análogos de rapamicina, compuestos de platino, carboplatino, cisplatino, straplatino, paclitaxel (Taxol®) , docetaxel (Taxotere®) , temsirolimus (CCI-779) , everolimus (RAD001) y combinaciones de los mismos, en el que el agente terapéutico hormonal preferentemente se selecciona de entre el grupo que consiste de inhibidores de aromatasa, moduladores selectivos de receptores de estrógeno, esteroides, finastérido, agonistas de hormona liberadora de gonadotropina, sales farmacéuticamente aceptables de los mismos, esteroisómeros de los mismos, derivados de los mismos, análogos de los mismos, y combinaciones de los mismos, en el que el agente radioterapéutico preferentemente se selecciona de entre el grupo que consiste de 47Sc, 64Cu, 67Cu, 89Sr, 86Y, 87Y, 90Y, 105Rh, 111Ag, 111In, 117mSn, 149Pm, 153Sm, 166Ho, 177Lu, 186Re, 188Re, 211At, 212Bi, y combinaciones de los mismos.
9. Método según cualquiera de las reivindicaciones 1 a 3, en el que uno o más analitos comprenden una pluralidad de moléculas de transducción de señales, en el que la pluralidad de moléculas de transducción de señales preferentemente se selecciona de entre el grupo que consiste de receptores de tirosina quinasa, no receptores de tirosina quinasa, componentes de la cascada de señalización de tirosina quinasa, receptores de hormona nuclear, coactivadores de receptor nuclear, represores de receptor nuclear, y combinaciones de los mismos, en el que la pluralidad de moléculas de transducción de señales preferentemente se selecciona de entre el grupo que consiste de EGFR (ErbB1) , HER-2 (ErbB2) , ErbB2 p95, HER-3 (ErbB3) , HER-4 (ErbB4) , Raf, SRC, Mek, NFkB-IkB, mTor, PI3K, VEGF, VEGFR-1, VEGFR-2, VEGFR-3, Eph-a, Eph-b, Eph-c, Eph-d, cMet, FGFR, cKit, Flt-3, Tie-1, Tie-2, Flt3, cFMS, PDGFRA, PDGFRB, Abl, FTL 3, RET, Kit, HGFR, FGFR1, FGFR2, FGFR3, FGFR4, IGF-1R, RE, RP, NCOR, AIB1, y combinaciones de los mismos, o en el que la pluralidad de moléculas de transducción de señales preferentemente se selecciona de entre el grupo que consiste de ErbB1, ErbB2, ErbB2 p95, ErbB3, ErbB4, VEGFR1, VEGFR-2, VEGFR-3, RE, PR y combinaciones de los mismos.
10. Método según cualquiera de las reivindicaciones 1 a 3, en el que el estado de activación se selecciona de entre el grupo que consiste de un estado de fosforilación, un estado de ubiquitinación, un estado de acomplejamiento y combinaciones de los mismos.
11. Método según cualquiera de las reivindicaciones 1 a 3, en el que el soporte sólido se selecciona de entre el grupo que consiste de vidrio, plástico, chips, agujas, filtros, perlas, papel, membranas, haces de fibras y combinaciones de los mismos.
12. Método según cualquiera de las reivindicaciones 1 a 3, en el que los anticuerpos de captura se inmovilizan sobre el soporte sólido en una matriz direccionable.
13. Método según cualquiera de las reivindicaciones 1 a 3, en el que los anticuerpos dependientes del estado de activación se marcan directamente con el primer miembro de la pareja de amplificación de señales, o en el que los anticuerpos dependientes del estado de activación se marcan con el primer miembro de la pareja de amplificación de señales mediante unión entre un primer miembro de una pareja de unión conjugada con los anticuerpos dependientes del estado de activación y un segundo miembro de la pareja de unión conjugada con el primer miembro de la pareja de amplificación de señales, en el que el primer miembro de la pareja de unión preferentemente es biotina, y en el que el segundo miembro de la pareja de unión preferentemente es estreptavidina.
14. Método según cualquiera de las reivindicaciones 1 a 3, en el que la molécula de dextrano activada por sulfhidrilo presenta un peso molecular de 500 kDa.
15. Método según cualquiera de las reivindicaciones 1 a 3, en el que el agente oxidante es el peróxido de hidrógeno (H2O2) .
16. Método según la reivindicación 15, en el que el primer miembro de la pareja de amplificación de señales es una peroxidasa, preferentemente peroxidasa de rábano picante (HRP) y/o en el que el segundo miembro de la pareja de amplificación de señales es un reactivo tiramida, preferentemente biotina-tiramida.
17. Método según la reivindicación 16, en el que la señal amplificada es generada por la oxidación con peroxidasa de la biotina-tiramida para producir una tiramida activada.
18. Método según la reivindicación 17, en el que la tiramida activada se detecta directamente, o en el que la
tiramida activada se detecta tras la adición de una reactivo detector de señales, en el que el reactivo detector de señales preferentemente es un fluoróforo marcado con estreptavidina o una combinación de una peroxidasa marcada con estreptavidina y un reactivo cromogénico, en el que el reactivo cromogénico preferentemente es 3, 3', 5, 5'-tetrametilbencidina (TMB) .
19. Utilización de una matriz que comprende una pluralidad de series de dilución de anticuerpos de captura inmovilizados sobre un soporte sólido, en el que los anticuerpos de captura en cada serie de dilución son específicos para uno o más analitos correspondientes a un componente de una ruta de transducción de señales en un extracto celular, para llevar a cabo el método según cualquiera de las reivindicaciones 1 a 3.
FIG. 4
FIG. 5 FIG.6
FIGURA 7 FIG, 8
FIG.9 FIG.10
FIG. 11 FIG. 12 FIG13
FIG.14
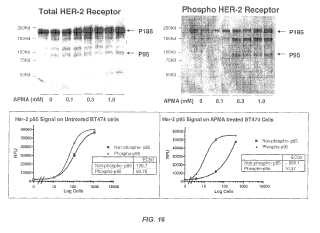
FIG.17
FIG.19
FIG. 21
FIG. 23
Patentes similares o relacionadas:
Cultivo de tejido tridimensional heterogéneamente diferenciado, del 22 de Julio de 2020, de IMBA-INSTITUT FÜR MOLEKULARE BIOTECHNOLOGIE GMBH: Un cultivo de tejido neuronal tridimensional artificial cultivado in vitro que comprende una población heterogénea de células humanas o células de primate no humanas […]
Gangliósidos para estandarizar y aumentar la sensibilidad de las células a las neurotoxinas botulínicas en los sistemas de prueba in vitro, del 15 de Julio de 2020, de MERZ PHARMA GMBH & CO. KGAA: Un método para determinar la actividad biológica de un polipéptido de neurotoxina, que comprende las etapas de: a) cultivar neuronas de diferentes […]
Procedimiento para evaluación de la función hepática y el flujo sanguíneo portal, del 15 de Julio de 2020, de The Regents of the University of Colorado, a body corporate: Procedimiento in vitro para la estimación del flujo sanguíneo portal en un individuo a partir de una única muestra de sangre o suero, comprendiendo el procedimiento: […]
ANTICUERPOS MONOCLONALES ESPECÍFICOS PARA EL ANTÍGENO PB2 DEL VIRUS DE LA INFLUENZA HUMANA (FLU), SECUENCIAS NUCLEOTÍDICAS; MÉTODO Y KIT DE DIAGNÓSTICO DE INFECCIÓN PRODUCIDA POR FLU, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína PB2 del virus de la influenza humana (Flu), […]
ANTICUERPO MONOCLONAL O UNA PORCIÓN DE UNIÓN A ANTÍGENO DEL MISMO QUE SE UNE A LA PROTEÍNA L DEL VIRUS PARAINFLUENZA HUMANO (PIV); MÉTODO Y KIT PARA DETECTAR AL VIRUS PIV, del 2 de Julio de 2020, de PONTIFICIA UNIVERSIDAD CATÓLICA DE CHILE: La invención presenta la generación de anticuerpos monoclonales, o fragmentos de los mismos, que reconocen la proteína L del virus parainfluenza humano (PIV), donde dichos […]
Diagnóstico y terapia de cáncer que implica células madre cancerosas, del 24 de Junio de 2020, de BioNTech SE: Un anticuerpo que tiene la capacidad de unirse a Claudina 6 (CLDN6) para usar en un método de tratamiento o prevención del cáncer que comprende inhibir y/o eliminar […]
Nueva inmunoterapia contra diversos tumores como el cáncer gastrointestinal y gástrico, del 24 de Junio de 2020, de IMMATICS BIOTECHNOLOGIES GMBH: Péptido seleccionado del grupo siguiente: a) péptido consistente en la secuencia conforme a la SEQ ID N.º 86, b) el péptido conforme a a), en la […]
Reactivos SIRP-alfa de alta afinidad, del 24 de Junio de 2020, de THE BOARD OF TRUSTEES OF THE LELAND STANFORD JUNIOR UNIVERSITY: Un polipéptido SIRPα de alta afinidad que comprende al menos una y no más de 15 modificaciones de aminoácidos dentro del dominio d1 de una secuencia SIRPα de tipo […]