Régimen de dosificación de ibuprofeno de liberación inmediata y de liberación sostenida.
Una forma de dosificación que comprende una parte de liberación inmediata que contiene una dosis de liberación inmediata de ibuprofeno,
o sales farmacéuticamente aceptables de los mismas, y una parte de liberación sostenida que contiene una segunda dosis de dicho ibuprofeno, o sales farmacéuticamente aceptables de las mismas, siendo dicha dosis inicial al menos el doble de dicha segunda dosis y, en el que la forma de dosificación se selecciona de:
a) Comprimido 1 bicapa (sin recubrimiento)
Formulación de liberación inmediata de ibuprofeno.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/075990.
Solicitante: MCNEIL-PPC, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: GRANDVIEW ROAD SKILLMAN, NJ 08558 ESTADOS UNIDOS DE AMERICA.
Inventor/es: LEE, DER-YANG, BUNICK,FRANK, SCHWING,JAMES.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/19 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Acidos carboxílicos, p. ej.ácido valproico (ácido salicílico A61K 31/60).
- A61K9/20 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › Píldoras, pastillas o comprimidos.
- A61K9/28 A61K 9/00 […] › Grageas; Píldoras o comprimidos con revestimientos.
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
PDF original: ES-2438267_T3.pdf
Fragmento de la descripción:
Régimen de dosificación de Ibuprofeno de liberación inmediata y de liberación sostenida.
La presente invención se refiere a un nuevo régimen de dosificación para los fármacos antiinflamatorios no esteroideos, particularmente los ácidos propiónicos. Este régimen de dosificación proporciona un efecto terapéutico sostenido sobre periodos de tiempo prolongados.
Antecedentes de la invención Los agentes terapéuticos para el tratamiento del dolor, la inflamación y la fiebre incluyen analgésicos, antiinflamatorios y antipiréticos. Los fármacos antiinflamatorios no esteroideos (AINES) son un tipo de dichos agentes terapéuticos. Incluyen derivados de ácido propiónico, derivados de ácido acético, derivados de ácido fenamico, derivados de ácido bifenilcarboxílico, oxicamas y ciclooxigenasa – 2 (COX – 2) selectiva de AINES.
Los ácidos propiónicos incluyen por ejemplo, ibuprofeno, naproxeno y ketoprofeno.
El ibuprofeno en particular, es ampliamente utilizado y un AINE muy conocido que posee propiedades analgésicas y antipiréticas. El ibuprofeno es químicamente conocido como ácido 2 – (4 – isobutilfenil) –propiónico. Ha estado disponible comercialmente como un fármaco de venta sin receta médica en muchas formas durante varios años.
Los AINES se administran típicamente en una base diaria de una a cuatro veces, con una dosis diaria que oscila entre 50 y 2000 miligramos, preferiblemente de 100 a 1600 y más preferiblemente entre 200 y 1200 miligramos.
Es conocida la administración de AINES y otros fármacos en dosis múltiples entre 12 o 24 horas. Por ejemplo, es conocida la administración de dosis múltiples que contienen las mismas cantidades de ibuprofeno entre 12 y 24 horas. Se conocen también formas de dosificación de liberación sostenida que contienen ibuprofeno.
En Palmisano et al., Advances in Therapy, Vol. 5, Nº 4, July / August 1988 se informa sobre el studio de ketoprofeno e ibuprofeno para el tratamiento de la dismenorrea primaria. Esta referencia describe el empleo de dosis múltiples de ketopreno (dosis inicial de 150 mg seguida por dosis posteriores de 75 mg) e ibuprofeno (dosis inicial de 800 mg seguida por dosis posteriores de 400 mg) .
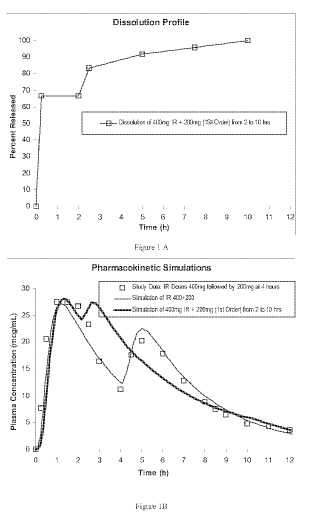
Se realizó un estudio PK / PD del dolor dental de una institución única aleatorizado paralelo de doble ciego controlado con placebo durante un periodo de observación de 12 horas para evaluar los perfiles de seguridad, eficacia, farmacodinámica, farmacocinética de algunos regímenes de dosificación de ibuprofeno. En concreto, se comparó una dosis única de comprimidos de liberación prolongada de 600 mg de ibuprofeno con la dosis total de comprimidos de 200 mg de liberación inmediata de ibuprofeno administradas en tres regímenes de dosificación diferentes además de placebo en el tratamiento del dolor dental post – operatorio que oscila entre moderado y severo. Se administró el ibuprofeno en comprimidos de liberación prolongada de 600 mg o en uno o más comprimidos de liberación inmediata de 200 mg de ibuprofeno. Un subgrupo de pacientes tenían tanto la evaluación farmacodinámica como la evaluación farmacocinética (grupo PK) . El otro subgrupo de pacientes tenían únicamente las evaluaciones de la eficacia analgésica (grupo sin PK) . Los pacientes de ambos grupos se asignaron al azar a uno de los cinco tratamientos siguientes:
Ibuprofeno de liberación prolongada Dosis única de 600 mg a las 0 horas
Ibuprofeno de liberación inmediata Dosis única de 600 mg a las 0 horas
Ibuprofeno de liberación inmediata 400 mg a las 0 horas; 200 mg a las 4 horas
Ibuprofeno de liberación inmediata 200 mg a las 0, 4 y 8 horas
Placebo
Se obtuvieron evaluaciones de los pacientes del intenso dolor y del alivio del dolor así como muestras de sangre para los análisis plasmáticos de ibuprofeno en el centro de estudio a las 0, 0, 25, 0, 5 1, 1, 5, 2, 2, 5, 3, 4, 4, 5, 5, 6, 7, 8, 8, 5, 9, 10, 11 y 12 horas. Se utilizó una técnica de cronometraje para medir el inicio del alivio del dolor significativo. El estudio reveló que la administración de ibuprofeno 400 / 200 / 0 proporciona un excelente alivio del dolor durante todo el periodo de estudio de 12 horas. Durante las primeras cuatro horas, el tratamiento 400 / 200 / 0, junto con el tratamiento de liberación inmediata 600 / 0 / 0, proporcionó un alivio superior del dolor sobre otros tratamientos. Durante el intervalo de 4 a 12 horas, el tratamiento 400 / 200 / 0 sólo proporciona las más altas puntuaciones del alivio del dolor, a pesar de que no se administró más ibuprofeno después de las primeras cuatro horas.
Los solicitantes han descubierto recientemente que el ibuprofeno puede proporcionarse a un mamífero, en la forma preferente a un ser humano, en una etapa de dosificación única específica para lograr el efecto terapéutico mejorado, especialmente del alivio del dolor, en comparación con los regímenes de dosificación conocidos y en una forma de dosis conveniente / conforme. En particular, puede proporcionarse ibuprofeno a mamíferos en una forma de dosificación para proporcionar una dosis inicial de liberación inmediata seguida por una segunda dosis de liberación sostenida de ibuprofeno. No se requieren más dosis para proporcionar una Cmim de 5 – 10 mcg / mL para un periodo de al menos 8 horas tras la administración de la forma de dosificación.
Resumen de la invención El documento WO9641617 revela un comprimido de doble capa que contiene una capa de liberación inmediata y una capa de liberación prolongada.
El documento EP0255002 revela una forma de dosificación que comprende una dosis de liberación inmediata de un componente activo que tiene una actividad antiinflamatoria y una dosis de liberación controlada del compuesto activo.
El documento US2004 / 186180 revela una forma de dosificación que comprende una parte de liberación inmediata que contiene una dosis inicial de un fármaco antiinflamatorio no esteroideo y una parte de liberación burst retardada que contiene una segunda dosis del fármaco antiinflamatorio no esteroideo.
En Lopes et al se revelan sistemas de entrega bifásicos de minicomprimidos comprimidos diseñados para liberar el fármaco de orden cero. (International Journal of Pharmaceutics, 2006, 323, 93 – 100)
En Maggi et al. se revelan comprimidos bicapa que comprenden una capa de liberación inmediata y una capa de liberación prolongada. (European Journal of Pharmaceutics and Biopharmaceutics, 1999, 48, 37 – 42)
La invención proporciona una forma de dosificación que comprende una parte de liberación inmediata que contiene una dosis de liberación inmediata de ibuprofeno, o sales farmacéuticamente aceptables de las mismas, y una parte de liberación sostenida que contiene una segunda dosis de dicho ibuprofeno, o sales farmacéuticamente aceptables de las mismas, siendo dicha dosis inicial al menos el doble de dicha segunda dosis y, en el que la forma de dosificación se selecciona de:
a) Comprimido 1 bicapa (sin recubrimiento) Formulación de liberación inmediata de ibuprofeno
Principio W / W %
Ibuprofeno en polvo (Grado 115) 94, 0
Croscarmelosa de sodio (Ac – Di - Sol®) 5, 50
Amarillo # 6 FD & C Trazas
Estearato de magnesio 0, 50
Formulación de liberación sostenida de ibuprofeno
Ibuprofeno en polvo (Grado 115) 29, 5
Lactosa (flujo rápido) 31, 0
Hidroxipropilmetilcelulosa (HPMC K4M, Grago CR) 13
Hidroxipropilcelulosa (HPC EXF) 26
Rojo # 40 FD & C 0, 50
Estearato de magnesio 0, 50
b) Comprimido 2 bicapa (sin recubrimiento) Formulación de liberación inmediata de ibuprofeno Formulación de liberación sostenida de ibuprofeno
Principio W / W %
Ibuprofeno en polvo (Grado 115) 70, 0
Croscarmelosa de sodio (Ac – Di - Sol®) 5, 50
Celulosa microcristalina (Avicel PH 101) 24, 0
Amarillo # 6 FD & C Trazas
Estearato de magnesio 0, 50
Principio W / W %
Ibuprofeno (Grado 115) 44, 0
Lactosa (flujo rápido) 16, 5
Hidroxipropilmetilcelulosa (HPMC K4M, Grago CR) 13
Hidroxipropilcelulosa (HPC EXF) 26
Rojo # 40 FD & C Trazas
Estearato de magnesio 0, 50
c) Comprimido 1 recubierto bicapa La parte de liberación inmediata del comprimido bicapa de la opción (a) se recubre con:
Principio W / W %
Gelatina (Bloom 275) 30
Agua 70
Total 100
La parte de liberación sostenida del comprimido bicapa de la opción (a) se recubre con:
Principio W / W %
Goma Gellan, LT 100 0, 53
Gelcarin GP 812 2, 43
Hidroxipropilmetilcelulosa (HPMC K4M, Grago CR) 12, 73
Agua 84, 30
Total 100, 00
d) Comprimido 2 recubierto... [Seguir leyendo]
Reivindicaciones:
1. Una forma de dosificación que comprende una parte de liberación inmediata que contiene una dosis de liberación inmediata de ibuprofeno, o sales farmacéuticamente aceptables de los mismas, y una parte de liberación sostenida que contiene una segunda dosis de dicho ibuprofeno, o sales farmacéuticamente aceptables de las mismas, siendo dicha dosis inicial al menos el doble de dicha segunda dosis y, en el que la forma de dosificación se selecciona de:
a) Comprimido 1 bicapa (sin recubrimiento) Formulación de liberación inmediata de ibuprofeno
Principio W / W %
Ibuprofeno en polvo (Grado 115) 94, 0
Croscarmelosa de sodio (Ac – Di - Sol®) 5, 50
Amarillo # 6 FD & C Trazas
Estearato de magnesio 0, 50
Formulación de liberación sostenida de ibuprofeno
Ibuprofeno en polvo (Grado 115) 29, 5
Lactosa (flujo rápido) 31, 0
Hidroxipropilmetilcelulosa (HPMC K4M, Grago CR) 13
Hidroxipropilcelulosa (HPC EXF) 26
Rojo # 40 FD & C 0, 50
Estearato de magnesio 0, 50
b) Comprimido 2 bicapa (sin recubrimiento) Formulación de liberación inmediata de ibuprofeno
Principio W / W %
Ibuprofeno en polvo (Grado 115) 70, 0
Croscarmelosa de sodio (Ac – Di - Sol®) 5, 50
Celulosa microcristalina (Avicel PH 101) 24, 0
Amarillo # 6 FD & C Trazas
Estearato de magnesio 0, 50
Formulación de liberación sostenida de ibuprofeno
Principio W / W %
Ibuprofeno (Grado 115) 44, 0
Lactosa (flujo rápido) 16, 5
Hidroxipropilmetilcelulosa (HPMC K4M, Grago CR) 13
Hidroxipropilcelulosa (HPC EXF) 26
Rojo # 40 FD & C Trazas
Estearato de magnesio 0, 50
c) Comprimido 1 recubierto bicapa La parte de liberación inmediata del comprimido bicapa de la opción (a) se recubre con:
Principio W / W %
Gelatina (Bloom 275) 30
Agua 70
Total 100
La parte de liberación sostenida del comprimido bicapa de la opción (a) se recubre con:
Principio W / W %
Goma Gellan, LT 100 0, 53
Gelcarin GP 812 2, 43
Hidroxipropilmetilcelulosa (HPMC K4M, Grago CR) 12, 73
Agua 84, 30
Total 100, 00
d) Comprimido 2 recubierto bicapa La parte de liberación inmediata del comprimido bicapa de la opción (b) se recubre con:
Principio W / W %
Gelatina (Bloom 275) 30
Agua 70
Total 100
La parte de liberación sostenido del comprimido bicapa de la opción (b) se recubre con:
Principio W / W %
Goma Gellan, LT 100 0, 53
Gelcarin GP 812 2, 43
Hidroxipropilmetilcelulosa (HPMC K4M, Grago CR) 12, 73
Agua 84, 30
Total 10, 00
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Formulación de vitamina D de liberación modificada estabilizada y método de administración de la misma, del 22 de Julio de 2020, de EirGen Pharma Ltd: Una formulacion oral de liberacion controlada de un compuesto de vitamina D que comprende uno o ambos de 25- hidroxivitamina D2 y 25-hidroxivitamina D3, la formulacion […]
Métodos y composiciones para la administración oral de proteínas, del 22 de Julio de 2020, de Entera Bio Ltd: Una única composición farmacéutica oral que comprende una proteína que tiene un peso molecular de hasta 100.000 Daltons, siendo dicha proteína PTH; […]
Composición farmacéutica que comprende un agente antipsicótico atípico y método para su preparación, del 15 de Julio de 2020, de PHARMATHEN S.A.: Comprimido de liberación controlada de Paliperidona en forma de comprimido de varias capas que comprende: a) un núcleo de matriz que comprende […]
Composiciones y métodos para tratar el virus de la hepatitis C, del 15 de Julio de 2020, de Gilead Pharmasset LLC: Una composición farmacéutica que comprende: a) de aproximadamente el 25% a aproximadamente el 35% p/p de GS-7977 cristalino que tiene la estructura **(Ver […]
Macrogols para aplicación a la mucosa, y sus usos terapéuticos, del 15 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Composición farmacéutica en forma sólida que comprende, por unidad de dosificación, entre 5 y 400 mg de un PEG con un grado de 3000 o más, para uso en el tratamiento […]
Composición farmacéutica novedosa, del 1 de Julio de 2020, de NOVARTIS AG: Un comprimido farmaceutico que comprende: a) un farmaco que es el solvato con sulfoxido de dimetilo de N-{3-[3-ciclopropil-5-(2-fluoro-4-5 yodofenilamino)-6,8- dimetil-2,4,7-trioxo-3,4,6,7-tetrahidro-2H-pirido[4,3-d]pirimidin-1-il]fenil}acetamida […]
Preparación para el control del peso corporal a base de quitosano y celulosa, del 1 de Julio de 2020, de S.I.I.T. S.R.L.-SERVIZIO INTERNAZIONALE IMBALLAGGI TERMOSALDANTI: Una composición oral sólida que contiene una combinación de quitosano de hongos o levaduras, celulosa amorfa en polvo y opcionalmente excipientes.