Nuevos análogos no selectivos de somatostatina.
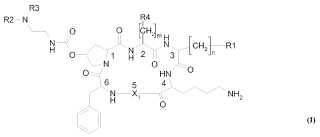
Compuestos de fórmula (I):**Fórmula**
Fórmula (I)
en donde m varía de 0 a 2;
n varía de 1 a 3; R1 es un grupo aromático, excluyendo indol, opcionalmentesustituido en una o más posiciones; R4 es un grupo aromático, opcionalmente sustituido; R2 y R3 son,independientemente, H o un grupo alquilo de C1-C4, o, juntos, son una cadena de alquileno de C4-C5, unida alátomo de nitrógeno para formar una estructura cíclica; o R3 es un catión o grupo quelante de metales;X1 es un residuo aminoacilo de fórmula (a), (b) o (c).
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/066081.
Solicitante: ITALFARMACO S.P.A..
Nacionalidad solicitante: Italia.
Dirección: VIALE FULVIO TESTI, 330 20126 MILANO ITALIA.
Inventor/es: MASCAGNI, PAOLO, PINORI, MASSIMO, VITALI,ANDREA.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/31 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Somatostatinas.
- A61K49/00 A61K […] › Preparaciones para examen in vivo.
- A61K49/08 A61K […] › A61K 49/00 Preparaciones para examen in vivo. › caracterizadas por el soporte.
- A61K49/14 A61K 49/00 […] › Péptidos, p. ej. proteínas.
- C07K14/655 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Somatostatinas.
PDF original: ES-2431573_T3.pdf
Fragmento de la descripción:
Nuevos análogos no selectivos de somatostatina La presente invención se refiere a nuevos ciclopéptidos análogos funcionales no selectivos de somatostatina, a sus conjugados y complejos, a procesos para la producción, a las formulaciones que los contienen y a sus usos en el campo farmacéutico.
Estado de la técnica Los agonistas peptídicos cíclicos de somatostatina se han conocido durante algún tiempo [J Pept Res 58 (2) , 91 (2001) ]: en particular, dos de estos, octreótido y lanreótido, se usan clínicamente para el cuidado de la acromegalia y para el tratamiento sintomático de carcinomas.
La somatostatina actúa mediante la interacción con 5 subtipos de receptores (SSTR1, 2, 3, 4 y 5) ; pero los análogos empleados hasta ahora en terapia son, sin embargo, esencialmente selectivos para el único receptor SSTR2.
La gran mayoría de los agonistas ya conocidos se caracteriza por la presencia, en la estructura del péptido, del
fragmento -DTrp-Lys-; por tanto, este fragmento parece ser esencial para la actividad de los análogos y de hecho está también está presente en octreótido y lanreótido.
Recientemente, se ha avanzado la hipótesis de que análogos menos selectivos, es decir, capaces de interaccionar también con otros subtipos de receptores, pueden ofrecer una ventaja desde el punto de vista del uso terapéutico [Nature Rev. Drug Discover y 2, 999 (2003) ].
En la solicitud de patente WO2002010192, se describe un ciclopéptido que tiene una fuerte afinidad para el receptor SSTR5, una menor afinidad para SSTR2 y SSTR3 y casi afinidad cero para SSTR4. Para SSTR1, se describe una afinidad de aproximadamente 60 veces menor que esa para SSTR5.
Los mismos inventores del documento WO2002010192, en una publicación posterior [Nature Rev. Drug Discover y 2, 999 (2003) ], sostienen la importancia de los receptores SSTR1, 2 y 5 para la actividad antisecretora de somatostatina, pero describen, para el mismo ciclopéptido descrito en la solicitud de patente anteriormente mencionada, una afinidad para SSTR1 de aproximadamente 300 menos que esa para SSTR5.
Está claro que, en este caso, una posible actividad terapéutica mediada por la interacción con el receptor SSTR1 solo se puede alcanzar en presencia de una sobredosis considerable con respecto a las acciones mediadas por la interacción con SSTR5.
Por tanto, mientras que el posible papel terapéutico de agonistas para el receptor SSTR4 no está claro, existe claramente la necesidad, y el posible uso, para nuevos análogos de somatostatina con un nivel de afinidad comparable para todos los otros cuatro receptores.
En particular, las potenciales ventajas terapéuticas de agonistas capaces de interaccionar con SSTR1 se describen 45 en la bibliografía: M.C. Zatelli y colaboradores ha estudiado, in vitro, el efecto de agonistas para SSTR1 en adenomas hipofisarios humanos, tanto secretores [J Clin End&Met 88, 2797 (2003) ] como clínicamente no funcionales [J Clin End&Met 89, 5181 (2004) ]; en ambos casos el estímulo de los receptores SSTR1 produjo una reducción de la actividad secretora y la viabilidad celular. Por otra parte, también se mostró la potencial ventaja terapéutica que puede derivar del uso de análogos pluripotentes de somatostatina (capaces de interaccionar con los 50 SSTR1, 2, 3 y 5) por J. van der Hoek y colaboradores en una revisión reciente [Curr. Pharm. Design 11, 1573 (2005) ]; de hecho se mostró cómo diferentes tumores, tanto hipofisarios como gastroenteropancreáticos (GEP) , expresan, en la superficie celular, porcentajes variables pero significativos de los cuatro receptores, mientras que el receptor SSTR4 está mucho menos presente.
La solicitud WO2005014624 describe la preparación de análogos cíclicos de somatostatina y los intermedios usados en su preparación. Estos análogos hexacíclicos tienen el residuo de triptófano en posición 3.
La solicitud WO2006066868 describe composiciones farmacéuticas para la administración parenteral de varias sales de análogos de somatostatina, que forman un depósito en gel después de la inyección en contacto con los líquidos 60 corporales. Mediante análogos de somatostatina, se quiere decir péptidos lineales o cíclicos derivados de somatostatina, que comprenden una secuencia de aminoácidos que comprende triptófano.
En Regulator y Peptides, 1 (1980) 97-113, se sostiene la importancia del grupo NH de indol para la actividad de somatostatina: la sustitución de Trp8 con naftilamina de hecho produce la pérdida de actividad.
Los datos de unión no se describen en el artículo, mientras que se evalúa la actividad de inhibición de la secreción gástrica in vivo. Estos resultados indican que, para la actividad gástrica, la sustitución de Trp8 con halógeno, análogos metilados o metoxilados (tabla II) tiene poca influencia sobre la potencia biológica, potencia que en su lugar casi se cancela en los análogos que contienen pentametil-fenilalanina (Pmp) o naftilamina (tabla III) , en lugar
de triptófano. Los compuestos que derivan de halógeno de D-Trp en su lugar parecen mejorar considerablemente la actividad inhibidora de la secreción de GH (tabla V) . Investigadores de Merck S&D (véase Veber D.F. en Proceedings of the 12th Am. Pep. Symp.: Smith, J.A. & Rivier J.E. editores, ESCOM 1992, pp. 3-14) describen que, en hexapéptidos cíclicos, la sustitución del triptófano con otro aminoácido aromático produce una pérdida considerable de actividad in vitro en la inhibición de la secreción de GH.
En J Med Chem (2005) 48, 507, se describen análogos selectivos de SSTR1 junto con su posible papel terapéutico de agonistas. Las estructuras analizadas aquí también tienen triptófano.
El artículo describe dos series de análogos derivados de dos ciclopéptidos: uno contiene D-Trp y el otro D-Nal; todos los análogos, como los padres, solo tienen afinidad por SSTR1; la serie con D-Nal es aproximadamente 10 veces menos poderosa que esa con D-Trp. Un detalle particular es estos péptidos, que son inactivos en todos los otros subtipos de receptores, es la sustitución de la lisina con p-aminofenilalanina.
De lo que se expone anteriormente, es por tanto evidente que un agonista pluripotente de somatostatina, es decir,
capaz de estimular SSTR1, SSTR2, SSTR3 y SSTR5, aumentará la posibilidad de respuestas positivas en pacientes afectados por tumores neuroendocrinos con respecto a agonistas cuya función activadora se restringe a un número menor de subreceptores de la somatostatina.
Descripción de la invención El solicitante ha encontrado sorprendentemente que el residuo de triptófano, presente en muchos análogos conocidos, se puede sustituir útilmente con otros residuos aromáticos adecuados, manteniendo la afinidad para la mayoría de los receptores de somatostatina.
En particular, se encontró que, usando aminoácidos cuyo grupo aromático es lo suficientemente rico con electrones (por ejemplo, al estar sustituido con grupos donantes de electrones) en sustitución del residuo de triptófano, se obtienen péptidos que muestran una buena afinidad por el receptor SSTR1, a valores de concentración similares a los necesarios para la unión a los receptores SSTR2, SSTR3 y SSTR5.
Por tanto, forman el objeto de la presente invención ciclohexapéptidos análogos de somatostatina, que tienen la fórmula (I) , donde mediante ciclohexapéptidos análogos de somatostatina se quiere decir péptidos con seis residuos de alfa aminoácidos, en los que un enlace peptídico directo está presente entre el grupo alfa-carboxilo del sexto residuo y el grupo alfa-amino del primer residuo, con una afinidad de unión a concentraciones nanomolares, para al menos uno de los receptores de somatostatina conocidos:
Fórmula (I) 45 donde: m = 0, 1 o 2 y n = 1, 2 o 3; preferiblemente m es igual a 1 y n es igual a 1 o 2; aún más preferiblemente n es igual a 1.
R1 representa un grupo aromático, excluyendo indol, que es preferiblemente fenilo, naftilo, benzhidrilo, fluorenilo, estirenilo, antranilo o bifenilo, opcionalmente sustituido en una o más posiciones. Los grupos de sustitución preferidos son esos donantes de electrones tales como alquilo, alquiloxilo, hidroxilo, alquilamina, acilamina, sulfuro o alquilsulfuro.
El grupo R1 es preferiblemente un grupo naftaleno, sustituido con uno o más grupos metiloxi, preferiblemente con 5 dos grupos metiloxi; en un aspecto aún más preferido de la invención R1 es 3, 8-dimetoxi-naftalen-2-ilo.
R4 representa un grupo aromático, opcionalmente sustituido. El grupo R4 es preferiblemente un grupo fenilo, posiblemente sustituido con un grupo hidroxilo, alcoxilo de C1-C4, alquilo de C1-C4, halógeno o nitro.
... [Seguir leyendo]
Reivindicaciones:
1. Compuestos de fórmula (I) :
Fórmula (I)
en donde m varía de 0 a 2; n varía de 1 a 3; R1 es un grupo aromático, excluyendo indol, opcionalmente sustituido en una o más posiciones; R4 es un grupo aromático, opcionalmente sustituido; R2 y R3 son, independientemente, H o un grupo alquilo de C1-C4, o, juntos, son una cadena de alquileno de C4-C5, unida al átomo de nitrógeno para formar una estructura cíclica; o R3 es un catión o grupo quelante de metales;
X1 es un residuo aminoacilo de fórmula (a) , (b) o (c)
2. Compuestos según la reivindicación 1, en donde el ion o grupo quelante de metales está directamente unido al grupo amino, o está unido a través de un espaciador, y en donde dicho espaciador es preferiblemente un grupo de fórmula -Z-R5-CO-, en donde R5 es alquileno de C1-11, alquenileno de C1-11 o -CH (R6) -, en donde R6 es la cadena lateral de un alfa aminoácido, y Z es un grupo funcional capaz de formar un enlace éter, un enlace éster o un enlace amídico con un grupo funcional presente en el grupo quelante, preferiblemente un átomo de oxígeno, un átomo de azufre, un radical carbonilo o un radical amino.
3. Compuestos según la reivindicación 1, en donde m es igual a 1 y n varía de 1 a 2, y preferiblemente n es igual a 1.
4. Compuestos según la reivindicación 1, en donde R1 es fenilo, naftilo, benzhidrilo, fluorenilo, estirenilo,
antranilo o bifenilo, opcionalmente sustituidos en una o más posiciones por grupos donantes de electrones preferiblemente elegidos de entre alquilos, alquiloxilos, hidroxilos, alquilaminas, acilaminas, sulfuros o alquilsulfuros.
5. Compuestos según la reivindicación 1, en donde R1 es un grupo naftaleno sustituido con uno o más grupos metiloxi, preferiblemente con dos grupos metiloxi, y, más preferiblemente R1 es 3, 8-dimetoxi-naftalen-2-ilo.
6. Compuestos según la reivindicación 1, en donde R4 es fenilo, opcionalmente sustituido con hidroxilos, 5 alcoxilos de C1-C4, alquilos de C1-C4, halógenos o grupos nitro y, preferiblemente R4 es 4-hidroxifenilo.
7. Compuestos según la reivindicación 1, en donde el grupo R3 es un agente quelante hidrofílico, preferiblemente derivado de ácido 1, 4, 7, 10-tetraazaciclododecano-N, N’, N’’, N’’’-tetraacético (DOTA) o ácido dietilentriaminopentaacético (DTPA) .
8. Compuestos según la reivindicación 1, en donde el grupo quelante R3 es un grupo quelante en forma libre, salificado o en complejo con cationes o elementos radioactivos (radionúclidos) , preferiblemente en complejo con un ion paramagnético, tales como Gd3+, Fe3+, o un ion fluorescente, tal como Eu3+ o un radionúclido que emite radiaciones α, β o γ, tal como 111In, 99mTc, 169Yb, 177Lu, 90Y o 213Bi.
9. Compuestos según la reivindicación 1, en donde X1 es un residuo aminoacilo de fórmula (c) .
10. Compuesto según la reivindicación 1, en donde los residuos aminoacilos del ciclohexapéptido en la fórmula (I) , tienen configuración L o D; preferiblemente, los residuos 1, 2 y 4-6 son L, y el residuo 3 es preferiblemente
D.
11. Compuestos según la reivindicación 1, en donde uno de los grupos amino puede estar opcionalmente en forma protegida, o en su forma salificada o en complejo, preferiblemente en forma mono-o disalificada, más preferiblemente en donde la sal es una sal de adición con ácidos orgánicos, ácidos polímeros o ácidos
inorgánicos.
12. Compuestos según la reivindicación 11, en donde las sales se eligen de entre acetatos, lactatos, benzoatos, aspartatos, pamoatos, polimetacrilatos, poliestirensulfonatos, clorhidratos, sulfatos o nitratos.
13. Compuesto según la reivindicación 1 elegido del grupo compuesto de
! ciclo[Tyr (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Phe- (D, L) [3- (3, 8-dimetoxi-naftalen-2-il) ]Ala-Lys] isómero B, ! ciclo[Tyr (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Phe- (D, L) (2, 5-dimetoxi) hPhe-Lys] isómero B, 35 ! ciclo[Tyr (Bn) -Phe-[4- (2-metilaminoetil) carbamoil]Pro-Phe- (D, L) [3- (3, 8-dimetoxi-naftalen-2-il) ]Ala-Lys] isómero B, ! ciclo[Tyr (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Phe- (D, L) [3- (1, 4-dimetoxi-naftalen-2-il) ]Ala-Lys] isómero A, ! ciclo[Tyr (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Phe- (D, L) [3- (1, 4-dimetoxi-naftalen-2-il) ]Ala-Lys] isómero B. ! ciclo[Tyr (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Phe- (D) [3- (naftalen-2-il) ]-Ala-Lys], ! ciclo[Tyr (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Phe- (D) hPhe-Lys], ! ciclo[Tyr (Bn) -Phe-[4- (2-metilaminoetil) carbamoil]Pro-Phg- (D) estirilAla-Lys], ! ciclo[Tyr (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Phg- (D) hPhe-Lys],
! ciclo[Tyr (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Tyr- (D, L) [3- (3, 8-dimetoxi-naftalen-2-il) ]Ala-Lys] isómero B, y ! ciclo[Ser (Bn) -Phe-[4- (2-aminoetil) carbamoil]Pro-Phe- (D, L) [3- (3, 8-dimetoxi-naftalen-2-il) ]Ala-Lys] isómero B,
y sus sales y complejos farmacéuticamente aceptables.
14. Un proceso para la preparación de los ciclohexapéptidos de la reivindicación 1, que comprende los siguientes pasos:
a) preparación de un hexapéptido lineal en el que los grupos funcionales opcionales presentes en las cadenas laterales de los aminoácidos están opcionalmente en forma protegida; b) ciclación de dicho hexapéptido por medio de uno o más agentes condensantes; c) eliminación opcional de los grupos protectores opcionales; d) purificación final del ciclopéptido obtenido de esta manera.
15. Proceso según la reivindicación 14, en donde el aminoácido C-terminal del péptido lineal obtenido en el punto a) es lisina.
16. Un proceso según la reivindicación 14, en donde uno de los residuos de aminoácidos del péptido lineal 65 obtenido en el punto a) es 4- (2-amino-etilcarbamoil-oxi) -prolina, protegido en el grupo amino de la cadena lateral, preferiblemente 4-hidroxi-prolina con el grupo 4-hidroxilo sin proteger, más preferiblemente en donde el grupo 2-amino-etilcarbamoilo se une al grupo hidroxilo de la 4-hidroxi-prolina, después de la ciclación de la fase b) , pero antes de la posible eliminación de los grupos protectores opcionales de la fase c) .
17. Los compuestos según cualquiera de las reivindicaciones 1-16, o una sal o complejo farmacéuticamente aceptable para su uso como un medicamento.
18. Una composición farmacéutica que comprende un compuesto según cualquiera de las reivindicaciones 1-16, o una sal farmacéuticamente aceptable del mismo, en asociación con al menos un excipiente 10 farmacéuticamente aceptable.
19. Una composición según la reivindicación 18, caracterizada por estar en una forma para la liberación modificada o la liberación tópica.
20. Compuestos según cualquiera de las reivindicaciones 1-16, para su uso en el tratamiento de angiogénesis, retinopatía proliferativa, edema macular, trastornos relacionados con enfermedades de neovascularización coroidea, enfermedades de injerto de vasos, estenosis de injerto venoso, restenosis y oclusiones vasculares después de daño vascular, fístulas enterocutáneas y pancreáticas cutáneas, síndrome del intestino irritable, enfermedades y trastornos inflamatorios, poliquistosis renal, síndrome de vaciado gástrico rápido, síndrome de diarrea acuosa, diarrea relacionada con SIDA, diarrea inducida por quimioterapia, pancreatitis aguda o crónica, hemorragia gastrointestinal, tumores y tumores malignos.
21. Compuestos según cualquiera de las reivindicaciones 1-16, para su uso en el tratamiento de acromegalia.
22. Compuestos según cualquiera de las reivindicaciones 1-16, para su uso en el tratamiento de tumores gastrointestinales que secretan hormonas, preferiblemente tumores carcinoides.
23. Un compuesto según cualquiera de las reivindicaciones 1-16, para su uso en combinación con un agente inmunosupresor, con un agente antiinflamatorio, con un agente modulador del receptor del secretagogo de GH, con un antagonista del receptor de GH, con un secretagogo de la insulina, con un promotor de la secreción de insulina, con un sensibilizante de insulina, con una dosis baja de insulina, con un agente que tiene efectos antiangiogénicos o con un agente quimioterapéutico.
Patentes similares o relacionadas:
Molécula de colorante y preparados de colorante, en particular para su uso en métodos quirúrgicos de cirugía oftálmica y para teñir proteínas, del 15 de Julio de 2020, de AL.CHI.MI.A. S.R.L.: Una molécula de colorante que tiene la estructura: **(Ver fórmula)** donde: R1 está conformado por un grupo SO3- unido con un enlace […]
Sonda fluorescente para detectar dipeptidil peptidasa IV, del 3 de Junio de 2020, de The University of Tokyo: Una sonda fluorescente para detectar la dipeptidil peptidasa IV (DPP-IV) que comprende un compuesto representado por la siguiente fórmula (I) o una sal del mismo: **(Ver […]
Kit y método para detectar hidroxiapatita dental porosa, del 27 de Mayo de 2020, de Incisive Technologies Pty Ltd: Una sonda para su uso en un método de detección de una afección in vivo que implica hidroxiapatita dental porosa, que comprende: un indicador coloreado […]
Composiciones para administración por vía oral que comprende una variante de una proteína de pliegue OB, del 29 de Abril de 2020, de AFFILOGIC: Composición para la administración por vía oral para un uso terapéutico o diagnóstico, que comprende una variante de una proteína salvaje de pliegue OB, presentando […]
Marcador molecular para células madre cancerosas, del 29 de Abril de 2020, de Sapporo Medical University: Un péptido seleccionado del grupo que consiste en: DNAJB8 : AFMEAFSSF (SEQ ID NO: 71); DNAJB8 : AYRKLALRW (SEQ ID NO: 68); y DNAJB8 : […]
Cepas bacterianas que expresan genes de metilasa y sus usos, del 22 de Abril de 2020, de LOMA LINDA UNIVERSITY: Una bacteria aislada para usar en la producción de ADN plasmídico metilado, en donde la bacteria comprende un polinucleótido exógeno que codifica una CpG metilasa […]
Composición de imagen de cartílago articular, del 8 de Abril de 2020, de Mercury Asset Management Co., Ltd: Una composición adecuada para uso en la visualización de una zona degenerativa de cartílago articular, que se caracteriza por contener una albúmina […]
Variantes de clorotoxina, conjugados y métodos para su utilización, del 8 de Abril de 2020, de FRED HUTCHINSON CANCER RESEARCH CENTER: Conjugado de clorotoxina que comprende un péptido de clorotoxina acoplado covalentemente a un marcador fluorescente seleccionado del grupo que consiste […]