Microesferas de embolización bioreabsorbibles.
Un material embólico que comprende:
una microesfera que comprende un diámetro entre 50 micrómetros y 2200 micrómetros,
en donde la microesfera comprende carboximetilquitosana reticulada con carboximetilcelulosa.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2010/051629.
Solicitante: REGENTS OF THE UNIVERSITY OF MINNESOTA.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1000 WESTGATE DRIVE, SUITE 160 ST. PAUL, MINNESOTA 55114-8658 ESTADOS UNIDOS DE AMERICA.
Inventor/es: WENG,LIHUI, GOLZARIAN,JAFAR.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61L24/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61L PROCEDIMIENTOS O APARATOS PARA ESTERILIZAR MATERIALES U OBJECTOS EN GENERAL; DESINFECCION, ESTERILIZACION O DESODORIZACION DEL AIRE; ASPECTOS QUIMICOS DE VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS; MATERIALES PARA VENDAS, APOSITOS, COMPRESAS ABSORBENTES O ARTICULOS QUIRURGICOS (conservación de cuerpos o desinfección caracterizada por los agentes empleados A01N; conservación, p. ej. esterilización de alimentos o productos alimenticios A23; preparaciones de uso medico, dental o para el aseo A61K). › Adhesivos o cementos quirúrgicos; Adhesivos para dispositivos de colostomía (adhesivos conductores de la electricidad que se utilizan en terapia o examen en vivo A61K 50/00).
- A61L24/08 A61L […] › A61L 24/00 Adhesivos o cementos quirúrgicos; Adhesivos para dispositivos de colostomía (adhesivos conductores de la electricidad que se utilizan en terapia o examen en vivo A61K 50/00). › Polisacáridos.
PDF original: ES-2445164_T3.pdf
Fragmento de la descripción:
Microesferas de embolización bioreabsorbibles
Campo técnico
La descripción se refiere a materiales embólicos.
ANTECEDENTES
La embolización arterial transcatéter (TAE) ha sido ampliamente aceptada por su eficacia al tratar varias enfermedades que incluyen tumores, lesiones vasculares, y hemorragias. Para un tratamiento seguro y eficaz, es importante la selección de un material embólico adecuado.
Microesferas con capacidades eluyentes de fármaco se usan en los procesos de Quimioembolización Transarterial para el tratamiento de cáncer del hígado. Kettenbach y otros Cardiovascular and Interventional Radiology, Springer-Verlag, vol. 31, núm. 3, págs. 468-476.
Resumen Generalmente, la descripción se dirige a un material embólico que comprende carboximetilquitosana (CCN) reticulada con carboximetilcelulosa (CMC) . El material embólico puede formarse en microesferas con un diámetro entre aproximadamente 50 micrómetros (µm) y aproximadamente 2200 µm. CCN y CMC son cada uno biodegradables y biocompatibles. Al preparar el material embólico, la CCN puede ser reticulada por la CMC parcialmente oxidada, sin usar un agente de reticulación de molécula pequeña. Debido a esto, se espera que el material embólico sea biodegradable y biocompatible. Además, debido a que el material embólico comprende una red tridimensional de CCN reticulada por CMC, las propiedades mecánicas, tales como, por ejemplo, la compresibilidad de las microesferas embólicas, puede ser suficiente para permitir la introducción de las microesferas en una arteria de un paciente a través de una jeringa, catéter, o similares.
En algunas modalidades, las microesferas embólicas pueden comprender además un agente terapéutico, tal como un agente contra el cáncer. Un ejemplo de un agente terapéutico que puede cargarse en las microesferas embólicas es doxorrubicina.
En un aspecto, la descripción se dirige a un material embólico que comprende una microesfera que tiene un diámetro entre aproximadamente 50 µm y aproximadamente 2200 µm, donde la microesfera comprende carboximetilquitosana reticulada con carboximetilcelulosa.
En otro aspecto, la descripción se dirige a una suspensión de embolización que comprende un solvente y una pluralidad de microesferas suspendidas en el solvente. De acuerdo con este aspecto de la descripción, al menos una de una pluralidad de microesferas comprende un diámetro entre aproximadamente 50 µm y aproximadamente 2200 µm, y al menos una de una pluralidad de microesferas comprende carboximetilquitosana reticulada con carboximetilcelulosa.
En un aspecto adicional, la descripción se dirige a un kit que comprende una pluralidad de microesferas, donde al menos una de una pluralidad de microesferas comprende un diámetro entre aproximadamente 50 µm y aproximadamente 2200 µm, y donde al menos una de una pluralidad de microesferas comprende carboximetilquitosana reticulada con carboximetilcelulosa. De acuerdo con este aspecto de la descripción, el kit comprende además una jeringa o frasco en el cual se disponga la pluralidad de microesferas.
En un aspecto adicional, la descripción se dirige a un método para formar una microesfera embólica. El método comprende oxidar al menos parcialmente carboximetilcelulosa (CMC) para formar CMC parcialmente oxidada; formar una emulsión de CMC parcialmente oxidada, carboximetilquitosana (CCN) , agua, y un aceite; y reticular la CCN con la CMC para formar la microesfera embólica.
En un aspecto adicional, la descripción se dirige a un método que comprende inyectar una microesfera embólica que comprende carboximetilquitosana reticulada con carboximetilcelulosa en un vaso sanguíneo de un paciente para ocluir una arteria del paciente.
BREVE DESCRIPCIÓN DE LAS FIGURAS
La FIG. 1 es un diagrama de proceso de un ejemplo de técnica para producir microesferas embólicas que comprenden carboximetilquitosana reticulada con carboximetilcelulosa.
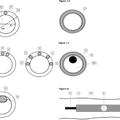
Las FIGS. 2A y 2B son una fotografía y una imagen de microscopio de luz, respectivamente, de microesferas de acuerdo con un aspecto de la descripción.
La FIG. 3 es un ejemplo de una imagen de microscopía electrónica de barrido de un exterior de una microesfera formada de acuerdo con aspectos de esta descripción.
Las FIGS. 4A y 4B son ejemplos de imágenes de SEM de la sección transversal de un hidrogel preparado con CCN reticulada con CMC.
Las FIGS. 5A-5F son imágenes de microscopio de luz que ilustran la carga de un colorante en las microesferas que comprenden CCN reticulada con CMC.
Las FIGS. 6A-6C ilustran ejemplos de microesferas de acuerdo con un aspecto de la descripción después que se cargan con varios colorantes.
Las FIGS. 7A-7D son imágenes de microscopio de luz que ilustran un ejemplo de carga de doxorrubicina en las microesferas que comprenden CCN reticulada con CMC.
La FIG. 8 es una imagen que ilustra un ejemplo de microesferas que comprenden CCN reticulada con CMC cargadas con doxorrubicina suspendidas en una mezcla de solvente.
La FIG. 9 es un diagrama de dispersión que ilustra ejemplos de dinámicas de carga de doxorrubicina en las microesferas que comprenden CCN reticulada con CMC de varios tamaños.
La FIG. 10 es un diagrama de dispersión que ilustra ejemplos de dinámicas de carga de doxorrubicina en las microesferas de varios tamaños.
La FIG. 11 es un diagrama de dispersión que ilustra ejemplos de cambios en el diámetro para las microesferas de diámetros iniciales diferentes durante la carga de doxorrubicina.
La FIG. 12 es un ejemplo de imagen de microscopía de fluorescencia de una microesfera cargada con doxorrubicina.
La FIG. 13 es un ejemplo de imagen que ilustra la intensidad de la fluorescencia como función de la distancia para una sola microesfera cargada con doxorrubicina.
La FIG. 14 es un diagrama de dispersión que ilustra ejemplos de un porcentaje de doxorrubicina liberada en función del tiempo para cada una de una pluralidad de muestras de microesferas que tienen características diferentes de acuerdo con la descripción.
La FIG.15 es un diagrama de dispersión que ilustra ejemplos de una cantidad de doxorrubicina liberada en función del tiempo para cada una de una pluralidad de muestras de microesferas que tienen características diferentes de acuerdo con la descripción.
La FIG. 16 es un diagrama de dispersión que ilustra ejemplos de una cantidad de doxorrubicina liberada en un medio salino en función del tiempo para cada una de una pluralidad de muestras de microesferas que tienen características diferentes de acuerdo con la descripción.
La FIG. 17 es un diagrama de dispersión que ilustra ejemplos de una cantidad de doxorrubicina liberada en un medio salino en función del tiempo para cada una de una pluralidad de muestras de microesferas que tienen características diferentes de acuerdo con la descripción.
La FIG. 18 es un diagrama de dispersión que ilustra ejemplos de una cantidad de doxorrubicina liberada en un medio salino en función del tiempo para cada una de una pluralidad de muestras de microesferas que tienen características diferentes de acuerdo con la descripción La FIG. 19 es un diagrama de línea que ilustra un ejemplo de comparación de velocidad de liberación de doxorrubicina entre microesferas de dos intervalos diferentes de diámetros.
La FIG. 20 es un diagrama de línea que ilustra ejemplos de liberación de doxorrubicina de microesferas en medios diferentes.
La FIG. 21 es un diagrama de línea que ilustra un ejemplo del efecto del grado de oxidación de la CMC que puede tener en la velocidad de liberación de doxorrubicina de microesferas que se forman de CCN reticulada con CMC.
La FIG. 22 es un diagrama de línea que ilustra un ejemplo del efecto del medio en la liberación de doxorrubicina de las microesferas.
La FIG. 23 es un diagrama de línea que ilustra un ejemplo de comparación entre las velocidades de liberación de doxorrubicina de las microesferas de acuerdo con un aspecto de la descripción actual y DC Beads™.
La FIG. 24 es un ejemplo de un gráfico de fuerza de compresión en función de la distancia para una sola microesfera que tiene un diámetro de aproximadamente 715 µm.
Las FIGS. 25A-25C son imágenes de microscopio de luz que ilustran un ejemplo de la compresibilidad de una microesfera que comprende CCN reticulada con CMC (teñida con azul de Evans) mientras la microesfera atraviesa un tubo de polietileno.
Las FIGS. 26A-26C son imágenes de microscopio de luz que ilustran otro ejemplo de la compresibilidad de una microesfera que comprende CCN reticulada con CMC (teñida con azul de Evans) mientras la... [Seguir leyendo]
Reivindicaciones:
1. Un material embólico que comprende:
una microesfera que comprende un diámetro entre 50 micrómetros y 2200 micrómetros, en donde la microesfera comprende carboximetilquitosana reticulada con carboximetilcelulosa.
2. El material embólico de la reivindicación 1, en donde la microesfera comprende un diámetro entre 1600 micrómetros y 2000 micrómetros, opcionalmente entre 500 micrómetros y 700 micrómetros.
3. El material embólico de cualquiera de las reivindicaciones 1 a 2, en donde la microesfera está sustancialmente libre de un agente de reticulación de molécula pequeña.
4. El material embólico de cualquiera de las reivindicaciones 1 a 3, en donde la microesfera es comprimible.
5. El material embólico de la reivindicación 4, en donde la microesfera tiene una tensión de fractura de entre 70% y 90%.
6. Una suspensión de embolización que comprende:
un solvente; y una pluralidad de las microesferas, en donde la pluralidad de microesferas comprende una microesfera de cualquiera de las reivindicaciones 1 a 5.
7. La suspensión de embolización de la reivindicación 6, en donde el solvente comprende una mezcla de medio de contraste y solución salina.
8. Un kit que comprende:
una pluralidad de las microesferas, en donde la pluralidad de microesferas comprende una microesfera de cualquiera de las reivindicaciones 1 a 5; y una jeringa o frasco en el cual se dispone la pluralidad de microesferas.
9. El kit de la reivindicación 8, que además comprende un solvente dispuesto en un contenedor de solvente.
10. El kit de la reivindicación 8 o 9, que además comprende un catéter y un alambre guía.
11. Un método para formar una microesfera embólica que comprende:
oxidar al menos parcialmente la carboximetilcelulosa (CMC) para formar CMC parcialmente oxidada; formar una emulsión de CMC parcialmente oxidada, carboximetilquitosana (CCN) , agua, y un aceite; y reticular la CCN con la CMC para formar la microesfera embólica.
12. El método de la reivindicación 11, en donde la reticulación de la CCN con la CMC para formar la microesfera embólica comprende mezclar la emulsión a una temperatura de entre aproximadamente 20°C y 70°C por al menos aproximadamente 12 horas, opcionalmente a una temperatura de aproximadamente 50 °C por al menos aproximadamente 12 horas.
13. El método de cualquiera de las reivindicaciones 11 a 12, en donde la reticulación de la CCN con la CMC para formar la microesfera embólica comprende reticular la CCN con la CMC para formar una microesfera embólica que comprende un diámetro entre 50 µm y 2200 µm.
Patentes similares o relacionadas:
Material celulósico combinado y método para producirlo y usarlo, del 15 de Julio de 2020, de ETHICON, INC.: Un material compuesto que comprende una mezcla de: (i) un primer componente en gel, de manera que el primer componente en gel contiene carboximetilcelulosa (CMC) […]
Material para prótesis de alta resistencia al impacto, transparente, con bajo contenido de MMA residual, del 1 de Julio de 2020, de KULZER GMBH: Material de base para prótesis bicomponente autopolimerizable, que comprende A) al menos un componente monomérico líquido, B) al menos un componente en polvo, […]
Composiciones poliméricas reabsorbibles para su uso en medicina, odontología y cirugía, del 17 de Junio de 2020, de Syncera, Inc: Una composición polimérica fluida o maleable en forma esencialmente seca, que comprende: (a) un copolímero de bloques de poli(alquileno)-poli(etilen […]
Hidrogeles reticulados por química clic y métodos de uso, del 3 de Junio de 2020, de PRESIDENT AND FELLOWS OF HARVARD COLLEGE: Un hidrogel que comprende un primer polímero y un segundo polímero, en el que el primer polímero y el segundo polímero son el mismo polímero, y en el que el primer […]
Material adhesivo tisular, del 29 de Abril de 2020, de Polyganics IP B.V: Mezcla de polímeros adhesivos tisulares que comprende un polímero portador bioabsorbible y un polímero reactivo al tejido sintético bioreabsorbible, en […]
 Dispositivos para escleroterapia usando adhesivos curables por luz, del 29 de Abril de 2020, de Swiss VX Venentherapie und Forschung GmbH: Un dispositivo de catéter de inyección que comprende una fuente de luz, donde el catéter se carga con adhesivo y gas, y donde dicho dispositivo se configura para aplicar […]
Dispositivos para escleroterapia usando adhesivos curables por luz, del 29 de Abril de 2020, de Swiss VX Venentherapie und Forschung GmbH: Un dispositivo de catéter de inyección que comprende una fuente de luz, donde el catéter se carga con adhesivo y gas, y donde dicho dispositivo se configura para aplicar […]
Cemento de apatita inyectable de sustitución iónica múltiple para vertebroplastia regenerativa y cifoplastia, del 15 de Abril de 2020, de CONSIGLIO NAZIONALE DELLE RICERCHE, C. N. R.: Cemento de apatita inyectable, en el que el calcio en el fosfato tricálcico en la fase α está parcialmente sustituido con estroncio y el fosfato […]
Empaque y stent hemostático biorreabsorbible flexible, del 1 de Abril de 2020, de MEDTRONIC XOMED, INC.: Un metodo para preparar una espuma biorreabsorbible flexible que comprende las etapas de: a) proporcionar un componente de carboximetilcelulosa que […]