Método para la purificación de alfa-1-antitripsina.
Un método para el aislamiento de α1-antitripsina (AAT) a partir de una disolución que contiene albúmina y AAT,
que comprende las etapas de:
(a) cargar la disolución sobre un primer sustrato de cromatografía de quelatos metálicos en condiciones en las que se retenga la AAT sobre el sustrato y no la albúmina;
(b) lavar el sustrato para retirar las proteínas no unidas o débilmente unidas y eluir entonces selectivamente la AAT desde el sustrato;
(c) cargar el eluido de AAT obtenido en la etapa (b) sobre un segundo sustrato de cromatografía de quelatos metálicos en condiciones en la que la AAT permanezca en disolución y no se retenga sobre el sustrato;
(d) recoger la disolución de AAT de la etapa (c); y
(e) llevar a cabo opcionalmente una o más etapas de purificación cromatográfica complementarias de la disolución de AAT.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/GB2006/004458.
Solicitante: Bio Products Laboratory Limited.
Nacionalidad solicitante: Reino Unido.
Dirección: Dagger Lane Elstree Hertfordshire WD6 3BX REINO UNIDO.
Inventor/es: DALTON,Joan, PODMORE,Adrian, KUMPALUME,Peter.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/57 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › que provienen de animales; que provienen de humanos.
- C07K1/22 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › Cromatografía de afinidad o técnicas análogas basadas en procesos de absorción selectiva.
- C07K14/81 C07K […] › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Inhibidores de proteasa.
- C12P21/02 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › que tienen una secuencia conocida de varios aminoácidos, p. ej. glutation.
PDF original: ES-2402208_T3.pdf
Fragmento de la descripción:
Metodo para la purificación de a-1-antitripsina La presente invención se refiere a metodos para la purificación de a-1-antitripsina.
La a-1-antitripsina (AAT) , tambien conocida como inhibidor de a-1-proteasa, es un inhibidor de proteasa esencial
encontrado principalmente en la sangre. La AAT protege normalmente al tejido conectivo, tal como los tejidos elasticos de los pulmones, de la degradación por elastasa, una enzima liberada por neutrófilos en sitios de inflamación.
El enfisema hereditario es una enfermedad resultante de una deficiencia genetica de AAT. El enfisema hereditario puede afectar tanto a la estructura como a la función de los pulmones y puede conducir a enfisema crónico y muerte prematura si se deja sin tratar. Se cree que la elast6lisis sin control es el mecanismo mediante el que el enfisema se desarrolla en estos individuos, y por tanto la administración intravenosa de AAT purificada es el tratamiento estandar para la deficiencia de AAT. La fibrosis quistica es otra patologia en la que el desequilibrio crónico de elastasa y AAT da como resultado el dano de tejido. Se usa el tratamiento con AAT para contrarrestar este desequilibrio y evitar el dano de tejido.
Los intentos tempranos de purificar grandes cantidades de AAT a partir de plasma se centraron en el uso de fracciones secundarias de procesos de fraccionamiento con etanol frio. El precipitado de la fracción de Cohn IV-1, una fracción de desecho en la fabricación de albumina, ha sido el mas frecuentemente seleccionado.
El documento EP-A 0067293 describe un metodo de purificación de AAT a partir de la fracción de Cohn IV-1 en que las proteinas del precipitado de la fracción de Cohn IV-1 se desestabilizan por exposición a agentes reductores que 20 rompen los enlaces disulfuro. Se precipitan entonces las proteinas desestabilizadas (precipitación salina) usando altas concentraciones salinas. Puesto que la AAT no esta estabilizada mediante puentes disulfuro, no se desestabiliza por los agentes reductores y por lo tanto puede recuperarse del sobrenadante mediante cromatografia.
Los documentos US 4.379.087 y US 4.439.358 usaban metodos mas convencionales para aislar AAT a partir de la fracción de Cohn IV-1. En los metodos de estas patentes, se usa PEG para retirar las impurezas de alto peso molecular y desnaturalizadas del material de partida mediante precipitación. Esto es seguido de cromatografia de intercambio aniónico para reducir la albumina y otros contaminantes de menor peso molecular. Sin embargo, los rendimientos eran extremadamente bajos con estos metodos.
El documento US 4.656.254 sugiere que los metodos de los documentos US 4.379.087 y US 4.439.358 podian conseguir un rendimiento del recipiente final de solo 4 a 6% cuando se usaba plasma combinado. El documento US
4.656.254 da a conocer que pueden conseguirse rendimientos aumentados de hasta 500 veces aumentando el volumen de la muestra de fracción de Cohn IV-1 en 24 volumenes y aumentando el pH a entre pH 9-10 antes de efectuar los metodos descritos en los documentos US 4.379.087 y US 4.439.358.
Se ha mostrado que otros metodos, tales como los del documento W02005/027821, consiguen un producto de mayor pureza a partir de la fracción de Cohn IV-1. El metodo del documento W02005/027821 usa una etapa de precipitación seguida de una cascada por etapas de cromatografia de intercambio aniónico, intercambio catiónico y un segundo intercambio aniónico.
Se han reconocido las limitaciones de la fracción de Cohn IV-1 como fuente de AAT y se han usado fracciones de Cohn alternativas tales como sobrenadantes de la fracción de Cohn II y III (tambien conocido como sobrenadante A en el metodo de fraccionamiento de Cohn modificado descrito por Kistler y Nitschmann, 1962, Vox Sang, 7, pag. 414
a 424) . Segun la bibliografia, el sobrenadante de la fracción de Cohn II y III contiene 2 o 3 veces mas AAT activa que la fracción de Cohn IV-1.
Puede prepararse sobrenadante A+1 como se muestra en la Figura 4. Sin embargo, purificar AAT a partir del sobrenadante A+1 tiene sus propias desventajas en comparación con usar la fracción de Cohn IV-1. En primer lugar, contiene enormes cantidades de albumina que deben retirarse de la corriente de procesamiento. En segundo lugar,
esta albumina es un producto esencial por si mismo y por tanto cualquier proceso comercialmente util debe permitir tambien la copurificación de la albumina. Por tanto, solo deberian emplearse metodos que no destruyan la estructura terciaria de la albumina. Para ser comercialmente util, cualquier metodo para la purificación de AAT que use el sobrenadante A+1 como material de partida debe poder proporcionar una producción económica de albumina y AAT, y potencialmente tambien otras proteinas plasmaticas de interes.
Los documentos. US 4.697.003 y EP-A 0282363 retiran el etanol del sobrenadante A mediante diafiltración o filtración en gel. Sin embargo, la retirada del etanol del sobrenadante A mediante diafiltración o filtración en gel se vuelve cara y consume mucho tiempo cuando se usan grandes volumenes de material de partida. Oespues de la retirada del etanol, se someten tanto albumina como AAT a cromatografia de intercambio aniónico en la que tanto AAT como albumina estan unidas a un soporte sólido. En el documento EP-A 0282363, se mejora la pureza de la 55 AAT eluyendo primero la albumina y aumentando entonces los niveles de acetato de sodio para eluir la AAT. En el documento US 4.697.003, se eluye la AAT sin eluir primero la albumina. Los metodos tanto del documento US
4.697.003 como EP-A 0282363 describen etapas de purificación suplementarias despues de la etapa de cromatografia de intercambio aniónico. El documento EP-A 0282363 describe filtración en gel, mientras que el documento US 4.697.003 usa precipitación con PEG. El metodo del documento EP-A 0282363 consigue un 80-90% de pureza y un 65-75% de rendimiento. Esto es equivalente a un 50-60% de recuperación de la AAT plasmatica.
Es el objetivo de la presente invención mejorar lo actualmente disponible para el aislamiento de AAT en uno o mas de los siguientes aspectos: rendimiento y/o pureza de AAT y reproducibilidad de la misma, simplicidad del proceso e idoneidad para uso a gran escala y/o comercial o proporcionar al menos un metodo alternativo para el aislamiento de AAT.
Se ha encontrado ahora que la AAT puede aislarse a partir de una disolución que contiene albumina y AAT usando al menos dos etapas de cromatografia de quelatos metalicos separadas. Este metodo sencillo da como resultado rendimientos altos y reproducibles de AAT, puede usarse económicamente a gran escala y puede proporcionar AAT suficientemente pura para aplicaciones terapeuticas. La cromatografia de quelatos metalicos es tambien conocida como cromatografia de afinidad por iones metalicos inmovilizados (IMAC) .
El uso de la cromatografia de quelatos metalicos (IMAC) para fraccionar proteinas plasmaticas se describió originalmente por Porath (Porath, J. et al., Nature 258: 598-599 (1975) ) . Su uso como etapa de un proceso multietapa para fraccionar proteinas a partir de suero de cabra se describe en Jain y Gupta, Applied Biochemistr y and Biotechnology, 2005, vol. 125, 53-62. Kurecki (Kurecki, T. et al., Anal. Biochem. 99: 415420 (1979) ) usaron un quelato de Zn para la purificación de a2-macroglobulina y AAT a partir de una fracción plasmatica con sulfato de amonio, pero la AAT requeria purificación suplementaria mediante cromatografia de intercambio aniónico. En el documento W095/35306, se us6 un quelato de Cu o Zn como etapa de refinado, posterior a la precipitación con PEG y cromatografia de intercambio aniónico. En el documento W097/09350, se us6 un quelato de Ni como quinta etapa en un proceso multietapa para purificar AAT a partir de leche de oveja transgenica. Al contrario que estos metodos de la tecnica anterior, en la presente invención se usa la cromatografia de quelatos metalicos como etapa de purificación principal, permitiendo un proceso sencillo y escalable para la purificación a gran escala de AAT.
En un aspecto, la presente invención proporciona por lo tanto un primer metodo para el aislamiento de a1antitripsina (AAT) a partir de una disolución que contiene albumina y AAT, que comprende las etapas de:
(a) cargar la disolución sobre un primer sustrato de cromatografia de quelatos metalicos en condiciones en las que se retenga la AAT sobre el sustrato y no la albumina;
(b) lavar el sustrato para retirar las proteinas no unidas o debilmente unidas y eluir entonces selectivamentela AAT del sustrato;
(c) cargar el eluido de AAT obtenido en la etapa (b) en un segundo sustrato de cromatografia de quelatos metalicos en condiciones en la que la AAT permanezca en... [Seguir leyendo]
Reivindicaciones:
1. Un metodo para el aislamiento de a1-antitripsina (AAT) a partir de una disolución que contiene albumina y AAT, que comprende las etapas de:
(a) cargar la disolución sobre un primer sustrato de cromatografia de quelatos metalicos en condiciones en 5 las que se retenga la AAT sobre el sustrato y no la albumina;
(b) lavar el sustrato para retirar las proteinas no unidas o debilmente unidas y eluir entonces selectivamente la AAT desde el sustrato;
(c) cargar el eluido de AAT obtenido en la etapa (b) sobre un segundo sustrato de cromatografia de
quelatos metalicos en condiciones en la que la AAT permanezca en disolución y no se retenga sobre el 10 sustrato;
(d) recoger la disolución de AAT de la etapa (c) ; y
(e) llevar a cabo opcionalmente una o mas etapas de purificación cromatografica complementarias de la disolución de AAT.
2. Un metodo segun la reivindicación 1, que comprende adicionalmente una etapa de purificación 15 cromatografica adicional entre las etapas (b) y (c) .
3. Un metodo segun la reivindicación 1 o la reivindicación 2, en el que la etapa de purificación cromatografica complementaria y/o la etapa de purificación cromatografica adicional es una etapa de cromatografia de intercambio aniónico.
4. Un metodo para el aislamiento de AAT a partir de una disolución que contiene albumina y AAT, 20 que comprende las etapas de:
(a1) retirar la albumina de la disolución; (b1) cargar la disolución desprovista de albumina sobre un primer sustrato de cromatografia de quelatos metalicos en condiciones en la que la AAT permanezca en disolución y no se retenga sobre el sustrato;
(c1) recoger la disolución que contiene AAT;
(d1) cargar la disolución obtenida en la etapa (c1) sobre un segundo sustrato de cromatografia de quelatos metalicos en condiciones en las que la AAT se retenga sobre el sustrato; y (e1) eluir selectivamente la AAT del segundo sustrato.
5. Un metodo para el aislamiento de AAT a partir de una disolución que contiene albumina y AAT, que comprende las etapas de:
(a2) retirar la albumina de la disolución; (b2) cargar la disolución exenta de albumina sobre un primer sustrato de cromatografia de quelatos metalicos en condiciones en las que la AAT se retenga sobre el sustrato;
(c2) eluir selectivamente la AAT del sustrato; (d2) cargar la disolución obtenida en la etapa (c2) sobre un segundo sustrato de cromatografia de quelatos 35 metalicos en condiciones en las que la AAT permanezca en disolución y no retenga sobre el sustrato; y (e2) recoger la disolución que contiene AAT.
6. Un metodo segun la reivindicación 4 o la reivindicación 5, en el que la etapa de retirada de albumina de la disolución es una etapa de cromatografia de intercambio aniónico.
7. Un metodo segun cualquier reivindicación precedente, en el que el ligando quelante del primer y/o segundo 40 sustrato de cromatografia de quelatos metalicos es acido nitrilotriacetico (NTA) o acido iminodiacetico.
8. Un metodo segun cualquier reivindicación precedente, en el que el ión metalico del sustrato de cromatografia de quelatos metalicos se selecciona del grupo consistente en Zn2+, Ni2+, Cu2+, Co2+ y Fe2+.
9. Un metodo segun cualquier reivindicación precedente, en el que el sustrato de cromatografia de quelatos metalicos sobre el que va a retenerse la AAT es agarosa con acido iminodiacetico cargado con iones Cu2+.
10. Un metodo segun cualquier reivindicación precedente, en el que el sustrato de cromatografia de quelatos metalicos usado en la etapa de cromatografia de quelatos metalicos en el que la AAT permanece en disolución es agarosa con NTA cargado con iones Cu2+.
11. Un metodo segun cualquier reivindicación precedente, en el que la disolución que contiene albumina y AAT 5 es plasma o una fracción plasmatica, preferiblemente plasma humano o una fracción plasmatica humana.
12. Un metodo segun cualquier reivindicación precedente, en el que la disolución que contiene albumina y AAT comprende principalmente AAT, glucoproteina acida a1, transferrina, haptoglobina, glucoproteina a2 HS, hemopexina, a2-macroglobulina, a1-antiquimotripsina y albumina.
13. Un metodo segun cualquier reivindicación precedente, que comprende adicionalmente al menos una etapa
de concentración y/o purificación, preferiblemente seleccionada del grupo consistente en diafiltración, ultrafiltración, cromatografia de flujo, cromatografia de quelatos metalicos suplementaria y cromatografia de hidroxiapatito.
14. Un metodo segun cualquier reivindicación precedente, que comprende adicionalmente al menos una etapa de retirada de contaminantes, preferiblemente una etapa de inactivación o retirada virica.
15. Un metodo segun la reivindicación 14, en el que la etapa de inactivación o retirada virica comprende 15 tratamiento con disolvente-detergente y/o filtración virica.
16. Un metodo segun la reivindicación 15, en el que la etapa de tratamiento con disolvente-detergente ocurre antes de la etapa en la que se retiene la AAT sobre un sustrato de cromatografia.
17. Un metodo segun cualquier reivindicación precedente, que comprende adicionalmente formular la AAT obtenida para uso farmaceutico.
Patentes similares o relacionadas:
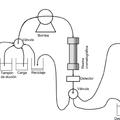 Purificación de proteínas, del 29 de Julio de 2020, de UCB Biopharma SRL: Un proceso para la purificación de una proteína de interés a partir de una mezcla que comprende las etapas de
a) en un ciclo de cromatografía operativo, […]
Purificación de proteínas, del 29 de Julio de 2020, de UCB Biopharma SRL: Un proceso para la purificación de una proteína de interés a partir de una mezcla que comprende las etapas de
a) en un ciclo de cromatografía operativo, […]
Membranas para cromatografía formadas por reacciones de polimerización clic de tiol-eno o tiol-ino, del 10 de Junio de 2020, de Merck Millipore Ltd: Un material compuesto, que comprende: un miembro de soporte, que comprende una pluralidad de poros que se extienden a través del miembro de […]
Un procedimiento de cromatografía de reparto débil, del 6 de Mayo de 2020, de WYETH LLC: Un procedimiento de recuperación de un producto purificado de un fluido de carga que incluye una o más impurezas, que comprende las etapas de: hacer pasar el fluido […]
Procedimiento de purificación de polipéptidos, del 22 de Abril de 2020, de CSL LIMITED: Procedimiento de purificación de un polipéptido de interés por cromatografía de intercambio catiónico en el que un compuesto químico se añade en una concentración de al menos […]
Etiqueta de epítopo y método de detección, captura y/o purificación de polipéptidos etiquetados, del 15 de Abril de 2020, de ChromoTek GmbH: Péptido epítopo aislado que tiene de 12 a 25 aminoácidos, en donde la secuencia de aminoácidos comprende una secuencia según se define en SEQ ID NO: 32 (X1X2RX4X5AX7SX9WX11X12), […]
Matriz de cromografía de afinidad, del 25 de Marzo de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES SOCIETE ANONYME: Matriz de cromatografía de afinidad, en forma de gel, que comprende unas partículas de polímero sobre las cuales se injerta al menos un oligosacárido […]
Sistema de tampón para purificación de proteína, del 26 de Febrero de 2020, de GLAXOSMITHKLINE LLC: Un sistema de cromatografía que comprende: (i) un sistema de tampón de múltiples componentes libre de cloruro de sodio para la purificación de una […]
Proteína mutante, del 19 de Febrero de 2020, de Cytiva BioProcess R&D AB: Una proteína de unión a inmunoglobulina que se une a regiones de una molécula de inmunoglobulina distintas de las regiones determinantes de […]