Injerto vascular de material compuesto que incluye recubrimiento de agente bioactivo y vaina biodegradable.
Un injerto vascular de material compuesto que comprende:
un miembro de injerto tubular flexible poroso (12);
una capa de recubrimiento de agente bioactivo biodegradable (14) dispuesta sobre dicho miembro deinjerto (12); estando dicha capa de recubrimiento (14) provista de al menos un agente bioactivo (16)incorporado en su interior;
caracterizándose el injerto vascular de material compuesto porque comprende:
una vaina biodegradable (18) dispuesta sobre dicha capa de recubrimiento (14), teniendo dichavaina (18) una rigidez superior a la de dicho miembro de injerto tubular flexible (12); y siendobiodegradable para exponer dicha capa de recubrimiento (14) de manera que se restablezca laflexibilidad de dicho miembro de injerto tubular (12).
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/024418.
Solicitante: BOSTON SCIENTIFIC LIMITED.
Nacionalidad solicitante: Barbados.
Dirección: P.O. BOX 1317 SEASTON HOUSE HASTINGS CHRIST CHURCH BARBADOS, WEST INDIES BARBADOS.
Inventor/es: MI LYN TAN,SHARON.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61F2/06 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61F FILTROS IMPLANTABLES EN LOS VASOS SANGUINEOS; PROTESIS; DISPOSITIVOS QUE MANTIENEN LA LUZ O QUE EVITAN EL COLAPSO DE ESTRUCTURAS TUBULARES, p. ej. STENTS; DISPOSITIVOS DE ORTOPEDIA, CURA O PARA LA CONTRACEPCION; FOMENTACION; TRATAMIENTO O PROTECCION DE OJOS Y OIDOS; VENDAJES, APOSITOS O COMPRESAS ABSORBENTES; BOTIQUINES DE PRIMEROS AUXILIOS (prótesis dentales A61C). › A61F 2/00 Filtros implantables en los vasos sanguíneos; Prótesis, es decir, elementos de sustitución o de reemplazo para partes del cuerpo; Dispositivos para unirlas al cuerpo; Dispositivos para proporcionar permeabilidad o para evitar que colapsen las estructuras tubulares del cuerpo, p. ej. stents (como artículos cosméticos, ver las subclases apropiadas, p. ej. pelucas o postizos, A41G 3/00, A41G 5/00, uñas artificiales A45D 31/00; prótesis dentales A61C 13/00; materiales para prótesis A61L 27/00; riñones artificiales A61M 1/14; corazones artificiales A61M 60/00). › Vasos sanguíneos.
PDF original: ES-2408332_T3.pdf
Fragmento de la descripción:
Injerto vascular de material compuesto que incluye recubrimiento de agente bioactivo y vaina biodegradable.
REFERENCIA CRUZADA A SOLICITUDES RELACIONADAS
La presente solicitud internacional reivindica el beneficio de la solicitud de EE.UU. nº 10/889.432 presentada el 12 de julio de 2004.
CAMPO DE LA INVENCIÓN
La presente invención se refiere a dispositivos médicos implantables que inhiben o reducen el crecimiento bacteriano durante su uso en un cuerpo vivo. Más particularmente, la presente invención se refiere a injertos vasculares de material compuesto que incorporan agentes bioactivos para administrar materiales terapéuticos y/o para inhibir o reducir el crecimiento bacteriano durante y tras la introducción del injerto al sitio de implantación en el cuerpo.
ANTECEDENTES DE LA INVENCIÓN
Con el fin de reparar o sustituir vasos sanguíneos enfermos o lesionados es muy conocido usar injertos vasculares implantables en las ciencias médicas. Estos injertos vasculares, que son normalmente estructuras tubulares poliméricas, pueden implantarse durante un procedimiento quirúrgico o pueden implantarse interluminalmente en un procedimiento percutáneo.
Tales procedimientos médicos que emplean injertos vasculares introducen un objeto extraño en el sistema vascular de un paciente. Por tanto, el riesgo de infección debe tratarse en cualquiera de tal procedimiento.
Se informa que la infección del injerto vascular se produce en de aproximadamente el 1% al 6% de los procedimientos. Más significativamente, las infecciones del injerto vascular están asociadas con una alta tasa de mortalidad de entre el 25% y el 75%. Además, las tasas de morbilidad para las infecciones de los injertos vasculares están en el intervalo de entre el 40% y el 75%. Las infecciones producidas por injertos vasculares también son conocidas por prolongar las estancias hospitalarias, aumentando así enormemente el coste del cuidado médico.
Numerosos factores contribuyen al riesgo de infección por injerto vascular. Tales factores incluyen el grado de experiencia del cirujano y el personal de quirófano. La edad del paciente y el grado al que el paciente está inmunodeprimido también son fuertes factores de riesgo con respecto a la inserción del injerto vascular. Otros factores comunes asociados a los riesgos de la infección por injerto vascular incluyen esterilidad de la piel del paciente, además de los materiales que se implantan.
Se ha encontrado que el mecanismo de infección para muchos dispositivos implantados se atribuye a la contaminación bacteriana local durante la cirugía. Las bacterias sobre el dispositivo producen un matriz de limo extracelular/biopelícula durante la colonización, que recubre la superficie del polímero. Esta biopelícula protege a las bacterias contra los mecanismos de defensa del paciente. La capa de biopelícula también reduce la penetración de antibióticos.
Los agentes infecciosos más comunes son: Staphylococcus aureus, Pseudomonas aeruginosa y Staphylococcus epidermidis. Estos agentes se han identificado en más del 75% de todas las infecciones vasculares informadas. Tanto Staphylococcus aureus como Pseudomonas aeruginosa muestran alta virulencia y pueden conducir a signos clínicos de infección tempranos en el periodo posoperatorio (menos de cuatro meses) . Es esta virulencia la que conduce a septicemia y es un factor clave en las altas tasas de mortalidad. Staphylococcus epidermidis se describe como un tipo de baja virulencia de bacteria. Aparece tarde, que significa que puede presentar signos clínicos de infección hasta cinco años posoperatorio. Se ha mostrado que este tipo de bacteria es responsable de hasta el 60% de todas las infecciones del injerto vascular. Las infecciones de este tipo frecuentemente requieren la escisión total del injerto, desbridamiento de tejido circundante y revascularización mediante una vía sin infectar.
Tales organismos de alta virulencia se introducen normalmente en el momento de la implantación. Por ejemplo, algunas de las cepas de Staphylococcus (incluyendo Staphylococcus aureus) tienen receptores para ligando de tejido tales como moléculas de fibrinógeno que están entre los primeros depósitos observados después de la implantación de un injerto. Esta unión a ligando de tejido proporciona una forma para que las bacterias se protejan de las defensas inmunitarias del huésped, además de antibióticos sistémicos. Las bacterias pueden entonces producir polímeros en forma de un polisacárido que puede conducir a la capa de limo anteriormente mencionada sobre la superficie externa del injerto. En este entorno protector se produce la reproducción bacteriana y se forman colonias dentro de la biopelícula que pueden derramar células a tejidos circundantes (Calligaro, K. y Veith, Frank, Surger y , 1991 V110-No. 5, 805-811) . La infección también puede originarse a partir de linfáticos cortados transversalmente, de trombo inter-arterial, o estar presente dentro de la pared arterial.
Hay graves complicaciones como resultado de las infecciones del injerto vascular. Por ejemplo, la rotura anastonómica debida a enzimas proteolíticas que producen los organismos más virulentos puede conducir a una degeneración de la pared arterial adyacente a la anastomosis. Esto puede conducir a una pseudoaneurisma que puede romper y producir inestabilidad hemodinámica. Otra complicación de una infección del injerto vascular puede ser embolias distales estípticas, que pueden conducir a la pérdida de una extremidad, o fístulas aortoentéricas, que son el resultado de una fuga de un injerto que se infecta y que conduce a hemorragia gastrointestinal (Greisler, H., Infected Vascular Grafts. Maywood, IL, 33-36) .
Deseablemente, sería beneficioso prevenir la adhesión de cualquier bacteria al injerto, o al área inmediata que rodea el injerto en el momento de la implantación. Sería adicionalmente deseable prevenir la formación de biopelícula bacteriana inicial descrita anteriormente estimulando el crecimiento de tejido normal hacia dentro del túnel, y protegiendo el propio implante de la formación de biopelícula.
Se conoce incorporar agentes antimicrobianos en un dispositivo médico. Por ejemplo, la técnica anterior desvela un injerto vascular de PTFEe, conteniendo una proporción sustancial de los intersticios una composición de recubrimiento que incluye: un poliuretano biomédico; poli (ácido láctico) , que es un polímero biodegradable; y los agentes antimicrobianos, acetato de clorhexidina y pipracil. La técnica anterior describe adicionalmente un parche para hernia de PTFEe que está impregnado con una composición que incluye sulfadiazina de plata y acetato de clorhexidina y poli (ácido láctico) .
Además, se conoce técnica anterior que desvela una prótesis endovascular o prótesis vascular que tienen una capa de recubrimiento biodegradable superior que contiene un fármaco. Se desvela que la capa de recubrimiento incluye un fármaco anticoagulante y, opcionalmente, otros aditivos tales como una sustancia antibiótica.
La técnica anterior describe adicionalmente un implante médico en el que un agente antimicrobiano penetra en las superficies expuestas del implante y se impregna con todo el material del implante. El implante médico puede ser un injerto vascular y el material del implante puede ser politetrafluoroetileno (PTFE) . El agente antimicrobiano está seleccionado de antibióticos, antisépticos y desinfectantes.
Además, hay técnica anterior que desvela que la plata, que es un agente antiséptico conocido, puede depositarse sobre la superficie de un sustrato polimérico poroso mediante deposición asistida mediante haces de ión plata antes de llenar los poros de un material polimérico poroso con un material biodegradable biocompatible insoluble. Esta técnica anterior desvela adicionalmente que pueden integrarse antimicrobianos en los poros del sustrato polimérico. El sustrato puede ser un injerto vascular poroso de PTFEe.
También se conoce proporcionar un artículo médico antiinfeccioso que incluye un polímero hidrófilo que tiene masa de cloruro de plata distribuida en su interior. El polímero hidrófilo puede ser un laminado sobre un polímero base. Polímeros hidrófilos preferidos se desvelan como poliuretanos procesables fundidos. El artículo médico puede ser un injerto vascular. Una desventaja de este injerto es que no está formado de PTFEe, que se sabe que tiene propiedades antitrombogénicas naturales. Otra desventaja es que la matriz de poliuretano hidrófila en la que la sal de plata está distribuida no controla por sí misma la liberación de plata en el fluido y tejido corporal circundante en el sitio de implantación del injerto.
Además, hay... [Seguir leyendo]
Reivindicaciones:
1. Un injerto vascular de material compuesto que comprende:
un miembro de injerto tubular flexible poroso (12) ; una capa de recubrimiento de agente bioactivo biodegradable (14) dispuesta sobre dicho miembro de injerto (12) ; estando dicha capa de recubrimiento (14) provista de al menos un agente bioactivo (16) incorporado en su interior; caracterizándose el injerto vascular de material compuesto porque comprende:
una vaina biodegradable (18) dispuesta sobre dicha capa de recubrimiento (14) , teniendo dicha vaina (18) una rigidez superior a la de dicho miembro de injerto tubular flexible (12) ; y siendo biodegradable para exponer dicha capa de recubrimiento (14) de manera que se restablezca la flexibilidad de dicho miembro de injerto tubular (12) .
2. El injerto vascular de las reivindicaciones 1, en el que dicho agente bioactivo (16) es un agente antimicrobiano.
3. El injerto vascular de la reivindicación 2, en el que dicho agente antimicrobiano es un agente antibiótico o antiséptico.
4. El injerto vascular de la reivindicación 3, en el que dicho agente antibiótico está seleccionado del grupo que consiste en ciprofloxacina, vancomicina, minociclina, rifampina, y combinaciones de las mismas.
5. El injerto vascular de la reivindicación 3, en el que el agente antiséptico está seleccionado del grupo que consiste en un agente de plata, clorhexidina, triclosano, yodo, cloruro de benzalconio, y combinaciones de los mismos.
6. El injerto vascular de una cualquiera de las reivindicaciones 1 a 5, en el que dicho miembro de injerto tubular poroso (12) comprende material de PTFEe.
7. El injerto vascular de una cualquiera de las reivindicaciones 1 a 6, en el que dicho miembro de injerto tubular poroso (12) comprende un material textil.
8. El injerto vascular de la reivindicación 7, en el que dicho material textil comprende una construcción seleccionada del grupo que consiste en ligamentos, galones, bobinados de filamentos, fibras tejidas y combinaciones de los mismos.
9. El injerto vascular de la reivindicación 7, en el que dicho material textil está formado de hilos sintéticos (40a, 40b) seleccionados del grupo que consiste en poliésteres, poliésteres de PET, polipropilenos, polietilenos, poliuretanos, politetrafluoroetilenos y combinaciones de los mismos.
10. El injerto vascular de una cualquiera de las reivindicaciones 1 a 9, en el que la capa de recubrimiento de agente bioactivo biodegradable (14) está compuesta de un polímero natural, natural modificado o sintético.
11. El injerto vascular de la reivindicación 10, en el que dicho polímero está seleccionado del grupo que consiste en fibrina, colágeno, celulosas, gelatina, vitronectina, fibronectina, laminina, matrices de la membrana basal reconstituidas, almidones, dextranos, alginatos, ácido hialurónico, poli (ácido láctico) , poli (ácido glicólico) , polipéptidos, glicosaminoglicanos, sus derivados y mezclas de los mismos.
12. El injerto vascular de la reivindicación 10, en el que dicho polímero está seleccionado del grupo que consiste en polidioxanos, polioxalatos, poli (a-ésteres) , polianhídridos, poliacetatos, policaprolactonas, poli (ortoésteres) , poliaminoácidos, poliamidas y mezclas y copolímeros de los mismos.
13. El injerto vascular de la reivindicación 10, en el que dicho polímero está seleccionado del grupo que consiste en estereopolímeros de ácido L- y D-láctico, copolímeros de ácido bis (p-carboxifenoxi) propanoico y ácido sebácico, copolímeros de ácido sebácico, copolímeros de caprolactona, copolímeros de poli (ácido láctico) /poli (ácido glicólico) /polietilenglicol, copolímeros de poliuretano y (poli (ácido láctico) , copolímeros de poliuretano y poli (ácido láctico) , copolímeros de a-aminoácidos, copolímeros dea -aminoácidos y ácido caproico, copolímeros de glutamato de a-bencilo y polietilenglicol, copolímeros de succinato y poli (glicoles) , polifosfaceno, polihidroxi-alcanoatos y mezclas de los mismos.
14. El injerto vascular de una cualquiera de las reivindicaciones 1 a 13, en el que dicho recubrimiento de agente bioactivo (14) se aplica a dicho miembro de injerto tubular (12) .
15. El injerto vascular de una cualquiera de las reivindicaciones 1 a 14, en el que dicho recubrimiento de agente bioactivo se aplica en múltiples capas (14a, 14b) .
16. El injerto vascular de una cualquiera de las reivindicaciones 1 a 15, en el que la vaina biodegradable (18) tiene una configuración tubular o similar a lámina para la disposición sobre dicha capa de recubrimiento de agente bioactivo (14) .
17. El injerto vascular de una cualquiera de las reivindicaciones 1 a 16, en el que la vaina biodegradable (18) está compuesta de un material seleccionado del grupo que consiste en polilactidas, polianhídridos, poli (alcohol vinílico) , polivinilpirrolidona, poliglicoles, derivados de gelatina, y combinaciones de los mismos.
18. El injerto vascular de una cualquiera de las reivindicaciones 1 a 17, en el que la vaina biodegradable (18) incluye al menos un agente antimicrobiano (16) .
19. Un procedimiento de preparación de un injerto vascular según la reivindicación 1 para la administración de un agente antimicrobiano asociado con el mismo a un sitio de implantación de dicho injerto, comprendiendo dicho procedimiento las etapas de:
proporcionar un miembro de injerto tubular flexible poroso (12) ; aplicar un material de recubrimiento biodegradable a dicho miembro de injerto tubular poroso (12) de manera que se forme una o más capas de recubrimiento de agente bioactivo biodegradables superiores (14, 14a, 14b) , teniendo dicho material de recubrimiento biodegradable al menos un agente bioactivo (16) incorporado en su interior; y disponer una vaina biodegradable (18) sobre dicha una o más capas de recubrimiento superiores (14, 14a, 14b) .
20. El procedimiento de la reivindicación 19, en el que la etapa de disposición incluye proporcionar la vaina (18) en una configuración tubular y disponer dicha vaina (18) sobre las una o más capas de recubrimiento (14, 14a, 14b) que recubren dicho miembro de injerto (12) .
21. El procedimiento de la reivindicación 19, en el que la etapa de disposición incluye proporcionar la vaina (18) en una configuración similar a lámina y envolver la lámina sobre la una o más capas de recubrimiento (14, 14a, 14b) que recubren dicho miembro de injerto (12) .
22. El procedimiento de una cualquiera de las reivindicaciones 19 a 21 que comprende además la etapa de interponer una prótesis endovascular protésica (32) entre dicho miembro de injerto tubular (12) y dicha una o más capas de recubrimiento de agente bioactivo (14, 14a, 14b) .
23. El procedimiento de una cualquiera de las reivindicaciones 19 a 22 que comprende además la etapa de incorporar dicho agente bioactivo (16) en dicho material de recubrimiento biodegradable.
24. El procedimiento de una cualquiera de las reivindicaciones 19 a 23, en el que dicho agente bioactivo (16) es un agente antimicrobiano seleccionado del grupo que consiste en agentes antisépticos, agentes antibióticos y combinaciones de los mismos.
Patentes similares o relacionadas:
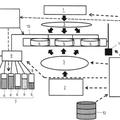 Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Procedimiento y dispositivo para producir un objeto multicelular tridimensional, del 29 de Julio de 2020, de TECHNISCHE UNIVERSITAT BERLIN: Procedimiento para producir un objeto multicelular tridimensional, con los pasos siguientes:
a) introducción de un primer líquido fotopolimerizable […]
Tapón de catéter extraíble y aplicaciones del mismo, del 3 de Junio de 2020, de Pristine Access Technologies Ltd: Tapón de catéter extraíble , que comprende: un cuerpo de tapón configurado para […]
Dispositivos de cierre automático, del 29 de Abril de 2020, de Solinas Medical Inc: Un puerto de acceso que se puede unir a una superficie dentro del cuerpo de un paciente, que comprende: un cuerpo del puerto que comprende un material […]
Dispositivo para el tratamiento del aneurisma de aorta, del 21 de Abril de 2020, de SERVICIO ANDALUZ DE SALUD: Dispositivo para el tratamiento del aneurisma de aorta. La invención describe un dispositivo para el tratamiento del aneurisma de aorta que comprende: un estent exterior […]
Endoprótesis y dispositivo de colocación para implantar tal endoprótesis, del 15 de Abril de 2020, de Kardiozis: Stent vascular o stent cardiaco que comprende al menos una parte de cuerpo, en el que están dispuestos elementos trombogénicos al menos […]
Dispositivos para tratar la vasculatura de la extremidad inferior, del 12 de Febrero de 2020, de LimFlow GmbH: Un sistema de prótesis implantable para tratar una oclusión en un primer vaso, el sistema de prótesis comprende: un estent (100, 134, 140, 150, 160, 200, 220, […]
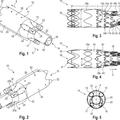 Prótesis vascular autoexpandible, del 29 de Enero de 2020, de JOTEC GMBH: Prótesis vascular autoexpandible para la implantación en un vaso sanguíneo de un paciente, con un cuerpo de base cilíndrico hueco , así […]
Prótesis vascular autoexpandible, del 29 de Enero de 2020, de JOTEC GMBH: Prótesis vascular autoexpandible para la implantación en un vaso sanguíneo de un paciente, con un cuerpo de base cilíndrico hueco , así […]
Dispositivo de protección de microválvula, del 22 de Enero de 2020, de Surefire Medical, Inc: Un dispositivo endovascular para reducir el reflujo de un agente de embolización en un vaso durante un procedimiento de terapia de embolización, comprendiendo […]