Inhibidores del VHC.
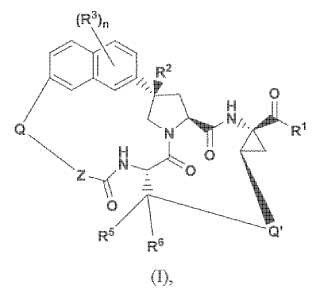
Un compuesto de fórmula (I)
o una sal farmacéuticamente aceptable del mismo,
en la que
n es 0, 1, 2, 3 o 4;
R1 está seleccionado de hidroxi y -NHSO2R4;
R2 está seleccionado de hidrógeno, alcoxi, alquilsulfanilo, alquilsulfonilo, alquilsulfoxilo e hidroxi;
cada R3 está seleccionado independientemente de alcoxi, alquilo, ciano, dialquilamino, halo, haloalquilo, haloalcoxi,un heterociclo monocíclico, hidroxilo y fenilo; en el que el heterociclo monocícliclo y el fenilo están cada unoopcionalmente sustituidos con uno, dos, tres, cuatro o cinco sustituyentes, seleccionados independientemente dealcoxi, alquilo, dialquilamino, halo, haloalcoxi y haloalquilo;
R4 está seleccionado de alquilo, arilo, aralquilo, cicloalquilo, (cicloalquil)alquilo, heterociclilo y NRaRb; en el que elalquilo y el cicloalquilo están cada uno opcionalmente sustituidos con un grupo seleccionado de alquilo, alcoxi, halo,haloalquilo, ciano, cianoalquilo y haloalcoxi;
R5 y R6 están seleccionados independientemente de hidrógeno, alcoxi C1-3, haloalcoxi C1-3 y alquilo C1-3opcionalmente sustituido con halo,
Ra y Rb están seleccionados independientemente de hidrógeno, alcoxi, alquilo, arilo, arilalquilo, cicloalquilo,(cicloalquil)alquilo, haloalquilo, heterociclilo y heterociclilalquilo;
Q es una cadena C4-8 saturada o insaturada que opcionalmente contiene un átomo de oxígeno y en la que la cadenaestá opcionalmente sustituida con uno, dos, tres o cuatro grupos seleccionados de forma independiente de alquilo,halo y haloalquilo, en el que los grupos alquilo y haloalquilo pueden formar opcionalmente un anillo de 3-7 miembroscon el átomo de carbono al que están unidos;
Q' es una cadena C4-8 saturada o insaturada que opcionalmente contiene un heteroátomo seleccionado de nitrógeno, oxígeno y azufre; estando la cadena opcionalmente sustituida con uno, dos, tres o cuatro gruposseleccionados de alquilo y halo;
Z está seleccionado de CH2, O y NRz; en el que Rz está seleccionado de hidrógeno y alquilo.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2009/066314.
Solicitante: BRISTOL-MYERS SQUIBB COMPANY.
Inventor/es: SCOLA,PAUL,MICHAEL, HIEBERT,SHELDON.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61P31/14 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › para virus ARN.
- C07K5/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 5/00 Péptidos con hasta cuatro aminoácidos en una secuencia totalmente determinada; Sus derivados. › Tripéptidos.
PDF original: ES-2414536_T3.pdf
Fragmento de la descripción:
Inhibidores del VHC
La presente divulgación se refiere, en general, a compuestos antivíricos y, más específicamente se refiere a compuestos que inhiben la función de la proteasa NS3 (también denominada en el presente documento como 5 “serina proteasa”) codificada por el virus de la hepatitis C (VHC) , a composiciones que comprenden dichos compuestos y a dichos compuestos para su uso en la inhibición de la función de la proteasa NS3.
El VHC es un importante patógeno humano, que se estima ha infectado a 170 millones de personas en todo el mundo – aproximadamente cinco veces el número de personas infectadas por el virus de la inmunodeficiencia humano de tipo 1. Una fracción sustancial de estos individuos infectados por el VHC desarrolla enfermedad hepática progresiva grave, que incluye cirrosis y carcinoma hepatocelular.
En la actualidad, la terapia más eficaz contra el VHC emplea una combinación de interferón alfa y ribavirina, conduciendo a una eficacia sustancial en el 40 % de los pacientes. No obstante, los resultados clínicos demuestran que el interferón alfa pegilado es superior al interferón alfa no modificado como monoterapia. No obstante, incluso con pautas terapéuticas experimentales que conllevan combinaciones de interferón alfa pegilado y ribavirina, una fracción sustancial de pacientes no experimenta una reducción sostenida en la carga vírica. Así, existe la necesidad clara y no satisfecha de desarrollar procedimientos terapéuticos eficaces para el tratamiento de infección por VHC.
El VHC es un virus de ARN de polaridad positiva. Tomando como base la comparación de la secuencia de aminoácidos deducida y la extensa similitud en la región sin traducir 5’, el VHC se ha clasificado como un género separado en la familia de Flaviviridae. Todos los miembros de la familia Flaviviridae presentan viriones encapsulados que contienen un genoma de ARN de polaridad positiva que codifica todas las proteínas específicas del virus conocidas mediante traducción de un marco de lectura abierto, ininterrumpido y único.
Dentro de la secuencia de nucleótidos y aminoácidos codificados en todo el genoma del VHC se encuentra una considerable heterogeneidad. Se han caracterizado al menos seis genotipos principales y se han descrito más de 50 subtipos. Los genotipos principales del VHC se diferencian en su distribución en todo el mundo y la significación clínica de la heterogeneidad genética del VHC sigue siendo difícil de conseguir a pesar de numerosos estudios del efecto positivo de genotipos sobre la patogénesis y el tratamiento.
El genoma del ARN monocatenario de VHC tiene una longitud de aproximadamente 9500 nucleótidos y tiene un único marco de lectura abierto (ORF) que codifica una única poliproteína grande de aproximadamente 3000 aminoácidos. En las células infectadas, esta poliproteína es escindida en múltiples sitios por proteasas celulares y 30 víricas para producir las proteínas estructurales y no estructurales (NS) . En el caso del VHC, la generación de proteínas no estructurales maduras (NS2, NS3, NS4A, NS4B, NS5A y NS5B) es llevada a cabo por dos proteasas víricas. La primera se escinde en la unión NS2-NS3; la segunda es una serina proteasa contenida dentro de la región N-terminal de NS3 y media todas las escisiones subsiguientes cadena abajo de NS3, tanto es cis, en el sitio de escisión NS3-NS4A, como en trans, para los sitios restantes NS4A-NS4B, NS4B-NS5A, NS5A-NS5B. La proteína NS4A parece servir para múltiples funciones, actuando como un cofactor para la proteasa NS3 y posiblemente ayudando en la localización de membrana de NS3 y otros componentes de la replicasa vírica. La formación del complejo de la proteína NS3 con NS4A es esencial para procesar eficazmente poliproteínas, potenciando la escisión proteolítica en todos los sitios. La proteína NS3 también muestra actividades de nucleósido trifosfatasa y ARN helicasa. NS5B es una ARN polimerasa dependiente de ARN que está implicada en la replicación del VHC.
El documento WO2008/057208 describe inhibidores de NS3 de VHC que son tripéptidos ciclados de modo que forman dos macrociclos, uno de los cuales a través de un grupo arilo o heterocíclico unido a prolina mediante un enlazador.
La presente divulgación proporciona compuestos peptídicos que pueden inhibir el funcionamiento de la proteasa NS3, por ejemplo en combinación con la proteasa NS4A. Además, la presente divulgación describe tales 45 compuestos para su uso en tratamiento de combinación en un paciente, por lo que, se puede administrar un compuesto de acuerdo con la presente divulgación, que sea eficaz para inhibir la proteasa NS3 del VHC, con uno o dos compuestos adicionales que tienen actividad contra el VHC.
En un primer aspecto, la presente divulgación proporciona un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo, en la que n es 0, 1, 2, 3 o 4;
R1 está seleccionado de hidroxi y NHSO2R4;
R2 está seleccionado de hidrógeno, alcoxi, alquilsulfanilo, alquilsulfonilo, alquilsulfoxilo e hidroxi;
cada R3 está seleccionado independientemente de alcoxi, alquilo, ciano, dialquilamino, halo, haloalquilo, haloalcoxi, un heterociclo monocíclico, hidroxilo y fenilo, en el que el heterociclo monocícliclo y el fenilo están cada uno opcionalmente sustituidos con uno, dos, tres, cuatro o cinco sustituyentes, seleccionados independientemente de alcoxi, alquilo, dialquilamino, halo, haloalcoxi y haloalquilo;
R4 está seleccionado de alquilo, arilo, aralquilo, cicloalquilo, (cicloalquil) alquilo, heterociclilo y NRaRb; en el que el alquilo y el cicloalquilo están cada uno opcionalmente sustituidos con un grupo seleccionado de alquilo, alcoxi, halo, haloalquilo, ciano, cianoalquilo y haloalcoxi;
R5 y R6 están seleccionados independientemente de hidrógeno, alcoxi C1-3, haloalcoxi C1-3 y alquilo C1-3 opcionalmente sustituido con halo,
Ra y Rb están seleccionados independientemente de hidrógeno, alcoxi, alquilo, arilo, arilalquilo, cicloalquilo, (cicloalquil) alquilo, haloalquilo, heterociclilo y heterociclilalquilo;
Q es una cadena C4-8 saturada o insaturada que opcionalmente contiene un átomo de oxígeno y en la que la cadena está opcionalmente sustituida con uno, dos, tres o cuatro grupos seleccionados de forma independiente de alquilo, halo y haloalquilo, en el que los grupos alquilo y haloalquilo pueden formar opcionalmente un anillo de 3-7 miembros con el átomo de carbono al que están unidos;
Q’ es una cadena C4-8 saturada o insaturada que opcionalmente contiene un heteroátomo seleccionado de nitrógeno, oxígeno y azufre; estando la cadena opcionalmente sustituida con uno, dos, tres o cuatro grupos seleccionados de alquilo y halo;
Z está seleccionado de CH2, O y NRz; en el que Rz está seleccionado de hidrógeno y alquilo.
En una primera realización del primer aspecto, la presente divulgación proporciona un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo, en la que R1 es NHSO2R4.
En una segunda realización del primer aspecto, la presente divulgación proporciona un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo, en la que R1 es NHSO2R4 y en la que n es 1.
En una tercera realización del primer aspecto, la presente divulgación proporciona un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo, en la que R1 es NHSO2R4, n es 1, Q es una cadena C4-6 saturada o insaturada opcionalmente sustituida con dos grupos alquilo, y Z es O.
En una cuarta realización del primer aspecto, la presente divulgación proporciona un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo, en la que R1 es NHSO2R4, n es 1, Q es una cadena C4-6 saturada o insaturada opcionalmente sustituida con dos grupos alquilo, Z es O y R3 es alcoxi.
En una quinta realización del primer aspecto, la presente divulgación proporciona un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo, en la que R1 es NHSO2R4, n es 1, Q es una cadena C4-6 saturada o insaturada opcionalmente sustituida con dos grupos alquilo, Z es O, R3 es alcoxi y R2 es alcoxi.
En una sexta realización del primer aspecto, la presente divulgación proporciona un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo, en la que R1 es NHSO2R4, n es 1, Q es una cadena C4-6 saturada o insaturada opcionalmente sustituida con dos grupos alquilo, Z es O, R3 es alcoxi, R2 es alcoxi y Q' es una cadena C68 saturada o insaturada.
En una séptima realización del primer aspecto, la presente divulgación proporciona un compuesto de fórmula (I) o una sal farmacéuticamente aceptable del mismo,... [Seguir leyendo]
Reivindicaciones:
1. Un compuesto de fórmula (I)
o una sal farmacéuticamente aceptable del mismo, en la que n es 0, 1, 2, 3 o 4;
R1 está seleccionado de hidroxi y -NHSO2R4;
R2 está seleccionado de hidrógeno, alcoxi, alquilsulfanilo, alquilsulfonilo, alquilsulfoxilo e hidroxi;
cada R3 está seleccionado independientemente de alcoxi, alquilo, ciano, dialquilamino, halo, haloalquilo, haloalcoxi,
un heterociclo monocíclico, hidroxilo y fenilo; en el que el heterociclo monocícliclo y el fenilo están cada uno opcionalmente sustituidos con uno, dos, tres, cuatro o cinco sustituyentes, seleccionados independientemente de alcoxi, alquilo, dialquilamino, halo, haloalcoxi y haloalquilo;
R4 está seleccionado de alquilo, arilo, aralquilo, cicloalquilo, (cicloalquil) alquilo, heterociclilo y NRaRb; en el que el alquilo y el cicloalquilo están cada uno opcionalmente sustituidos con un grupo seleccionado de alquilo, alcoxi, halo,
haloalquilo, ciano, cianoalquilo y haloalcoxi;
R5 y R6 están seleccionados independientemente de hidrógeno, alcoxi C1-3, haloalcoxi C1-3 y alquilo C1-3 opcionalmente sustituido con halo,
Ra y Rb están seleccionados independientemente de hidrógeno, alcoxi, alquilo, arilo, arilalquilo, cicloalquilo, (cicloalquil) alquilo, haloalquilo, heterociclilo y heterociclilalquilo;
Q es una cadena C4-8 saturada o insaturada que opcionalmente contiene un átomo de oxígeno y en la que la cadena está opcionalmente sustituida con uno, dos, tres o cuatro grupos seleccionados de forma independiente de alquilo, halo y haloalquilo, en el que los grupos alquilo y haloalquilo pueden formar opcionalmente un anillo de 3-7 miembros con el átomo de carbono al que están unidos;
Q’ es una cadena C4-8 saturada o insaturada que opcionalmente contiene un heteroátomo seleccionado de nitrógeno, oxígeno y azufre; estando la cadena opcionalmente sustituida con uno, dos, tres o cuatro grupos seleccionados de alquilo y halo;
Z está seleccionado de CH2, O y NRz; en el que Rz está seleccionado de hidrógeno y alquilo.
2. Un compuesto de la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que R1 es NHSO2R4.
3. Un compuesto de la reivindicación 2, o una sal farmacéuticamente aceptable del mismo, en el que n es 1.
4. Un compuesto de la reivindicación 3, o una sal farmacéuticamente aceptable del mismo, en el que Q es una
cadena C4-6 saturada o insaturada opcionalmente sustituida con dos grupos alquilo y Z es O.
5. Un compuesto de la reivindicación 4, o una sal farmacéuticamente aceptable del mismo, en el que R3 es alcoxi.
6. Un compuesto de la reivindicación 5, o una sal farmacéuticamente aceptable del mismo, en el que R2 es alcoxi.
7. Un compuesto de la reivindicación 6, o una sal farmacéuticamente aceptable del mismo, en el que Q’ es una 5 cadena C6-8 saturada o insaturada.
8. Un compuesto de acuerdo con la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que R1 es -NHSO2R4;
R2 es alcoxi; R4 es cicloalquilo; y 10 R5 y R6 son hidrógeno.
9. Un compuesto de la reivindicación 1, o una sal farmacéuticamente aceptable del mismo, en el que n es 1; R1 es NHSO2R4; en el que R4 es cicloalquilo; R2 es alcoxi;
R3 es alcoxi; R5 y R6 son cada uno hidrógeno; Q es una cadena C4-6 saturada o no sustituida opcionalmente sustituida con dos grupos alquilo; Q’ es una cadena C4-6 saturada o no sustituida opcionalmente sustituida con dos grupos alquilo; Z es O.
10. Un compuesto seleccionado de:
y o una sal farmacéuticamente aceptable del mismo.
11. Una composición que comprende el compuesto de una cualquiera de las reivindicaciones 1 a 10 o una sal farmacéuticamente aceptable del mismo, y un vehículo farmacéuticamente aceptable.
12. La composición de la reivindicación 11, que comprende además al menos un compuesto adicional que tiene actividad contra el VHC.
13. La composición de la reivindicación 12, en la que al menos uno de los compuestos adicionales es un interferón o una ribavirina.
14. La composición de la reivindicación 13, en la que el interferón está seleccionado de interferón alfa 2B, interferón 10 alfa pegilado, interferón de consenso, interferón alfa 2A e interferón tau linfoblastoide.
15. La composición de la reivindicación 12, en la que al menos uno de los compuestos adicionales está seleccionado de interleucina 2, interleucina 6, interleucina 12, un compuesto que potencia el desarrollo de la respuesta de linfocitos T auxiliares de tipo 1, ARN de interferencia, ARN antisentido, imiqimod, ribavirina, un inhibidor de inosin.
5. monofosfato deshidrogenasa, amantadina y rimantadina.
16. La composición de la reivindicación 12, en la que al menos uno de los compuestos adicionales es eficaz para inhibir la función de una diana seleccionada de metaloproteasa del VHC, serina proteasa del VHC, polimerasa del VHC, helicasa del VHC, proteína NS4B del VHC, entrada del VHC, ensamblaje del VHC, salida del VHC, proteína NS5A del VHC e IMPDH para el tratamiento de la infección por VHC.
17. El compuesto de una cualquiera de las reivindicaciones 1 a 10, o una sal farmacéuticamente aceptable del 20 mismo para su uso en un procedimiento de tratamiento de una infección por VHC en un paciente.
18. El compuesto o sal para su uso en un procedimiento de acuerdo con la reivindicación 17, en el que, en el procedimiento, se administra al menos un compuesto adicional que tiene actividad contra el VHC antes de, después de, o de forma simultánea, con el compuesto de una cualquiera de las reivindicaciones 1 a 10, o una sal farmacéuticamente aceptable del mismo.
19. El compuesto o sal para su uso en un procedimiento de acuerdo con la reivindicación 18, en el que al menos uno de los compuestos adicionales es un interferón o una ribavirina.
20. El compuesto o sal para su uso en un procedimiento de acuerdo con la reivindicación 19, en el que el interferón está seleccionado de interferón alfa 2B, interferón alfa pegilado, interferón de consenso, interferón alfa 2A e interferón tau linfoblastoide.
21. El compuesto o sal para su uso en un procedimiento de acuerdo con la reivindicación 18, en el que al menos uno de los compuestos adicionales está seleccionado de interleucina 2, interleucina 6, interleucina 12, un compuesto que potencia el desarrollo de la respuesta de linfocitos T auxiliares de tipo 1, ARN de interferencia, ARN antisentido, imiqimod, ribavirina, un inhibidor de inosin.
5. monofosfato deshidrogenasa, amantadina y rimantadina.
22. El compuesto o sal para su uso en un procedimiento de acuerdo con la reivindicación 18, en el que al menos uno de los compuestos adicionales es eficaz para inhibir la función de una diana seleccionada de metaloproteasa del VHC, serina proteasa del VHC, polimerasa del VHC, helicasa del VHC, proteína NS4B del VHC, entrada del VHC, ensamblaje del VHC, salida del VHC, proteína NS5A del VHC e IMPDH para el tratamiento de la infección por VHC.
Patentes similares o relacionadas:
Composiciones enzimáticas líquidas estabilizadas, del 6 de Mayo de 2020, de NOVOZYMES A/S: Aldehído peptídico con la fórmula B2-B1-B0-H, donde: H es hidrógeno; B0 es un residuo de Tyr; B1 es un residuo de aminoácido de alanina, cisteína, glicina, […]
Composición que comprende un péptido derivado de adinopectina, del 11 de Diciembre de 2019, de KNU-Industry Cooperation Foundation: Una composición farmacéutica adecuada para prevenir o tratar una enfermedad de la piel, que comprende un péptido seleccionado del grupo que consiste en los péptidos de las […]
Método para producir un péptido recombinante y péptido resultante, del 6 de Noviembre de 2019, de "IVIX" Company Limited: Una composición farmacéutica que comprende un péptido de fórmula: Thr-Lys-Pro-Arg-Pro-X, en donde X es un grupo OH, OCH3 o NH2.
Formulaciones de tripéptidos liofilizados estables en almacenamiento, del 15 de Octubre de 2019, de DR. AUGUST WOLFF GMBH & CO. KG ARZNEIMITTEL: Formulación liofilizada que comprende lisil-prolil-treonina o una sal farmacéuticamente aceptable de la misma, que comprende además uno o […]
Composiciones de péptidos, del 14 de Mayo de 2019, de DSM IP ASSETS B.V.: Una composición, que comprende: (i) 0,001-12,5% en peso de un péptido con 2-12 aminoácidos sustituido con un resto lipófilo, (ii) 0,00001-2% […]
Inhibidores homomultivalentes y heteromultivalentes de antígeno de membrana específico de próstata (PMSA) y usos de los mismos, del 1 de Mayo de 2019, de THE JOHNS HOPKINS UNIVERSITY: Un compuesto de fórmula II:**Fórmula** - en la que Z es H, CO2H, NH2, SH u OH; - en la que cada R1 es el mismo resto o uno diferente y se selecciona entre el grupo […]
Método de producción de péptidos, del 3 de Abril de 2019, de KANEKA CORPORATION: Método de producción de un péptido mediante un método de síntesis en fase líquida, que comprende etapas de: etapa A: una etapa de hacer […]
Formulación de compuestos de ácido borónico, del 5 de Marzo de 2019, de THE UNITED STATES OF AMERICA, REPRESENTED BY THE SECRETARY, DEPARTMENT OF HEALTH AND HUMAN SERVICES: Procedimiento de preparación de un compuesto lifolizado de la fórmula :**Fórmula** en la que: P es hidrógeno o un resto de protección de grupo amino; R es […]