Forma cristalina de pregabalina y co-formadores en el tratamiento del dolor.
La presente invención se refiere a nuevas formas cristalinas de pregabalina y co-formadores,
a procedimientos para la preparación de las mismas y a su uso como medicamento o en formulaciones farmacéuticas, más particularmente para el tratamiento del dolor.
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P201230753.
Solicitante: LABORATORIOS DEL DR. ESTEVE, S.A..
Nacionalidad solicitante: España.
Inventor/es: TESSON,NICOLAS, PLATA SALAMAN,Carlos Ramón, TRILLA CASTAÑO,Montserrat, CARDENAS ROMAÑA,Lydia.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/197 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › estando los grupos amino y carboxílico unidos a la misma cadena carbonada acíclica, p. ej. ácido gama-aminobutírico (GABA), beta-alanina, ácido epsilon-aminocaproico, ácido pantoténico (carnitina A61K 31/205).
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
- C07C229/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 229/00 Compuestos que contienen grupos amino y carboxilo unidos a la misma estructura carbonada. › estando el átomo de nitrógeno del grupo amino unido a átomos de hidrógeno.
- C07C53/126 C07C […] › C07C 53/00 Compuestos saturados que no tienen más que un grupo carboxilo unido a un átomo de carbono acíclico o a un átomo de hidrógeno. › Acidos que contienen al menos cinco átomos de carbono.
- C07C57/145 C07C […] › C07C 57/00 Compuestos insaturados que tienen grupos carboxilo unidos a átomos de carbono acíclicos. › Acido maleico.
- C07C59/245 C07C […] › C07C 59/00 Compuestos que tienen grupos carboxilo unidos a átomos de carbono acíclicos y conteniendo uno de de los grupos OH, O-metal,—CHO, cetona, éter, grupos, grupos, o grupos. › conteniendo grupos hidroxilo u O-metal.
- C07C59/255 C07C 59/00 […] › Acido tartárico.
- C07C63/06 C07C […] › C07C 63/00 Compuestos que tienen grupos carboxilo unidos a los átomos de carbono de ciclos aromáticos de seis miembros. › Acido benzoico.
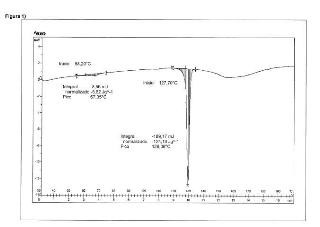
Fragmento de la descripción:
eficacia en el tratamiento del dolor neuropático y la interferencia del sueño asociada con la neuropatía diabética periférica y neuralgia posherpética.
Se sugirieron sales de pregabalina farmacéutica mente aceptables formadas con ácidos o bases orgánicos o inorgánicos en una familia de patentes basada en el documento WO 93/23383 (por ejemplo, el documento EP 641 330) . Aunque no se prepararon realmente sales, se dio a conocer que "las sales de adición de ácido [ ... ] se preparan o bien disolviendo la base libre en una disolución acuosa o bien en una alcohólica acuosa u otros disolventes apropiados que contienen el ácido apropiado y aislando la sal evaporando la disolución. Ejemplos de sales farmacéuticamente aceptables son los clorhidratos, bromhidratos, hidrosulfatos, etc., así como sales de sodio, potasio y magnesio, etc." (Véase el documento WO 93/23383 en las páginas 6
7.)
Parece que sólo se han preparado dos sales de adición de ácido de pregabalina: clorhidrato de pregabalina (documento WO 2005/041927) y (S) -mandelato de pregabalina (documento WO 96/40617) .
El co-cristal de 5-metilhexanoato de (S) -3- (amoniometilo) y ácido (S) -mandélico se da a conocer en Acta Cr y stallographica, Section E: Structure Reports Online (2007) , E63 (10) , 03938, S03938/1-S03938/11. Este documento da a conocer el co-cristal de (S) -pregabalina y ácido (S) -mandélico que se usa para resolver la pregabalina racémica a escala industrial. Sin embargo, no da a conocer ninguna ventaja específica del propio co-cristal. Ejemplos de esto incluirían: mejora de solubilidad, biodisponibilidad de pregabalina o cualquier otra mejora en las propiedades fisicoquímicas.
Aunque la pregabalina se usa como la forma libre en el producto farmacéutico comercializado, es deseable proporcionar un compuesto farmacéutica mente alternativo. En particular, la forma libre de pregabalina tiene una solubilidad en agua de 32 mg/ml a pH 7, 4. Una salo co-cristal más soluble en agua podría ser más conveniente para su uso en formulaciones farmacéuticas acuosas para una liberación inmediata o más rápida. Sin embargo para otros usos, podría ser ventajoso si la forma cristalina (el co-cristal o la sal) fuera menos soluble que la forma libre. Esto podría ser entonces útil para obtener formulaciones de liberación sostenida o lenta. Además, la sal o co-cristal debe ser suficientemente estable, tanto en estado sólido como en disolución, y debe poder obtenerse en forma cristalina sólida.
Por tanto, sería deseable encontrar una forma cristalina, como una sal o un co-cristal de pregabalina y al menos un co-formador con una solubilidad diferente a la de la pregabalina libre, siendo por tanto o bien más soluble o bien menos soluble en agua o bien (preferiblemente también) suficientemente estable o bien (de nuevo preferiblemente también) estable frente a la formación de impurezas.
Por tanto, por un lado con el fin de aumentar la velocidad y el grado de absorción y por tanto la biodisponibilidad de pregabalina, es un objeto de la presente invención mejorar la solubilidad acuosa y velocidad de disolución de la pregabalina o (o así como) el retardo de la precipitación de pregabalina disuelta proporcionando nuevas formas farmacológicas de pregabalina a través de una nueva forma cristalina de pregabalina con un ca-formador. Un objeto paralelo o adicional de la presente invención sería el retardo de la precipitación de pregabalina disuelta proporcionando nuevas formas farmacológicas de pregabalina a través de una nueva forma cristalina de pregabalina con un co-formador.
Otro objeto de la presente invención sería proporcionar nuevos medios para mejorar las propiedades de la pregabalina, especialmente con respecto al tratamiento del dolor, proporcionando nuevas formas farmacológicas de pregabalina a través de una nueva forma cristalina de pregabalina con un co-formador. Las mejoras/ventajas especialmente deseables de la nueva forma farmacológica incluirían:
• mejora de las propiedades fisicoquímicas con el fin de facilitar la formulación, la fabricación, o potenciar la absorción y/o la biodisponibilidad
• ser fácilmente obtenible, fácil de fabricar
• permitir más flexibilidad en la formulación, o facilitar su formulación,
• ser altamente soluble, permitiendo así mejores velocidades de disolución, especialmente si se disuelve en un entorno fisiológico acuoso; o
• ser menos soluble, permitiendo así la obtención de formulaciones de liberación sostenida o lenta mejorada, especialmente si se disuelve en un entorno fisiológico acuoso
• mejorar la estabilidad del co-cristal en comparación con la pregabalina sola
• permitir nuevas vías de administración.
Otras posibles ventajas, especialmente clínicas, que se proporcionarían de manera deseable en nuevas formas farmacológicas mediante la nueva forma cristalina de pregabalina y al menos un co-formador (especialmente si se compara con cualquiera de los principios activos solos) se indican a continuación:
• proporcionar un alivio del dolor más eficaz para un espectro más amplio de dolor,
• reducir las reacciones farmacológicas adversas proporcionando un perfil de seguridad mejor a altas dosis,
• potenciar la adhesión al tratamiento o el cumplimiento de los pacientes,
• aumentar el nivel de eficacia o alcanzar al menos una eficacia similar a la que puede
lograrse mediante pregabalina usada sola a altas dosis asociadas con un perfil de seguridad mejor, o • permitir una reducción de la dosis, con la actividad deseada, aún reduciendo los efectos secundarios.
lOSe logró este objetivo proporcionando nuevas formas cristalinas de pregabalina y diferentes coformadores. Estas nuevas formas cristalinas muestran propiedades mejoradas si se comparan con la pregabalina sola. Las nuevas formas cristalinas así obtenidas tienen una estequiometría específica que depende de la estructura de cada co-formador. En la circunstancia apropiada esto es también otra ventaja de esta nueva forma farmacológica sólida que logra posiblemente cierta modulación de los efectos farmacológicos.
"Co-formador" tal como se usa en el presente documento se define como un componente con el que la pregabalina puede formar co-cristales o sales. El co-formador es parte de la red cristalina. Normalmente, los co-formadores tendrán la capacidad para formar interacciones no covalentes complementarias con el agente activo, por ejemplo la capacidad para formar puentes de hidrógeno con el agente activo en el caso de co-cristales.
Se mejoran las propiedades fisicoquímicas. La formulación de la asociación es incluso más fácil de manipular con un sólido y tiene una estabilidad potenciada. La solubilidad también puede 25 potenciarse o, si se desea (véase anteriormente) , disminuirse.
Otra ventaja es que la combinación de un principio activo y un co-formador en una única especie parece permitir para una mejor farmacocinética/farmacodinámica (PKPD) lo que ayuda en el tratamiento del dolor.
Parece que se han alcanzado mejoras/ventajas especialmente deseables de la nueva forma farmacológica como se requiere anteriormente -como la mejora de las propiedades fisicoquímicas. Las propiedades fisicoquímicas probadas incluyen higroscopicidad y solubilidad.
Por consiguiente, el objeto principal de la invención es una forma cristalina de pregabalina con al menos un ca-formador.
En una realización (condición) se excluye la forma cristalina de la sal de clorhidrato de pregabalina. En una realización adicional (condición) se excluye la forma cristalina de la sal de (S) mandelato de pregabalina. En una realización adicional (condición) se excluye el co-cristal de (S) -pregabalina y ácido (S) mandélico. En una realización adicional (condición) se excluye la forma cristalina de las sales de adición de ácido de pregabalina siendo las sales de clorhidrato, bromhidrato, hidrosulfato. En una realización adicional (condición) se excluye la forma cristalina de la sal de sodio, potasio y magnesio de pregabalina.
En otra realización (condición) se excluyen
• la forma cristalina de la sal de clorhidrato de pregabalina,
• la forma cristalina de la sal de (S) -mandelato de pregabalina,
• el co-cristal de (S) -pregabalina y ácido (S) -mandélico,
• la forma cristalina de las sales de adición de ácido de pregabalina siendo las sales de clorhidrato, bromhidrato, hidrosulfato,
• la forma cristalina de la sal de sodio, potasio y magnesio de pregabalina.
En una realización de la forma cristalina según...
Reivindicaciones:
1. Forma cristalina de pregabalina con al menos un co-formador con las condiciones de que se excluyen
• la forma cristalina de la sal de clorhidrato de pregabalina,
• la forma cristalina de la sal de (S) -mandelato de pregabalina,
• el co-cristal de (S) -pregabalina y ácido (S) -mandélico,
• la forma cristalina de las sales de adición de ácido de pregabalina que son sales de clorhidrato, bromhidrato, hidrosulfato,
• la forma cristalina de la sal de sodio, potasio y magnesio de pregabalina.
2. Forma cristalina según la reivindicación 1, en la que la forma cristalina es la forma cristalina de una salo es un co-cristal.
3. Forma cristalina según cualquiera de las reivindicaciones 1 ó 2, en la que el co-formador se selecciona entre el grupo que consiste en ácido tartárico, ácido benzoico, ácido cáprico, ácido caprílico, ácido láurico, ácido maleico, L-prolina, nicotinamida, ácido málico, urea o sus estereoisómeros; más preferiblemente en la que el co-formador se selecciona entre el grupo que consiste en ácido tartárico, ácido málico, ácido benzoico, ácido cáprico, ácido caprílico, ácido láurico, ácido maleico, L-prolina.
4. Forma cristalina según una cualquiera de las reivindicaciones 1 a 3, en la que la forma cristalina es la forma cristalina de una sal de pregabalina y un ca-formador que es un coformador de sal.
5. Forma cristalina según la reivindicación 4, en la que la pregabalina es (S) -pregabalina.
6. Forma cristalina según una cualquiera de las reivindicaciones 4 ó 5, en la que el coformador de sal se selecciona entre el grupo que consiste en ácido tartárico, ácido benzoico, ácido cáprico, ácido caprílico, ácido láurico, ácido maleico, L-prolina, nicotinamida, ácido málico, urea o sus estereoisómeros; más preferiblemente en la que el ca-formador se selecciona entre el grupo que consiste en ácido tartárico, ácido málico, ácido maleico o sus estereoisómeros; lo más preferiblemente en la que el ca-formador se selecciona entre el grupo que consiste en ácido L- (+) -tartárico, ácido L-málico o ácido maleico.
7. Forma cristalina según cualquiera de las reivindicaciones 4 a 6, en la que la sal se selecciona entre el grupo que consiste en (S) -pregabalina-ácido L- (+) -tartárico (1:1) , (S) pregabalina-ácido L- ( + ) -tartárico-H20 (1:1:1) , (S) -pregabalina-ácido L-málico (1: 1) , (S) pregabalina-ácido maleico (1: 1) , (S) -pregabalina-ácido maleico-H20 (1: 1 :0, 5) o (S) pregabalina-ácido maleico anhidro (1 :1) ; preferiblemente en la que la sal se selecciona entre el grupo que consiste en (S) pregabalina-ácido L- (+ ) -tartárico-H20 (1: 1: 1) , (S) -pregabalina-ácido L-málico (1: 1) o (S) pregabalina-ácido maleico (1 : 1 ) .
8. Forma cristalina según una cualquiera de las reivindicaciones 1 a 3, en la que el compuesto es un co-cristal que comprende pregabalina como base libre o como su sal farmacéuticamente aceptable y al menos un co-formador que es un formador de co-cristal.
9. Forma cristalina según la reivindicación 8, en la que la pregabalina es (S) -pregabalina.
10. Forma cristalina según una cualquiera de las reivindicaciones 8 ó 9, en la que el formador de co-cristal se selecciona entre el grupo que consiste en ácido tartárico, ácido benzoico, ácido cáprico, ácido caprílico. ácido láurico, ácido maleico, prolina o sus estereoisómeros; más preferiblemente en la que el co-formador se selecciona entre el grupo que consiste en ácido tartárico, ácido benzoico, ácido maleico. prolina, ácido caprílico, ácido cáprico. ácido láurico o sus estereoisómeros; lo más preferiblemente en la que el co-formador se selecciona entre el grupo que consiste en ácido benzoico, L-prolina, ácido caprílico, ácido cáprico o ácido láurico.
11. Forma cristalina según una cualquiera de las reivindicaciones 8 a 10, en la que el co-cristal se selecciona entre (S) -pregabalina-ácido L -tartárico (1: 1) , (S) -pregabalina-ácido benzoico (1:1) , (S) -pregabalina-L-prolina-HCI (1 :1:1) , (S) -pregabalina-ácido maleico-H20 (1:1 :0, 5) , (S) -pregabalina-ácido caprílico (1: 1) , (S) -pregabalina-ácido cáprico (1: 1) , (S) -pregabalinaácido maleico anhidro (1:1) o (S) -pregabalina-ácido láurico (1:1) ; más preferiblemente en la que el co-cristal se selecciona entre (S) -pregabalina-ácido benzoico (1: 1) , (S) -pregabalina-L-prolina-HCI (1:1: 1) , (S) -pregabalina-ácido caprílico (1: 1) , (S) -pregabalina-ácido cáprico (1: 1) ; o (S) -pregabalina-ácido láurico (1: 1) .
12. Forma cristalina según la reivindicación 2, en la que la forma de cristal se selecciona entre formas de (S) -pregabalina-ácido L - ( + ) -tartárico (1: 1) , (S) -pregabalina-ácido maleico-H20
(1:1 :0, 5) o (S) -pregabalina-ácido maleico anhidro (1:1) .
Patentes similares o relacionadas:
 Hidrolizado de caseína para uso en el tratamiento de enfermedades inflamatorias, del 29 de Julio de 2020, de MJN U.S. Holdings, LLC: Una composición nutricional, que comprende un lípido o una fase grasa, una fuente de proteína y un hidrolizado de caseína para uso en el tratamiento […]
Hidrolizado de caseína para uso en el tratamiento de enfermedades inflamatorias, del 29 de Julio de 2020, de MJN U.S. Holdings, LLC: Una composición nutricional, que comprende un lípido o una fase grasa, una fuente de proteína y un hidrolizado de caseína para uso en el tratamiento […]
 Compuestos que modulan la actividad de señalización de las interleucinas 17 y 23, del 29 de Julio de 2020, de Sarepta Therapeutics, Inc: Un método ex vivo de modulación de la actividad de señalización de IL-17 en una célula, que comprende poner en contacto la célula con un oligómero antisentido de morfolino […]
Compuestos que modulan la actividad de señalización de las interleucinas 17 y 23, del 29 de Julio de 2020, de Sarepta Therapeutics, Inc: Un método ex vivo de modulación de la actividad de señalización de IL-17 en una célula, que comprende poner en contacto la célula con un oligómero antisentido de morfolino […]
Formas cristalinas de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, del 29 de Julio de 2020, de Hutchison Medipharma Limited: Forma I de 6-((6,7-dimetoxiquinazolin-4-il)oxi)-N,2-dimetilbenzofuran-3-carboxamida, en donde el difractograma de rayos X de polvo de la Forma […]
Bloqueador de canales de sodio, del 29 de Julio de 2020, de DAEWOONG PHARMACEUTICAL CO., LTD.: Un compuesto representado por la Fórmula Química 1 más abajo, o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la Fórmula […]
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Compuestos que tienen actividad antagonista del receptor muscarínico y agonista del receptor beta2 adrenérgico, del 29 de Julio de 2020, de CHIESI FARMACEUTICI S.P.A.: Un compuesto de fórmula general I **(Ver fórmula)** en la que Q es un grupo de fórmula Q1 **(Ver fórmula)** Z es H u OH; […]
Composición farmacéutica en forma de solución oral de la sal de ibuprofeno con lisina, del 27 de Julio de 2020, de MMC INTERNATIONAL HEALTH HOLDING, S.L: La presente invención se refiere a una composición farmacéutica en forma de solución oral de la sal de ibuprofeno con lisina, que comprende un sistema viscosizante […]
Derivado heteroarilo o sal farmacéuticamente aceptable del mismo, método de preparación del mismo y composición farmacéutica para prevenir o tratar enfermedades asociadas con PI3 quinasas, que contiene el mismo como principio activo, del 22 de Julio de 2020, de KOREA RESEARCH INSTITUTE OF CHEMICAL TECHNOLOGY: Un compuesto representado por la fórmula 1, un isómero óptico del mismo o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en la fórmula […]