Cocristales de tramadol y coxibs.
Un cocristal que comprende tramadol o como base libre o en forma de una sal fisiológicamente aceptable y por lomenos un coxib.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2010/002385.
Solicitante: LABORATORIOS DEL DR. ESTEVE, S.A..
Nacionalidad solicitante: España.
Inventor/es: TESSON,NICOLAS, PLATA SALAMAN,Carlos Ramón.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/135 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen ciclos aromáticos, p. ej. metadona.
- A61K31/415 A61K 31/00 […] › 1,2-Diazoles.
- A61P29/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes analgésicos, antipiréticos o antiinflamatorios que no actúan sobre el sistema nervioso central, p. ej. agentes antirreumáticos; Antiinflamatorios no esteroideos (AINEs).
PDF original: ES-2402112_T3.pdf
Fragmento de la descripción:
Cocristales de tramadol y coxibs La presente invención se refiere a cocristales de tramadol y AINE, como los coxibs, a procedimientos para preparación de los mismos y a sus usos como medicamentos o en formulaciones farmacéuticas, más particularmente para el tratamiento del dolor.
El dolor es una respuesta compleja que se ha clasificado funcionalmente en componentes sensoriales, autónomos, motores y emocionales. El aspecto sensorial incluye información acerca de la ubicación del estímulo y la intensidad, mientras que el componente de adaptación puede considerarse que es la activación de la modulación del dolor endógeno y la planificación motora para las respuestas de escape. El componente emocional parece incluir la evaluación de lo desagradable del dolor y la amenaza del estímulo, así como también las emociones negativas desencadenadas por la memoria y el contexto del estímulo doloroso.
En general, las condiciones de dolor lo pueden dividir en crónico y agudo. El dolor crónico incluye dolor neuropático y dolor inflamatorio crónico, por ejemplo artritis, o dolor de origen desconocido, como fibromialgia. El dolor agudo generalmente sigue a una lesión del tejido no–neural, por ejemplo daño en tejidos por cirugía o inflamación, o migraña.
Se conocen muchos fármacos que son útiles en el tratamiento o la gestión del dolor. Los opioides con frecuencia se usan como analgésicos en el dolor. Los derivados de la morfina están indicados para el tratamiento del dolor moderado o agudo en seres humanos. El efecto analgésico se obtiene a través de su acción sobre los receptores morfínicos, preferentemente los receptores μ. Entre estos derivados de morfina se pueden mencionar morfina, codeína, petidina, dextropropoxifenometadona, lenefopan y otros.
Uno de los derivados morfínicos que ha mostrado muy buenos resultados cuando se administra por vía oral, y que se encuentra ampliamente comercializado es el tramadol, también disponible como una sal fisiológicamente aceptable, particularmente como un clorhidrato. El tramadol, cuyo nombre químico es 2– (dimetilaminometil) –1– (3– metoxifenil) ciclohexanol, tiene la fórmula siguiente:
CH3
N H3C
H3C O
Tramadol
Esta estructura muestra dos centros quirales diferentes y, por tanto, puede existir en diferentes diastereoisómeros entre los cuales el tramadol es el cis-diastereisómero: (1R, 2R) , o (1S, 2S) , ambos también conocidos como (+) – tramadol y (–) –tramadol y los dos contribuyen de diferentes formas a su actividad.
Por la técnica parece que este compuesto no es ni completamente de tipo opioide, ni de tipo no–opioide. En algunos estudios se ha demostrado que el tramadol es un agonista opioide, mientras que las experiencias clínicas indican que carece de muchos de los efectos secundarios típicos de los agonistas opiodes, por ejemplo depresión respiratoria, estreñimiento o tolerancia.
Debido a sus desventajas, los opioides no siempre pueden administrarse repetidamente o a dosis más altas como analgésicos para tratar el dolor. Los efectos secundarios de los opioides se conocen en la técnica, incluidos en por ejemplo, J. Jaffe en “Goodman and Gilman’s, The Pharmacological Basis of Therapeutics”, 8ª-edición; Gilman y col.; Pergamon Press, New York, 1990, Capítulo 22, páginas 522–573.
En consecuencia se ha propuesto combinar los opioides con otros fármacos que no son agentes analgésicos opioides, con el fin de disminuir la cantidad de opioides necesaria para producir un grado equivalente de analgesia. Entre estas combinaciones, se ha comunicado que la asociación de tramadol con fármacos antiinflamatorios no esteroideos (AINE) son de particular interés (documento EP–0 546 676) . El documento WO 2008/08567 divulga un cocristal de celecoxib (un AINE) y nicotinamida.
Por lo tanto, el objetivo de la presente invención era proporcionar medios nuevos para mejorar las propiedades del tramadol, especialmente con respecto al tratamiento del dolor, ofreciendo nuevas formas de tramadol candidatos a fármaco.
Las mejoras/ventajas especialmente deseables de la nueva forma candidata a ser un fármaco incluirían:
• mejora de las propiedades fisicoquímicas con el fin de facilitar la formulación, la fabricación o para potenciar la absorción y/o la biodisponibilidad:
por lo tanto
• ser más activo en comparación con el tramadol base o la sal clorhidrato; o
• proporcionar una forma de tramadol con un agente activo adicional que tenga un efecto farmacológico beneficioso en sí mismo, lo que permite una relación dosis/peso altamente eficaz del principio activo final o pareja
• permitir el uso de una dosis terapéutica más baja ya sea de tramadol o el agente activo adicional, un AINE – el coxib –, o de ambos;
• tener un efecto sinérgico a través de la combinación de tramadol y el agente activo adicional, un AINE – el coxib –, en la misma nueva forma candidata a fármaco; o
adicionalmente
• no tener o tener atenuado el sabor amargo del tramadol;
• ser de fácil obtención, de fácil fabricación o
• permitir más flexibilidad en la formulación, o facilitar su formulación,
• ser altamente soluble, lo que permite mejores índices de disolución, especialmente si se disuelve en un entorno fisiológico acuoso, o
• mejorar la estabilidad del cocristal en comparación con la mezcla física de Tramadol/Agente Activo (un AINE – el coxib –) en la misma proporción;
• permitir nuevas vías de administración;
también
• permitir, en caso de ser necesario, combinar tramadol con un agente activo químico normalmente no compatible en la misma formulación o incluso en contacto inmediato, sin tener que aislar el tramadol;
o, por último
• minimizar/reducir los efectos secundarios, especialmente los efectos secundarios graves, asignados al tramadol.
Otras mejoras/ventajas deseables de la nueva forma candidata a fármaco incluirían ser activo en enfermedades o síntomas que son o se relacionan con el dolor y sus subtipos, en especial aquellos en en los que el tratamiento actual es insuficiente, como ciática u hombro doloroso, o dolor relacionado con la sensibilización central (síndrome del dolor central) .
Más deseablemente, las nuevas formas candidatas a fármaco deberían combinar más de una, la mayoría de estas ventajas.
Este objetivo se logó proporcionando nuevos cocristales de tramadol. Se encontró que el tramadol era capaz de formar cocristales con AINE, como coxib, en especial con celecoxib. Estos cocristales muestran propiedades mejoradas si se comparan con tramadol solo, y también buena actividad analgésica. Los cocristales obtenidos de este modo tienen una estequiometría específica. Bajo la circunstancia adecuada, es también otra ventaja de estas nuevas formas sólidas candidatas a fármaco la posibilidad de alcanzar alguna modulación de los efectos farmacológicos. Aunque se ha reconocido que los API (siglas en inglés para Ingredientes Farmacéuticos Activos) como el tramadol forman polimorfos cristalinos, solvatos, hidratos y formas amorías durante un número de años, existe poco conocimiento acerca de qué API formarán cocristales. Los cocristales son un tipo específico de forma cristalina que provee una nueva ruta para modular la forma API y, de este modo, modular las propiedades API. Los cocristales contienen un API y al menos uno de otro componente que cristalizan juntos. La elección del otro componente ayuda a determinar si se formará un cocristal y qué propiedades tendrá el cocristal. Al igual que un polimorfo, solvato, hidrato o forma amoría de un API puede modular la estabilidad, la solubilidad y la higroscopicidad, un cocristal puede modular esas mismas propiedades.
De este modo el objetivo principal de la presente invención es un cocristal que comprenda tramadol ya sea como una base libre o como una sal fisiológicamente aceptable y al menos un AINE/coxib.
Los coxibs son AINE sumamente interesantes por ser los formadores de cocristal con tramadol. Son inhibidores selectivos de la COX–2. El más importante de estos es el fármaco comercializado celecoxib. Su nombre químico es 4–[5– (4–metilfenil) –3– (trifluorometil) –pirazol–1–il]bencenosulfonamida. Su fórmula empírica es C17H14F3N3O2S.
F
F
N N F
O
SH2N O
Celecoxib
Los AINE como los coxibs tienen actividad analgésica en una serie de síntomas de dolor.... [Seguir leyendo]
Reivindicaciones:
1. Un cocristal que comprende tramadol o como base libre o en forma de una sal fisiológicamente aceptable y por lo menos un coxib.
2. Un cocristal de acuerdo con la reivindicación 1, en el que el coxib se elige de tal manera que si se compara tanto con tramadol solo, como con una mezcla de tramadol y el correspondiente coxib, como agente/s activo/s:
• la solubilidad del cocristal se ha incrementado; y/o
• la respuesta de dosis del cocristal se ha incrementado; y/o
• la eficacia del cocristal se ha incrementado; y/o
• la disolución del cocristal se ha incrementado; y/o
• la biodisponibilidad del cocristal se ha incrementado; y/o
• la estabilidad del cocristal se ha incrementado; y/o
• la higroscopicidad del cocristal ha disminuido; y/o
• la diversidad de forma del cocristal ha disminuido; y/o
• la morfología del cocristal se ha modulado
3. El cocristal de acuerdo con cualquiera de las reivindicaciones 1 o 2, en el que el AINE se selecciona de:
- Celecoxib,
- Etoricoxib,
- Lumiracoxib,
- Parecoxib,
- Rofecoxib,
- Valdecoxib, o
- Cimicoxib.
4. El cocristal de acuerdo con cualquiera de las revindicaciones 1 a 3, en el que el tramadol es (–) –tramadol o (+) – tramadol o es (rac) –tramadol o una sal del mismo.
5. El cocristal de acuerdo con cualquiera de las reivindicaciones 1 a 4, en el que el coxib es celecoxib o sales del mismo.
6. Un cocristal de acuerdo con la reivindicación 5, seleccionado de:
• un cocristal que comprende (rac) –tramadol ya sea tanto como una base libre o como una sal fisiológicamente aceptable y celecoxib;
• un cocristal que comprende (+) –tramadol ya sea tanto como una base libre o como una sal fisiológicamente aceptable y celecoxib;
• un cocristal que comprende (–) –tramadol ya sea tanto como una base libre o como una sal fisiológicamente aceptable y celecoxib; o preferentemente
• un cocristal que comprende (rac) –tramadol·HCl y celecoxib
7. El cocristal de acuerdo con cualquiera de las reivindicaciones 1 a 6, que comprende (rac) –tramadol·HCl y celecoxib.
8. El cocristal de acuerdo con la reivindicación 7, en el que la relación molecular entre el (rac) –tramadol·HCl y celecoxib es 1:1.
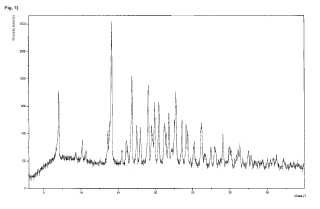
9. Un cocristal de acuerdo con la reivindicación 8 que comprende (rac) –tramadol·HCl y celecoxib en una relación molecular de 1:1, caracterizado porque muestra un patrón de Difracción de Rayos X en polvo con picos [28] en 7, 1, 9, 3, 10, 2, 10, 7, 13, 6, 13, 9, 14, 1, 15, 5, 16, 1, 16, 2, 16, 8, 17, 5, 18, 0, 19, 0, 19, 5, 19, 9, 20, 5, 21, 2, 21, 3, 21, 4, 21, 8, 22, 1,
22, 6, 22, 7, 23, 6, 24, 1, 24, 4, 25, 2, 26, 1, 26, 6, 26, 8, 27, 4, 27, 9, 28, 1, 29, 1, 29, 9, 30, 1, 31, 1, 31, 3, 31, 7, 32, 5, 32, 8, 34, 4, 35, 0, 35, 8, 36, 2 y 37, 2[°], habiéndose obtenido los valores 28 usando radiación de cobre (CuKa1 1, 54060Å) .
10. Un cocristal de acuerdo con la reivindicación 8 que comprende (rac) –tramadol·HCl y celecoxib en una relación molecular de 1:1, caracterizado porque muestra un patrón infrarrojo por Transformada de Fourier con bandas de absorción a 3481, 6 (m) , 3133, 5 (m) , 2923, 0 (m) , 2667, 7 (m) , 1596, 0 (m) , 1472, 4 (m) , 1458, 0 (m) , 1335, 1 (m) , 1288, 7 (m) , 1271, 8 (m) , 1168, 7 (s) , 1237, 3 (m) , 1168, 7 (s) , 1122, 6 (s) , 1100, 9 (m) , 1042, 2 (m) , 976, 8 (m) , 844, 6 (m) , 820, 1 (m) , 786, 5 (m) 625, 9 (m) cm–1.
11. Un cocristal de acuerdo con la reivindicación 8 que comprende (rac) –tramadol·HCl y celecoxib en una relación molecular de 1:1, caracterizado porque tiene una celda unitaria ortorrómbica con las siguientes dimensiones:
a = 11, 0323 (7) Å
b = 18, 1095 (12) Å
c = 17, 3206 (12) Å
12. Un cocristal de acuerdo con la reivindicación 8 que comprende (rac) –tramadol·HCl y celecoxib en una relación molar de 1:1, caracterizado porque el pico endotérmico agudo que corresponde al punto de fusión tiene un inicio a 164 ºC.
13. Un procedimiento para la producción de un cocristal de acuerdo con reivindicación 1 que comprende las etapas de:
(a) disolver o suspender el coxib en un disolvente; opcionalmente calentando la solución o dispersión hasta una temperatura por encima de temperatura ambiente y por debajo del punto de ebullición de la solución o dispersión;
(b) disolver junto con, o después de, o antes de la etapa (a) tramadol ya sea como base libre o como una sal en un disolvente, opcionalmente combinado con la etapa (a) mediante disolución de tramadol ya junto con el coxib en la etapa (a)
(c) opcionalmente añadir la solución de (b) a una solución de (a) y mezclarlas;
(d) opcionalmente añadir un disolvente a la solución of (a) , (b) o (c) y mezclarlos;
(e) enfriar la solución/dispersión mezclada de la etapa (a) , (b) , (c) o (d) a temperatura ambiente o menor;
(f) opcionalmente evaporar parte o todo el disolvente; y
(g) recoger mediante filtración los cocristales resultantes.
14. Una composición farmacéutica caracterizada porque comprende una cantidad terapéuticamente eficaz del cocristal de acuerdo con cualquiera de las reivindicaciones 1 a 12 en un medio fisiológicamente aceptable
15. Un cocristal de acuerdo con una cualquiera de las reivindicaciones 1 a 12 para uso en el tratamiento del dolor, preferentemente del dolor agudo, el dolor crónico, el dolor neuropático, el dolor nociceptivo, el dolor leve y de intenso a moderado, la hiperalgesia, el dolor relacionado con la sensibilización central, la alodinia o el dolor por cáncer, incluidas la neuropatía diabética o la neuropatía diabética periférica y la osteoartritis, la fibromialgia; la artritis reumatoide, la espondilitis anquilosante, el hombro doloroso o la ciática.
Patentes similares o relacionadas:
Uso de (1R,2R)-3-(3-dimetilamino-1-etil-2-metil-propil)-fenol para tratar el dolor inflamatorio, del 22 de Julio de 2020, de GRUNENTHAL GMBH: (1R, 2R)-3-(3-Dimetilamino-1-etil-2-metil-propil)-fenol para uso en el tratamiento del dolor inflamatorio.
Régimen de dosificación para un agonista del receptor S1P, del 3 de Junio de 2020, de NOVARTIS AG: Uso de un modulador o agonista del receptor S1P en la fabricación de un medicamento para el tratamiento de una enfermedad autoinmune, mediante […]
Métodos de administración de terapia con pirfenidona, del 13 de Mayo de 2020, de Intermune, Inc: Pirfenidona para su uso en el tratamiento de un paciente que necesita terapia con pirfenidona, caracterizada por que el tratamiento comprende reducir la dosis de […]
Composiciones congeladas fluidas que comprenden un agente terapéutico, del 8 de Abril de 2020, de Tavakoli, Zahra: Una composición fluida congelada que comprende un agente terapéutico y al menos un agente aromatizante para su uso en terapia, donde dicha composición […]
Sistema terapéutico transdérmico para la administración de principios activos hidrosolubles, del 18 de Marzo de 2020, de LTS LOHMANN THERAPIE-SYSTEME AG: Sistema terapéutico transdérmico para la administración controlada de un principio activo farmacéutico soluble en agua a partir de una fase acuosa que comprende una […]
COMBINACIÓN FARMACÉUTICA SINÉRGICA QUE COMPRENDE TRAMADOL CLORHIDRATO Y PREGABALINA, Y SU USO PARA EL TRATAMIENTO DEL DOLOR NEUROPÁTICO, del 5 de Marzo de 2020, de GRUNENTHAL GMBH: Combinación farmacéutica sinérgica que contiene tramadol clorhidrato y pregabalina en una razón p/p entre 1 :1,5 a 1 :2,5 y excipientes farmacéuticamente […]
COMBINACIÓN FARMACÉUTICA SINÉRGICA QUE COMPRENDE TRAMADOL CLORHIDRATO Y PREGABALINA, Y SU USO PARA EL TRATAMIENTO DEL DOLOR NEUROPÁTICO, del 5 de Marzo de 2020, de GRUNENTHAL GMBH: Combinación farmacéutica sinérgica que contiene tramadol clorhidrato y pregabalina en una razón p/p entre 1 :1,5 a 12,5 y excipientes farmaceuticamente aceptables, […]
Composiciones antimicrobianas mejoradas, del 5 de Febrero de 2020, de NOVAPHARM RESEARCH (AUSTRALIA) PTY LTD: Una composición antiséptica para frotado de manos que cuando es usada a una tasa menor que 6 ml de composición durante hasta 60 segundos produce un nivel de eficacia biocida […]