Activadores de urea glucoquinasa.
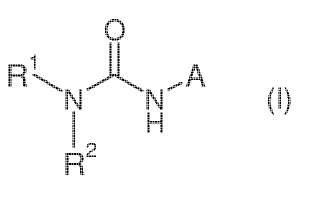
Compuesto que liene la fórmula: **Fórmula**
donde
R3 es seleccionado del grupo que consiste en fenoxi y benciloxi
cada uno de los cuales es opcionalmente sustituido con
uno o más suslituyentes independientemente seleccionados de R 2;
R12 es F, CI, Br, -CF3, CN, metilo, etilo, isopropilo, tere-butilo, metoxi, metillio, etoxi, ciclopropil-metoxi, -NHC(O)CH3, o -S(O)2-CH3;R30 es metilo, etilo, propilo, isopropilo, terc-butilo, ciclopropilo, ciclobutilo, ciclopenlilo, ciclohexilo, fen ilo, metoxi, etoxipropoxi, butoxi, terc-butoxi, benciloxi, o ciclopropil-metoxi, cada uno de los cuales es opcionalmente sustituido con uno omás sustituyentes independientemente seleccionados de R 12; **Fórmula**
R8 es metillio, isopropiltio, etiltio, o 2-metilpropiltio, cada uno de los cuales se susutuye con uno o más su stituyentesindependientemente seleccionados de Rl4
; donde R34 es carboxi; o una sal derivada farmacéuticamente aceptable.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2006/064289.
Solicitante: NOVO NORDISK A/S.
Nacionalidad solicitante: Dinamarca.
Dirección: Novo Allé 2880 Bagsværd DINAMARCA.
Inventor/es: JEPPESEN, LONE, LAU, JESPER, KRISTIANSEN, MARIT, MURRAY,Anthony , VEDSØ,Per.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/426 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › 1,3-Tiazoles.
- C07D277/48 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 277/00 Compuestos heterocíclicos que contienen ciclos de tiazol-1,3 o tiazol-1,3 hidrogenado. › por radicales derivados del ácido carbónico, o sus análogos de azufre o nitrógeno, p. ej. carbonilguanidinas.
- C07D285/08 C07D […] › C07D 285/00 Compuestos heterocíclicos que contienen ciclos que tienen átomos de nitrógeno y azufre como únicos heteroátomos del ciclo, no previstos por los grupos del C07D 275/00 - C07D 283/00. › Tiadiazoles-1,2,4; Tiadiazoles-1,2,4 hidrogenados.
- C07D285/12 C07D 285/00 […] › Tiadiazoles-1,3,4; Tiadiazoles-1,3,4 hidrogenados.
PDF original: ES-2422383_T3.pdf
Fragmento de la descripción:
Activadores de urea glucoquinasa Campo de la invención [0001) Esta solicitud se refiere a activadores de urea glucoquinasa nuevos y su uso en el tratamiento de distintas enfermedades.
Antecedentes de la invención [0002) Glucoquinasa (GK) es una de las cuatro hexoquinasas que se encuentran en mamíferos [Golowick, S. P., en The Enzymes, Vol. 9 (P. Boyer, ed.) Academic Press, New York, páginas 1-48, 1973]. Las hexoquinasas catalizan el primer paso en el metabolismo de glucosa, es decir, la conversión de glucosa en glucosa-6-fosfato. La glucoquinasa tiene una distribución celular limitada, encontrándose principalmente en células J3 pancreáticas y células parenquimales hepáticas. Además, la GK es una enzima de control del índice en el metabolismo de la glucosa en estos dos tipos de células que se conocen por desempeñar funciones fundamentales en la homeostasis de la glucosa de todo el cuerpo [Chipkin, S. R., Kelly,
K. L., Y Ruderman, N. B. en Joslin's Diabetes (C. R. Khan y G. C. Wier, eds.) Lea y, Febiger, Philadelphia, Pa., páginas 97115, 1994]. La concentración de glucosa en la que GK demuestra la mitad de la actividad máxima es aproximadamente 8 mM. Las otras tres hexoquinasas se saturan con glucosa a concentraciones muy inferiores «1 mM) . Por lo tanto, el flujo de glucosa a través de la ruta de la vía GK aumenta conforme aumenta la concentración de glucosa en la sangre en ayunas (5 mM) a niveles posprandiales (=10-15 mM) después de una comida que contiene calbohidratos [Printz, R. G. , Magnuson, M. A., Y Granner, D. K. en Ann. Rev. Nutrition Vol. 13 (R. E. Olson, D. M. Bier, y O. B. McCormick, eds.) Annual Review, Inc., Palo Alto, Calit., páginas 463-496, 1993]. Estas conclusiones contribuyeron hace una década a la hipótesis que la GK funciona como un sensor de 91ucosa en células J3 y hepatocitos (Meglasson, M. D. Y Matschinsky, F. M. Amer. J. Physiol. 246; El-E13, 1984) . En los últimos anos, estudios en animales transgénicos han confirmado que la GK tiene un papel fundamental en la homeostasis de la glucosa de todo el cuerpo. Animales que no expresan GK mueren en pocos días desde el nacimiento con diabetes aguda mientras los animales que sobreexpresan GK han mejoradO la tolerancia a la glucosa (Grupe, A., Hultgren, B., Ryan, A. et al., Gell 83, 69-78, 1995; Ferrie, T., Riu, E., Bosch, F. et al., FASEB J., 10, 1213-1218, 1996) . Un aumento en la exposición de glucosa se acopla a través de GK en células J3 hasta una secreción de insulina aumentada yen hepatocitos hasta una deposición de glic6geno aumentada y quizá una producción de glucosa disminuida.
El hallazgo de que el tipo 11 de diabetes de aparición en la madurez de una persona joven (MOOY-2) está provocado por pérdida de mutaciones funcionales en el gen GK sugiere que la GK también funciona como un sensor de glucosa en seres humanos (Liang, Y., Kesavan, P., Wang, L. et al., Biochem. J. 309, 167-173, 1995) . Pruebas adicionales que indican un papel importante de la GK en la regulación del metabolismo de la glucosa en seres humanos fueron proporcionadas por la identificación de pacientes que expresan una forma mutante de GK con actividad enzimática aumentada. Estos pacientes muestran una hipoglucemia de ayuno asociada a un nivel inapropiadamente elevado de insulina en el plasma (Glaser, B., Kesavan, P., Heyman, M. et al., New England J. Med. 338, 226-230, 1998) . Mientras que las mutaciones del gen GK no se encuentran en la mayoria de pacientes con diabetes de tipo 2, los compuestos que activan GK y, por tanto, aumentan la sensibilidad del sistema sensor de la GK todavfa será útil en el tratamiento de la hiperglucemia característica de todas las diabetes de tipo 2. Activadores de glucoquinasa aumentarán el flujO del metabolismo de la glucosa en células J3 y hepatocitos, que serán acoplados a secreción de insulina aumentada. Tales agentes serian útiles para tratar diabetes tipo 11. Varios activadores de GK son conocidos, ver, por ejemplo, US 2004/0014968 (Hofmann-La Roche Inc.) , WO 2003/055482 (Novo Nordisk NS) y WO 2004/002481 (Novo Nordisk NS) .
La diabetes se caracteriza por un metabolismo incorrecto de la glucosa que se manifiesta entre otras cosas por un nivel de glucosa en sangre elevado en los pacientes diabéticos. Defectos subyacentes llevan a una clasificación de la diabetes en dos grupos mayores: diabetes de tipo 1, o diabetes mellilus insulinodependiente (100M) , que surge con pacientes que carecen de células J3 que producen insulina en sus glándulas pancreáticas, y diabetes de tipo 2, o diabetes mellitus no insulinodependiente (NIDO M) , que aparece en pacientes con una función dañada de células J3 además de una gama de otras anomalías.
10005] Pacientes diabéticos de tipo 1 son habitualmente tratados con insulina, mientras la mayoría de pacientes diabéticos de tipo 2 se tratan bien con sulfonilureas que estimulan la función de las células J3 o con agentes que mejoran la sensibilidad de tejidos de los pacientes hacia insulina o con insulina. Entre los agentes aplicados para mejorar la sensibilidad de tejidos hacia la insulina la metformina es un ejemplo representativo.
10006] Aunque sulfonilureas son muy usadas en el tratamiento de NIDO M esta terapia es, en la mayoría de los casos, insatisfactoria: en un gran número de pacientes de NIDOM las sulfonilureas no bastan para nonnalizar los niveles de azúcar en sangre y los pacientes están, por lo tanto, en alto riesgo de contraer complicaciones diabéticas. También, muchos pacientes pierden gradualmente la capacidad para responder al tratamiento con sulfonilureas y por tanto están gradualmente forzados al tratamiento con insulina. Este cambio de los pacientes de agentes hipoglucémicos orales a terapia con insulina es nonnalmente asignado al agotamiento de células J3 en pacientes con NIDDM.
[0007) En sujetos normales al igual que en sujetos diabéticos, el hígado produce glucosa para evitar hipoglucemia. Esta producción de glucosa se deriva bien de la liberación de glucosa de los depósitos de glucógeno o de gluconeogénesis, que es una srntesis intracelular de novo de glucosa. En la diabetes de tipo 2, no obstante, la regulación del rendimiento de glucosa hepática es mal controlada y aumenta, y se puede duplicar después de un ayuno durante la noche. Por otra parte, en estos pacientes existe una correlación fuerte entre los niveles de glucosa en plasma en ayuno aumentados y el índice de producción de glucosa hepática. De forma similar, la producción de glucosa hepática será aumentada en la diabetes de tipo 1, si la enfermedad no es debidamente controlada por un tratamiento con insulina. Debido a que las formas existentes de terapia con diabetes no lleva a un control glucémico suficiente y por lo tanto son insatisfactorias, hay una gran demanda de métodos terapéuticos nuevos. La aterosclerosis, una enfennedad de las arterias, se reconoce como la causa avanzada de muerte en los Estados Unidos y Europa occidental. La secuencia patológica conduciendo a aterosclerosis y cardiopatía oclusiva es bien conocida. l a fase más temprana en esta secuencia es la formación de "estrías grasas" en la carótida, arterias cerebrales y coronarias y en la aorta. Estas lesiones son de color amarillo debido a la presencia de depósitos lipídicos encontrados principalmente dentro de las células del músculo liso y en macrófagos de la capa íntima de las arterias y aorta. Además, se postula que la mayor parte del colesterol encontrado en las estrias grasas, sucesivamente, darán lugar a desarrollo de la "placa fibrosa", que consiste en células acumuladas en el músculo liso interno cargadas con lipido y rodeadas por lípido extracelular, colágeno, elastina y proteoglicanos. Las células más la matriz fonnan un tapón fibroso que cubre un depósito más profundo de detrito celular y más lípKlo extracelular. El lípido es principalmente colesterol libre y esterificado. La placa fibrosa se forma lentamente, y es posible que con el tiempo se vuelva calcificada y necrótica, avanzando hasta una "lesión complicada" que representa la oclusión arterial y tendencia a trombosis mural y espasmo del músculo arterial que caracterizan la aterosclerosis avanzada. Pruebas epidemiológicas han establecido firmemente la hiperlipidemia como un factor de riesgo primario en causar enfennedad cardiovascular (eVD) debido a aterosclerosis. En los últimos años, líderes de la profesión médica han puesto énfasis renovado en reducir los niveles de colesterol en plasma, y colesterol de ipoproteína de baja densidad en particular, como una fase esencial en la prevención de evo. Los límites superiores "normales" son ahora conocidos por ser significativamente inferiores Que aquellos hasta ahora apreciados. Como resultado, segmentos grandes de poblaciones occidentales han demostrado estar ahora... [Seguir leyendo]
Reivindicaciones:
1. Compuesto que liene la fónnula:
donde R3 es seleccionado del grupo que consiste en fenoxi y benciloxi1cada uno de los cuales es opcionalmente sustituido con uno o más suslituyentes independientemente seleccionados de R 2;
R12
es F, CI, Br, -CF3, CN, metilo, etilo, isopropilo, tere-butilo, metoxi, metillio, etoxi, ciclopropil-metoxi, -NHC (O) CH3, o -
8\\>n-eH, ;
R es metilo, etilo, propilo, isopropilo, terc-butilo, ciclopropilo, ciclobutilo, ciclopenlilo, ciclohexilo, fenilo, metoxi, etoxi propoxi, butoxi, terc-butoxi, benciloxi, o ciclopropil-metoxi, cada uno de los cuales es opcionalmente sustituido con uno o más sustituyentes independientemente seleccionados de R 12;
Ae,
R8 es metillio, isopropiltio, etiltio, o 2-metilpropiltio, cada uno de los cuales se susutuye con uno o más su stituyentes independientemente seleccionados de Rl4 ; donde R34 es carboxi; o una sal derivada farmacéuticamente aceptable.
2. Compuesto según la Reivindicación 1, donde R'2 es F, CI, Sr, metilo, o etilo.
3. Compuesto según la Reivindicación 1, donde R30 es metilo °etilo.
4. Compuesto según la Reivindicación 1, donde el compuesto es: ácido 2-{2-¡3-12-{2-cloro-benciloxi) -etiij-3- ( 4-trans-melil-ciclohexil}-ureido }-tiazol-5-ilsulfanil}-2-meül-propiónico; o una sal derivada fannacéuticamente aceptable.
5. Compuesto según la Reivindicación 4, donde el compuesto es: ácido 2-{2 -[3-{2- (2 -cloro-benciloxi}-etil) -3- ( 4-trans-metil-ciclohexil) -u reido) -liazol-5-ilsulfanil}-2-meli I-propión ico.
6. Compuesto de la Reivindicación 1, donde el compuesto es:
ácido 2-{2-¡3-12- (2-f1uoro-benciloxi}-eIil) -3- (4-trans-metil-ciclohexil) -ure ido) -üazo 1-5-ilsulfanil) -2-melil-propiónico; o una sal derivada falTTlacéuticamente aceptable.
7. Compuesto según la Reivindicación 6, donde el compuesto es ácido 2-{2 - (3-{2- (2 -f1uoro-benciloxi}-etil) -3-.
4. trans-metil-ciclohexil) -ureido) -tiazol-5-ilsulfanil}-2-metil-propiónico.
8. Composición falTTlacéutica que comprende un compuesto según cualquiera de las reivindicaciones 1 a 7 y un portador farmacéuticamente aceptable.
9. Composición farmacéutica según la reivindicación 8, donde la composición está en una forma de dosificación unitaria que 40 comprende de aproximadamente 0, 05 mg a aproximadamente 1000 mg del compuesto.
10. Composición farmacéutica según la reivindicación 9, donde la forma de dosificación unitaria comprende de aproximadamente 0, 1 mg a aproximadamente 500 mg del compuesto.
11. Composición farmacéutica según la reivindicación la, donde la fonna de dosificación unitaria comprende de aproximadamente 0, 5 mg a aproximadamente 200 mg del compuesto.
12. Composición farmacéutica según la reivindicación 8, que comprende además una o más sustancias activas adicionales seleccionadas del grupo que consiste en agentes contra la diabetes, agentes antihiperlipidémicos, agentes antiobesidad, agentes anlihipertensivos, y agentes para el tratamiento de complicaciones que resultan de o asociadas a la diabetes.
13. Composición fannacéutica según la reivindicación 12, donde la sustancia activa adicional es metformina.
14. Compuesto según cualquiera de las reivindicaciones 1 a 7 para uso como medicamento.
15. Compuesto según cualquiera de las reivindicaciones 1 a 7 o composición fannacéutica según cualquiera de las reivindicaciones 8 a 13 para uso en el tratamiento de una indicación seleccionada del grupo que consiste en hiperglicemia, IGT, síndrome de resistencia a la insulina, síndrome X, diabetes de tipo 2, diabetes de tipo 1, dislipidemia, hipertensión, y obesidad.
16. Uso de un compuesto según cualquiera de las reivindicaciones 1 a 7 en la preparación de un medicamento para el tratamiento de una indicación seleccionada del grupo que consiste en hiperglicemia, IGT, síndrome de resistencia a la insulina, síndrome X, diabetes de tipo 2, diabetes de tipo 1, dislipidemia, hipertensión, y obesidad.
17. Uso según la reivindicación 16, donde el tratamiento comprende además administrar al menos una o más sustancias activas adicionales seleccionadas del grupo que consiste en agentes contra la diabetes, agentes antihiperlipidémicos, agentes antiobesidad, agentes antihipertensivos, y agentes para el tratamiento de complicaciones que resultan de o asociadas a la diabetes.
20. Ácido 2-{2-[3-[2- (2-f1uoro-benciloxi) -etil]-3- ( 4-trans-metil-ciclohexil) -ureido ) -tiazol-5-ilsulfanil}-2-metil-propiónico o una sal derivada falTTlacéuticamente aceptable para uso como un medicamento.
21. Ácido 2-{2 -[3-[2- (2-f1uoro-benciloxi) -etil]-3- ( 4-trans-metil-ciclohexil) -u reido]-tiazol-5-ilsulfanil}-2 -metil-propiónico o una sal derivada farmacéutica mente aceptable para uso en el tratamiento de una indicación seleccionada del grupo que consiste en hiperglicemia, IGT, síndrome de resistencia a la insulina, síndrome X, diabetes de tipo 2, diabetes de tipo 1, dislipidemia, hipertensión, y obesidad.
Patentes similares o relacionadas:
Inhibidores de btk de tipo nicotinimida sustituida y su preparación y uso en el tratamiento del cáncer, la inflamación y las enfermedades autoinmunitarias, del 15 de Julio de 2020, de Guangzhou InnoCare Pharma Tech Co., Ltd: Un compuesto seleccionado del grupo que consiste en: 6-(1-acriloilpiperidin-4-il)-2-(4-fenoxifenil)nicotinamida; **(Ver fórmula)** 6-(4-acriloilpiperazin-1-il)-2-(4-fenoxifenil)nicotinamida; […]
Inhibidores de lisina gingipaína, del 1 de Julio de 2020, de Cortexyme, Inc: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde Z es ariloximetil-carbonilo sustituido con halógeno; […]
Uso de principios activos refrescantes fisiológicos y agentes que contienen tales principios activos, del 17 de Junio de 2020, de Symrise AG: Procedimiento no terapéutico para la modulación in-vitro del receptor de mentol frío TRPM8, en el que se lleva a contacto el receptor con al menos un modulador, que se selecciona […]
Compuestos de tiazolida para tratar infecciones virales, del 10 de Junio de 2020, de ROMARK LABORATORIES, L.C.: Composición farmacéutica que comprende al menos uno de nitazoxanida o tizoxanida o sal farmacéuticamente aceptable de los mismos para su […]
Compuestos para el tratamiento del cáncer, del 3 de Junio de 2020, de Oncternal Therapeutics, Inc: Un compuesto representado por la fórmula II: **(Ver fórmula)** en donde Q es S, NH, u O; Z es CH o N; A es fenilo sustituido o no sustituido; indolilo […]
Inhibidores de la replicación del virus de la inmunodeficiencia humana, del 13 de Mayo de 2020, de VIIV Healthcare UK (No.5) Limited: Un compuesto de fórmula I, incluyendo las sales farmacéuticamente aceptables del mismo: **(Ver fórmula)** en la que: cada uno de R1a y R1b se selecciona independientemente […]
Un canal catiónico no selectivo en células neurales y compuestos que bloquean el canal para su uso en el tratamiento de la inflamación del cerebro, del 6 de Mayo de 2020, de UNIVERSITY OF MARYLAND, BALTIMORE: Un antagonista de SUR1 que bloquea el canal de NCCa-ATP para su uso en (a) la prevención o el tratamiento de la inflamación de las células neurales […]
Tratamiento combinado con un agonista de TLR7 y un inhibidor de ensamblaje de la cápside del VHB, del 15 de Abril de 2020, de F. HOFFMANN-LA ROCHE AG: Una composición farmacéutica que comprende un agonista de TLR7 y un inhibidor de ensamblaje de la cápside del VHB en un vehículo farmacéuticamente aceptable, en la que […]