Uso del PIG para el tratamiento de trastornos asociados a la transmisión sináptica desfuncional.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/007337.
Solicitante: UUTECH LIMITED.
Nacionalidad solicitante: Reino Unido.
Dirección: SCIENCE INNOVATION CENTRE UNIVERSITY OF ULSTER CROMORE ROAD COLERAINE, COUNTY LONDONDERRY REINO UNIDO.
Inventor/es: FLATT, PETER, RAYMOND, HOLSCHER,CHRISTIAN, GAULT,VICTOR ALAN.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K38/10 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos que tienen de 12 a 20 aminoácidos.
- A61K38/17 A61K 38/00 […] › que provienen de animales; que provienen de humanos.
- A61P25/14 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › para el tratamiento de movimientos anormales, p.ej. corea, disquinesia.
- A61P25/18 A61P 25/00 […] › Antipsicóticos, es decir, neurolépticos; Medicamentos para el tratamiento de la esquizofrenia o de las fobias.
- A61P25/28 A61P 25/00 […] › de los problemas neurodegenerativos del sistema nervioso central, p. ej. noótropos, activadores del conocimiento, medicamentos para el tratamiento del Alzheimer o de otras formas de demencia.
PDF original: ES-2389670_T3.pdf
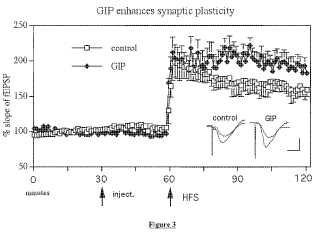
Fragmento de la descripción:
Uso del PIG para el tratamiento de trastornos asociados a la transmisión sináptica disfuncional
Antecedentes
El polipéptido inhibidor gástrico (PIG) es una hormona incretina de la familia de la secretina. Se denominó así porque originalmente se mostró que inhibía la secreción de ácidos gástricos inducida por histamina en bolsas gástricas de tipo Bickel caninas inervadas. Sin embargo, los estudios posteriores realizados para elucidar sus propiedades fisiológicas más amplias establecieron que las concentraciones fisiológicas del PIG eran capaces de estimular la secreción de insulina en las células beta pancreáticas. Por lo tanto, la hormona también se conoce como "polipéptido insulinotrópico dependiente de glucosa".
El PIG humano es un péptido de 42 aminoácidos derivado del procesamiento de un precursor de 153 aminoácidos, cuyo gen está localizado en el cromosoma 17 y abarca 10 kb. Las hormonas incretinas son liberadas en respuesta a la ingestión de nutrientes y actúan potenciando la respuesta de insulina inducida por glucosa. El PIG es liberado por las células K intestinales y su papel principal reside en modular la secreción de insulina dependiente de glucosa. El PIG también puede estimular la transcripción y traducción del gen de la proinsulina. Además, el PIG actúa como factor mitogénico sobre las células beta, potenciando el crecimiento, la diferenciación y la proliferación de las células beta pancreáticas. También se ha mostrado que el PIG inhibe la producción de glucosa hepática y estimula el transporte de glucosa, la síntesis de ácidos grasos y la actividad de la lipoproteína lipasa en los adipocitos.
El efecto insulinotrópico sobre los islotes pancreáticos y el efecto de reducir la glucosa en los tejidos periféricos convierte al PIG en un candidato atractivo como posible agente terapéutico para el tratamiento de la diabetes, la obesidad y los trastornos metabólicos relacionados.
La neuroplasticidad es un proceso que implica la continua formación de nuevas conexiones neuronales, que ocurre durante la (re) organización del cerebro en respuesta a la actividad y experiencia. La plasticidad sináptica dependiente de actividad desempeña un papel crucial en esculpir conexiones sinápticas durante el desarrollo. Sin embargo, aunque se sabe a ciencia cierta que ocurre durante el desarrollo, el proceso también constituye una característica central del cerebro adulto. La naturaleza plástica de las conexiones neuronales permite al cerebro desarrollarse continuamente en respuesta a experiencias y evitar la señalización neuronal deteriorada que se produce como consecuencia de un traumatismo o daño neuronal.
Existen dos tipos de modificaciones que se cree ocurren en el cerebro durante este proceso: 1) cambios morfológicos en las propias neuronas, específicamente en el área de las sinapsis; y 2) un aumento del número de sinapsis entre neuronas. La eficacia de la señalización sináptica depende a menudo de una (o ambas) de estas modificaciones. De hecho, está ampliamente aceptado que los procesos tales como la formación de memoria y la capacidad de aprendizaje dependen de alteraciones en la eficacia sináptica que permiten fortalecer las asociaciones entre neuronas. Además, se cree que la plasticidad sináptica de ciertas sinapsis es necesaria y suficiente para el proceso de almacenamiento de información en el cerebro.
La potenciación a largo plazo (PLP) se ha propuesto hace mucho tiempo como modelo para el mecanismo por medio del cual se puede lograr el fortalecimiento de las conexiones sinápticas. Se ha demostrado ampliamente que la estimulación de alta frecuencia puede provocar un incremento mantenido en la eficacia de la transmisión sináptica. En base a estos hallazgos, se cree que los cambios sinápticos que sustentan al menos ciertas formas de aprendizaje y memoria son similares a aquellos cambios necesarios para la expresión de la PLP.
Además, está ampliamente aceptado que una PLP deteriorada con frecuencia está asociada a una función cognitiva deteriorada. A este respecto, los estudios han descrito durante una serie de años deficiencias cognitivas en ratas viejas. En particular, se ha mostrado que las ratas viejas presentan deficiencias en el procesamiento de la información espacial. Se ha correlacionado una deficiencia en la PLP en la región CA1 del cerebro del roedor con deficiencias de rendimiento en el aprendizaje espacial; los animales deteriorados de forma grave no mantenían la PLP, mientras que se observó una PLP en aquellos animales cuyo aprendizaje espacial estaba relativamente poco deteriorado.
Por lo tanto, las deficiencias cognitivas constituyen un distintivo de una serie de trastornos neurológicos. Por ejemplo, los síntomas del deterioro de la memoria relacionado con la edad a menudo son similares a los síntomas asociados a las etapas tempranas de enfermedades neurodegenerativas, tales como la enfermedad de Alzheimer. Naturalmente, un objetivo primordial en el campo de la neurociencia consiste en mantener la PLP en circunstancias en las que la PLP está deteriorada, bien por causas asociadas a la edad o a enfermedades o bien por cualquier otro caso que conduzca a un deterioro de la transmisión sináptica.
Sin embargo, existen cada vez más evidencias de que las neuronas maduras también pueden poseer mecanismos para evitar el fortalecimiento de sinapsis entrantes. Tal regulación homeostática asegura que una neurona trabaja dentro de un intervalo de actividad óptimo, un proceso que es esencial para mantener la naturaleza altamente plástica del cerebro. Esto resulta evidente en el hipocampo, en el que las células piramidales de la región CA1 reciben cada una miles de entradas excitatorias con el potencial para una potenciación dependiente de actividad de la transmisión sináptica. En ausencia de un mecanismo para limitar el fortalecimiento sináptico puede quedar comprometido el equilibrio fisiológico, dando como resultado que el proceso de PLP cese y conduciendo, finalmente, a una reducción de la capacidad de todo el circuito neuronal para almacenar información. Por lo tanto, el proceso de despotenciación también actúa como mediador crítico en la regulación de la homeostasis neuronal y asegura el control coordinado de la fuerza de la transmisión sináptica. Actualmente se piensa que la despotenciación desempeña un papel en la eliminación de información redundante de la memoria. Como tal, la despotenciación podría actuar como posible medida terapéutica en trastornos asociados a procesos cognitivos hiperactivos.
Un objetivo de la presente invención es prevenir de forma profiláctica, mejorar o invertir la función cognitiva disminuida asociada a estos tipos de trastornos aumentando (o manteniendo) la PLP de la transmisión sináptica. Además, el mantenimiento de la PLP puede ser de utilidad en la profilaxis de enfermedades neurológicas retrasando el inicio del deterioro de procesos cognitivos, y podría servir como tratamiento no solo para la función cognitiva disminuida causada por neurodegeneración, sino también para los procesos cognitivos disfuncionales asociados a traumatismos o a la edad. Otro objetivo de la presente invención es mejorar la función cognitiva alterada asociada a trastornos de hiperexcitabilidad, reduciendo el alto nivel de la PLP de la transmisión sináptica.
Resumen de la invención
De acuerdo con un primer aspecto de la presente invención, se proporciona el uso de un péptido que comprende al menos 12 restos de aminoácido del extremo N-terminal del polipéptido inhibidor gástrico, o un análogo del mismo, para el tratamiento y la profilaxis de trastornos neurológicos que son causados por una disfunción de la potenciación a largo plazo de la transmisión sináptica o que están asociados a ella.
De acuerdo con un segundo aspecto de la presente invención, se proporciona el uso de un péptido que comprende al menos 12 restos de aminoácido del extremo N-terminal del polipéptido inhibidor gástrico, o un análogo del mismo, para la producción de un medicamento para el tratamiento y la profilaxis de trastornos neurológicos que son causados por una disfunción de la potenciación a largo plazo de la transmisión sináptica o que están asociados a ella.
De acuerdo con otro aspecto de la presente invención, se proporciona un procedimiento para el tratamiento de trastornos neurológicos que son causados por una disfunción de la potenciación a largo plazo de la transmisión sináptica o que están asociados a ella; en el que el procedimiento... [Seguir leyendo]
Reivindicaciones:
1. Un péptido que comprende al menos 12 restos de aminoácido del extremo N-terminal del polipéptido inhibidor gástrico o un análogo del mismo para el uso en el tratamiento y la profilaxis de trastornos neurológicos que son causados por una disfunción de la potenciación a largo plazo de la transmisión sináptica o que están asociados a ella.
2. Uso de un péptido que comprende al menos 12 restos de aminoácido del extremo N-terminal del polipéptido inhibidor gástrico o un análogo del mismo para la producción de un medicamento para el tratamiento y la profilaxis de trastornos neurológicos que son causados por una disfunción de la potenciación a largo plazo de la transmisión sináptica o que están asociados a ella.
3. Un péptido para el uso de acuerdo con la reivindicación 1, en el que el péptido comprende al menos 12 restos de aminoácido del extremo N-terminal de un polipéptido con la secuencia de aminoácidos mostrada en SEQ ID NO: 1 o un análogo del mismo.
4. Un análogo peptídico para el uso de acuerdo con la reivindicación 1 o 3, en el que el análogo peptídico comprende una o más sustituciones o modificaciones de aminoácidos seleccionadas del grupo formado por: una sustitución o modificación de aminoácidos en la posición 1; una sustitución o modificación de aminoácidos en la posición 2; una sustitución o modificación de aminoácidos en la posición 3; una modificación por unión de un resto polimérico de la fórmula general HO- (CH2-O-CH2) n-H; y una modificación por adición de radicales acilo, con la condición de que el análogo no sea Tyr (1) glucitol PIG (1-42) .
5. Un análogo peptídico para el uso de acuerdo con cualquiera de las reivindicaciones 1, 3 y 4, en el que el análogo peptídico comprende al menos una modificación de aminoácidos que comprende la unión de un resto polimérico de la fórmula general HO- (CH2-O-CH2) n-H, en la que n es un número entero entre 1 y aproximadamente 22; en el que, opcionalmente, el o cada resto polimérico está unido a los grupos amino alfa o épsilon de un resto de lisina elegido del grupo formado por Lys (16) , Lys (30) , Lys (32) , Lys (33) y Lys (37) .
6. Un análogo peptídico para el uso de acuerdo con cualquiera de las reivindicaciones 1 y 3 a 5, en el que el análogo peptídico comprende una modificación por adición de ácidos grasos a un grupo amino épsilon de al menos un resto de lisina elegido del grupo formado por Lys (16) , Lys (30) , Lys (32) , Lys (33) y Lys (37) ; en el que, opcionalmente, el ácido graso se selecciona del grupo que comprende, pero no se limita a, un grupo octanoílo C-8, un grupo decanoílo C-10, un grupo lauroílo C-12, un grupo miristoílo C-14, un grupo palmitoílo C-16, un grupo estearoílo C-18 o un grupo acilo C-20.
7. Un análogo peptídico para el uso de acuerdo con cualquiera de las reivindicaciones 1 y 3 a 6, en el que el análogo peptídico aumenta la PLP de la transmisión sináptica, comprendiendo el análogo peptídico:
(a) una glicación N-terminal y una sustitución de aminoácidos en la posición 2;
(b) una modificación de aminoácidos en la posición 1 y una sustitución de aminoácidos en la posición 2;
(c) una modificación de aminoácidos en la posición 1 o una sustitución de aminoácidos en la posición 2, con la condición de que el análogo no sea Tyr (1) glucitol PIG (1-42) , seleccionándose la sustitución o modificación de aminoácidos del grupo formado por:
i. glicación en la posición 1;
ii. alquilación en la posición 1;
iii. acetilación en la posición 1;
iv. acilación en la posición 1;
v. la adición de un grupo isopropilo en la posición 1;
vi. la adición de un ácido piroglutámico en la posición 1;
vii. sustitución en la posición 2 por un L-aminoácido, seleccionado opcionalmente entre prolina, lisina, serina y glicina;
viii. sustitución en la posición 2 por ácido aminoisobutírico o sarcosina;
ix. sustitución en la posición 2 por un D-aminoácido, tal como D-Ala (2) PIG;
x. conversión del enlace Ala (2) -Glu (3) en un enlace \[CH2NH];
xi. conversión del enlace Ala (2) -Glu (3) en un enlace isostérico estable; y
xii. sustitución en la posición 2 por beta-alanina, un omega-aminoácido, ácido 3-aminopropiónico, ácido 4-aminobutírico, ornitina, citrulina, homoarginina, t-butilalanina, t-butilglicina, N-metilisoleucina, fenilglicina y ciclohexilalanina, norleucina, ácido cisteico y sulfóxido de metionina;
(d) una modificación de aminoácido que comprende la unión de un resto polimérico de la fórmula general HO- (CH2-O-CH2) n-H; y
(e) una modificación por adición de radicales acilo, opcionalmente una adición de ácidos grasos, a un grupo amino épsilon de un resto de aminoácido.
8. Un análogo peptídico para el uso de acuerdo con la reivindicación 7, en el que existe una sustitución de aminoácidos en la posición 2 y una modificación de aminoácidos en la posición 1, y cada sustitución y/o modificación de aminoácidos se selecciona del grupo formado por:
i. glicación en la posición 1;
ii. alquilación en la posición 1;
iii. acetilación en la posición 1;
iv. acilación en la posición 1;
v. la adición de un grupo isopropilo en la posición 1;
vi. la adición de un ácido piroglutámico en la posición 1;
vii. sustitución en la posición 2 por un D-aminoácido;
viii. sustitución en la posición 2 por un L-aminoácido, seleccionado opcionalmente entre prolina, lisina, serina y glicina;
ix. sustitución en la posición 2 por ácido aminoisobutírico o sarcosina;
x. conversión del enlace Ala (2) -Glu (3) en un enlace \[CH2NH];
xi. conversión del enlace Ala (2) -Glu (3) en un enlace isostérico estable; y
xii. sustitución en la posición 2 por beta-alanina, un omega-aminoácido, ácido 3-aminopropiónico, ácido 4-aminobutírico, ornitina, citrulina, homoarginina, t-butilalanina, t-butilglicina, N-metilisoleucina, fenilglicina, ciclohexilalanina, norleucina, ácido cisteico y sulfóxido de metionina.
9. Un análogo peptídico para el uso de acuerdo con la reivindicación 7 u 8, en el que la modificación de aminoácidos en la posición 1 es una acetilación en la amina alfa N-terminal.
10. Un análogo peptídico para el uso de acuerdo con cualquiera de las reivindicaciones 7 a 9, en el que el análogo peptídico comprende al menos una sustitución o modificación de aminoácidos seleccionada entre: una modificación de aminoácidos en la posición 1; una sustitución de aminoácidos en la posición 2; y en el que el análogo peptídico comprende además la unión de un resto polimérico de la fórmula general HO- (CH2-O-CH2) n-H, en la que n es un número entero entre 1 y aproximadamente 22; y/o una modificación por adición de radicales acilo, opcionalmente una adición de ácidos grasos, a un grupo amino épsilon de un resto de aminoácido.
11. Un análogo peptídico para el uso de acuerdo con cualquiera de las reivindicaciones 1 y 3 a 6, en el que el análogo peptídico atenúa la PLP de la transmisión sináptica, comprendiendo el análogo peptídico:
(a) una sustitución de aminoácidos en cada una de las posiciones 1 y 3; y
(b) una sustitución de aminoácidos en una de las posiciones 1 y 3, seleccionándose la sustitución de aminoácidos del grupo formado por:
(i) sustitución en la posición 1 por un L-aminoácido, seleccionado opcionalmente entre prolina, lisina y serina;
(ii) sustitución en la posición 1 por un D-aminoácido;
(iii) sustitución en la posición 3 por un L-aminoácido, seleccionado opcionalmente entre prolina, lisina y serina;
(iv) sustitución en la posición 3 por ácido aminoisobutírico o sarcosina;
(v) sustitución en la posición 3 por un D-aminoácido;
(vi) conversión del enlace Ala (2) -Glu (3) en un enlace \[CH2NH];
(vii) conversión del enlace Ala (2) -Glu (3) en un enlace isostérico estable; y
(viii) sustitución en la posición 1 o 3 por beta-alanina, un omega-aminoácido, ácido 3-aminopropiónico, ácido 4-aminobutírico, ornitina, citrulina, homoarginina, t-butilalanina, t-butilglicina, N-metilisoleucina, fenilglicina y ciclohexilalanina, norleucina, ácido cisteico y sulfóxido de metionina.
12. Un análogo peptídico para el uso de acuerdo con la reivindicación 11, en el que existe una sustitución de aminoácidos en ambas posiciones 1 y 3, y cada sustitución de aminoácidos se selecciona del grupo formado por:
(a) sustitución en la posición 1 por un D-aminoácido;
(b) sustitución en la posición 1 por un L-aminoácido, seleccionado opcionalmente entre prolina, lisina y serina;
(c) sustitución en la posición 3 por un D-aminoácido;
(d) sustitución en la posición 3 por un L-aminoácido, seleccionado opcionalmente entre prolina, lisina y serina;
(e) sustitución en la posición 1 y/o 3 por ácido aminoisobutírico o sarcosina;
(f) conversión del enlace Ala (2) -Glu (3) en un enlace \[CH2NH];
(g) conversión del enlace Ala (2) -Glu (3) en un enlace isostérico estable; y
(h) sustitución en la posición 1 y/o 3 por beta-alanina, un omega-aminoácido, ácido 3-aminopropiónico, ácido 4-aminobutírico, ornitina, citrulina, homoarginina, t-butilalanina, t-butilglicina, N-metilisoleucina, fenilglicina y ciclohexilalanina, norleucina, ácido cisteico y sulfóxido de metionina.
13. Un análogo peptídico para el uso de acuerdo con la reivindicación 11 o 12, en el que el análogo peptídico comprende una sustitución de aminoácidos en una o ambas posiciones 1 y 3, y en el que el análogo peptídico comprende además una o ambas de la unión de un resto polimérico de la fórmula general HO- (CH2-O
CH2) n-H, en la que n es un número entero entre 1 y aproximadamente 22; y una modificación por adición de radicales acilo, opcionalmente una adición de ácidos grasos, a un grupo amino épsilon de un resto de aminoácido.
14. Un péptido o análogo peptídico para el uso de acuerdo con cualquiera de las reivindicaciones 1 y 3 a
13, en el que el trastorno neurológico comprende un trastorno seleccionado del grupo de trastornos que afectan a la función cognitiva, seleccionado opcionalmente entre demencia, ictus, esquizofrenia, trastorno bipolar, enfermedades neurodegenerativas tales como la enfermedad de Alzheimer (EA) , la enfermedad de Creutzfeld-Jacob (ECJ) , la enfermedad de Huntington y la enfermedad de Parkinson; trastorno por estrés postraumático, epilepsia, el síndrome de Tourette y alucinaciones; y procesos cognitivos disfuncionales, seleccionados opcionalmente entre atención,
cálculo, memoria, juicio, iluminación repentina, aprendizaje y razonamiento.
Patentes similares o relacionadas:
Tratamientos de combinación que comprenden imidazopirazinonas para el tratamiento de trastornos psiquiátricos y/o cognitivos, del 29 de Julio de 2020, de H. LUNDBECK A/S: Un compuesto de Fórmula (I) **(Ver fórmula)** en donde n es 0 o 1; q es 0 o 1; R1 se selecciona del grupo que consiste en bencilo, indanilo, indolina y heteroarilos […]
Composición farmacéutica que comprende un agente antipsicótico atípico y método para su preparación, del 15 de Julio de 2020, de PHARMATHEN S.A.: Comprimido de liberación controlada de Paliperidona en forma de comprimido de varias capas que comprende: a) un núcleo de matriz que comprende […]
Composición que comprende cinamaldehído y cinc, del 8 de Julio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Composición que comprende cinamaldehído y cinc para la utilización en la mejora de uno o más de rendimiento cognitivo, cognición, humor o memoria en un […]
Moduladores heteroaromáticos del receptor NMDA y usos de los mismos, del 24 de Junio de 2020, de Cadent Therapeutics, Inc: Un compuesto representado por la Fórmula I **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en el que: los anillos A y B son un sistema heteroaromático […]
Compuesto de tetrahidrooxepinopiridina, del 17 de Junio de 2020, de ASTELLAS PHARMA INC.: Compuesto de fórmula (I) o sal del mismo: **(Ver fórmula)** (en la fórmula, R1 es H o alquilo inferior, R2 es H o CN, uno cualquiera […]
Derivados de indolin-2-ona, del 27 de Mayo de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto de fórmula **(Ver fórmula)** en la que A es fenilo o un grupo heteroarilo de cinco o seis miembros, que contiene […]
Esteroides neuroactivos, composiciones y usos de los mismos, del 29 de Abril de 2020, de Sage Therapeutics, Inc: Un compuesto de la fórmula: **(Ver fórmula)** o sal farmacéuticamente aceptable del mismo.
Régimen de dosificación para dosis olvidadas para ésteres de paliperidona inyectables de acción prolongada, del 22 de Abril de 2020, de Janssen Pharmaceuticals, Inc: Un depósito de palmitato de paliperidona inyectable para su uso en el tratamiento de un paciente con necesidad de tratamiento psiquiátrico seleccionado […]