MOLÉCULAS DE ANTICUERPO FV DE CADENA SENCILLA BIESPECÍFICAS Y MÉTODOS DE USO DE LOS MISMOS.
Un anticuerpo biespecífico que comprende un primer anticuerpo y un segundo anticuerpo unidos entre sí,
en el que dicho primer anticuerpo tiene especificidad de unión por al menos un epítopo en HER2/neu y el segundo anticuerpo tiene especificidad de unión por un segundo epítopo en HER3 y en el que dicho primer anticuerpo comprende:
un dominio VH que comprende la secuencia de CDR1 de VH de C6B1D2 SYWIA, la secuencia de CDR2 de VH de C6B1D2 LIYPGDSDTKYSPSFQG, la secuencia de CDR3 de VH de C6B1D2 HDVGYCTDRTCAKWPEWLGV, la región flanqueante 1 de C6B1D2 que comprende la secuencia QVQLVQSGAEVKKPGESLKISCKGSGYSFT o QVQLLQSGAEVKKPGESLKISCKGSGYSFT, la región flanqueante 2 de C6B1D2 que comprende la secuencia WVRQMPGKGLEYMG, la región flanqueante 3 de C6B1D2 que comprende la secuencia QVTISVDKSVSTAYLQWSSLKPSDSAVYFCAR, y la región flanqueante 4 de CGB1D2 que comprende la secuencia WGQGTLVTVSS; y un dominio VL que comprende la secuencia de CDR1 de VL de C6B1D2 SGSSSNIGNNYVS, la secuencia de CDR2 de VL de C6B1D2 DHTNRPA, la secuencia de CDR3 de VL de C6B1D2 ASWDYTLSGWV, la región flanqueante 1 de C6B1D2 que comprende la secuencia QSVLTQPPSVSAAPGQKVTISC o ESVLTQPPSVSAAPGQKVTISC, la región flanqueante 2 de C6B1D2 que comprende la secuencia WYQQLPGTAPKLLIY, la región flanqueante 3 de C6B1D2 que comprende la secuencia GVPDRFSGSKSGTSASLAISGFRSEDEADYYC; y la región flanqueante 4 de C6B1D2, que comprende la secuencia FGGGTKVTVLG o FGGGTKLTVLG; y en el que además dicho segundo anticuerpo comprende las CDR del anticuerpo HER3.H3 (SEC ID Nº : 4) .
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/023479.
Solicitante: THE REGENTS OF THE UNIVERSITY OF CALIFORNIA.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1111 Franklin Street, 12th Floor Oakland, CA 94607-5200 ESTADOS UNIDOS DE AMERICA.
Inventor/es: MARKS,JAMES,D, ADAMS,Gregory P, HORAK,Eva M, WEINER,Louis M.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K39/395 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Anticuerpos (aglutininas A61K 38/36 ); Inmunoglobulinas; Inmunosuero, p. ej. suero antilinfocitario.
- C07K16/28 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra receptores, antígenos celulares de superficie o determinantes celulares de superficie.
- C07K16/32 C07K 16/00 […] › contra productos de traducción de oncogenes.
- C07K16/44 C07K 16/00 […] › contra material no previsto.
PDF original: ES-2377098_T3.pdf
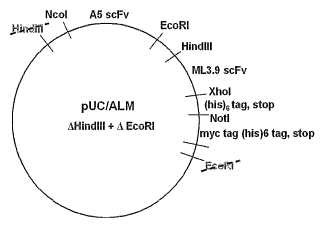
Fragmento de la descripción:
Moléculas de anticuerpo Fv de cadena sencilla biespecíficas y métodos de uso de las mismas [0001]
CAMPO DE LA INVENCIÓN
La presente invención se refiere a los campos de la inmunología y de la oncología y, más específicamente, a moléculas de anticuerpos biespecíficos (por ejemplo, bs scFv) que pueden usarse para aprovecharse en la detección y/o tratamiento de diversos cánceres que sobreexpresan la familia de proteínas del receptor del factor de crecimiento epidérmico (EGFR) . Ciertas moléculas de anticuerpos scFv biespecíficos ilustrativas de la invención tienen especificidades de unión por dos epítopos distintos de un solo miembro de la familia de EGFR o, como alternativa, especificidad por dos miembros distintos de la familia de EGFR.
ANTECEDENTES DE LA INVENCIÓN
La ruta de señalización del receptor del factor de crecimiento epidérmico (EGFR) desempeña un papel importante en el desarrollo y la propagación del cáncer por todo el cuerpo. El EGFR, también conocido como erb-bl, es un miembro de una familia de cuatro genes que también incluye a HER2/neu (erb-b2) , HER3 (erb-b3) y HER4 (erb-b4) . El EGFR se expresa en una amplia variedad de tumores sólidos, incluyendo cánceres de colon, cánceres de cabeza y cuello, cánceres pancreáticos, cánceres de ovario y cánceres de mama.
El HGER2/neu es una proteína receptora de superficie celular con actividad tirosina quinasa. La proteína completa consiste en tres partes: un dominio citoplasmático intracelular, un segmento transmembrana hidrófobo corto y un dominio extracelular (ECD) que es responsable de la unión a ligando. Esta proteína receptora se expresa en la membrana celular de una diversidad de tipos de células epiteliales y, a través de la unión de factores de crecimiento específicos, regula diversos aspectos de la división del crecimiento celular.
Her2/neu, el gen que codifica la proteína HER2/neu, es un miembro de un grupo de genes conocidos como protooncogenes. Los protooncogenes codifican proteínas importantes, tales como factores de crecimiento, receptores de factores de crecimiento y proteínas apoptóticas, que están implicadas en el crecimiento y la diferenciación celular normales. Cuando los protooncogenes se alteran por mutación puntual, translocación o amplificación génica, producen señales de crecimiento que pueden conducir a una transformación celular aberrante y al desarrollo de cáncer.
Aunque Her2/neu puede expresarse a bajos niveles en muchas células normales, típicamente está sobreexpresado en una diversidad de cánceres. La sobreexpresión de Her2/neu está causada en la mayoría de los casos por un aumento en el número de copias del gen (amplificación génica) y/o por un aumento en el nivel de expresión de los genes Her2/neu en la célula. La sobreexpresión de este receptor de factor de crecimiento desempeña un papel clave en la progresión tumoral, causando un mayor índice de crecimiento celular y transformación oncogénica. La amplificación génica del gen Her2/neu se ha observado en una diversidad de tipos de cáncer, incluyendo de mama, ovárico, endometrial, gástrico, pancreático, de próstata y glándula salival (Hynes y Stem (1994) Biochim Biophys Acta, 1198: 165-184) . En pacientes de cáncer de mama, HER2/neu también ha demostrado ser de importancia clínica ya que está asociado con un mal pronóstico, con el recidivado del tumor y con una supervivencia acortada en pacientes con cáncer de mama (Seshadri et al (1993) J Clin. Oncol., 11: 1936-1942; Berger et al (1988) Cancer Res., 48: 1238 1243; O'Reilly et al (1991) Br. J. Cancer, 63: 444-446) .
Actualmente, una gran cantidad de atención se ha centrado en el desarrollo de nuevas estrategias de inmunoterapia para el tratamiento del cáncer. Una estrategia de este tipo es la terapia del cáncer basada en anticuerpos. Un objetivo principal de la terapia del cáncer basada en anticuerpos es administrar específicamente cargas útiles tóxicas tales como radioisótopos, toxinas o fármacos a tumores. El intervalo de tamaño de las moléculas basadas en sitios de unión de anticuerpos incluye: IgM (1000 kDa) , IgG (150 kDa) , F (ab=) 2 (100 kDa) , Fab (50 kDa) , (scFv=) 2 (55 kDa) y scFv (25 kDa) . En ratones inmunodeficientes, moléculas de mayor tamaño tales como IgG y fragmentos F (ab=) 2 se retienen a altos niveles en xenoinjertos de tumores humanos con un bajo grado de especificidad (Adams et al (1992) , Antibody, Immimoconj. Radiopharm., 5: 81-95; Milenic et al (1991) J. Cancer Res. 51: 6363-6371) , mientras que moléculas de menor tamaño tales como scFv, (scFv=) 2 y Fab se retienen en tumores a niveles comparativamente inferiores con una especificidad enormemente mejorada (Milenic et al (1991) J. Cancer Res. 51: 6363-6371; Adams et al (1993) Cancer Res. 53: 4026-4034; Beaumier et al (1985) J Nuc/.Med. 26: 1172-1179; Colcher et al (1990) J. Natl. Cancer Inst. 82: 1191-1197) .
El determinante más destacado de las propiedades de direccionamiento anteriores es el tamaño de la molécula basada en anticuerpo respecto al umbral renal para el aclaramiento de primer paso. Otra característica importante de las moléculas basadas en anticuerpos es la valencia, ya que una retención tumoral significativamente mayor se ha asociado con una unión multivalente a antígeno a diana (Milenic et al (1991) J. Cancer Res. 51: 63636371; Adams et al (1993) Cancer Res. 53: 4026-4034; Adams et al (1996) Proc. Amer. Assoc. Cancer Res 37: 472; Wolf et al (1993) Cancer Res. 53: 2560-2565) .
La herceptina7, una nueva forma de inmunoterapia que se dirige al cáncer de mama, se ha desarrollado recientemente para dirigirse a células cancerosas que sobreexpresen Her2/neu. Se ha demostrado en ensayos clínicos que este tratamiento proporciona un tratamiento eficaz para pacientes con cáncer de mama metastásico positivo para HER2/neu. Sin embargo, este tratamiento farmacológico es costoso y está asociado con una morbilidad y mortalidad significativas.
Varios otros tipos de terapia han demostrado ser más o menos eficaces en pacientes con cáncer de mama cuyos tumores se expresan niveles elevados de Her2/neu . Estos incluyen terapia con antraciclinas, que se cree que es más eficaz en pacientes con una expresión de Her2/neu amplificada, y terapia hormonal, que es menos eficaz en pacientes cuyo nivel de expresión de Her2/neu es elevado.
La atención también se ha centrado en la generación de moléculas de anticuerpos basados en Fv de cadena sencilla bivalentes con pesos moleculares en el intervalo del umbral renal para el aclaramiento de primer paso. Éstas incluyen diacuerpos de 50 kDa (Holliger et al (1993) Proc. Natl. Acad. Sci. USA, 90: 6444-6448) , (scFv=) 2 de 55 kDa (Adams et al (1993) Cancer Res. 53: 4026-4034) , dímeros de scFv basados en hélices anfipáticas de 60-65 kDa (Pack et al (1993) Bio/Technology 11: 1271-1277; Pack (1992) Biochemistr y 31: 15791584) y minicuerpos (scFv-CH3) 2 LD de 80 kDa y minicuerpos Flex (Hu et al (1996) Cancer Res. 56: 3055-3061) . Aunque cada una de estas proteínas es capaz de unirse a dos moléculas de antígeno, difieren en la orientación, la flexibilidad y la extensión de sus sitios de unión. Se cree que estas nuevas e innovadoras inmunoterapias contribuirán a mejorar los resultados en el cáncer de mama y otros cánceres que, demasiado frecuentemente, recidivan o progresan a pesar de una terapia multimodalidad agresiva.
DESCRIPCIÓN RESUMIDA DE LA INVENCIÓN
Esta invención se refiere a la identificación de moléculas de anticuerpos biespecíficos (por ejemplo, bs scFv) que pueden usarse para aprovecharse en la detección y/o tratamiento de diversos cánceres que sobreexpresan la familia de proteínas del receptor del factor de crecimiento epidérmico (EGFR) . Por lo tanto, esta invención proporciona un anticuerpo biespecífico que comprende un primer anticuerpo y un segundo anticuerpo unidos entre sí, en el que dicho primer anticuerpo tiene especificidad de unión por al menos un epítopo en HER2/neu y el segundo anticuerpo tiene especificidad de unión por un segundo epítopo en HER3, y en el que dicho primer anticuerpo comprende:
un dominio VH que comprende la secuencia de CDR1 de VH de C6B1D2 SYWIA, la secuencia de CDR2 de VH de C6B1D2 LIYPGDSDTKYSPSFQG, la secuencia de CDR3 de VH de C6B1D2 HDVGYCTDRTCAKWPEWLGV, la región flanqueante 1 de C6B1D2, que comprende la secuencia QVQLVQSGAEVKKPGESLKISCKGSGYSFT o QVQLLQSGAEVKKPGESLKISCKGSGYSFT, la región flanqueante 2 de C6B1D2, que comprende la secuencia WVRQMPGKGLEYMG, la región flanqueante 3 de C6B1D2, que comprende la secuencia QVTISVDKSVSTAYLQWSSLKPSDSAVYFCAR,... [Seguir leyendo]
Reivindicaciones:
1. Un anticuerpo biespecífico que comprende un primer anticuerpo y un segundo anticuerpo unidos entre sí, en el que dicho primer anticuerpo tiene especificidad de unión por al menos un epítopo en HER2/neu y el segundo anticuerpo tiene especificidad de unión por un segundo epítopo en HER3 y en el que dicho primer anticuerpo comprende:
un dominio VH que comprende la secuencia de CDR1 de VH de C6B1D2 SYWIA, la secuencia de CDR2 de VH de C6B1D2 LIYPGDSDTKYSPSFQG, la secuencia de CDR3 de VH de C6B1D2 HDVGYCTDRTCAKWPEWLGV, la región flanqueante 1 de C6B1D2 que comprende la secuencia QVQLVQSGAEVKKPGESLKISCKGSGYSFT o QVQLLQSGAEVKKPGESLKISCKGSGYSFT, la región flanqueante 2 de C6B1D2 que comprende la secuencia WVRQMPGKGLEYMG, la región flanqueante 3 de C6B1D2 que comprende la secuencia QVTISVDKSVSTAYLQWSSLKPSDSAVYFCAR, y la región flanqueante 4 de CGB1D2 que comprende la secuencia WGQGTLVTVSS; y un dominio VL que comprende la secuencia de CDR1 de VL de C6B1D2 SGSSSNIGNNYVS, la secuencia de CDR2 de VL de C6B1D2 DHTNRPA, la secuencia de CDR3 de VL de C6B1D2 ASWDYTLSGWV, la región flanqueante 1 de C6B1D2 que comprende la secuencia QSVLTQPPSVSAAPGQKVTISC o ESVLTQPPSVSAAPGQKVTISC, la región flanqueante 2 de C6B1D2 que comprende la secuencia WYQQLPGTAPKLLIY, la región flanqueante 3 de C6B1D2 que comprende la secuencia GVPDRFSGSKSGTSASLAISGFRSEDEADYYC; y la región flanqueante 4 de C6B1D2, que comprende la secuencia FGGGTKVTVLG o FGGGTKLTVLG; y en el que además dicho segundo anticuerpo comprende las CDR del anticuerpo HER3.H3 (SEC ID Nº : 4) .
2. El anticuerpo biespecífico de acuerdo con la reivindicación 1, en el que dicho primer anticuerpo es un Fv de cadena sencilla y dicho segundo anticuerpo es un Fv de cadena sencilla.
3. El anticuerpo biespecífico de la reivindicación 2, en el que dicho primer anticuerpo se une a un segundo anticuerpo por un polipéptido que tiene la secuencia de aminoácidos de SEC ID Nº : 37.
4. El anticuerpo biespecífico de acuerdo con cualquiera de las reivindicaciones 1-3, en el que dicho anticuerpo biespecífico está en un portador farmacéuticamente aceptable.
5. El anticuerpo biespecífico de acuerdo con cualquiera de las reivindicaciones 1-4, para su uso en terapia.
6. El anticuerpo biespecífico de acuerdo con cualquiera de las reivindicaciones 1-5, para su uso en el tratamiento del cáncer.
7. El uso de un anticuerpo biespecífico de acuerdo con cualquiera de las reivindicaciones 1-6, para la fabricación de un medicamento para el tratamiento del cáncer.
8. El anticuerpo biespecífico de la reivindicación 6, o el uso de la reivindicación 7, en el que dicho cáncer se selecciona del grupo que consiste en cáncer de mama, colon, ovario, endometrial, gástrico, pancreático, próstata y glándula salival.
9. El anticuerpo biespecífico de acuerdo con cualquiera de las reivindicaciones 1-6, para su uso para inhibir específicamente el crecimiento y/o proliferación de una célula cancerosa que lleva un receptor HER2/neu y un receptor HER3.
10. Uso de un anticuerpo biespecífico de acuerdo con cualquiera de las reivindicaciones 1-6 en la fabricación de un medicamento para inhibir específicamente el crecimiento y/o proliferación de una célula cancerosa que lleva un receptor HER2/neu y un receptor HER3.
11. El anticuerpo biespecífico de acuerdo con cualquiera de las reivindicaciones 5, 6 u 8, o el uso de acuerdo con cualquiera de las reivindicaciones 7, 8 ó 10, en el que el uso es en el tratamiento del cáncer y el anticuerpo biespecífico o medicamento se administra a un paciente en combinación con otro agente citotóxico seleccionado del grupo que consiste en un agente quimioterápico, radiación de haz externo, un radioisótopo dirigido y un inhibidor de la transducción de señal.
12. El anticuerpo biespecífico de acuerdo con cualquiera de las reivindicaciones 1-6, en el que un anticuerpo que comprende dicho anticuerpo biespecífico se une a un marcador detectable, para su uso en un método de detección de una célula o tejido que expresa uno o más miembros de la familia del receptor del factor de crecimiento epidérmico, comprendiendo el método
poner en contacto una célula o tejido con el anticuerpo biespecífico unido a un marcador; y detectar dicho marcador, en el que la detección de dicho marcador en asociación con dicha célula o tejido indica la presencia de una célula o tejido que expresa uno o más miembros de la familia de proteínas del receptor del factor de crecimiento epidérmico.
13. El anticuerpo biespecífico de la reivindicación 12, en el que dicho marcador detectable se selecciona del grupo que consiste en un emisor de gamma, un emisor de positrones, un marcador de MRI y un marcador fluorescente. 5
14. El anticuerpo biespecífico de la reivindicación 12 ó 13, en el que dicha célula o tejido es una célula o tejido canceroso.
15. El anticuerpo biespecífico de la reivindicación 14, en el que la célula o tejido es una célula o tejido canceroso
seleccionado del grupo que consiste en cáncer de mama, colon, ovario, endometrial, gástrico, pancreático, próstata y glándula salival.
16. Un vector que comprende una secuencia de ácido nucleico que codifica el anticuerpo biespecífico de acuerdo con la reivindicación 2. 15
17. El vector de la reivindicación 16, que se selecciona del grupo que consiste en un plásmido, cósmido, fago y virus.
18. Una célula hospedadora transformada con el vector de la reivindicación 16 ó 17.
REFERENCIAS CITADAS EN LA DESCRIPCIÓN
Esta lista de referencias citadas por el solicitante es únicamente para la comodidad del lector. No forma parte del documento de la patente europea. A pesar del cuidado tenido en la recopilación de las referencias, no se pueden excluir errores u omisiones y la EPO niega toda responsabilidad en este sentido.
Documentos de patentes citados en la descripción
Literatura diferente de patentes citadas en la descripción
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Anticuerpos anti-alfa-sinucleína y procedimientos de uso, del 29 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un anticuerpo anti-alfa-sinucleína humana que comprende (a) HVR-H1 que comprende la secuencia de aminoácidos de SEQ ID NO: 21; (b) HVR-H2 que […]
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Métodos y composiciones para tratar y prevenir enfermedades asociadas con la integrina AVB8, del 29 de Julio de 2020, de THE REGENTS OF THE UNIVERSITY OF CALIFORNIA: Un anticuerpo aislado que se une específicamente a la integrina β8 humana e inhibe la adhesión del péptido asociado a latencia (LAP) a ανβ8, en donde el […]
Anticuerpos anti-PD-L1 y usos de los mismos, del 22 de Julio de 2020, de MERCK PATENT GMBH: Un anticuerpo anti-PD-L1 aislado o su fragmento de union a antigeno que comprende una secuencia de region variable de cadena pesada y de cadena ligera, en donde: […]
Utilización de anticuerpos optimizados en ADCC para tratar a los pacientes con bajo nivel de respuesta, del 22 de Julio de 2020, de LABORATOIRE FRANCAIS DU FRACTIONNEMENT ET DES BIOTECHNOLOGIES: Utilización de una composición de anticuerpo monoclonal quimérico, humanizado o humano de isotipo IgG1 anti- Rhesus del glóbulo rojo humano cuya […]
Proteínas de unión al antígeno ST2, del 22 de Julio de 2020, de AMGEN INC.: Un anticuerpo aislado que se une a un antígeno ST2 que tiene la secuencia de aminoácidos 19-556 del SEQ ID NO: 1, comprendiendo dicho anticuerpo una secuencia de […]
Método para producir inmunoconjugados de anticuerpo-SN-38 con un enlazador CL2A, del 22 de Julio de 2020, de IMMUNOMEDICS, INC.: Un método para producir un compuesto, CL2A-SN-38, que presenta la estructura, **(Ver fórmula)** que comprende realizar un esquema de reacción como el que se muestra: **(Ver […]