Procedimiento para la producción de 1-formamido-3,5-dimetiladamantano.
Procedimiento para la producción de 1-formamido-3, 5-dimetiladamantano mediante la formamidación directa de 1,
3-dimetiladamantano, caracterizado porque se hace reaccionar el 1, 3-dimetiladamantano con formamida en ácidios concentrados, pero evitando ácido sulfúrico que contiene SO3 o ácido nítrico al 100%, utilizándose como ácidos concentrados ácido nítrico al 30-70% y ácido sulfúrico al 90-100%.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2007/001433.
Solicitante: MERZ PHARMA GMBH & CO. KGAA.
Nacionalidad solicitante: Alemania.
Dirección: ECKENHEIMER LANDSTRASSE 100 60318 FRANKFURT ALEMANIA.
Inventor/es: SCHREINER,PETER R, FOKIN,ANDREY A, WANKA,LUKAS, WOLFE,DEREK M.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C231/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › C07C 231/00 Preparación de amidas de ácidos carboxílicos. › a partir de amidas por reacción sobre los átomos de nitrógeno de grupos carboxamido.
- C07C233/03 C07C […] › C07C 233/00 Amidas de ácidos carboxílicos. › con átomos de carbono de grupos carboxamido unidos a átomos de hidrógeno.
PDF original: ES-2392550_T3.pdf
Descripción:
Procedimiento para la producción de 1-formamido-3, 5-dimetiladamantano
El objeto de la invención es un procedimiento para la producción de 1-formamido-3, 5-dimetiladamantano, que es un producto intermedio importante para la producción del 1-amino-3, 5-dimetiladamantano usado contra la enfermedad de Alzheimer, que se conoce con el nombre de principio activo memantina. Se comercializa en Europa (y numerosos países extraeuropeos) bajo las marcas Axura® y Ebixa® y en los EE.UU. bajo Namenda®.
La preparación del 1-formamido-3, 5-dimetiladamantano a partir de 1-bromo-3, 5-dimetiladamantano y formamida ya se conoce en sí (documento CN 155 60 75) .
El 1-amino-3, 5-dimetiladamantano se conoce como sustancia ya desde hace tiempo por el documento DE 2 318 461 A1. Su uso para la prevención y el tratamiento de la isquemia cerebral se describe en el documento EP 0 392 059
B1. La síntesis del 1-formamido-3, 5-dimetiladamantano usado para su obtención tiene lugar por tanto hasta la fecha mediante una halogenación del 1, 3-dimetiladamantano con una formamidación posterior. Después se hidroliza el 1formamido-3, 5-dimetiladamantano con ácido clorhídrico diluido para dar una amina.
Sin embargo, este procedimiento de síntesis requiere tres etapas de síntesis para llegar del 1, 3-dimetiladamantano a
la memantina: halogenación, formamidación e hidrólisis ácida. A este respecto es necesaria la utilización de cloro o bromo elemental tóxico en exceso; esto provoca costes adicionales en la eliminación de desechos y puede conducir a productos secundarios no deseados.
Se planteaba por tanto el objetivo de proporcionar un procedimiento para la formamidación del 1, 325 dimetiladamantano, que fuera más sencillo y pudiera realizarse con reactivos menos tóxicos o caros.
En la solicitud de patente internacional WO2006/010362 A1 ya se describe un procedimiento para la producción de derivados de 1-aminoadamantano 3, 5-sustituidos, en el que se suspende un derivado de adamantano 1, 3disustituido en HNO3 y H2SO4, y tras la adición de óleum se hace reaccionar con un nitrilo. Por el contrario, en el 30 procedimiento según la invención tiene lugar la producción de 1-formamido-3, 5-dimetiladamantano en sólo dos etapas de reacción mediante la formamidación directa de 1, 3-dimetiladamantano con formamida en ácidos concentrados, utilizándose como ácidos concentrados ácido nítrico al 30-70%, en particular al 65%, y ácido sulfúrico al 90-100%, pero sobre todo al 95-98%. La reacción tiene lugar en general a de -40ºC a 50ºC, sin embargo preferiblemente a 0ºC. En el procedimiento según la invención se consiguen en la mayoría de los casos
rendimientos del 40-95%.
Este procedimiento se caracteriza no sólo por su ausencia de halógenos, sino que en la mayoría de los casos presenta también un perfil de impurezas más favorable, puesto que transcurre con rendimientos elevados y con un porcentaje sólo reducido de productos secundarios y a este respecto tolera incluso impurezas en los materiales de
partida. Según CG-EM, en la formamidación pudieron detectarse como productos secundarios sólo educto sin reaccionar así como 3, 5-dimetiladamantan-1-ol.
Incluso es posible una producción in situ del material de partida a partir de precursores baratos, de modo que el producto final deseado puede obtener en un procedimiento “en un solo recipiente”. A este respecto, el 1, 3
45 dimetiladamantano que debe hacerse reaccionar con formamida se obtiene in situ a partir de un hidrocarburo de fórmula elemental C12H20 mediante transposición catiónica en condiciones de reacción comparables, como las que se emplearían también para la formamidación. Los precursores se obtienen por ejemplo mediante la perhidrogenación de acenafteno, acenaftaleno o dímero de metilciclopentadieno. A continuación se realiza en el mismo recipiente de reacción la formamidación del dimetiladamantano generado en condiciones ácidas.
50 El tratamiento de dímero de metilciclopentadieno perhidrogenado con ácidos concentrados posibilita la preparación del material de partida 1, 3-dimetiladamantano in situ antes de la formamidación según la siguiente reacción:
El procedimiento descrito en la solicitud internacional WO 2006/020362 A1 se basa en la generación de carbocationes en ácidos concentrados, que se captan por un nucleófilo, tal como por ejemplo un nitrilo, y que con un reacondicionamiento acuoso se transforman en los derivados de 1-amidoadamantano correspondientes según la
2
siguiente reacción:
Por el contrario, el procedimiento según la invención para la síntesis de 1-formamido-3, 5-dimetiladamantano permite condiciones de reacción más suaves evitando completamente el empleo de óleum o ácido nítrico al 100%. Además, como nucleófilo se usa formamida, generándose como producto de reacción 1-formamido-3, 5-dimetiladamantano, que con respecto a otras amidas puede hidrolizarse en condiciones claramente más suaves. Así, por ejemplo, se desdobla 1-acetamido-3, 5-dimetiladamantano mediante el calentamiento durante varias horas de NaOH en una base acuosa o alcohólica o ácido clorhídrico concentrado (al 36-37%) para dar 1-amino-3, 5-dimetiladamantano libre, mientras que el desdoblamiento de la formamida se consigue con ácido clorhídrico diluido ya en el plazo de dos horas a 100ºC.
La invención se explica más detalladamente mediante los siguientes ejemplos:
Ejemplo 1 – Preparación de 1-formamido-3, 5-dimetiladamantano
A 6, 572 g (40 mmol) de 1, 3-dimetiladamantano se le añaden a 0ºC sucesivamente 4 ml de ácido nítrico comercial al 65% y después de ello en el plazo de tres horas 50 ml de ácido sulfúrico comercial al 98%. Se agita durante la noche a 0ºC y se vierte la mezcla a 0ºC en 100 ml de formamida en un matraz de fondo redondo, que se dota de un tubo secador. Se agita adicionalmente esta mezcla durante 30 minutos a 0ºC y durante 90 minutos a temperatura ambiente y se le añaden 200 ml de diclorometano y 200 ml de agua. Tras la separación de las fases se lava la fase orgánica con agua y disolución de NaHCO3 al 2%, se seca con Na2SO4 y se libera de disolventes en un evaporador rotatorio. Se purifica cromatográficamente el aceite restante (SiO2, CHCl3/acetona (20:1) , Rf = 0, 39) . Se obtienen 7, 41 g (89, 3%) de la formamida como sólido prácticamente incoloro.
1H-RMN (CDCl3, TMS, 400, 13 MHz) : 8 = 0, 87 ppm, s, 6 H; 1, 15 ppm, s, 2 H; 1, 2 - 1, 35 ppm, m, 4 H; 1, 35 - 1, 55 ppm, m, 4 H; 1, 65 - 1, 78 ppm, m, 2 H; 2, 10 - 2, 27 ppm, m 1H; 5, 90 y 7, 21 ppm; en cada caso s a, 1H; 8, 02, 8, 20 y 8, 27 ppm, en cada caso s, 1H.
13C-RMN (CDCl3, TMS, 100, 61 MHz) : 8 = 29, 46, 30, 01, 32, 00, 40, 21, 41, 85, 47, 63, 49, 94, 51, 83, 160, 15/162, 24 ppm. EM: m/z = 207 (M+) , 192, 150, 136, 106, 91, 79.
Ejemplo 2 – Hidrólisis del 1-formamido-3, 5-dimetiladamantano para dar clorhidrato de 1-amino-3, 5dimetiladamantano (memantina)
Se calientan 0, 02 mmol de 1-formamido-3, 5-dimetiladamantano (4, 14 g) en 100 ml de ácido clorhídrico al 15% durante 24 horas hasta reflujo. Tras el enfriamiento se separa mediante filtración el sedimento, se disuelve en metanol y se hace precipitar mediante la adición de éster etílico del ácido acético (rendimiento del 80%) .
3
Reivindicaciones:
1. Procedimiento para la producción de 1-formamido-3, 5-dimetiladamantano mediante la formamidación directa de 1, 3-dimetiladamantano, caracterizado porque se hace reaccionar el 1, 3-dimetiladamantano con formamida en ácidos
concentrados, pero evitando ácido sulfúrico que contiene SO3 o ácido nítrico al 100%, utilizándose como ácidos concentrados ácido nítrico a.
3. 70% y ácido sulfúrico a.
9. 100%.
2. Procedimiento según la reivindicación 1, caracterizado porque se produce el 1, 3-dimetiladamantano antes de la
formamidación directa a partir de un precursor hidrocarbonado de fórmula elemental C12H20 mediante transposición 10 catiónica en una reacción separada o in situ.
3. Procedimiento según las reivindicaciones 1 y 2, caracterizado porque se transforma el 1-formamido-3, 5dimetiladamantano mediante hidrólisis en el 1-amino-3, 5-dimetiladamantano.
4. Procedimiento según la reivindicación 3, caracterizado porque la hidrólisis tiene lugar con ácido clorhídrico acuoso.
4
Patentes similares o relacionadas:
Compuestos útiles como inmunomoduladores, del 13 de Julio de 2016, de BRISTOL-MYERS SQUIBB COMPANY: Un compuesto de Fórmula (I):**Fórmula** o sales del mismo, en la que: el Anillo B es fenilo o tienilo; el Anillo A es:**Fórmula** […]
Proceso para fabricar derivados de adamantano con alto rendimiento, del 27 de Enero de 2016, de MERZ PHARMA GMBH & CO. KGAA: Proceso para la amidación de un 1-bromo-adamantano sustituido que comprende una etapa de hacer reaccionar un adamantano sustituido con un exceso de bromo para […]
Procedimiento para la preparación de formamidas aromáticas, del 6 de Agosto de 2014, de BASF SE: Procedimiento para la preparación de formamidas mediante reacción de aminas aromáticas con un éster del ácido fórmico en presencia de un catalizador, […]
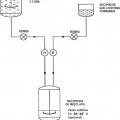 Proceso para la fabricación de Memantina y producto intermedio, del 9 de Julio de 2014, de MERZ PHARMA GMBH & CO. KGAA: Un proceso para la fabricación de N-Formil-1-amino-3,5-dimetiladamantano que comprende las siguientes etapas:
(a) hacer reaccionar 1,3-dimetiladamantano […]
Proceso para la fabricación de Memantina y producto intermedio, del 9 de Julio de 2014, de MERZ PHARMA GMBH & CO. KGAA: Un proceso para la fabricación de N-Formil-1-amino-3,5-dimetiladamantano que comprende las siguientes etapas:
(a) hacer reaccionar 1,3-dimetiladamantano […]
COMPUESTOS DE ACIDO CARBONICO QUE COMPRENDEN UN ENLACE AMINO COMO INHIBIDORES HDAC., del 1 de Agosto de 2006, de PROLIFIX LIMITED: Compuesto de fórmula (I) en la que: A es un grupo arilo: Q1 es un grupo arilo principal que tiene un esqueleto de por lo menos dos átomos de carbono; J es un enlace […]
FORMAMIDAS N,N-DISUSTITUIDAS COMO CATALIZADORES DE HALOGENACION., del 1 de Diciembre de 2004, de ROHM AND HAAS COMPANY: FORMAMIDAS N,N-DISUSTITUIDAS DE LA FORMULA: EN LA QUE R SUP,1} Y R{SUP,1} SE SELECCIONAN INDEPENDIENTEMENTE DEL: A. ALKILO C{SUB,5}-C{SUB,30} SUSTITUIDO O NO SUSTITUIDO, […]
PROCESO PARA LA ELABORACION DE N - AMIDAS DE ACIDO CARBOXILICO ALQUENILO, del 16 de Junio de 1998, de BASF AKTIENGESELLSCHAFT: ELABORACION DE N - AMIDAS DE ACIDO CARBOXILICO ALQUENILO DE LA FORMULA GENERAL I DONDE AL MENOS UNO DE LOS RESTOS R{SUP, 1} SIGNIFICA HIDROGENO, EL SEGUNDO […]
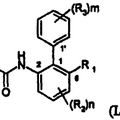 DERIVADOS DE BIFENILO Y SU USO COMO FUNGICIDAS, del 1 de Noviembre de 2008, de SYNGENTA PARTICIPATIONS AG: Un compuesto de fórmula (I) (Ver fórmula) en la que Het es un anillo pirazol, pirrol o tiazol, estando el anillo substituido con uno, dos o tres grupos R y […]
DERIVADOS DE BIFENILO Y SU USO COMO FUNGICIDAS, del 1 de Noviembre de 2008, de SYNGENTA PARTICIPATIONS AG: Un compuesto de fórmula (I) (Ver fórmula) en la que Het es un anillo pirazol, pirrol o tiazol, estando el anillo substituido con uno, dos o tres grupos R y […]