Formulación de fármaco de moléculas pequeñas de liberación prolongada.
Una formulación de liberación prolongada inyectable, que comprende:
un polímero biocompatible que es un copolímero basado en ácido láctico y ácido glicólico que tiene unarelación monomérica de ácido láctico y ácido glicólico en el intervalo de 60:40 a 75:25;
un disolvente orgánico combinado con el polímero biocompatible para formar un gel viscoso, seleccionándoseel disolvente de alcohol bencílico, bencil benzoato, etil benzoato, hidróxido de etilo, triacetina, N-metil-2-pirrolidona y mezclas de los mismos; y
un fármaco de moléculas pequeñas seleccionado a partir de formas básicas y salinas de risperidonaincorporada en el gel viscoso de modo que la formulación muestre un perfil de liberación in vivo que tienerelación de Cmax y Cmin menor de 200 y desfase temporal menor de 0,2.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/038268.
Solicitante: DURECT CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 10260 Bubb Road Cupertino, CA 95014 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CHEN, GUOHUA, LUK,Andrew S, JUNNARKAR,Gunjan H.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K9/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales caracterizadas por un aspecto particular.
PDF original: ES-2385384_T3.pdf
Fragmento de la descripción:
Formulación de fármaco de moléculas pequeñas de liberación prolongada
5 Antecedentes de la invención
La invención se refiere en general al suministro de fármacos de moléculas pequeñas.
El término “fármaco de moléculas pequeñas”, como se usa en este documento, se refiere a agentes beneficiosos que tienen bajo peso molecular. Los agentes beneficiosos se sintetizan habitualmente por química orgánica, pero también pueden aislarse de fuentes naturales tales como plantas, hongos y microbios. Las vías habituales para suministrar fármacos de moléculas pequeñas son oral, inyección, pulmonar y transdérmica.
Muchos fármacos psicoterapéuticos son fármacos de moléculas pequeñas y se proporcionan habitualmente como píldoras orales o inyecciones de embolada que pueden suministrarse una o más veces al día. Sin embargo, las píldoras orales e inyecciones de embolada pueden no ser vías óptimas para administrar fármacos psicoterapéuticos de moléculas pequeñas debido a los picos y depresiones observados en la concentración en plasma después de la dosificación. Se han asociado efectos adversos y pérdida de efecto terapéutico con los picos y depresiones de la concentración en plasma, respectivamente.
A partir de lo anterior, la psicoterapia así como otras formas de terapia que actualmente se basan en fármacos de moléculas pequeñas administrados en forma de píldoras orales e inyecciones de embolada pueden beneficiarse de una forma de dosificación de liberación prolongada diseñada para minimizar las variaciones en la concentración en plasma después de la dosificación. La administración de agentes psicoterapéuticos como formulaciones de liberación prolongada también aumentará la conformidad de los pacientes.
El documento WO 2005/048989 describe composiciones de gel de depósito inyectable y kits que proporcionan un excipiente para modular una velocidad de liberación y estabilizar agentes beneficiosos. El documento WO 00/24374 describe una composición polimérica controlada que incluye un polímero o copolímero de base, un disolvente orgánico, un aditivo de liberación controlada polimérico y un agente biológicamente activo. El aditivo de liberación controlada polimérico reduce la ráfaga inicial de agente biológicamente activo liberado de la composición polimérica a medida que se solidifica para formar el implante sólido. El aditivo de liberación controlada es preferiblemente un copolímero en bloque de poli (lactida-coglicolida) /polietilenglicol.
35 Breve sumario de la invención
En un aspecto, la invención se refiere a una formulación de liberación prolongada inyectable que comprende un polímero biocompatible, un disolvente orgánico combinado con el polímero biocompatible para formar un gel viscoso y un fármaco de moléculas pequeñas incorporado en el gel viscoso de modo que la formulación muestre un perfil de liberación in vivo que tiene relación de Cmax yCmin menor de 200 y desfase temporal menor de 0, 2.
El polímero biocompatible es un copolímero basado en ácido láctico y ácido glicólico con una relación de 60:40 a 75:25.
45 El disolvente orgánico se selecciona de alcohol bencílico, bencil benzoato, etil benzoato, hidróxido de etilo, triacetina, N-metil-2-pirrolidona y mezclas de los mismos. El fármaco de moléculas pequeñas se selecciona de formas básicas y salinas de risperidona.
En otro aspecto, la invención se refiere a un uso para tratamiento del cuerpo humano o animal administrando este 50 fármaco de moléculas pequeñas a un sujeto de una manera controlada que comprende implantar en el sujeto una cantidad eficaz de una formulación de liberación prolongada inyectable que comprende el polímero biocompatible descrito, el disolvente orgánico descrito combinado con el polímero biocompatible para formar un gel viscoso y el fármaco de moléculas pequeñas incorporado en el gel viscoso de modo que la formulación muestre un perfil de liberación in vivo que tiene relación de Cmax yCmin menor de 200 y desfase temporal menor de 0, 2.
Breve descripción de los dibujos
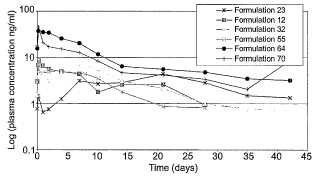
La FIGURA 1 muestra la influencia de la forma salina del fármaco en el perfil de liberación in vivo de formulaciones de acuerdo con realizaciones de la invención.
60 La FIGURA 2 muestra la influencia del tipo de disolvente en el perfil de liberación in vivo de formulaciones de acuerdo con realizaciones de la invención.
La FIGURA 3 muestra la influencia del tipo de polímero en el perfil de liberación in vivo de las formulaciones de 65 acuerdo con realizaciones de la invención.
La FIGURA 4 muestra formulaciones que tienen perfiles de liberación de orden cercano a cero de acuerdo con realizaciones de la invención.
Descripción detallada de la invención
La invención se describirá ahora en detalle con referencia a las realizaciones preferidas, como se ilustra en los dibujos adjuntos. En la siguiente descripción, se exponen numerosos detalles específicos para proporcionar un entendimiento exhaustivo de la invención. Sin embargo, resultará evidente para un experto en la materia que la invención puede practicarse sin algunos o todos estos detalles específicos. En otros casos, no se han descrito características y/o etapas de proceso bien conocidas en detalle para no complicar innecesariamente la invención. Las características y ventajas de la invención pueden entenderse mejor con referencia a los dibujos y análisis a continuación.
La invención se basa en parte en el descubrimiento de que la incorporación de un fármaco de moléculas pequeñas poco soluble en un vehículo de gel de depósito produce una formulación farmacológica de moléculas pequeñas que tiene liberación de orden casi cero in vivo. El perfil de liberación muestra ráfaga y desfase temporal mínimos. Para una formulación de liberación prolongada, este perfil de liberación es sorprendente debido a que el pensamiento predominante de la técnica es que una liberación de ráfaga baja, de orden casi cero es prácticamente imposible de conseguir a no ser que se realicen etapas especiales, tales como recubrimientos para fármacos y microencapsulación. Se han identificado varias formulaciones de fármacos pequeños en la presente invención con perfiles de liberación in vivo que tienen una relación de Cmax yCmin menor de 200 y desfase temporal, Tlag, menor de 0, 2.
La variable “Cmin” es la concentración de fármaco mínima en plasma o suero. La variable “Cmax” es la concentración máxima de fármaco en plasma o suero. La variable “Tlag” es la relación de Tvalle y Ttotal, en la que Tvalle es menor que Ttotal. La variable “Tvalle” es el tiempo para alcanzar Cvalle. La variable “Cvalle” es la primera depresión de concentración de fármaco en plasma o suero durante la liberación. La variable “Ttotal” es la duración de liberación total.
Las formulaciones farmacológicas de moléculas pequeñas de acuerdo con realizaciones de la invención se preparan como inyecciones de liberación prolongada. El ambiente de uso es un ambiente fluido y puede incluir una parte subcutánea, intramuscular, intramiocárdica, adventicia, intratumoral o intracerebral, un sitio de herida, o espacios de articulaciones estrechos o cavidad corporal de un ser humano o animal. Pueden administrarse inyecciones múltiples o repetidas al sujeto, por ejemplo, cuando el efecto terapéutico del fármaco ha disminuido o el periodo de tiempo durante el que el fármaco tiene un efecto terapéutico ha pasado o cuando el sujeto requiere administración adicional del fármaco por cualquier razón. La formulación actúa como un sistema de suministro de fármaco de liberación prolongada implantado después de su inyección en el sujeto. Dicha liberación controlada puede ser durante un periodo de una semana, más de una semana, un mes o más de un mes. Preferiblemente, la liberación controlada es durante al menos un periodo de una semana, más preferiblemente durante un periodo de al menos un mes.
Una formulación farmacológica de moléculas pequeñas de acuerdo con una realización de la invención incluye un vehículo de gel de liberación prolongada. El vehículo de gel de liberación prolongada incluye un polímero biocompatible, es decir, un polímero que no provocaría irritación o necrosis en el ambiente de uso. Los polímeros biocompatibles que pueden ser útiles en la invención pueden ser bioerosionables, es decir, se descomponen, disuelven,... [Seguir leyendo]
Reivindicaciones:
1. Una formulación de liberación prolongada inyectable, que comprende:
un polímero biocompatible que es un copolímero basado en ácido láctico y ácido glicólico que tiene una relación monomérica de ácido láctico y ácido glicólico en el intervalo de 60:40 a 75:25; un disolvente orgánico combinado con el polímero biocompatible para formar un gel viscoso, seleccionándose el disolvente de alcohol bencílico, bencil benzoato, etil benzoato, hidróxido de etilo, triacetina, N-metil-2pirrolidona y mezclas de los mismos; y un fármaco de moléculas pequeñas seleccionado a partir de formas básicas y salinas de risperidona incorporada en el gel viscoso de modo que la formulación muestre un perfil de liberación in vivo que tiene relación de Cmax yCmin menor de 200 y desfase temporal menor de 0, 2.
2. La formulación de la reivindicación 1, en la que el perfil de liberación in vivo tiene relación de Cmax yCmin menor de 15 30.
3. La formulación de la reivindicación 1, en la que el fármaco de moléculas pequeñas está en forma de partículas que tienen un tamaño de partícula medio en un intervalo de 0, 1 a 125 μm.
4. La formulación de una cualquiera de las reivindicaciones precedentes, que libera el fármaco de moléculas pequeñas a, o cerca de, una velocidad diana durante al menos una semana.
5. La formulación de una cualquiera de las reivindicaciones 1, que libera el fármaco de moléculas pequeñas a, o cerca de, la velocidad diana durante hasta un mes. 25
6. La formulación de una cualquiera de las reivindicaciones precedentes para su uso en el tratamiento del cuerpo humano o animal mediante terapia por la administración de un fármaco de moléculas pequeñas de una manera controlada.
7. La formulación de la reivindicación 6, en la que el fármaco de moléculas pequeñas se suministra por vía sistémica de una manera controlada durante una duración de liberación.
8. La formulación de la reivindicación 6, en la que la duración de la liberación es al menos una semana.
Patentes similares o relacionadas:
Administración intravascular de composiciones de nanopartículas y usos de las mismas, del 29 de Julio de 2020, de ABRAXIS BIOSCIENCE, LLC: Una composición que comprende nanopartículas que comprenden rapamicina y albúmina para su uso en un procedimiento para inhibir la remodelación […]
 Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Formulaciones estabilizadas que contienen anticuerpos anti-receptor de interleucina 4 (IL-4R), del 29 de Julio de 2020, de REGENERON PHARMACEUTICALS, INC.: Una jeringuilla precargada que contiene una formulación farmacéutica líquida estable, en la que la formulación farmacéutica líquida comprende: […]
Neuregulina para tratar la insuficiencia cardíaca, del 29 de Julio de 2020, de Zensun (Shanghai) Science & Technology, Co., Ltd: Neuregulina para usar en un método para tratar la insuficiencia cardíaca crónica en un paciente, donde el paciente tiene un nivel plasmático de NT-proBNP […]
Matrices de microagujas obtenidas mediante disolución y colada que contienen un principio activo, del 29 de Julio de 2020, de Corium, Inc: Un método para formar una matriz de microprotusiones, que comprende: (a) dispensar en un molde que tiene una matriz de cavidades correspondientes al negativo […]
Potenciador de la conservación, del 29 de Julio de 2020, de DSM IP ASSETS B.V.: Una composición tópica que comprende fitantriol y eritrulosa.
 Formulaciones de finasterida para la liberación de fármacos en el cabello y el cuero cabelludo, del 29 de Julio de 2020, de POLICHEM SA: Una composición que contiene:
(a) hidroxipropil-quitosano o una sal fisiológicamente aceptable de este en una cantidad de un 0,25 a un 2,0 % […]
Formulaciones de finasterida para la liberación de fármacos en el cabello y el cuero cabelludo, del 29 de Julio de 2020, de POLICHEM SA: Una composición que contiene:
(a) hidroxipropil-quitosano o una sal fisiológicamente aceptable de este en una cantidad de un 0,25 a un 2,0 % […]
Reducción de tejido adiposo, del 22 de Julio de 2020, de Dobak, John, Daniel: Una formulacion farmaceutica inyectable que comprende: (i) polidocanol en una cantidad del 0,5 % p/v al 2,0 % p/v; e (ii) un alcohol C3-C6 en una cantidad del […]