Formulación de aripiprazol inyectable estéril de liberación controlada y procedimiento.
Formulación inyectable de aripiprazol estéril de liberación controlada que,
tras la inyección, libera aripiprazol a lo largo de un período, por lo menos, de una semana, la cual comprende: (a) aripiprazol con un tamaño promedio de partícula comprendido entre 1 y 10 micrones; (b) un vehículo para la misma, y (c) agua para inyección.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/034367.
Solicitante: OTSUKA PHARMACEUTICAL CO., LTD..
Nacionalidad solicitante: Japón.
Dirección: 2-9 KANDA TSUKASA-CHO CHIYODA-KU TOKYO 101-8535 JAPON.
Inventor/es: NARINGREKAR, VIJAY H., KOSTANSKI,JANUSZ W, NERURKAR,MANOJ, MATSUDA,Takakuni.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/496 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › Piperazinas no condensadas conteniendo otros heterociclos, p. ej. rifampicina, tiotixeno.
- A61K47/26 A61K […] › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Hidratos de carbono, p. ej. alcoholes de azúcares, amino azúcares, ácidos nucleicos, mono-, di- u oligo-sacáridos; Sus derivados, p. ej. polisorbatos, ésteres de ácidos grasos sorbitano o glicirricina.
- A61K47/38 A61K 47/00 […] › Celulosa; Sus derivados.
- A61K9/19 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › liofilizados.
- A61P25/18 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 25/00 Medicamentos para el tratamiento de trastornos del sistema nervioso. › Antipsicóticos, es decir, neurolépticos; Medicamentos para el tratamiento de la esquizofrenia o de las fobias.
PDF original: ES-2315721_T3.pdf
Fragmento de la descripción:
Formulación de aripiprazol inyectable estéril de liberación controlada y procedimiento.
Campo de la invención
La presente invención se refiere a una formulación de aripiprazol liofilizado estéril de liberación controlada, a una formulación inyectable que contiene el aripiprazol liofilizado estéril y que libera aripiprazol a lo largo de un período, por lo menos, de una semana, a un procedimiento para preparar la formulación anterior, y a un procedimiento para tratar la esquizofrenia y trastornos relacionados utilizando la formulación anterior.
Antecedentes de la invención
La patente US nº 5.006.528, de Oshiro et al, da a conocer 7-[(4-fenilpiperazino)-butoxi]carboestirilos, que incluyen aripiprazol, como antagonistas de neurotransmisores dopaminérgicos.
El aripiprazol, que presenta la estructura
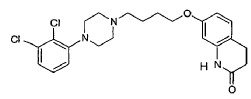
es un agente antipsicótico atípico, útil en el tratamiento de la esquizofrenia. Tiene una solubilidad baja en agua (<1 μg/ml a temperatura ambiente).
La patente US nº 6.267.989, de Liversidge et al, da a conocer un procedimiento para impedir el crecimiento cristalino y la agregación de partículas en composiciones nanoparticuladas, en el que una composición nanoparticulada se reduce a un tamaño de partícula promedio efectivo óptimo utilizando técnicas de molienda acuosa, incluyendo la molienda de bolas.
La patente US nº 5.314.506, de Midler et al, se refiere a un procedimiento para la cristalización directa de una sustancia farmacéutica que presenta partículas con un área de superficie elevada, de pureza y estabilidad elevadas, en el que se utilizan chorros de impacto a efectos de alcanzar micromezclado de alta intensidad de la sustancia farmacéutica, seguido de nucleación y producción directa de pequeños cristales.
Una formulación inyectable estéril de aripiprazol con efecto prolongado supone una forma de dosificación beneficiosa por el hecho de que puede hacer aumentar la aceptación de los pacientes y, en consecuencia, disminuir la proporción de recaídas en el tratamiento de la esquizofrenia. Los ejemplos de productos farmacéuticos conocidos de efecto prolongado para el tratamiento de la esquizofrenia incluyen decanoato de haloperidol y decanoato de flufenazina, presentando los dos un compuesto éster con baja solubilidad en agua disuelto en aceite de sésamo. Asimismo, se conocen microcápsulas que contienen risperidona (WO95/13814) y olanzapina (WO99/12549).
Breve descripción de la invención
Según la presente invención, se da a conocer una formulación de aripiprazol liofilizada estéril que, tras su constitución con agua para su inyección, libera aripiprazol en cantidades terapéuticas a lo largo de un período, por lo menos, de aproximadamente una semana, y preferentemente a lo largo de un período de dos, tres o cuatro semanas y de hasta seis semanas o más. La formulación de aripiprazol liofilizado según la invención incluye:
formando dicha formulación, tras su constitución con agua, una suspensión inyectable que, tras la inyección, preferentemente por vía intramuscular, libera cantidades terapéuticas de aripiprazol a lo largo de un período, por lo menos, de una semana, preferentemente dos, tres o cuatro semanas, y de hasta seis semanas o más.
La formulación de aripiprazol liofilizado según la invención incluye preferentemente:
Un tamaño de partícula promedio de la formulación de aripiprazol liofilizado comprendido dentro del intervalo de 1 a 10 micrones resulta esencial en la formulación de un inyectable que libere aripiprazol a lo largo de un período, por lo menos, de aproximadamente una semana y de hasta seis semanas o más, por ejemplo hasta 8 semanas.
Se ha puesto de manifiesto que, cuanto menor es el tamaño promedio de partícula del aripiprazol liofilizado, más breve es el período de liberación prolongada. De este modo, según la presente invención, cuando el tamaño promedio de partícula es de aproximadamente 1 micrón, el aripiprazol se libera a lo largo de un período menor de tres semanas, preferentemente de aproximadamente dos semanas. Cuando el tamaño promedio de partícula es mayor de aproximadamente 1 micrón, el aripiprazol se libera durante un periodo, por lo menos, de dos semanas, preferentemente de aproximadamente tres a cuatro semanas, y de hasta seis semanas o más. De este modo, según la presente invención, la duración de la liberación de aripiprazol se puede modificar cambiando el tamaño de partícula del aripiprazol en la formación liofilizada.
La expresión "tamaño promedio de partícula" se refiere al diámetro promedio de volumen medido por métodos de dispersión de luz láser (LLS). La distribución de tamaños de partícula se mide mediante métodos de LLS, y el tamaño promedio de partícula se calcula a partir de dicha distribución de tamaños de partícula.
Además, según la presente invención, se da a conocer una formulación de aripiprazol inyectable estéril de liberación controlada en forma de suspensión estéril, es decir, la formulación liofilizada de la invención suspendida en agua para su inyección, la cual, tras la inyección, preferentemente por vía intramuscular, libera cantidades terapéuticas de aripiprazol a lo largo de un periodo, por lo menos, de una semana, y la cual incluye:
La formulación inyectable estéril de liberación controlada según la invención en forma de suspensión estéril permite cargas elevadas de fármaco por unidad de volumen de la formulación y, en consecuencia, permite el suministro de dosis relativamente elevadas de aripiprazol en un pequeño volumen de inyección (0,1-600 mg de fármaco por 1 ml de suspensión).
Además, según la presente invención, se da a conocer un procedimiento para preparar la formulación de aripiprazol liofilizado estéril descrito anteriormente, que incluye las siguientes etapas:
En la forma de realización del procedimiento anterior, la reducción del tamaño promedio de partícula de la suspensión primaria estéril al tamaño promedio de partícula deseado se lleva a cabo utilizando un procedimiento de molienda aséptico en húmedo, preferentemente molienda aséptica en húmedo de bolas. La molienda aséptica en húmedo resulta esencial para formar una formulación de aripiprazol estéril y homogéneo con la distribución de tamaños promedio de partícula deseada.
Además, según la presente invención, se da a conocer un procedimiento para liofilizar la suspensión estéril final de aripiprazol que produce un aripiprazol liofilizado... [Seguir leyendo]
Reivindicaciones:
1. Formulación inyectable de aripiprazol estéril de liberación controlada que, tras la inyección, libera aripiprazol a lo largo de un período, por lo menos, de una semana, la cual comprende:
2. Formulación según la reivindicación 1, en la que dicho vehículo comprende uno o más agentes de suspensión.
3. Formulación según la reivindicación 1, en la que dicho vehículo comprende:
4. Formulación según la reivindicación 3, que incluye asimismo un agente de ajuste del pH.
5. Formulación según la reivindicación 3, en forma de suspensión estéril.
6. Formulación según la reivindicación 3, diseñada para liberar aripiprazol a una velocidad controlada a lo largo de un periodo comprendido entre dos y cuatro semanas.
7. Formulación según la reivindicación 3, en forma de suspensión en la que:
estando expresados todos los % anteriores en % en peso/volumen en base al volumen de suspensión.
8. Formulación según la reivindicación 3, en la que el agente de suspensión es carboximetilcelulosa o su sal sódica, hidroxipropilcelulosa, carboximetilcelulosa, hidroxipropiletilcelulosa, hidroxipropilmetilcelulosa, o polivinilpirrolidona, siendo el agente de carga manitol, sucrosa, maltosa, lactosa, xilitol o sorbitol, y siendo el tampón fosfato de sodio, fosfato de potasio o tampón TRIS.
9. Formulación según la reivindicación 3, que, tras la inyección, libera aripiprazol a lo largo de un período de dos a cuatro semanas, que comprende:
10. Formulación según la reivindicación 9, que comprende:
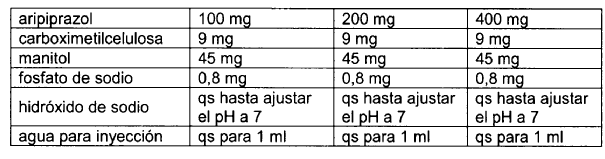
11. Formulación según la reivindicación 4, que permite el suministro de entre 0,1 y 600 mg de aripiprazol por 1 ml de suspensión.
12. Formulación según la reivindicación 1, en la que el aripiprazol se encuentra en forma anhídrida o en forma de monohidrato.
13. Formulación según la reivindicación 12, en la que el aripiprazol se encuentra en forma de cristales de aripiprazol anhídrido B o en forma de aripiprazol hidrato A.
14. Formulación de aripiprazol de liberación controlada liofilizada que comprende:
formando dicha formulación, tras su constitución con agua, una formulación inyectable estéril que, tras la inyección, libera aripiprazol a lo largo de un período, por lo menos, de aproximadamente dos semanas.
15. Formulación liofilizada según la reivindicación 14, que, tras su constitución con agua y su inyección, libera aripiprazol a lo largo de un período, por lo menos, de aproximadamente tres semanas.
16. Formulación liofilizada según la reivindicación 15, que presenta un tamaño promedio de partícula de aproximadamente 2,5 micrones.
17. Formulación liofilizada según la reivindicación 14, en la que dicho vehículo comprende:
18. Formulación liofilizada según la reivindicación 17, que incluye asimismo un agente de ajuste del pH.
19. Formulación liofilizada según la reivindicación 17, que, tras su constitución con agua y su inyección, libera aripiprazol a lo largo de un período, por lo menos, de aproximadamente tres semanas, la cual comprende:
20. Formulación liofilizada según la reivindicación 19, que, tras su reconstitución con agua y su inyección, libera aripiprazol a lo largo de un período de aproximadamente cuatro semanas.
21. Formulación liofilizada según la reivindicación 20, en la que el aripiprazol se encuentra en forma de cristales anhídridos o en forma de monohidrato.
22. Procedimiento para preparar la formulación liofilizada estéril según la reivindicación 14, que comprende las siguientes etapas:
23. Procedimiento según la reivindicación 22, en el que la etapa de reducir el tamaño promedio de partícula de la mezcla estéril de sólidos en dicha suspensión primaria estéril se lleva a cabo utilizando molienda en húmedo.
24. Procedimiento según la reivindicación 23, en el que la molienda en húmedo comprende molienda de bolas en húmedo.
25. Procedimiento según la reivindicación 22, en el que dicha etapa de liofilización se lleva a cabo enfriando la suspensión final estéril a aproximadamente -40ºC y secando dicha suspensión final estéril enfriada a una temperatura inferior a aproximadamente 0ºC, para obtener aripiprazol liofilizado en forma de su monohidrato.
26. Procedimiento según la reivindicación 22, en el que la etapa de liofilización de la suspensión final estéril se lleva a cabo en tres fases: (1) fase de congelación, que incluye el enfriamiento de la suspensión final estéril a aproximadamente -40ºC, (2) una fase de secado primario que se lleva a cabo a una temperatura inferior a aproximadamente 0ºC, y (3) una fase de secado secundario que se lleva a cabo a una temperatura superior a aproximadamente 0ºC, para obtener aripiprazol en forma anhídrida.
27. Utilización de la formulación según cualquiera de las reivindicaciones 1 a 21 para la preparación de un medicamento destinado al tratamiento de la esquizofrenia.
28. Utilización según la reivindicación 27, en la que la formulación se administra por vía intramuscular o subcutánea.
Patentes similares o relacionadas:
Tratamientos de combinación que comprenden imidazopirazinonas para el tratamiento de trastornos psiquiátricos y/o cognitivos, del 29 de Julio de 2020, de H. LUNDBECK A/S: Un compuesto de Fórmula (I) **(Ver fórmula)** en donde n es 0 o 1; q es 0 o 1; R1 se selecciona del grupo que consiste en bencilo, indanilo, indolina y heteroarilos […]
Composición farmacéutica que comprende un agente antipsicótico atípico y método para su preparación, del 15 de Julio de 2020, de PHARMATHEN S.A.: Comprimido de liberación controlada de Paliperidona en forma de comprimido de varias capas que comprende: a) un núcleo de matriz que comprende […]
Composición que comprende cinamaldehído y cinc, del 8 de Julio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Composición que comprende cinamaldehído y cinc para la utilización en la mejora de uno o más de rendimiento cognitivo, cognición, humor o memoria en un […]
Moduladores heteroaromáticos del receptor NMDA y usos de los mismos, del 24 de Junio de 2020, de Cadent Therapeutics, Inc: Un compuesto representado por la Fórmula I **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en el que: los anillos A y B son un sistema heteroaromático […]
Compuesto de tetrahidrooxepinopiridina, del 17 de Junio de 2020, de ASTELLAS PHARMA INC.: Compuesto de fórmula (I) o sal del mismo: **(Ver fórmula)** (en la fórmula, R1 es H o alquilo inferior, R2 es H o CN, uno cualquiera […]
Derivados de indolin-2-ona, del 27 de Mayo de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto de fórmula **(Ver fórmula)** en la que A es fenilo o un grupo heteroarilo de cinco o seis miembros, que contiene […]
Esteroides neuroactivos, composiciones y usos de los mismos, del 29 de Abril de 2020, de Sage Therapeutics, Inc: Un compuesto de la fórmula: **(Ver fórmula)** o sal farmacéuticamente aceptable del mismo.
Régimen de dosificación para dosis olvidadas para ésteres de paliperidona inyectables de acción prolongada, del 22 de Abril de 2020, de Janssen Pharmaceuticals, Inc: Un depósito de palmitato de paliperidona inyectable para su uso en el tratamiento de un paciente con necesidad de tratamiento psiquiátrico seleccionado […]