Cisteamina con recubrimiento entérico, cistamina y derivados de las mismas.
Una composición que comprende cistamina o cisteamina con recubrimiento entérico en forma de una sal,
éster oamida farmacéuticamente aceptable, para usar en el tratamiento de la cistinosis administrando dosis dos veces aldía.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2007/002325.
Solicitante: THE REGENTS OF THE UNIVERSITY OF CALIFORNIA.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1111 FRANKLIN STREET 5TH FLOOR OAKLAND, CA 94607-5200 ESTADOS UNIDOS DE AMERICA.
Inventor/es: DOHIL,RANJAN, SCHNEIDER,JERRY.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/145 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › que tienen átomos de azufre p. ej. tiuranos ( N—C(S)—S—C(S)—N o N—C(S)—S—S—C(S)—N ); Sulfinilaminas (—N=SO); Sulfonilaminas (—N=SO 2 ) (isotioureas A61K 31/155).
- A61K9/32 A61K […] › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › que contienen polímeros sintéticos sólidos.
- A61P43/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para usos específicos, no previstos en los grupos A61P 1/00 - A61P 41/00.
PDF original: ES-2388310_T3.pdf
Fragmento de la descripción:
Cisteamina con recubrimiento entérico, cistamina y derivados de las mismas
Campo de la invención
La invención se refiere a una composición para usar en el tratamiento de la cistinosis.
Antecedentes
La cistinosis es una rara enfermedad autosómica recesiva causada por acumulación intralisosomal del aminoácido cistina en varios tejidos, incluido el bazo, el hígado, los ganglios linfáticos, el riñón, la médula ósea y los ojos. La cistinosis neuropática se asocia con insuficiencia renal que requiere transplante renal. Hasta la fecha, el único tratamiento especifico de la cistinosis nefropática es el agente sulfhidrilo, cisteamina. Se ha demostrado que la cisteamina muestra niveles bajos de cistina, de modo que se reduce la velocidad de la progresión de la insuficiencia renal en niños.
La cisteamina, a través de un mecanismo del incremento de la gastrina y la producción de ácido gástrico, es ulcerogénica. Cuando se administra por vía oral a los niños con cistinosis, también se ha demostrado que la cisteamina triplica la producción de ácido gástrico y un aumento del 50 % de los niveles de gastrina en suero. Como consecuencia, los sujetos que usan cisteamina sufren síntomas gastrointestinales (GI) y a menudo son incapaces de tomar cisteamina con regularidad o a una dosis completa.
Levtchenko y col. divulgan que se requiere un régimen estricto de dosis de cisteamina para prevenir la acumulación de cistina nocturna en la cistinosis (Pediatric Nephrology (2006) , 21: 110-113) .
Para conseguir una reducción sostenida de los niveles leucocitarios de cistina, normalmente es necesario que los pacientes tomen cisteamina oral cada 6 horas, lo que invariablemente significa tener que despertarse del sueño. No obstante, cuando se administró una única dosis de cisteamina por vía intravenosa, el nivel leucocitario de cistina permaneció suprimido durante más de 24 horas, posiblemente porque las concentraciones de cisteamina en plasma eran mayores y se alcanzaron con mayor rapidez que cuando el fármaco se administra por vía oral. La administración intravenosa regular de cisteamina no sería práctica. De acuerdo con esto, existe la necesidad de formulaciones y procedimientos de liberación que den lugar a mayores concentraciones en plasma, y por tanto intracelulares, así como a una disminución del número de dosis diarias y, por consiguiente, a una mejora de la calidad de vida para los pacientes.
Sumario
La invención proporciona una composición que comprende cistamina o cisteamina con recubrimiento entérico en forma de una sal, éster o amida farmacéuticamente aceptable, para usar en el tratamiento de la cistinosis administrando dosis dos veces al día.
Además, se proporciona una composición que comprende una cistamina o cisteamina con recubrimiento entérico en forma de una sal, éster o amida farmacéuticamente aceptable.
También se proporciona una composición que comprende un agente terapéutico recubierto para la cistinosis que ha aumentado la captación en el intestino delgado en comparación con un agente terapéutico no recubierto para la cistinosis cuando se administra o vía oral. El agente terapéutico recubierto para la cistinosis comprende una sal, éster o amida de cistamina o cisteamina con farmacéuticamente aceptables.
En e presente documento se describe una composición para usar en el tratamiento de un sujeto con cistinosis, que comprende administrar al sujeto la composición como se ha descrito anteriormente.
También se describe una composición para usar en el tratamiento de un sujeto con una enfermedad o trastorno neurodegenerativo, que comprende administrar al sujeto la composición como se ha descrito anteriormente, que comprende cistamina o un derivado de cistamina con recubrimiento entérico.
Además, se proporciona una formulación farmacéutica que comprende la composición como se ha descrito anteriormente, que además incluye varios agentes farmacéuticamente aceptables (p. ej., aromatizantes, aglutinantes y similares) en un vehículo farmacéuticamente aceptable.
También se describe una composición para usar en el tratamiento de la cistinosis o de una enfermedad o trastorno neurodegenerativo, que comprende administrar la composición como se ha descrito anteriormente y un segundo agente terapéutico.
Breve descripción de las figuras
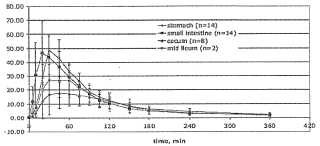
La figura 1 muestra un tubo enterocolónico. (A) es una radiografía abdominal que muestra la punta ponderada radioopaca del tubo que entra en el colon ascendente. (B) es una imagen de infusión de contraste. El tubo ha pasado a través del intestino delgado y se confirma la punta. La Figura 2 muestra los niveles medios en plasma de cisteamina tomados de pacientes con cistinosis y sujetos control tras la liberación del fármaco en varios puntos intestinales. Las barras de error muestran el error estándar de la media. En 2 sujetos control, el punto más distal de la liberación del fármaco era la región media-ileal.
La Figura 3 muestra el cambio medio en los niveles leucocitarios de cistina en comparación con los niveles basales en un periodo de 12 horas tras la liberación de cisteamina en varios sitios intestinales. Los niveles negativos significan un incremento de la depleción de la cistina leucocitaria en comparación con el valor basal.
La Figura 4 muestra un gráfico en escalera de la Cmáx de cisteamina en plasma frente a la AOC de los cambios de cistina leucocitaria con respecto al valor basal. Los valores medios positivos disminuyen con respecto a los valores basales. Los valores medios negativos aumentan con respecto a los valores basales. El cambo de ACO con respecto al valor basal se vio afectado por la Cmáx para cisteamina (P < 0, 001) .
La Figura 5 muestra los niveles de cistina leucocitarios en serie tras la administración del fármaco como Cystagon normal y cisteamina con recubrimiento entérico (RE) en días alternos. Estos niveles en serie se tomaron durante la fase no ambulatoria del estudio. Los niveles deseados de cistina están por debajo de 1 nmol ½ de cistina/mg de proteína. La dosis mayor del fármaco con recubrimiento entérico (amarillo) tuvo como resultado una prolongación de la supresión de cistina con niveles a 12 horas todavía dentro del intervalo deseado.
La Figura 6 muestra los niveles de cisteamina en sangre tras una única dosis de 450 mg de Cystagon (serie 1) , 450 mg de cisteamina-RE (serie 2) y 900 mg de cisteamina-RE (serie 3) . La Cmáx es mayor tras el fármaco con RE. Además, el tiempo hasta la Cmáx es más largo tras el fármaco con RE, lo que sugiere que el fármaco se libera de la cápsula dentro del intestino delgado en lugar de en el estómago.
Descripción detallada
Como se usa en la presente memoria descriptiva y las reivindicaciones adjuntas, las formas “uno”, “una” y “el" incluyen las referencias en plural a menos que el contenido indique claramente lo contrario. Por tanto, por ejemplo, la referencia a “un derivado” incluye una pluralidad de dichos derivados y una referencia a “un sujeto” incluye la referencia a uno o más sujetos conocidos para los expertos en la técnica, y así sucesivamente.
A menos que se defina otra cosa, todos los términos técnicos y científicos usados en la presente memoria descriptiva tienen el mismo significado que un experto en la técnica a la que la presente divulgación pertenece entiende habitualmente. Aunque se pueden usar materiales y procedimientos similares o equivalentes a aquellos descritos en el presente documento se pueden usar en la práctica de los procedimientos y composiciones divulgados, los procedimientos de ejemplo, dispositivos y materiales se describen en el presente documento.
Las publicaciones tratadas anteriormente y a lo largo del texto se proporcionan ricamente para su divulgación antes de la fecha de presentación de la presente solicitud. En el presente documento nada se tiene que interpretar como admisión de que los inventores no tienen el derecho de antedatar dicha divulgación en virtud de la divulgación previa.
La cistinosis es una enfermedad metabólica que se caracteriza por una cumulación anormal del aminoácido cistina en varios órganos del cuerpo, tal como los riñones, los ojos, los músculos, el páncreas y el cerebro. A diferentes... [Seguir leyendo]
Reivindicaciones:
1. Una composición que comprende cistamina o cisteamina con recubrimiento entérico en forma de una sal, éster o
amida farmacéuticamente aceptable, para usar en el tratamiento de la cistinosis administrando dosis dos veces al 5 día.
2. La composición para usar de acuerdo con la reivindicación 1, que comprende un recubrimiento entérico que libera la cistamina o cisteamina a un pH mayor que el pH de 4, 5.
3. La composición para usar de acuerdo con cualquiera de las reivindicaciones 1 o 2, en la que la composición aumenta la liberación de cistamina o cisteamina, en forma de una sal, éster o amida farmacológicamente aceptable, en el intestino delgado.
4. La composición para usar de acuerdo con una cualquiera de las reivindicaciones 1 a 3, en la que el recubrimiento
entérico se selecciona del grupo constituido por gelatina polimerizada, goma shellac, copolímero de ácido metacrílico de tipo C NF, ftalato de butirato de celulosa, ftalato de hidrógeno de celulosa, ftalato de propionato de celulosa, ftalato de acetato de polivinilo (PVAP) , ftalato de acetato de celulosa (CAP) , trimelitato acetato de celulosa (CAT) , ftalato de hidroxipropilmetilcelulosa, succinato acetato de hidroxipropilmetilcelulosa (HPMCAS) y polímeros y copolímeros de ácido acrílico, normalmente formados a partir de acrilato de metilo, acrilato de etilo, metacrilato de
metilo y/o metacrilato de etilo con copolímeros de ésteres de ácido acrílico y metacrílico.
5. La composición para usar de acuerdo con una cualquiera de las reivindicaciones 1 a 4, que comprende un transportador o estabilizante farmacéuticamente aceptable.
6. La composición para usar de acuerdo con una cualquiera de las reivindicaciones 1 a 5, para administración a una dosis diaria total de aproximadamente 0, 5 a 1, 0 g/m2 de área de superficie corporal.
7. La composición para usar de acuerdo con cualquiera de las reivindicaciones 1 a 6, para proporcionar un nivel de
cistina en leucocitos a las 12 horas por debajo de 1 nmol/1/2 de cistina/mg de proteína. 30
8. La composición para usar de acuerdo con cualquiera de las reivindicaciones 1-7, en la que el recubrimiento entérico proporciona un incremento de la absorción en el intestino delgado.
9. La composición para usar de acuerdo con una cualquiera de las reivindicaciones 1 a 8, que está en forma de un 35 comprimido o que se granula y carga en una cápsula.
10. La composición para usar de acuerdo con cualquiera de las reivindicaciones 1-9, en la que la composición es capaz de aumentar la liberación de la cistamina o cisteamina o sales farmacéuticamente aceptables de los mismos en el intestino delgado.
FIGURA 1
Patentes similares o relacionadas:
 Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
Composiciones y métodos para el tratamiento de trastornos de células plasmáticas y trastornos prolinfocíticos de células b, del 29 de Julio de 2020, de Knopp Biosciences LLC: Una composición que comprende una cantidad terapéuticamente eficaz de dexpramipexol para su uso en el tratamiento de un trastorno de células B caracterizado por niveles elevados […]
 Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Inhibidor de galactósido de galectina-3 y su uso para tratar fibrosis pulmonar, del 29 de Julio de 2020, de Galecto Biotech AB: Un dispositivo adecuado para administración pulmonar en el que dicho dispositivo es un inhalador de polvo seco que comprende una composición que comprende un compuesto de […]
Derivado de dihidropiridazin-3,5-diona, del 15 de Julio de 2020, de CHUGAI SEIYAKU KABUSHIKI KAISHA: Un compuesto representado por la fórmula (I) o una sal del mismo, o un solvato del compuesto o la sal: **(Ver fórmula)** en donde R1, R4 y R5 se definen […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]
Compuestos utilizados como inhibidores de la quinasa reordenada durante la transfección (RET), del 1 de Julio de 2020, de GlaxoSmithKline Intellectual Property Development Limited: Un compuesto de acuerdo con la Fórmula (I), o una sal farmacéuticamente aceptable del mismo: **(Ver fórmula)** en donde: X es N o CR5; Y es un enlace; […]
Derivado de dihidroindolizinona, del 1 de Julio de 2020, de ONO PHARMACEUTICAL CO., LTD.: (3S)-3-[2-(6-amino-2-fluoro-3-piridinil)-4-fluoro-1H-imidazol-5-il]-7-[5-cloro-2-(1H-tetrazol-1-il)fenil]-2,3-dihidro- (1H)-indolizinona, una…
Inhibidor de fibrosis, del 1 de Julio de 2020, de NIPPON SHINYAKU CO., LTD.: Composición farmacéutica que comprende un derivado heterocíclico seleccionado de ácido 2-{4-[N-(5,6-difenilpirazin-2-il)-N-isopropilamino]butiloxi}acético […]
Métodos de monitorización terapéutica de profármacos de ácido fenilacético, del 24 de Junio de 2020, de Immedica Pharma AB: Glicerilo tri-[4-fenilbutirato] (HPN-100) para su uso en un método para tratar un trastorno del ciclo de la urea en un sujeto que tiene discapacidad […]