Procedimiento para la preparación de cetonas a partir de alfa-oxacarboxilatos y bromuros de arilo.
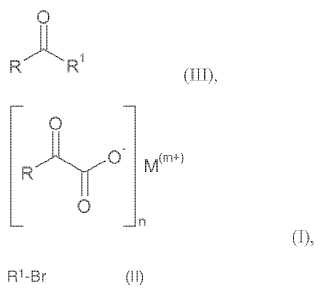
Procedimiento para la preparación de cetonas de la fórmula general (III)
en la que
R es un resto carbocíclico aromático de 6 a 24 átomos de carbono dado el caso substituido o un resto alquilo dado elcaso substituido o un resto heteroaromático de 5 a 24 átomos de carbono dado el caso substituido yR1 es un resto carbocíclico aromático de 6 a 24 átomos de carbono dado el caso substituido o un restoheteroaromático de 5 a 24 átomos de carbono dado el caso substituido,
por reacción de alfa-oxocarboxilatos de la fórmula general (I)
en la que
n y m es un número en el intervalo de 1 a 6,M(m+) es un catión y
R tiene el significado indicado para la fórmula (III),
con bromuros de arilo de la fórmula general (II)
R1-Br (II)
en la que
R1 tiene el significado indicado para la fórmula (III),
caracterizado porque como catalizador se utiliza una combinación de bromuro de cobre(I) con 1,10-fenantrolina comoligando y bis(1,1,1,5,5,5-hexafluoroacetilacetonato)paladio con tris(o-tolil)fosfina como ligando.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E09153525.
Solicitante: SALTIGO GMBH.
Nacionalidad solicitante: Alemania.
Dirección: KATZBERGSTRASSE 1 40764 LANGENFELD ALEMANIA.
Inventor/es: Gotta,Matthias, Cotté,Alain, Goossen,Lukas, Rudolphi,Felix, Oppel,Christoph, Garrido,Nuria Rodriguez.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07C221/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07C COMPUESTOS ACICLICOS O CARBOCICLICOS (compuestos macromoleculares C08; producción de compuestos orgánicos por electrolisiso electroforesis C25B 3/00, C25B 7/00). › Preparación de compuestos que contienen grupos amino y átomos de oxígeno, unidos por enlaces dobles, unidos a la misma estructura carbonada.
- C07C253/30 C07C […] › C07C 253/00 Preparación de nitrilos de ácidos carboxílicos (de cianógeno o sus compuestos C01C 3/00). › por reacciones que no implican la formación de grupos ciano.
- C07C255/22 C07C […] › C07C 255/00 Nitrilos de ácidos carboxílicos (cianógeno o sus compuestos C01C 3/00). › que contienen grupos ciano y al menos dos grupos carboxilo unidos a la estructura carbonada.
- C07C255/56 C07C 255/00 […] › que contienen grupos ciano y átomos de oxígeno unidos por enlaces dobles, unidos a la estructura carbonada.
- C07C45/68 C07C […] › C07C 45/00 Preparación de compuestos que tienen grupos C=O unidos únicamente a átomos de carbono o hidrógeno; Preparación de los quelatos de estos compuestos. › por aumento del número de átomos de carbono.
- C07D213/50 C07 […] › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 213/00 Compuestos heterocíclicos que contienen ciclos de seis miembros, no condensados con otros ciclos, con un átomo de nitrógeno como el único heteroátomo del ciclo y tres o más enlaces dobles entre miembros cíclicos o entre miembros cíclicos y miembros no cíclicos. › Radicales cetónicos.
- C07D307/46 C07D […] › C07D 307/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros que tienen un átomo de oxígeno como único heteroátomo del ciclo. › Atomos de oxígeno doblemente enlazados, o dos átomos de oxígeno unidos por un enlace sencillo al mismo átomo de carbono.
- C07D333/22 C07D […] › C07D 333/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros que tienen un átomo de azufre como único heteroátomo del ciclo. › Radicales sustituidos por heteroátomos unidos por un enlace doble, o por dos heteroátomos distintos al halógeno, unidos por un enlace sencillo al mismo átomo de carbono.
PDF original: ES-2383482_T3.pdf
Fragmento de la descripción:
Procedimiento para la preparación de cetonas a partir de alfa-oxacarboxilatos y bromuros de arilo La presente invención se refiere a un nuevo procedimiento para la preparación de cetonas a partir de alfa-oxocarboxilatos y bromuros de arilo por acoplamiento cruzado descarboxilante catalizado con Cu/Pd.
Las arilcetonas son elementos estructurales importantes en principios activos y materiales funcionales (P. J. Masson, D. Coup, J. Millet, N.L. Brown, J. Biol.. Chem. 1994, 270, 2662-2668) . Además de las acilaciones de Friedel-Crafts clásicas que se llevan a cabo a escala industrial, pero que en la mayoría de los casos conducen inconvenientemente a mezclas de isómeros, se utilizan para su síntesis igualmente reacciones de derivados de ácidos carboxílicos con reactivos organometálicos como p.ej. amidas de Weinreb con compuestos de Grignard (S. Nahm, S. M. Weinreb, Tetrahedron Lett.
1981, 22, 3815-3818) . Mediante el uso de catalizadores de metales de transición puede aumentarse más la eficiencia de tales acoplamientos cruzados, de modo que se hacen reaccionar incluso nucleófilos de carbono poco reactivos, por ejemplo compuestos de organocinc o ácidos borónicos (E. Negishi, V. Bagheri, S. Chatterjee, F. T. Luo, J. A. Miller, A. T. Stoll, Tetrahedron Lett. 1983, 24, 5181-5184; P. Knochel, M. C. P. Yeh, S. C. Berk. J. Talbert, J. Org. Chem. 1988, 53, 2392-2394; M. Haddach, J. R. McCarthy, Tetrahedron Lett. 1999, 40, 3109-3122) .
Son más convenientes variantes de reacción en las que se activan in situ ácidos carboxílicos, como p.ej. síntesis directas catalizadas con paladio de arilcetonas a partir de ácidos arilborónicos y ácidos carboxílicos en presencia de anhídridos (L.
J. Goossen, L. Winkel, A. Döhring, K. Ghosh, J. Paetzold, Synlett 2002, 8, 1237-1240) o reactivos de acoplamiento (L. J. Goossen, K. Ghosh, Chem. Comm. 2001, 2084-2085) . Mediante estos métodos se mejora ciertamente claramente la tolerancia de grupos funcionales, sin embargo este modo de proceder tiene graves inconvenientes debido a la difícil accesibilidad de los ácidos borónicos (metalación de haluros de arilo y subsiguiente reacción con boratos de trialquilo) o por la mala manipulación de los compuestos de organocinc.
Un modo de proceder inverso, en el que se acoplan equivalentes de aniones acilo con electrófilos de carbono, se utiliza principalmente en la síntesis de alquilcetonas (E. J. Corey, D. Seebach, Angew. Chem. 1965, 77, 1134-1135; Angew. Chem. Int. Ed. 1965, 4, 1075-1077) . Para la arilación catalítica de equivalentes de aniones acilo hay solo pocos ejemplos, 25 entre ellos el acoplamiento descrito por Hartwig y col. de bromuros de arilo con N-terc-butilhidrazonas (A. Takemiya, J. F. Hartwig, J. Am. Chem. Soc. 2006, 128, 14800-14801) . Es un inconveniente en todas las reacciones de este tipo los pasos de derivatización y saponificación adicionales, así como el uso de bases fuertes. Las arilaciones de aldehídos con activación C-H ofrecen una alternativa atomoeconómica, pero hasta ahora son solo posibles con un espectro limitado de yoduros de arilo caros (Y. C. Huang, K. K. Majumdar, C. H. Cheng, J. Org. Chem. 2002, 67, 1682-1684; S. Ko, B. Kang, S.
Chang, Angew. Chem. 2005, 117, 459-461; Angew. Chem. Int. Ed. 2005, 44, 455-457) .
En la síntesis de biarilos a partir de sales de ácido benzoico y haluros de arilo se llega ya a la comprobación de que acoplamientos cruzados descarboxilantes pueden representar alternativas valiosas a reacciones correspondientes de compuestos organometálicos (documento WO 2006/136135) .
Ha sido objetivo de la presente invención encontrar un procedimiento para la preparación de cetonas, en especial de 35 arilcetonas, en el que partiendo de compuestos bien accesibles se utilicen catalizadores bien manejables y baratos.
Si la descarboxilación de ácidos alfa-oxocarboxílicos de fórmula (I) se lleva a cabo en presencia de un catalizador de Cu y se combina con un acoplamiento cruzado mediado con Pd con bromuros de arilo de fórmula (II) se llega a las cetonas de fórmula (III)
45 Es una ventaja de este acoplamiento cruzado descarboxilante para la preparación de cetonas que al contrario de las reacciones de acoplamiento cruzado tradicionales no son necesarios reactivos organometálicos. En lugar de estos se utilizan sales de ácidos alfa-oxocarboxílicos estables fácilmente manipulables y bien accesibles que en parte están disponibles industrialmente como productos intermedios en la preparación de aminoácidos como fuente de acilnucleófilos.
Es por consiguiente objeto de la invención un procedimiento para la preparación de cetonas de la fórmula general (III)
en la que R es un resto carbocíclico aromático de 6 a 24 átomos de carbono dado el caso substituido o un resto alquilo dado el caso substituido o un resto heteroaromático de 5 a 24 átomos de carbono dado el caso substituido y R1 es un resto carbocíclico aromático de 6 a 24 átomos de carbono dado el caso substituido o un resto heteroaromático de 5 a 24 átomos de carbono dado el caso substituido, por reacción de alfa-oxocarboxilatos de la fórmula general (I)
en la que n y m es un número en el intervalo de 1 a 6, M (m+)
es un catión y R tiene el significado indicado para la fórmula (III) , con bromuros de arilo de la fórmula general (II) R1-Br (II)
en la que R1 tiene el significado indicado para la fórmula (III) , en la que como catalizador se utiliza una combinación de bromuro de cobre (I) con 1, 10-fenantrolina como ligando y bis (1, 1, 1, 5, 5, 5-hexafluoroacetilacetonato) paladio con tris (o-tolil) fosfina como ligando. Mediante la adición del ligando de fosfina se influye ventajosamente en la reacción. Se utiliza tris (o-tolil) fosfina ( (o-Tol) 3P) . Para el procedimiento conforme a la invención como sistema de catalizador se utiliza una combinación de bromuro de cobre (I) con 1, 10-fenantrolina como ligando y Pd (F6acac) 2 con tris (o-tolil) fosfina como ligando. Según el procedimiento conforme a la invención se utilizan ambos catalizadores independientemente entre sí en cantidades de 0, 001% en moles a 100% en moles referidas al electrófilo de carbono (R1-Br) , preferiblemente se utilizan cantidades de 0, 01% en moles a 15% en moles. El procedimiento conforme a la invención se lleva a cabo a temperaturas de 20ºC a 220ºC, preferiblemente de 80ºC a 200ºC y con especial preferencia de 120ºC a 180ºC. El procedimiento conforme a la invención se lleva a cabo habitualmente en presencia de un disolvente. Por ejemplo como disolventes pueden utilizarse una o mezclas de las substancias de uso, hidrocarburos aromáticos (por ejemplo benceno, tolueno, xilenos, etilbenceno, mesitileno) , éteres (por ejemplo 1, 4-dioxano, tetrahidrofurano, metiltetrahidrofurano, dibutiléter, metil-t-butiléter, diisopropiléter, dietilenglicol-dimetiléter) , amidas (por ejemplo dimetilformamida, dietilformamida, N-metilpirrolidona, dimetilacetamida, aminas aromáticas (quinolina, piridina) , dimetilsulfóxido, sulfolano, acetonitrilo, isobutironitrilo, propionitrilo, carbonato de propileno e hidrocarburos alifáticos y aromáticos clorados. Preferiblemente se utilizan amidas (por ejemplo dimetilformamida, N-metilpirrolidona) y aminas aromáticas (por ejemplo quinolina, piridina) o mezclas amidas/aminas.
El procedimiento conforme a la invención puede llevarse a cabo preferiblemente de modo que durante la reacción puedan eliminarse trazas de agua por destilación azeotrópica continua. Para conseguir la temperatura de reacción necesaria también puede trabajarse bajo presión.
R y R1 representan en el marco de la invención preferiblemente restos carbocíclicos aromáticos con 6 a 24 átomos de carbono en la estructura o restos heteroaromáticos con 5 a 24 átomos de carbono en la estructura, en los que ninguno, uno, dos o tres átomos de carbono en la estructura por ciclo, en la molécula completa sin embargo al menos un átomo de carbono en la estructura, pueden estar substituidos por heteroátomos seleccionados del grupo de nitrógeno, azufre u oxígeno. Además los restos carbocíclicos aromáticos o los restos heteroaromáticos pueden estar substituidos con hasta cinco substituyentes iguales o distintos por ciclo, seleccionados del grupo de hidroxi, halógeno, nitro, amino, mercapto, ciano, formilo libre o protegido, alquilo C1-C12, haloalquilo C1-C12, alquiltio C1-C12, arilo C5-C14, aril C6-C15-alquilo, alcoxi C1-C12 y alcoxicarbonilo C1-C12. Por ejemplo R1 representa fenilo, tolilo, tienilo o naftilo, que dado el caso está substituido una vez, dos veces... [Seguir leyendo]
Reivindicaciones:
1. Procedimiento para la preparación de cetonas de la fórmula general (III)
en la que R es un resto carbocíclico aromático de 6 a 24 átomos de carbono dado el caso substituido o un resto alquilo dado el caso substituido o un resto heteroaromático de 5 a 24 átomos de carbono dado el caso substituido y R1 es un resto carbocíclico aromático de 6 a 24 átomos de carbono dado el caso substituido o un resto heteroaromático de 5 a 24 átomos de carbono dado el caso substituido, por reacción de alfa-oxocarboxilatos de la fórmula general (I)
en la que n y m es un número en el intervalo de 1 a 6, M (m+)
es un catión y R tiene el significado indicado para la fórmula (III) , con bromuros de arilo de la fórmula general (II) R1-Br (II) en la que R1 tiene el significado indicado para la fórmula (III) , caracterizado porque como catalizador se utiliza una combinación de bromuro de cobre (I) con 1, 10-fenantrolina como ligando y bis (1, 1, 1, 5, 5, 5-hexafluoroacetilacetonato) paladio con tris (o-tolil) fosfina como ligando.
2. Procedimiento conforme a la reivindicación 1, en el que de ambos catalizadores se utilizan independientemente entre sí cantidades de 0, 001% en moles a 100% en moles referidas al compuesto de fórmula (II) .
3. Procedimiento conforme a una de las reivindicaciones 1 a 2, caracterizado porque el resto R en el compuesto de fórmula (III) es un resto fenilo, cianofenilo o terc-butilo.
4. Procedimiento conforme a una de las reivindicaciones 1 a 3, caracterizado porque el resto R1 en el compuesto de fórmula (III) es un resto tolilo, cianofenilo o metoxifenilo.
Patentes similares o relacionadas:
Inhibidores de lisina gingipaína, del 1 de Julio de 2020, de Cortexyme, Inc: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, en donde Z es ariloximetil-carbonilo sustituido con halógeno; […]
Derivados de 2,3-dihidro-1h-inden-1-ona como antagonistas de receptores huérfanos relacionados con el ácido retinoico gamma (ROR gamma) para el tratamiento de la esclerosis múltiple, del 1 de Abril de 2020, de Arrien Pharmaceuticals LLC: Un compuesto de acuerdo con la Fórmula I: **(Ver fórmula)** o una sal aceptable farmacéuticamente de este, en donde: X es O; R1 es **(Ver […]
Gamma-dicetonas como activadores de la ruta de señalización Wnt/beta-catenina, del 17 de Abril de 2019, de Samumed, LLC: Compuesto de fórmula: **Fórmula** 5 o una sal farmacéuticamente aceptable del mismo
PROCEDIMIENTO PARA PREPARAR ÉSTER METÍLICO DEL ÁCIDO 3-[(3S)-7-BROMO-2-OXO-5-(PIRIDIN-2-IL)-2,3-DIHIDRO-1H-[1,4]-BENZODIAZEPIN-3-IL] PROPIÓNICO, Y COMPUESTOS ÚTILES EN ESE PROCEDIMIENTO, del 29 de Enero de 2019, de MOEHS IBERICA, S.L.: Procedimiento para preparar éster metílico del ácido 3-[(3S)-7-bromo-2-oxo-5-(piridin-2-il)-2,3-dihidro-1H-[1,4]-benzodiazepin-3-il] propiónico, […]
Compuestos útiles como moduladores de TRPM8, del 9 de Enero de 2019, de SENOMYX INC.: Un compuesto heterocíclico de cinco miembros que tiene la fórmula estructural (Ia):**Fórmula** o una sal o un solvato del mismo; en la que R1 es arilo opcionalmente […]
Compuestos de diona cíclica activos como herbicidas, o derivados de los mismos, sustituidos por un fenilo que tiene un sustituyente que contiene alquinilo, del 17 de Enero de 2018, de SYNGENTA LIMITED: Un compuesto de fórmula (I): **(Ver fórmula)** , en donde: X es metilo o cloro; R1 es metilo o cloro; R2 es hidrógeno, metilo, etilo, […]
Dicetonas e hidroxicetonas como activadores de la vía de señalización de catenina, del 8 de Noviembre de 2017, de Samumed, LLC: Un compuesto o sal farmacéuticamente aceptable del mismo que tiene la estructura de Fórmula I: **(Ver fórmula)** en la que R1 es un heteroarilo sustituido o no sustituido, […]
PROCEDIMIENTO PARA LA SÍNTESIS DE DERIVADOS 1,2-DI(HETERO)ARILETANONAS Y 1,2,2-TRI(HETERO)ARILETANONAS EN AGUA, del 5 de Octubre de 2017, de UNIVERSIDAD DEL PAIS VASCO-EUSKAL HERRIKO UNIBERTSITATEA: Procedimiento para la síntesis de derivados 1,2-di(hetero)ariletanonas y 1,2,2-tri(hetero)ariletanonas en agua. La invención describe un nuevo procedimiento […]