CATÁLISIS DE LA SÍNTESIS DE DICETOPIPERAZINA.
Un método para la síntesis de 2,5-dicetopiperazina bis-3, 6 - [4-aminobutil] N-protegida que comprende la etapa de calentar una solución de lisina ε
-amino protegida en presencia de un catalizador seleccionado del grupo que consiste en ácido sulfúrico, ácido fosfórico, y pentóxido de fósforo y un disolvente seleccionado del grupo que consiste en m-cresol, glicol de etileno, tolueno y xilenos.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/029777.
Solicitante: MANNKIND CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 28903 NORTH AVENUE PAINE VALENCIA, CA 91355 ESTADOS UNIDOS DE AMERICA.
Inventor/es: MOYE-SHERMAN, DESTARDI, STEVENSON,John J.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07D241/08 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 241/00 Compuestos heterocíclicos que contienen ciclos de diazina-1,4 o diazina-1,4 hidrogenada. › con átomos de oxígeno unidos directamente a los átomos de carbono del ciclo.
PDF original: ES-2385934_T3.pdf
Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
A
Esta invención está generalmente en el campo de la síntesis química. Más particularmente se relaciona con la síntesis mejorada de las 2, 5-dicetopiperazina bis -3, 6 - [4aminobutil] N-protegidas.
ANTECEDENTES DE LA INVENCIÓN
La administración de medicamentos ha sido un problema persistente en el campo de la farmacéutica, en particular cuando un fármaco es inestable y / o mal absorbido en el locus en el cuerpo al que se administra. Dicha clase de medicamentos incluye 2, 5 dicetopiperazinas que tienen la estructura general de la Fórmula 1.
Estas 2, 5-dicetopiperazinas han demostrado ser útiles en la administración de fármacos, especialmente los que lleven grupos R acídicos (véase, por ejemplo la patente de EE.UU. N º 5, 352, 461 titulado " Sistemas auto-acoplables de administración del fármaco dicetopiperazina "; 5, 503, 852 titulado "Método para hacer sistemas auto-acoplables de administración del fármaco dicetopiperazina”, 6, 071, 497 titulado "micropartículas para la administración al pulmón comprendiendo dicetopiperazina;” y el 6.331.318 titulado "Sistema de administración de dicetopiperazina carbono-sustituido”, cada uno de los cuales se incorpora al presente por referencia en su totalidad por todo lo que enseña sobre dicetopiperazinas y la administración del fármaco mediada por dicetopiperazina) . Las dicetopiperazinas se pueden formar en las partículas que incorporan un fármaco o partículas a las que un medicamento puede ser adsorbido. La combinación de un medicamento y una dicetopiperazina puede impartir una mejora a la estabilidad del medicamento. Las partículas pueden ser administradas por distintas vías de administración. Como polvos secos estas partículas pueden ser administradas a áreas específicas del sistema respiratorio, dependiendo del tamaño de partícula. Las partículas se pueden hacer suficientemente pequeñas para su incorporación en dosis en forma de suspensión por vía intravenosa. También es posible la administración oral usada en suspensión, o como partículas comprimidas en pastillas o contenidas en una cápsula. Estas [0004] Un paso convencional en la síntesis de 2, 5-dicetopiperazina incluye la preparación de 2, 5-dicetopiperazina bis -3, 6 - [4-aminobutil] N-protegida por condensación térmica de la lisina. Los procesos convencionales de fabricación comercial utilizan (N-benciloxicarbonil) -lisina (Cbz-L-lisina) para producir 2, 5-dicetopiperazina bis-3, 6 - [ (N-benciloxicarbonil) -4-aminobutil] (DKP1) . Este proceso implica calentar Cbz-L-lisina en m-cresol de 18 a 22 horas a 160° C170°C, y proporciona DKP1 con un rendimiento promedio de 47, 5% después de la recristalización a partir de ácido acético glacial. [0005] Por lo tanto, el objeto de la presente invención es proporcionar mejores métodos de síntesis para dicetopiperazinas.
A
RESUMEN DE LA INVENCION
La presente invención proporciona métodos para la síntesis de dicetopiperazinas utilizando catalizadores de tal manera que se obtienen tiempos de reacción más rápidos y rendimientos mayores con respecto a método (s) de etapa (s) convencional (es) . Utilizar el catalizador de la presente invención, pentóxido fosfórico, en una reacción de ciclocondensación, facilita la síntesis de dicetopiperazinas de mayor rendimiento y una mayor pureza en tiempos de reacción más cortos sobre los método (s) de etapa (s) convencionales (es) . [0007] La presente invención proporciona un método para la síntesis de 2, 5-dicetopiperazina bis -3, 6 - [4-aminobutil] N-protegida que comprende el paso de calentar una solución de lisina protegida E –amino en presencia de un catalizador seleccionado del grupo consistente en ácido sulfúrico (H2SO4) , ácido fosfórico (H3PO4) y pentóxido de fósforo (P2O5) . [0008] Una realización de la presente invención proporciona un método para la síntesis de 2, 5dicetopiperazina bis -3, 6 - [4-aminobutil] N-protegida donde la lisina E-amino protegida es (Nbenciloxicarbonil) -lisina (Cbz-L-lisina) y el producto es el 2, 5-dicetopiperazina bis-3, 6 - [ (Nbenciloxicarbonil) -4-aminobutil] (DKP1) . [0009] Otra forma de realización de la presente invención proporciona un método para la síntesis de 2, 5-dicetopiperazina bis -3, 6 - [4-aminobutil] N-protegida en donde la solución se calienta a una temperatura nominal de unos 160° C hasta 170° C. Esta temperatura deseada se alcanza preferiblemente en aproximadamente 4 a 6 horas. [0010] En otra realización de la presente invención se facilita un método para la síntesis de 2, 5dicetopiperazina bis -3, 6 - [4-aminobutil] N-protegida que comprende el paso de calentamiento de una solución de lisina E-amino protegida en presencia de un catalizador con lo que la síntesis se completa sustancialmente en aproximadamente 10 horas para llegar a la temperatura objetivo. Más preferiblemente, la síntesis se completa en aproximadamente 8 horas, 6 horas, 4 horas, 3 horas, o 2 horas de alcanzar la temperatura objetivo. Más preferiblemente, la síntesis estará completa en alrededor de 1, 5 horas de llegar a la
temperatura objetivo. [0011] Otra forma de realización de la presente invención proporciona un método para la síntesis de 2, 5-dicetopiperazina bis -3, 6 - [4-aminobutil] N-protegida que comprende la etapa de calentamiento de una solución de lisina E-amino protegida, tales como (N-benziloxicarbonil)
A
lisina (Cbz-L-lisina) , en presencia de un catalizador, como el pentóxido de fósforo, en donde la síntesis tiene un rendimiento de más del 50%. [0012] Otra realización de la presente invención proporciona un método para la síntesis de 2, 5dicetopiperazina bis -3, 6 - [4-aminobutil] N-protegida n presencia del catalizador de pentóxido de fósforo, la concentración de fósforo pentóxido es cerca de 5% a 10%. [0013] Estos y otros objetos, ventajas y características de la invención serán plenamente comprendidos y apreciados en función de la especificación escrita.
BREVE DESCRIPCIÓN DE LOS DIBUJOS
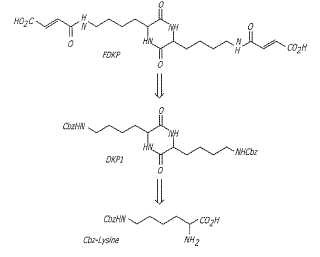
La figura. 1 representa en síntesis un diagrama de flujo de 2, 5-diceto-3 , 6-di (4fumarilaminobutil) piperazina (fumaril dicetopiperazina, FDKP) de acuerdo a un aspecto de la presente invención. [0015]La figura. 2 representa en síntesis un diagrama de flujo de 2, 5-dicetopiperazina bis-3, 6 -[ (N-benciloxicarbonil) -4-aminobutil] (DKP1) de acuerdo con un aspecto de la invención. [0016] La figura. 3 representa la conversión de (N-benciloxicarbonil) -lisina) Cbz-L-lisina para DKP1 utilizando los métodos de catálisis de ácido sulfúrico de acuerdo a un aspecto de la presente invención. [0017] La figura. 4 representa la conversión de Cbz-L-lisina para DKP1 utilizando los métodos de catálisis de ácido fosfórico de acuerdo con un aspecto de la presente invención. [0018]LLa figura. 5 representa la conversión de Cbz-L-lisina para DKP1 utilizando los métodos de catálisis de pentóxido fosforoso de acuerdo con un aspecto de la presente invención. [0019] La figura. 6 muestra una comparación de los tres catalizadores de acuerdo a un aspecto de la presente invención. [0020] La figura. 7 representa la secuencia de la reacción de la ciclodimerización P2O5catalizada de acuerdo a un aspecto de la presente invención. [0021] La figura. 8 representa el rendimiento global de DKP1 en función del tiempo utilizando el catalizador de pentóxido de fósforo en la presente invención (reacción a escala 5 litros) .
DESCRIPCIÓN DETALLADA DE LA INVENCIÓN
La presente invención proporciona métodos para la síntesis de dicetopiperazinas utilizando catalizadores de manera que se obtienen tiempos más rápidos de reacción y mayores rendimiento con respecto a método (s) de etapa (s) convencionales (es) . Utilizando el catalizador de la invención, anhídrido fosfórico, en una reacción ciclocondensación, prevé la
síntesis de dicetopiperazinas de mayor rendimiento y una mayor pureza en los tiempos de reacción más cortos que en los paso (s) o método (s) convencionales. [0023] La síntesis convencional de dicetopiperazinas útil en la administración de fármacos, tales como 2, 5-diceto-3 , 6-di (4-fumarilaminobutil) piperazina (fumaril dicetopiperazina, FDKP) , comienza comúnmente en la ciclocondensación térmica de lisina 0 amino protegida, por ejemplo (N-benciloxicarbonil) -lisina (Cbz-L-lisina) (ver Fig.. 1 y 2) . La reacción no catalizada es larga, 18 a 33 horas, con rendimientos por debajo del 50% y en algunos casos tan poco como 25%. Estas largas reacciones y rendimientos relativamente... [Seguir leyendo]
Reivindicaciones:
ReiVindicaciones
1.
6. [4-aminobutil] N-protegida que comprende la etapa de calentar una solución de lisina E-amino protegida en presencia de un catalizador seleccionado del grupo que consiste en ácido sulfúrico, ácido fosfórico, y pentóxido de fósforo y un disolvente seleccionado del grupo que consiste en m-cresol, glicol de etileno, tolueno y xilenos.
2. El método de la reivindicación 1 donde dicha lisina E-amino protegida es (Nbenciloxicarbonil) -lisina (Cbz-L-lisina) .
3. El método de la reivindicación 1 en donde el catalizador es ácido sulfúrico.
4. El método de la reivindicación 1 en donde el catalizador es ácido fosfórico.
5. El método de la reivindicación 1 en donde el catalizador es pentóxido de fósforo.
6. El método de la reivindicación 5 en donde la concentración de pentóxido de fósforo es del 5% al 10%.
7. El método de la reivindicación 6 en donde la concentración de pentóxido de fósforo es de 7, 5%.
8. El método de la reivindicación 1 en donde la solución se calienta a una temperatura objetivo de 160 ° C a 170 ° C.
9. El método de la reivindicación 8 en donde la temperatura deseada se alcanza en 4-6 horas.
10. El método de la reivindicación 8 en donde la síntesis se mantiene a una temperatura objetivo durante un máximo de 10 horas.
11. El método de la reivindicación 8 en donde la síntesis se mantiene a una temperatura objetivo durante un máximo de 8 horas.
12. El método de la reivindicación 8 en donde la síntesis se mantiene a una temperatura objetivo durante un máximo de 4 horas.
13. El método de la reivindicación 8 en donde la síntesis se mantiene a una temperatura objetivo durante un máximo de 3 horas.
14. El método de la reivindicación 8 en donde la síntesis se mantieneabo a una temperatura objetivo durante un máximo de 1, 5 horas.
15. El método de las reivindicaciones 4 y 5 en donde dicha síntesis tiene un rendimiento de más del 50%. FIG 1
A
A
A
A
A
A
REFERENCIAS CITADAS EN LA DESCRIPCI0N
Este listado de referencias citadas por el solicitante tiene como único fin la conveniencia del lector. No forma parte del documento de la Patente Europea. Aunque se ha puesto gran
cuidado en la compilación de las referencias, no pueden excluirse errores u omisiones y la OEP rechaza cualquier responsabilidad en este sentido.
Documentos de patente citados en la descripcion
• US 5352461 A [0003] • US 6071497 A [0003]
• US 5503852 A [0003] • US 6331318 B [0003] 10 Literatura no relacionada con patentes citada en la descripcion
•
39. 3[0024]
•
12. 134 [0024]
• Erlanger. Pentóxido de fósforo como un reactivo en síntesis péptido J. Org. Chem., 1961, vol. 26, 2534-6 [0024]
Patentes similares o relacionadas:
Extracto vegetal que contiene dicetopiperazina y método de producción del mismo, del 18 de Marzo de 2020, de SUNTORY HOLDINGS LIMITED: Un extracto vegetal que comprende al menos uno de ciclo-alanil-glutamina, ciclo-alanil-alanina, ciclo-seril-tirosina, ciclo-glicil-leucina, ciclo-glicil-triptófano, ciclo-valil-valina, […]
Inhibidores de benzimidazol del canal de sodio, del 18 de Diciembre de 2019, de Zalicus Pharmaceuticals Ltd: Un compuesto seleccionado del grupo que consiste en **(Ver fórmula)** o una sal o solvato farmacéuticamente aceptable del mismo.
Derivados de N-acetil-L-cisteína sustituidos y compuestos relacionados, del 6 de Noviembre de 2019, de Promentis Pharmaceuticals, Inc: Un compuesto de la fórmula I **(Ver fórmula)** o una sal aceptable farmacéuticamente de este.
Composiciones y métodos de dicetopiperazina microcristalina, del 21 de Agosto de 2019, de MANNKIND CORPORATION: Una composición cristalina de 3,6-bis(N-fumaril-4-aminobutil)-2,5-dicetopiperazina que comprende una pluralidad de partículas microcristalinas de tamaño uniforme […]
Nueva síntesis quiral de N-acil-(3-sustituida)-(8-sustituida)-5,6-dihidro-[1,2,4]triazolo [4,3-a] pirazinas, del 30 de Abril de 2019, de OGEDA SA: Un procedimiento de preparación de N-acil-(3-sustituida)-(8-sustituida)-5,6-dihidro-[1,2,4]triazolo[4,3-a] pirazina quiral de fórmula general I:**Fórmula** o solvatos […]
Compuestos de indanilurea inhibidores de MAP quinasa P38, del 27 de Marzo de 2019, de Torrent Pharmaceuticals Limited: Un Compuesto de la fórmula (I)**Fórmula** sus sales farmacéuticamente aceptables y sus estereoisómeros, atropisómeros, conformadores, tautómeros, polimorfos, hidratos, […]
Compuestos inhibidores de Apaf-1, del 27 de Febrero de 2019, de Spiral Therapeutics, Inc: Los derivados de 2,5-piperazinadiona de fórmula (I) son inhibidores del factor 1 activador de Ia peptidasa apoptótica (Apaf-1, Apoptotic Peptidase […]
Arilsulfonamidas 2,5-disustituidas antagonistas de CCR3, del 20 de Diciembre de 2017, de SMA Therapeutics, Inc: Un compuesto de Fórmula II, o una sal, un solvato, un hidrato, un estereoisómero o un tautómero farmacéuticamente aceptable del mismo: **(Ver fórmula)** […]