Aparato para analizar muestras de fluidos biológicos sustancialmente no diluidas.
Un aparato para ensayar una muestra de fluido biológico que reside de manera estable dentro de una cámara (20),
comprendiendo dicho aparato:
un iluminador (40) de campo para iluminar de manera selectiva un campo de la muestra, teniendo dicho campo un área conocida o averiguable;
un posicionador (86), que es operable para cambiar de manera selectiva la posición de uno de la cámara (20) o dicho iluminador de campo en relación al otro de la cámara o dicho iluminador de campo, permitiendo de este modo la iluminación selectiva de una pluralidad de dichos campos de muestra dentro de la cámara;
un disector (42) de imágenes, para convertir una imagen de la luz que pasa a través o emana de cada uno de dichos campos de la muestra en un formato de datos electrónico útil para fines de ensayo; caracterizado por comprender además:
medios para determinar uno de un grosor (78) de plano transversal o un volumen de cada uno de dichos campos de muestra.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US1999/004513.
Solicitante: WARDLAW, STEPHEN CLARK.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: HIGHROCK LYME, CT 06371 ESTADOS UNIDOS DE AMERICA.
Inventor/es: LEVINE, ROBERT AARON, WARDLAW, STEPHEN CLARK.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- G01N15/00 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › Investigación de características de partículas; Investigación de la permeabilidad, del volumen de los poros o del área superficial efectiva de los materiales porosos (identificación de microorganismos C12Q).
- G01N15/05 G01N […] › G01N 15/00 Investigación de características de partículas; Investigación de la permeabilidad, del volumen de los poros o del área superficial efectiva de los materiales porosos (identificación de microorganismos C12Q). › en la sangre.
- G01N15/14 G01N 15/00 […] › Investigación por medios electroópticos.
- G01N21/64 G01N […] › G01N 21/00 Investigación o análisis de los materiales por la utilización de medios ópticos, es decir, utilizando rayos infrarrojos, visibles o ultravioletas (G01N 3/00 - G01N 19/00 tienen prioridad). › Fluorescencia; Fosforescencia.
- G01N33/48 G01N […] › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Material biológico, p. ej. sangre, orina (G01N 33/02, G01N 33/26, G01N 33/44, G01N 33/46 tienen prioridad ); Hemocitómetros (cómputo de glóbulos repartidos sobre una superficie por barrido óptico de la superficie G06M 11/02).
- G01N33/483 G01N 33/00 […] › Análisis físico de material biológico.
- G01N33/49 G01N 33/00 […] › de sangre.
- G01N33/50 G01N 33/00 […] › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
PDF original: ES-2380511_T3.pdf
Fragmento de la descripción:
Aparato para analizar muestras de fluidos biológicos sustancialmente no diluidas ANTECEDENTES DE LA INVENCIÓN
1. Campo técnico
La presente invención se refiere a un aparato para analizar muestras de fluidos biológicos en general, y a aparatos capaces de realizar análisis en diversas disciplinas, que incluyen hematología, química biológica, inmunoquímica, serología, inmunología y urinálisis en particular.
2. Información de los antecedentes
Históricamente, las muestras de fluidos biológicos tales como sangre entera, orina, fluido cerebroespinal, fluidos de cavidades corporales, etc. han sido evaluadas en cuanto a su contenido de partículas o células haciendo un frotis de una pequeña cantidad sin diluir del fluido en un portaobjetos y evaluando ese frotis bajo un microscopio. Se pueden obtener resultados razonables a partir de tal frotis, pero la exactitud y fiabilidad de los datos dependen en gran medida de la experiencia y técnica del técnico. Además, aunque los frotis de muestras de fluidos biológicos se usan ampliamente para fines de evaluación, la naturaleza intensiva de su trabajo hace que generalmente no sean favorables para aplicaciones comerciales.
Otro método conocido para evaluar una muestra de fluido biológico implica diluir un volumen de la muestra, colocarla dentro de una cámara, y evaluar y enumerar manualmente los constituyentes dentro de la muestra diluida. La dilución es necesaria si hay una alta concentración de constituyentes dentro de la muestra, y para recuentos de sangre rutinarios se pueden requerir varias diluciones diferentes, porque no es práctico tener cámaras o aparatos de 20 recuento que puedan examinar volúmenes variables como medios para compensar las disparidades en las poblaciones constituyentes dentro de la muestra. En una muestra de sangre entera de un individuo típico, por ejemplo, hay aproximadamente 4, 5 x 106 células rojas de la sangre (RBCs, por sus siglas en inglés) por microlitro (1l) de muestra de sangre, pero sólo aproximadamente 0, 25 x 106 de plaquetas y 0, 007 x 106 de células blancas de la sangre (WBCs, por sus siglas en inglés) por 1l de muestra de sangre. Para determinar un recuento de WBCs, la 25 muestra de sangre entera debe ser diluida dentro de un intervalo de aproximadamente una parte de sangre a veinte partes de diluyente (1:20) hasta una dilución de aproximadamente 1:256 dependiendo de la técnica de dilución exacta usada, y es también necesario, de manera general, lisar de manera selectiva los RBCs con uno o más reactivos. Lisar los RBCs los retira de manera eficaz de la visión, de tal modo que los WBCs se pueden ver. Para determinar un recuento de plaquetas, la muestra de sangre se debe diluir dentro de un intervalo de 1:100 a 1:50.000.
Los recuentos de plaquetas, sin embargo, no requieren una lisis de los RBCs en la muestra. Una desventaja de evaluar una muestra de sangre entera de esta manera es que el procedimiento de dilución requiere mucho tiempo y es caro. Además, añadir diluyentes a la muestra de sangre entera aumenta la probabilidad de error en los datos de la muestra. Añadir diluyentes también aumenta la cantidad de material residual que debe ser desechado tras completarse el ensayo.
Un método moderno para evaluar una muestra de fluido biológico es la citometría de flujo óptica o por impedancia. La citometría de flujo implica hacer circular una muestra de fluido diluida a través de uno o más orificios de pequeño diámetro, empleando cada una un sensor de tipo impedancia o de tipo óptico que evalúa los constituyentes según pasan a través del orificio en fila de a uno. Usando el ejemplo de la sangre entera de nuevo, la muestra debe ser diluida para mitigar el abrumador número de RBCs en relación a los WBCs y las plaquetas, y para proporcionar un espaciado célula a célula adecuado, de tal modo que se puedan analizar células individuales. Aunque más apropiados y consistentes que los métodos descritos anteriormente, los citómetros de flujo también poseen numerosas desventajas. Algunas de esas desventajas provienen de la instalación de tuberías requerida para llevar la muestra a, y los controles de fluido necesarios para controlar la velocidad de flujo del fluido a través de, los medios sensores. El control preciso de este flujo es esencial para el funcionamiento exacto del citómetro. La 45 instalación de tuberías dentro de los citómetros de flujo puede, y a menudo lo hace, tener fugas, comprometiendo potencialmente la exactitud y la seguridad del equipo. Los controles de flujo del fluido y el equipo de dilución requieren una recalibración periódica. De hecho, la necesidad de recalibración ilustra el potencial para que haya resultados inexactos y los indeseables costes de funcionamiento que existen con muchos analizadores de hematología disponibles en la actualidad que usan orificios de citómetros de flujo y/o de impedancia. El volumen de 50 reactivos requeridos para satisfacer grandes relaciones de dilución aumenta el coste de funcionamiento, inicialmente en virtud del precio de compra de los reactivos y posteriormente debido a los costes adicionales de desecho de residuos.
Otro método moderno para evaluar muestras de fluidos biológicos es uno que se centra en evaluar subtipos específicos de WBCs. Este método utiliza una cubeta que tiene una cámara interna de aproximadamente 25 55 micrómetros de grosor con un panel transparente. Un rayo láser de luz que pasa a través del panel transparente escanea la cubeta en cuanto a los WBCs. Los reactivos añadidos a la muestra causan que cada WBC fluorezca cuando es excitado por el rayo láser. La fluorescencia de los WBCs particulares proporciona una indicación de qué tipos particulares de WBCs están presentes. Como las células rojas de la sangre forman una capa parcialmente
oscurecedora en este método, no pueden ser enumeradas o evaluadas de otro modo en sí mismas, ni tampoco las plaquetas.
Hay una multitud de métodos para determinar la presencia de constituyentes solubles, tales como componentes químicos, anticuerpos, etc., dentro de una muestra de fluido biológico tal como orina, plasma o suero. La mayoría de los métodos requieren la dilución de la muestra y la adición de uno o más reactivos a la muestra. Otros métodos requieren que una pequeña pero cuidadosamente medida gota de muestra de fluido biológico sea añadida a un trozo de película reactiva. Se requieren usualmente diferentes instrumentos analíticos para cada método de análisis, y esos instrumentos son caros, no sólo en términos de coste de capital inicial, sino también en términos del mantenimiento a lo largo de la vida de los diversos instrumentos, y la formación de los operadores necesaria para proveer de personal apropiadamente a los diversos instrumentos. La función de los operadores puede variar considerablemente de instrumento a instrumento, aumentando de este modo la complejidad de la formación de los operadores y el potencial para el error de los operadores. Hasta la fecha, debido a los ampliamente diferentes requerimientos de los diversos ensayos, no hay una única plataforma de instrumentos que realice ensayos interdisciplinares, lo más especialmente ensayos de hematología, que requieren análisis de partículas, y ensayos de química/inmunología o serología, que requieren análisis de luz cuantitativos.
Lo que se necesita es un método y un aparato para evaluar una muestra de fluido biológico sustancialmente sin diluir, uno capaz de proporcionar resultados exactos, uno que no use un volumen significativo de reactivo (s) , uno que no requiera flujo del fluido de muestra durante la evaluación, uno que pueda realizar análisis de componentes en partículas y de componentes químicos, y uno que sea rentable.
El documento US-5646046 describe un instrumento para realizar automáticamente análisis en relación con la trombosis y hemostasis.
El documento US-5547849 describe un aparato y método para citometría capilar volumétrica. El documento US4171866 describe un portaobjetos volumétrico desechable.
DESCRIPCIÓN DE LA INVENCIÓN
Es, por tanto, un objeto de la presente invención proporcionar un aparato para analizar muestras de fluidos biológicos que tiene la capacidad de proporcionar datos analíticos para diversas disciplinas, que incluyen, pero no se limitan a, hematología, química biológica, inmunoquímica, serología, inmunología, urinálisis, inmunoensayo, sensi- bilidad a antibióticos y crecimiento bacteriano.
Es otro objeto de la presente invención proporcionar un único aparato para analizar muestras de fluidos biológicos... [Seguir leyendo]
Reivindicaciones:
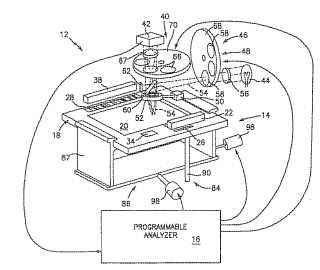
1. Un aparato para ensayar una muestra de fluido biológico que reside de manera estable dentro de una cámara (20) , comprendiendo dicho aparato:
un iluminador (40) de campo para iluminar de manera selectiva un campo de la muestra, teniendo dicho campo un área conocida o averiguable;
un posicionador (86) , que es operable para cambiar de manera selectiva la posición de uno de la cámara (20) o dicho iluminador de campo en relación al otro de la cámara o dicho iluminador de campo, permitiendo de este modo la iluminación selectiva de una pluralidad de dichos campos de muestra dentro de la cámara;
un disector (42) de imágenes, para convertir una imagen de la luz que pasa a través o emana de cada uno de dichos campos de la muestra en un formato de datos electrónico útil para fines de ensayo; caracterizado por comprender además:
medios para determinar uno de un grosor (78) de plano transversal o un volumen de cada uno de dichos campos de muestra.
2. Un aparato según la reivindicación 1, que comprende además medios para recuperar información que concierne al recipiente (18) , información que se usa en la realización de uno o más ensayos en la muestra de fluido biológico por dicho aparato.
3. Un aparato según la reivindicación 2, en el que dichos medios para recuperar información incluyen un lector (38) de etiquetas para leer una etiqueta (28) relacionada con la cámara (20) .
4. Un aparato según la reivindicación 3, en el que dicho lector (38) de etiquetas lee ópticamente las etiquetas (28) .
5. Un aparato según la reivindicación 3, en el que dicho lector (38) de etiquetas lee magnéticamente las etiquetas (28) .
6. Un aparato según la reivindicación 3, que comprende además:
un analizador (16) programable que tiene una unidad central de proceso;
en el que dicho lector (38) de etiquetas transfiere dicha información a dicho analizador programable, y dicho analizador programable interpreta dicha información, identificando dichos uno o más ensayos a ser realizados en la muestra de fluido biológico.
7. Un aparato según la reivindicación 6, en el que dicho analizador programable (16) contiene una pluralidad de instrucciones para realizar dichos uno o más ensayos.
8. Un aparato según la reivindicación 7, en el que dicha pluralidad de instrucciones están contenidas de manera remota de dicho analizador (16) programable y son accedidas mediante dicho analizador programable.
9. Un aparato según la reivindicación 7, en el que dicha pluralidad de instrucciones incluye medios para controlar dicho iluminador (40) de campo y dicho posicionador (86) .
10. Un aparato según la reivindicación 9, en el que dicho posicionador (86) incluye medios para situar espacialmente dicha cámara (20) en relación a dicho iluminador (40) de campo;
en el que dichos medios para situar espacialmente dicha cámara en relación a dicho iluminador permiten que dicho iluminador de campo sea alineado con cualquier ubicación espacial particular dentro de dicha cámara.
11. Un aparato según la reivindicación 10, en el que se usa una dirección de coordenadas para describir ubicaciones espaciales particulares dentro de dicha cámara (20) .
12. Un aparato según la reivindicación 11, en el que dicha información recuperada por dicho lector (38) de etiquetas se refiere a rasgos dentro de la cámara (20) .
13. Un aparato según la reivindicación 1, en el que dicho iluminador (40) de campo comprende:
una fuente (44) de luz que produce luz dentro de un intervalo de longitudes de onda lo suficientemente amplio para ser útil para una pluralidad de ensayos en la muestra de fluido biológico; y un montaje de óptica (46) de objetivo, en el que dicha óptica dirige la luz que emana de dicho campo de muestra o es transmitida a través de dicho campo de muestra hacia una imagen de área conocida o averiguable de luz en dicho disector (42) de imágenes.
14. Un aparato según la reivindicación 13, en el que dicho montaje de la óptica (46) de objetivo comprende:
una lente (52) de objetivo; un mecanismo (50) de enfoque, dicho mecanismo para ajustar de manera selectiva la posición de dicha lente (52) de objetivo en relación a la cámara (20) ; y un filtro (58, 66) de la luz para bloquear o dejar pasar ciertas longitudes de onda de dicha luz;
en donde otras longitudes de onda de dicha luz que emanan de dicha fuente de luz pasan a través de dicha lente (52) de objetivo y dicho filtro (58, 66) de la luz y hacia dicho disector (42) de imágenes, o son bloqueadas, respecti- vamente.
15. Un aparato según la reivindicación 14, en el que dicho iluminador (40) de campo dirige la luz hacia dicha muestra dentro de la cámara (20) y recoge la luz que fluoresce de dicha muestra.
16. Un aparato según la reivindicación 15, en el que dicho filtro de la luz comprende: una pluralidad de filtros (58) de excitación de la fuente de luz; una pluralidad de filtros (66) de emisión de la muestra; en el que dichos filtros de excitación de la fuente de luz bloquean longitudes de onda seleccionadas de dicha luz
que emana de dicha fuente (44) de luz y dichos filtros de emisión de la muestra bloquean longitudes de onda seleccionadas de dicha luz que fluoresce de dicha muestra.
17. Un aparato según la reivindicación 16, en el que dichos filtros (58) de excitación de la fuente de luz están montados en una primera rueda (68) y dichos filtros (66) de emisión de la muestra están montados en una segunda rueda (70) y ambos de dichos filtros son giratorios dentro y fuera de un camino de dicha luz; y
en el que dicho iluminador (40) de campo comprende además medios para sincronizar dicha primera rueda y dicha segunda rueda de tal modo que todas las combinaciones deseables de dichos filtros de excitación de la fuente de luz y dichos filtros de emisión de la muestra se pueden usar durante dichos ensayos.
18. Un aparato según la reivindicación 16, en el que dicho iluminador (40) de campo comprende además:
un prisma (60) desviador de la luz; y un detector (62) de referencia que tiene medios para cuantificar un nivel de energía de dicha luz que emana de dicha fuente (44) de luz, en donde dicho nivel de energía cuantificado se usa de manera selectiva en la evaluación de dicha luz que fluoresce de dicha muestra.
19. Un aparato según la reivindicación 14, en el que dicho iluminador (40) de campo dirige la luz hacia dicha cámara (20) que contiene dicha muestra y recoge la luz producida por transmitancia que pasa a través de dicha muestra.
20. Un aparato según la reivindicación 19, en el que dicho filtro de luz comprende: una pluralidad de filtros (58) de excitación de la fuente de luz; una pluralidad de filtros (66) de emisión de la muestra; en el que dichos filtros de excitación de la fuente de luz bloquean longitudes de onda de dicha luz que emana de
dicha fuente (44) de luz y dichos filtros de emisión de la muestra bloquean longitudes de onda de dicha luz que emana de dicha muestra.
21. Un aparato según la reivindicación 20, en el que dichos filtros (58) de excitación de la fuente de luz están montados en una primera rueda (68) y dichos filtros (66) de emisión de la muestra están montados en una segunda rueda
(70) y ambas de dichas ruedas permiten la rotación de dichos filtros dentro y fuera de un camino de dicha luz; y en el que dicho iluminador (40) de campo comprende además medios para sincronizar dicha primera rueda y dicha segunda rueda de tal modo que todas las combinaciones deseables de dichos filtros de excitación de la fuente de luz y dichos filtros de emisión de la muestra se pueden usar durante dichos ensayos.
22. Un aparato según la reivindicación 21, en el que dicho iluminador (40) de campo comprende además:
un prisma (60) desviador de la luz; y un detector (62) de referencia que tiene medios para cuantificar un nivel de energía de dicha luz que emana de dicha fuente (44) de luz, en donde dicho nivel de energía cuantificado se usa de manera selectiva en la evaluación de dicha luz que emana de dicha muestra por fluorescencia.
23. Un aparato según la reivindicación 2, en el que dichos medios para determinar uno de dicho grosor de plano
transversal o dicho volumen de dicho campo de muestra incluyen dichos medios de recuperación de información que recuperan información de una etiqueta (28) concerniente a la cámara (20) , información que incluye uno de dicho grosor de plano transversal de dicho campo de muestra o dicho volumen de dicho campo de muestra.
24. Un método para ensayar una muestra de fluido biológico, que comprende las etapas de:
proporcionar un recipiente (18) para contener la muestra, teniendo dicho recipiente una cámara (20) con una primera pared (30) y una segunda pared (32) transparente, y una etiqueta (28) unida a dicho recipiente, conteniendo dicha etiqueta información que se usa en la realización de uno o más ensayos;
proporcionar un módulo (14) lector que recibe dicho recipiente, incluyendo dicho módulo lector un lector (38) de etiquetas para leer dicha etiqueta y un iluminador (40) de campo para iluminar de manera selectiva un campo de la muestra, teniendo dicho campo un área conocida o averiguable;
depositar dicha muestra dentro de dicha cámara, en donde dicha muestra reside de manera estable en dicha cámara después de eso;
leer dicha etiqueta con dicho lector de etiquetas, comunicando de este modo a dicho módulo lector desde dicho recipiente dicha información, que se usa en la realización de dichos uno o más ensayos;
producir una imagen de manera selectiva de una pluralidad de dichos campos de muestra usando dicho iluminador de campo; y determinar uno de un grosor (78) de plano transversal o un volumen de cada uno de dichos campos de muestra.
25. Un método según la reivindicación 24, que comprende además las etapas de:
proporcionar un posicionador (86) dentro de dicho módulo (14) lector, siendo dicho posicionador operable para cambiar de manera selectiva la posición de uno de dicha cámara (20) o dicho iluminador (40) de campo en relación al otro de dicha cámara o dicho iluminador de campo;
posicionar de manera selectiva dicha cámara en relación a dicho iluminador de campo.
26. Un método según la reivindicación 25, que comprende además las etapas de:
proporcionar medios para ubicar espacialmente dicha cámara (20) en relación a dicho iluminador (40) de campo;
posicionar dicho iluminador de campo en relación a dicha cámara usando dichos medios ubicadores espacialmente.
27. Un método según la reivindicación 26, que proporciona además la etapa de:
proporcionar un grosor de plano transversal o un volumen de dicho campo de muestra y una ubicación espacial de dicho campo de muestra como parte de dicha información usada en la realización de dichos uno o más ensayos.
28. Un método según la reivindicación 26, que comprende además las etapas de:
proporcionar una concentración conocida de un colorante sensible distribuido uniformemente dentro de la muestra, teniendo dicho colorante sensible una relación señal a concentración conocida; proporcionar dicha concentración, dicha relación señal a concentración, y una ubicación espacial de dicho campo de muestra como parte de dicha información usada en la realización de dichos uno o más ensayos;
posicionar dicho iluminador (40) de campo para alinearlo con dicho campo de muestra en dicha ubicación espacial; producir una imagen de dicho campo de muestra; determinar un volumen de dicho campo de muestra usando dicha información, que incluye dicha imagen de dicho campo de muestra, dicha concentración y dicha relación señal a concentración.
29. Un método según la reivindicación 28, que comprende además las etapas de:
proporcionar un reservorio (22) unido a dicho recipiente (18) y una válvula (26) operable de manera selectiva, dispuesta funcionalmente entre dicho reservorio y dicha cámara (20) ; depositar dicha muestra dentro de dicho reservorio antes de dichos uno o más ensayos;
iniciar un periodo de tiempo de ensayo accionando de manera selectiva dicha válvula para dejar que dicha muestra se transfiera de dicho reservorio a dicha cámara.
30. Un método según la reivindicación 26, en el que dicha etapa de determinar uno de un grosor (78) de plano transversal o un volumen incluye:
proporcionar un colorante sensible distribuido uniformemente dentro de la muestra, teniendo dicho colorante sensible una relación señal a concentración;
proporcionar, como parte de dicha información usada en la realización de los uno o más ensayos, una primera ubicación espacial para ubicar un primer campo de muestra, una segunda ubicación espacial para ubicar un segundo campo de muestra, en donde dichos primer y segundo campos tienen volúmenes iguales, y una característica geométrica que tiene un volumen conocido, estando dicha característica posicionada dentro de uno de dichos primer o segundo campos de muestra;
posicionar dicho iluminador (40) de campo para alinearlo con dicha primera ubicación espacial;
producir una imagen de dicho primer campo de muestra;
posicionar dicho iluminador de campo para alinearlo con dicha segunda ubicación espacial;
producir una imagen de dicho segundo campo de muestra;
determinar dicho volumen de uno de dichos primer o segundo campo de muestras usando dichas imágenes de dichos primer y segundo campos de muestra, dicho volumen conocido de dicha característica geométrica, y dicha relación señal a concentración.
31. Un método según la reivindicación 26, en el que dicha etapa de determinar uno de un grosor (78) de plano transversal o un volumen incluye:
proporcionar un colorante sensible distribuido uniformemente dentro de la muestra, teniendo dicho colorante sensible una relación señal a concentración;
proporcionar, como parte de dicha información usada en la realización de los uno o más ensayos, una primera ubicación espacial para ubicar un primer campo de muestra, una segunda ubicación espacial para ubicar un segundo campo de muestra, en el que dichos primer y segundo campos tienen volúmenes iguales, y una característica geométrica posicionada dentro de uno de dichos primer o segundo campos de muestra, teniendo dicha característica una altura conocida;
posicionar dicho iluminador (40) de campo para alinearlo con dicha primera ubicación espacial;
producir una imagen de dicho primer campo de muestra;
posicionar dicho iluminador de campo para alinearlo con dicha segunda ubicación espacial;
producir una imagen de dicho segundo campo de muestra;
determinar dicho volumen de uno de dichos primer o segundo campo de muestras usando dichas imágenes de dichos primer y segundo campos de muestra, dicha altura conocida de dicha característica geométrica, y dicha relación señal a concentración.
Patentes similares o relacionadas:
Método para analizar ácido nucleico molde, método para analizar sustancia objetivo, kit de análisis para ácido nucleico molde o sustancia objetivo y analizador para ácido nucleico molde o sustancia objetivo, del 29 de Julio de 2020, de Kabushiki Kaisha DNAFORM: Un método para analizar un ácido nucleico molde, que comprende las etapas de: fraccionar una muestra que comprende un ácido nucleico molde […]
Nanoparticulas de AG2S súper fluorescentes en la región del infrarrojo cercano y metódo de obtención, del 15 de Julio de 2020, de UNIVERSIDAD COMPLUTENSE DE MADRID: Nanopartículas de Ag2S súper fluorescentes en la región del infrarrojo cercano y método de obtención. El marcaje con sondas fluorescentes […]
DISPOSITIVO DE MONITORIZACIÓN DE SUSTANCIAS TÓXICAS EN AGUA Y SISTEMA QUE LO COMPRENDE, del 7 de Julio de 2020, de UNIVERSITAT ROVIRA I VIRGILI: Dispositivo de monitorización de sustancias tóxicas en agua y sistema que lo comprende. El dispositivo incorpora una cámara de referencia con un filtro depurativo […]
Ensayo de toxina botulínica con sensibilidad mejorada, del 1 de Julio de 2020, de BioMadison, Inc: Un método para aumentar la sensibilidad de la detección basada en células de una toxina botulínica, que comprende: (i) proporcionar una célula […]
Kit, su uso y procedimiento para la calibración de un sistema de medición de fotoluminiscencia, del 24 de Junio de 2020, de BAM BUNDESANSTALT FUR MATERIALFORSCHUNG UND -PRUFUNG: Kit para la calibracion trazable de un sistema de medicion de fotoluminiscencia, que comprende: a) al menos en cada caso uno de los siguientes patrones de fluorescencia (i) […]
Monitor de aerosol en tiempo real, del 17 de Junio de 2020, de Wuxi Maitong Scientific Instrument Co., Ltd: Un monitor de aerosol en tiempo real, que comprende: un conjunto de fuente de luz láser , configurado para emitir un rayo láser y generar […]
Un sistema óptico integrado para el examen de materiales de muestra, del 10 de Junio de 2020, de Iris Technology Solutions SL: Un sistema óptico que comprende: una fuente de luz ; un sistema de suministro de luz que comprende un reflector de una primera abertura […]
Dispositivo de soporte de elementos cromóforos, del 3 de Junio de 2020, de Genewave: Dispositivo de tipo biochip que comprende un sustrato cuya capa superficial forma una guía de onda plana , llevando dicha capa superficial elementos […]