Anticuerpos humanizados que reconocen el péptido beta amiloide.
Una inmunoglobulina 12A11 humanizada o fragmento de unión a antígeno de la misma que comprende una cadena ligera de inmunoglobulina humanizada que comprende las regiones determinantes de complementariedad (CDR) de región variable de la secuencia de región variable de cadena ligera de inmunoglobulina 12A11 de SEC ID Nº:
2 y una cadena pesada de inmunoglobulina humanizada que comprende las regiones determinantes de complementariedad (CDR) de región variable de la secuencia de región variable de cadena pesada de inmunoglobulina 12A11 de SEC ID Nº: 4.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2004/017514.
Solicitante: WYETH LLC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: FIVE GIRALDA FARMS MADISON, NJ 07940 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BASI,GURIQ, SALDANHA,JOSE W, BARD,Frédérique.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C07H21/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07H AZUCARES; SUS DERIVADOS; NUCLEOSIDOS; NUCLEOTIDOS; ACIDOS NUCLEICOS (derivados de ácidos aldónicos o sacáricos C07C, C07D; ácidos aldónicos, ácidos sacáricos C07C 59/105, C07C 59/285; cianohidrinas C07C 255/16; glicales C07D; compuestos de constitución indeterminada C07G; polisacáridos, sus derivados C08B; ADN o ARN concerniente a la ingeniería genética, vectores, p. ej. plásmidos o su aislamiento, preparación o purificación C12N 15/00; industria del azúcar C13). › C07H 21/00 Compuestos que contienen al menos dos unidades mononucleótido que tienen cada una grupos fosfato o polifosfato distintos unidos a los radicales sacárido de los grupos nucleósido, p. ej. ácidos nucleicos. › con desoxirribosilo como radical sacárido.
- C07K16/18 C07 […] › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 16/00 Inmunoglobulinas, p. ej. anticuerpos mono o policlonales. › contra materiales animales o humanos.
- C07K16/44 C07K 16/00 […] › contra material no previsto.
- C12P21/04 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 21/00 Preparación de péptidos o de proteínas (proteína monocelular C12N 1/00). › Péptidos o polipéptidos cíclicos o puenteados, p. ej. bacitracina.
- G01N33/53 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Ensayos inmunológicos; Ensayos en los que interviene la formación de uniones bioespecíficas; Materiales a este efecto.
- G01N33/567 G01N 33/00 […] › utilizando un extracto de tejido o de órgano como agente de unión.
PDF original: ES-2382547_T3.pdf
Fragmento de la descripción:
Anticuerpos humanizados que reconocen el péptido beta amiloide Campo de la invención La enfermedad de Alzheimer (EA) es una enfermedad progresiva que da como resultado demencia senil. Véase en general Selkoe, TINS 16:403 (1993) ; Hardy y col., documento WO 92/13069; Selkoe, J. Neuropathol. Exp. Neurol.
53:438 (1994) ; Duff y col, Nature 373:476 (1995) ; Games y col, Nature 373:523 (1995) . En términos generales, la enfermedad queda en dos categorías: aparición tardía, que se produce a edad avanzada (+ de 65 años) y aparición temprana, que se desarrolla mucho antes del periodo senil, es decir, entre los 35 y 60 años. En ambos tipos de enfermedades, la patología es la misma pero las anomalías tienden a ser más graves y generalizadas en casos que comienzan a una edad más temprana. La enfermedad se caracteriza por al menos dos tipos de lesiones en el cerebro, ovillos neurofibrilares y placas seniles. Los ovillos neurofibrilares son depósitos intracelulares de proteína tau asociada a microtúbulos que consisten en dos filamentos enrollados entre sí en pares. Las placas seniles (es decir, placas amiloides) son áreas de neuropilos desorganizados hasta 150 μm transversalmente con depósitos amiloides extracelulares en el centro que son visibles por análisis microscópico de secciones de tejido cerebral. La acumulación de placas amiloides dentro del cerebro también está asociada con síndrome de Down y otros trastornos cognitivos.
El principal constituyente de las placas es un péptido denominado péptido Aβ o β-amiloide. El péptido Aβ es un fragmento interno de 4 kDa de 39-43 aminoácidos de una glucoproteína transmembrana más grande llamada proteína precursora amiloide (APP) . Como resultado del procesamiento proteolítico de APP por diferentes enzimas secretasa, Aβ se encuentra principalmente tanto en una forma corta, 40 aminoácidos de longitud, como en una forma larga, que varía de 42 a 43 aminoácidos de longitud. Parte del dominio transmembrana hidrófobo de APP se encuentra en el extremo carboxilo de Aβ, y puede explicar la capacidad de Aβ para agregarse en placas, particularmente en el caso de la forma larga. La acumulación de placas amiloides en el cerebro conduce con el tiempo a muerte de las células neuronales. Los síntomas físicos asociados con este tipo de deterioro neural caracterizan la enfermedad de Alzheimer.
Se han correlacionado varias mutaciones dentro de la proteína APP con la presencia de la enfermedad de Alzheimer. Véase, por ejemplo, Goate y col, Nature 349:704) (1991) (valina717 a isoleucina) ; Chartier Harlan y col, Nature 353:844 (1991) ) (valina717 a glicina) ; Murrell y col, Science 254:97 (1991) (valina717 a fenilalanina) ; Mullan y col, Nature Genet. 1:345 (1992) (una doble mutación que cambia lisina595 - metionina 596 a asparagina595 -leucina596) . Se cree que tales mutaciones provocan la enfermedad de Alzheimer por procesamiento aumentado o alterado de APP a Aβ, particularmente procesamiento de APP a cantidades aumentadas de la forma larga de Aβ (es decir, Aβ142 y Aβ1-43) . Se cree que las mutaciones en otros genes, tales como los genes de presenilina, PS1 y PS2, afectan indirectamente al procesamiento de APP para generar cantidades aumentadas de la forma larga de Aβ (véase Hardy, TINS 20:154 (1997) ) .
Se han usado con éxito modelos de ratón para determinar la importancia de las placas amiloides en Alzheimer (Games y col, mencionado anteriormente, Jonson-Wood y col, Proc. Natl. Acad Sci. USA 94:1550 (1997) ) . En particular, cuando se inyecta a ratones transgénicos PDAPP (que expresan una forma mutante de APP humana y desarrollan enfermedad de Alzheimer a una edad joven) la forma larga de Aβ, estos presentan tanto una reducción de la progresión de Alzheimer como un aumento de las titulaciones de anticuerpo para el péptido Aβ (Schenk y col, Nature 400, 173 (1999) ) . Las observaciones analizadas anteriormente indican que Aβ, particularmente en su forma larga, es un elemento causante de la enfermedad de Alzheimer.
En consecuencia, existe la necesidad de nuevas terapias y reactivos para el tratamiento de la enfermedad de Alzheimer, en particular, terapias y reactivos capaces de efectuar un beneficio terapéutico a dosis fisiológicas (por ejemplo, no tóxicas) .
El documento WO-A-02/088306 desvela formas humanizadas del anticuerpo de ratón 3D6 que conservan las propiedades de unión de 3D6 de ratón, y el uso de estos anticuerpos en el tratamiento del síndrome de Down, enfermedad de Alzheimer y angiopatía amiloide cerebral.
El documento EP-A-0921189 desvela animales transgénicos, especialmente ratones, que expresan de forma constitutiva una molécula de tipo anticuerpo codificada por el transgén y que tiene una región constante de cadena pesada de IgE y es específica para un antígeno predefinido.
El documento WO-A-95/07301 desvela anticuerpos monoclonales quiméricos y humanizados IL4 derivados de anticuerpos monoclonales de alta afinidad, y el uso de estos anticuerpos en procedimientos de tratamiento.
Sumario de la invención La presente invención presenta nuevos reactivos inmunológicos, en particular, reactivos de anticuerpos terapéuticos para la prevención y el tratamiento de enfermedad amiloidogénica (por ejemplo, enfermedad de Alzheimer) . La invención se basa en la identificación y caracterización de un anticuerpo monoclonal, 12A11, que se une específicamente a péptido Aβ y es eficaz en la reducción de la carga de placas asociada con trastornos amiloidogénicos. El análisis estructural y funcional de este anticuerpo conduce al diseño de anticuerpos 12A11 humanizados para uso profiláctico y/o terapéutico. En particular, la invención presenta humanización de las regiones variables de este anticuerpo y, en consecuencia, posibilita las cadenas de anticuerpo o inmunoglobulina 12A11 humanizadas, inmunoglobulinas 12A11 humanizadas intactas o anticuerpos, y fragmentos de anticuerpo o inmunoglobulina 12A11 funcionales, en particular, fragmentos de unión a antígeno, del anticuerpo 12A11.
También se desvelan polipéptidos que comprenden las regiones determinantes de complementariedad (CDR) del anticuerpo monoclonal 12A11, así como reactivos polinucleotídicos, vectores y células huésped adecuadas para codificar dichos polipéptidos.
Se desvelan procedimientos para tratar enfermedades o trastornos amiloidogénicos (por ejemplo, enfermedad de Alzheimer) , así como composiciones farmacéuticas y kits para su uso en tales aplicaciones.
También se presentan procedimientos para identificar restos dentro del 12A11 presentado que son importantes para la función inmunológica apropiada y para identificar restos que sean susceptibles de sustitución en el diseño de anticuerpos humanizados que tengan afinidades de unión mejoradas y/o inmunogenicidad reducida, cuando se usan como reactivos terapéuticos.
También se presentan anticuerpos 12A11 (por ejemplo, anticuerpos humanizados) que tienen funciones efectoras alteradas y usos terapéuticos de los mismos.
Breve descripción de los dibujos La Figura 1 representa gráficamente los resultados de un experimento que examina la eficacia de diversos anticuerpos, incluyendo 12A11, en la eliminación de placas Aβ en un ensayo de fagocitosis ex vivo. La Figura 2A representa gráficamente los resultados de un experimento que examina la eficacia de diversos anticuerpos, incluyendo 12A11, en la reducción de niveles de Aβ totales. Las barras representan los valores de la mediana, y la línea horizontal discontinua indica el nivel de control. La Figura 2B representa gráficamente resultados de un experimento que analiza la eficacia de diversos anticuerpos, incluyendo 12A11, en la reducción de la distrofia neurítica. Las barras representan valores de la mediana y la línea horizontal discontinua indica el nivel de control. Se muestran datos para animales individuales y se expresan como el porcentaje de distrofia neurítica en relación con la media del control (establecida al 100 %) . La Figura 3A representa una secuencia de ADN que incluye la secuencia de cadena VL de 12A11 murino y la secuencia de aminoácidos deducida para la cadena VL (SEC ID Nº: 5 y 2, respectivamente) . La cadena VL madura se indica por una barra negra sólida. Las CDR se indican por barras abiertas. La Figura 3B representa una secuencia de ADN que incluyen la secuencia de cadena VH de 12A11 murino y la secuencia de aminoácidos deducida para la cadena VH (SEC ID Nº: 6 y 3, respectivamente) . La cadena VH madura se indica por una barra negra sólida.... [Seguir leyendo]
Reivindicaciones:
1. Una inmunoglobulina 12A11 humanizada o fragmento de unión a antígeno de la misma que comprende una cadena ligera de inmunoglobulina humanizada que comprende las regiones determinantes de complementariedad (CDR) de región variable de la secuencia de región variable de cadena ligera de inmunoglobulina 12A11 de SEC ID Nº: 2 y una cadena pesada de inmunoglobulina humanizada que comprende las regiones determinantes de complementariedad (CDR) de región variable de la secuencia de región variable de cadena pesada de inmunoglobulina 12A11 de SEC ID Nº: 4.
2. La inmunoglobulina 12A11 humanizada o fragmento de unión a antígeno de la reivindicación 1 que comprende una cadena ligera humanizada y una cadena pesada humanizada, en la que
(a) la cadena ligera humanizada comprende tres regiones determinantes de complementariedad (CDR1, CDR2 y CDR3) que tienen secuencias de aminoácidos de las regiones determinantes de complementariedad correspondientes del dominio variable de cadena ligera de inmunoglobulina 12A11 de ratón designado SEC ID Nº: 2 y un armazón de región variable de una secuencia flanqueante de región variable de cadena ligera humana, siempre que al menos un resto flanqueante seleccionado del grupo que consiste en un resto canónico, un resto de vernier, un resto de empaquetamiento y un resto poco común esté ocupado por el mismo resto aminoacídico presente en la posición equivalente del armazón de región variable de cadena ligera de inmunoglobulina 12A11 de ratón; y
(b) la cadena pesada humanizada comprende tres regiones determinantes de complementariedad (CDR1, CDR2 y CRD3) que tienen secuencias de aminoácidos de las regiones determinantes de complementariedad correspondientes del dominio variable de cadena pesada de inmunoglobulina 12A11 de ratón designado SEC ID Nº: 4 y un armazón de región variable de una secuencia flanqueante de región variable de cadena pesada humana, siempre que al menos un resto flanqueante seleccionado de un segundo grupo que consiste en un resto canónico, un resto de vernier, un resto de empaquetamiento y un resto poco común esté ocupado por el mismo resto aminoacídico presente en la posición equivalente del armazón de región variable de cadena pesada de inmunoglobulina 12A11 de ratón;
uniéndose la inmunoglobulina humanizada o fragmento de unión a antígeno de la misma específicamente a péptido beta amiloide (Aβ) con una afinidad de unión de al menos 107 M-1, teniendo la inmunoglobulina 12A11 de ratón la cadena ligera con un dominio variable designado SEC ID Nº: 2 y la cadena pesada con un dominio variable designado SEC ID Nº: 4.
3. La inmunoglobulina humanizada de la reivindicación 2, en la que al menos un resto flanqueante en la cadena ligera está ocupado por el mismo aminoácido presente en la posición equivalente de la cadena ligera de 12A11 en una posición seleccionada del grupo que consiste en L2, L4, L36, L38, L40, L44, L46, L47, L48, L49, L64, L66, L68, L69, L71, L87 y L98 numeradas de acuerdo con Kabat y al menos un resto flanqueante en la cadena pesada está ocupado por el mismo aminoácido presente en la posición equivalente de la cadena pesada de 12A11 en una posición seleccionada del grupo que consiste en H2, H24, H26, H27, H28, H29, H37, H39, H45, H47, H48, H 67, H71, H73, H78, H91, H93, H94 y H103 numeradas de acuerdo con Kabat.
4. La inmunoglobulina humanizada de la reivindicación 2, en la que al menos tres restos flanqueantes en la cadena ligera están ocupados por el mismo aminoácido presente en la posición equivalente de la cadena ligera de 12A11 en posiciones seleccionadas del grupo que consiste en L2, L4, L36, L38, L40, L44, L46, L47, L48, L49, L64, L66, L68, L69, L71, L87 y L98 numeradas de acuerdo con Kabat y al menos tres restos flanqueantes en la cadena pesada están ocupados por el mismo aminoácido presente en la posición equivalente de la cadena pesada de 12A11 en posiciones seleccionadas del grupo que consiste en H2, H24, H26, H27, H28, H29, H37, H39, H45, H47, H48, H67, H71, H73, H78, H91, H93, H94 y H103 numeradas de acuerdo con Kabat.
5. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de la reivindicación 2, en la que todas las posiciones de cadena ligera seleccionadas del grupo que consiste en L2, L4, L36, L38, L40, L44, L46, L47, L48, L49, L64, L66, L68, L69, L71, L87 y L98 numeradas de acuerdo con Kabat están ocupadas por el mismo aminoácido presente en la posición equivalente de la cadena ligera de 12A11 de ratón de SEC ID Nº: 2.
6. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de la reivindicación 2, en la que todas las posiciones de cadena pesada seleccionadas del grupo que consiste en H2, H24, H26, H27, H28, H29, H37, H39, H45, H47, H48, H67, H71, H73, H78, H91, H93, H94 y H103 numeradas de acuerdo con Kabat están ocupadas por el mismo aminoácido presente en la posición equivalente de la cadena pesada de 12A11 de ratón de SEC ID Nº: 4.
7. La inmunoglobulina humanizada o fragmento de unión a antígeno de una cualquiera de las reivindicaciones 2-6, en la que el armazón de región variable de cadena ligera humanizada es un armazón de región variable de cadena ligera humano de un anticuerpo del subgrupo II humano K64 (AIMS4) (nº de acceso BAC01733) .
8. La inmunoglobulina humanizada o fragmento de unión a antígeno de una cualquiera de las reivindicaciones 2-6, en la que el armazón de región variable de cadena pesada humanizada es un armazón de región variable de cadena pesada humano de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) .
9. La inmunoglobulina humanizada o fragmento de unión a antígeno de una cualquiera de las reivindicaciones 2-8, en la que la cadena ligera de región variable humanizada se designa SEC ID Nº 7.
10. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H48, H67, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, L, L, K, T y V, respectivamente.
11. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37, H71 y H73 numeradas de acuerdo con Kabat están ocupadas por F, L, I, K y T, respectivamente.
12. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37 y H71 numeradas de acuerdo con Kabat están ocupadas por F, L, I y K, respectivamente.
13. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29 y H37 numeradas de acuerdo con Kabat están ocupadas por F, L e I, respectivamente.
14. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37, H48, H67, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, L, I, L, L, K, T y V, respectivamente
15. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H67, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, L, K, T y V, respectivamente.
16. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H48, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, L, K, T y V, respectivamente.
17. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H48, H67, H71 y H73 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, L, L, K y T, respectivamente.
18. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37, H67, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, L, I, L, K, T y V, respectivamente.
19. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37, H48, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, L, I, L, K, T y V, respectivamente.
20. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37, H48, H67, H71 y H73 numeradas de acuerdo con Kabat están ocupadas por F, L, I, L, L, K y T, respectivamente
21. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo de subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, K, T y V, respectivamente.
22. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H67, H71 y H73 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, L, K y T, respectivamente.
23. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H48, H71 y H73 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, L, K y T, respectivamente.
24. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, L, I, K, T y V, respectivamente.
25. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37, H67, H71 y H73 numeradas de acuerdo con Kabat están ocupadas por F, L, I, L, K y T, respectivamente.
26. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H37, H48, H71 y H73 numeradas de acuerdo con Kabat están ocupadas por F, L, I, L, K y T, respectivamente.
27. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H71 y H73 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, K y T, respectivamente.
28. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H29, H48, H67, H71, H73 y H78 numeradas de acuerdo con Kabat están ocupadas por F, L, L, L, K, T y V, respectivamente.
29. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 2-5 y 7-9, en la que el armazón de región variable de cadena pesada humanizada es de un anticuerpo del subgrupo III humano M72 (nº de acceso AAA69734) y en la que las posiciones H24, H28, H29, H37, H48, H67, H71 y H78 numeradas de acuerdo con Kabat están ocupadas por F, S, L, I, L, L, K y V, respectivamente.
30. Una inmunoglobulina humanizada o fragmento de unión a antígeno que tiene una región variable de cadena ligera humanizada que comprende los aminoácidos 1-112 de SEC ID Nº: 7 y una región variable de cadena pesada humanizada que comprende los aminoácidos 1-120 de SEC ID Nº: 10.
31. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de la reivindicación 2, en la que la región variable de cadena pesada humanizada tiene una secuencia de aminoácidos que comprende los aminoácidos 1-120 de una secuencia seleccionada del grupo que consiste en: SEC ID Nº: 13, SEC ID Nº: 14, SEC ID Nº: 15, SEC ID Nº: 16, SEC ID Nº: 17, SEC ID Nº: 18, SEC ID Nº: 19, SEC ID Nº: 20, SEC ID Nº: 21, SEC ID Nº: 24, SEC ID Nº: 25, SEC ID Nº: 26, SEC ID Nº: 27, SEC ID Nº: 28, SEC ID Nº: 29, SEC ID Nº: 30 y SEC ID Nº: 31; y en la que la región variable de cadena ligera humanizada tiene una secuencia de aminoácidos que comprende los aminoácidos 1-112 2 de SEC ID Nº: 7.
32. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de la reivindicación 2, en la que la región variable de cadena pesada humanizada tiene una secuencia de aminoácidos que comprende los aminoácidos 1-121 de SEC ID Nº: 22 o SEC ID Nº: 23; y en la que la región variable de cadena ligera humanizada tiene una secuencia de aminoácidos que comprende los aminoácidos 1-112 de SEC ID Nº: 7.
33. La inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de una cualquiera de las reivindicaciones 1-32, en la que el isotipo es IgG1 humana.
34. La inmunoglobulina humanizada de una cualquiera de las reivindicaciones 1-33, que comprende una región Fc que tiene una función efectora alterada.
35. Una composición farmacéutica que comprende una inmunoglobulina humanizada o fragmento de unión a antígeno de la misma de cualquiera de las reivindicaciones 1-34 y un vehículo farmacéutico.
36. La inmunoglobulina humanizada de una cualquiera de las reivindicaciones 1-34, para su uso en la prevención o el tratamiento de una enfermedad amiloidogénica.
37. La inmunoglobulina humanizada de la reivindicación 36, para su uso en la reducción de la carga neurítica.
38. La inmunoglobulina humanizada de la reivindicación 36, en la que la enfermedad es enfermedad de Alzheimer.
39. La inmunoglobulina humanizada de la reivindicación 36, para su uso en una dosificación eficaz en el intervalo de
0, 01 a 5 mg/kg de peso corporal.
40. La inmunoglobulina humanizada de la reivindicación 39, para uso en una dosificación eficaz de 1 mg/kg de peso corporal.
41. Una inmunoglobulina quimérica o fragmento de unión a antígeno de la misma, que comprende la secuencia de región variable de cadena ligera de SEC ID Nº: 2 y la región variable de cadena pesada de SEC ID Nº: 4 y secuencias de región constante de una inmunoglobulina humana.
42. Un ácido nucleico aislado que codifica una región variable de cadena pesada humanizada de cualquiera de las reivindicaciones 1-32.
43. Un ácido nucleico aislado que codifica una región variable de cadena ligera humanizada de cualquiera de las reivindicaciones 1-5, 7 y 9.
44. Ácidos nucleicos aislados que codifican respectivamente una región variable de cadena pesada humanizada de cualquiera de las reivindicaciones 1-4, 6, 8 y 10-32 y una región variable de cadena ligera humanizada de cualquiera de las reivindicaciones 1-5, 7 y 9.
45. Una molécula de ácido nucleico aislada que comprende la secuencia de nucleótidos de SEC ID Nº: 1 o SEC ID Nº: 3.
46. Un vector o vectores que comprenden un ácido nucleico o ácidos nucleicos de una cualquiera de las reivindicacione.
4. 45.
47. Una célula huésped aislada que comprende un vector o vectores de la reivindicación 46.
48. Un procedimiento para producir una inmunoglobulina humanizada o fragmento de unión a antígeno de la misma, que comprende cultivar la célula huésped de la reivindicación 47 en condiciones tales que se produzca la inmunoglobulina o fragmento de unión a antígeno y aislar el anticuerpo de la célula huésped o del cultivo.
49. Un animal transgénico no humano que expresa un polipéptido codificado por la molécula de ácido nucleico de una cualquiera de las reivindicacione.
4. 46.
50. El animal transgénico no humano de la reivindicación 49, en el que el polipéptido se expresa en la leche de dicho animal.
Patentes similares o relacionadas:
Composiciones farmacéuticas que contienen una leucocidina E mutada, del 22 de Julio de 2020, de NEW YORK UNIVERSITY: Una composición que comprende: una proteína Leucocidina E (LukE) aislada que comprende la secuencia de aminoácidos de la SEQ ID NO: 4, o un polipéptido […]
Composiciones y métodos para inmunomodulación en un organismo, del 19 de Febrero de 2020, de UNIVERSITY OF CONNECTICUT: Una composicion para su uso en un metodo de (i) tratamiento de cancer en un ser humano; (ii) mejora de la vacunacion en un ser humano; (iii) aumento de las respuestas […]
CD33 soluble para tratar síndromes mielodisplásicos (MDS), del 8 de Enero de 2020, de H. Lee Moffitt Cancer Center And Research Institute, Inc: Una proteína de fusión recombinante quimérica, que comprende: (a) una combinación de al menos dos fracciones de unión a S100A9 seleccionados de entre el grupo que […]
Métodos para la diferenciación y transducción in vitro de células b de memoria con vectores virales pseudotipados vsv-g, del 1 de Enero de 2020, de Immusoft Corporation: Un método in vitro para expresar un ácido nucleico de interés en una célula B, que comprende (a) poner en contacto células B de memoria con una composición que comprende […]
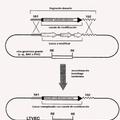 Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Producción de anticuerpos híbridos que contienen regiones variables humanas y regiones constantes de roedor, del 26 de Junio de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento para modificar genéticamente un locus génico endógeno de la región variable de cadena pesada de inmunoglobulina en una célula madre embrionaria (ES) de […]
Intercambio de casetes de la región variable de la inmunoglobulina, del 12 de Junio de 2019, de Humanigen, Inc: Un método de modificación genética de un anticuerpo que retiene la especificidad de unión de un anticuerpo de referencia con un antígeno diana, comprendiendo el método: […]
Procedimiento de modificar células eucariotas, del 3 de Abril de 2019, de REGENERON PHARMACEUTICALS, INC.: Un procedimiento de reemplazar in situ, en parte, en una célula madre embrionaria (ES) de ratón, un locus génico endógeno de región variable de […]
Diacuerpos covalentes y usos de los mismos, del 2 de Abril de 2019, de MACROGENICS, INC: Una molécula de diacuerpo que comprende una primera cadena polipeptídica y una segunda cadena polipeptídica, en la que: (a) dicha primera cadena […]