VACUNA QUIMÉRICA PARA UNA ENFERMEDAD INDUCIDA POR HAEMOPHILUS INFLUENZAE.
Proteína quimérica que comprende una parte de la proteína PilA de H.
influenzae no tipificable (NTHi) (SEC ID nº: 2) y una parte del péptido LB1 (SEC ID nº: 53), pudiendo provocar la proteína quimérica una respuesta inmunitaria a las bacterias NTHi
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/026183.
Solicitante: NATIONWIDE CHILDREN'S HOSPITAL, INC.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 700 CHILDREN'S DRIVE COLUMBUS, OH 43205 ESTADOS UNIDOS DE AMERICA.
Inventor/es: BAKALETZ, LAUREN O., MUNSON, ROBERT, S., JR.
Fecha de Publicación: .
Fecha Solicitud PCT: 5 de Julio de 2006.
Clasificación PCT:
- C07K14/195 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de origen bacteriano.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia.
PDF original: ES-2356077_T3.pdf
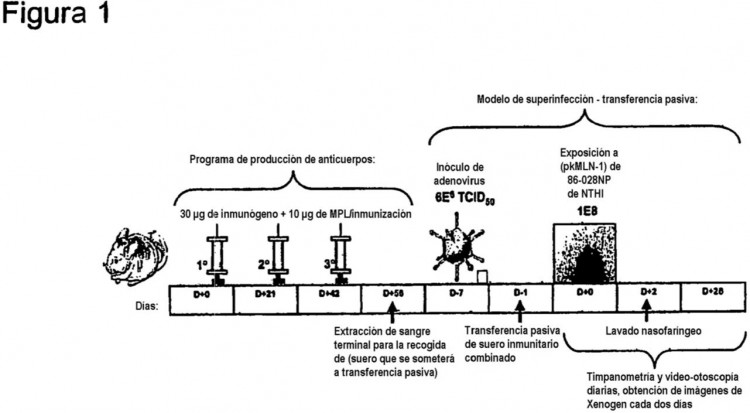
Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
La invención descrita en la presente memoria se refiere a una proteína quimérica que comprende la proteína de subunidad principal de pilus contráctil (PilA) de NTHi que presenta una parte de la proteína OMP P5 de NTHi. La invención proporciona composiciones de vacuna que comprenden la proteína quimérica y procedimientos para provocar 5 una respuesta inmunitaria utilizando las proteínas quiméricas de la invención.
ANTECEDENTES
El término clínico para las infecciones del oído medio es otitis media (OM). Según Klein, Vaccine, 19 (Supl. 1): S2-S8, 2000, la OM es el motivo más común para que un niño enfermo reciba atención médica y para que un niño en los Estados Unidos reciba antibióticos o se someta a una anestesia general. Las estadísticas indican que 24,5 millones de 10 visitas a la consulta del médico se realizaron por OM en 1990, lo que representa un aumento superior al 200% con respecto a las notificadas en la década de 1980. Aunque en pocas ocasiones va asociada con mortalidad, la morbilidad asociada con la OM es significativa. La pérdida de audición es un problema común asociado con esta enfermedad, afectando a menudo al comportamiento, a la educación y al desarrollo de las habilidades lingüísticas del niño (Baldwin, Am. J. Otol., 14: 601-604, 1993; Hunter et al., Ann. Otol. Rhinol. Laryngol. Supl., 163: 59-61, 1994; Teele et al., J. Infect. 15 Dis., 162: 685-694, 1990). El impacto socioeconómico de la OM también es grande, con costes directos e indirectos de diagnóstico y tratamiento de la OM que superan los 5 mil millones de $ anualmente sólo en los US (Kaplan et al., Pediatr. Infect. Dis. J., 16: S9-11, 1997).
Se cree que la OM es el resultado de factores infecciosos, ambientales y genéticos del huésped. Bacterias tales como Haemophilus influenzae, Streptococcus pneumoniae y Moraxella catarrhalis son los organismos infecciosos más 20 comunes en la OM. La OM aguda es una enfermedad caracterizada por una rápida aparición y una corta duración de signos y síntomas de inflamación en el oído medio, mientras que la OM crónica se refiere a un estado que se define por la presencia relativamente asintomática de líquido (o efusión) en el oído medio. Sin embargo, en la OM crónica, a pesar de la ausencia de ciertos signos de infección aguda (es decir, dolor de oídos o fiebre), estos fluidos anómalos del oído medio pueden persistir durante periodos que superan los tres meses. El tratamiento de la OM aguda mediante terapia 25 con antibióticos es común, pero han surgido múltiples bacterias resistentes a los antibióticos en los tres géneros de bacterias responsables de la OM. El tratamiento quirúrgico de la OM crónica implica la inserción de tubos de timpanostomía a través de la membrana timpánica del oído mientras el niño está bajo anestesia general. Aunque este procedimiento es común (las tasas de prevalencia son de ~1 millón de tubos insertados al año en US Bright et al., Am. J. Public Health, 83(7): 1026-8, 1993) y es sumamente eficaz en cuanto a aliviar los síntomas dolorosos drenando los 30 líquidos acumulados en el oído medio, es invasivo y conlleva riesgos importantes (Berman et al., Pediatrics, 93(3):353-63, 1994; Bright et al., citado anteriormente; Cimons, ASM News, 60: 527-528; Paap, Ann. Pharmacother., 30(11): 1291-7, 1996). Resultan por tanto necesarios otros enfoques para el tratamiento y, preferentemente, la prevención de la OM.
El desarrollo de un vacuna contra la OM está más avanzado para S. pneumoniae, el agente causante principal de la OM aguda (OMA), tal como demuestra la reciente aprobación y autorización de una vacuna de conjugado capsular 35 heptavalente, PREVNAR® (Eskola y Kilpi, Pedriatr. Infect. Dis. J. 16: S72-78, 2000). Aunque PREVNAR® ha sido sumamente eficaz para la enfermedad neumocócica invasiva, la cobertura para la OM ha sido decepcionante (6-8%) con notificaciones de un número aumentado de casos de OM debido a serotipos no incluidos en la vacuna (Black et al., Pedriatr. Infect. Dis J, 19: 187-195, 2000; Eskola et al., Pedriatr. Infect. Dis J., 19: S72-78, 2000; Eskola et al., N. Engl. J. Med., 344: 403-409, 2001; Snow et al., Otol. Neurotol., 23: 1-2, 2002). 40
La H. influenzae es una bacteria gram-negativa que, tal como se indicó anteriormente, desempeña un papel en la OM. Los aislados clínicos de H. infuenzae se clasifican o bien como serotipos “a” a “f” o como no tipificables dependiendo de la presencia o ausencia, respectivamente, de cápsulas de polisacárido específicas del tipo en las bacterias. Se ha desarrollado una vacuna contra H. influenzae tipo b. Como PREVNAR®, las vacunas contra H. influenzae tipo b se dirigen a la cápsula de polisacárido de este organismos y por tanto la vacuna está compuesta por un 45 polisacárido capsular que se ha conjugado con un portador proteico. Ni PREVNAR® ni la vacuna contra H. influenzae tipo b presentan ninguna eficacia para las enfermedades del aparato respiratorio inducidas por NTHI, incluyendo la OM. Se han realizado menos avances para una vacuna contra H. influenzae no tipificable (NTHi) que provoca aproximadamente el 20% de la OM aguda en niños y predomina en la OM crónica con efusión (Coleman et al., Inf and Immunity, 59(5), 1716-1722, 1991; Klein, Pedriatr. Infect. Dis J., 16, S5-8, 1997; Spinola et al., J. Infect. Dis., 154, 100-50 109, 1986). La NTHi también puede provocar neumonía, sinusitis, septicemia, endocarditis, epiglotitis, artritis séptica, meningitis, infecciones puerperales y neonatales, sepsis puerperal y neonatal, salpingitis aguda y crónica, pericarditis, celulitis, osteomielitis, endocarditis, colecistitis, infecciones intraabdominales, infección de las vías urinarias, mastoiditis, infección de injerto aórtico, conjuntivitis, fiebre purpúrica brasileña, bacteriemia oculta y exacerbación de enfermedades pulmonares subyacentes tales como bronquitis crónica, bronquiectasia y fibrosis quística. Un aislado de NTHi prototipo 55 es el aislado con número de pases bajo 86-028NP que se recuperó de un niño con OM crónica. Esta cepa se ha caracterizado bien in vitro (Bakaletz et al., Infect. Immun., 53: 331-5, 1988; Holmes et al., Microb. Pathog., 23: 157-66, 1997) así como en modelos de OM de chinchilla (Bakaletz et al., Vaccine, 15: 955-61, 1997; Suzuki et al., Infect. Immun., 62: 1710-8, 1994; DeMaria et al., Infect. Immun., 64: 5187-92, 1996). La cepa 86-026N de NTHi se depositó en la American Type Culture Collection, 10801 University Blvd., Manassas, VA 20110, el 16 de octubre de 2001 y se le 60
asignó el nº de registro PTA-4764. Puede encontrarse un conjunto de secuencias contiguas del genoma de la cepa 86-028NP en la página web del Columbus Children's Research Institute Center for Microbial Pathogenesis.
La adherencia y colonización se reconocen como las primeras etapas en la patogénesis de enfermedades inducidas por H. influenzae. Como tal, H. influenzae expresa múltiples adhesinas que incluyen adhesinas no fimbriales, fimbrias y pili hemaglutinantes (Gilsdorf et al., Pediatr Res 39, 343-348, 1996; Gilsdorf., Infect. Immun., 65, 2997-3002, 5 1997; y St. Geme III, Cell. Microbiol., 4, 191-200, 2002). Particularmente, ninguna de las adhesinas descritas se ha asociado previamente con una función de motilidad. Además, H. influenzae no expresa flagelos que también están asociados con la motilidad. La motilidad contráctil es una forma independiente de los flagelos de traslocación bacteriana sobre superficies húmedas y se produce mediante extensión, atado y después retracción de estructuras polares conocidas como pili de tipo IV (Bardy, Microbiology, 149, 295-304, 2003; Tonjum y Koomey, Gene, 192, 155-163, 1997; 10 Wolfgang et al., EMBO J., 19; 6408-6418; Mattick, Annu. Rev. Microbiol., 56, 289-314, 2002). Los pili de tipo IV presentan normalmente 5-7 nm de diámetro, varios micrómetros de longitud y están compuestos por una única subunidad de proteína ensamblada en una conformación helicoidal con ~5 subunidades por vuelta (Bardy et al., Microbiology, 149, 295-304, 2003; Wall y Kaiser, Mol. Microbiol., 32, 1-10, 1999). Las subunidades de pilina de tipo IV presentan habitualmente 145-160 aminoácidos de longitud y pueden estar glicosiladas o fosforiladas. Existen dos clases 15 de subunidades de pilina, tipo IVa y tipo IVb, que se distinguen entre sí por la longitud promedio del péptido líder y la subunidad madura, cuyo aminoácido N-metilado ocupa la posición N-terminal de la proteína madura, y la longitud promedio de la región D (para región disulfuro). La mayoría de los patógenos respiratorios expresan pilinas de clase IVa, mientras que los enteropatógenos expresan más normalmente... [Seguir leyendo]
Reivindicaciones:
1. Proteína quimérica que comprende una parte de la proteína PilA de H. influenzae no tipificable (NTHi) (SEC ID nº: 2) y una parte del péptido LB1 (SEC ID nº: 53), pudiendo provocar la proteína quimérica una respuesta inmunitaria a las bacterias NTHi.
2. Proteína quimérica según la reivindicación 1, en la que la parte del péptido LB1 comprende el epítopo de 5 células B del péptido LB1.
3. Proteína quimérica según la reivindicación 2, en la que la parte del péptido LB1 comprende la secuencia de aminoácidos de SEC ID nº: 4, SEC ID nº: 5, SEC ID nº: 6, SEC ID nº: 7 o SEC ID nº: 8.
4. Proteína quimérica según la reivindicación 1, que comprende la secuencia de aminoácidos de SEC ID nº: 9, SEC ID nº: 10, SEC ID nº: 11, SEC ID nº: 12, SEC ID nº: 13, SEC ID nº: 14, SEC ID nº: 15, SEC ID nº: 16, SEC ID nº: 10 17, SEC ID nº: 18, SEC ID nº: 19, SEC ID nº: 20, SEC ID nº: 21, SEC ID nº: 22, SEC ID nº: 23, SEC ID nº: 24, SEC ID nº: 25, SEC ID nº: 26, SEC ID nº: 27, SEC ID nº:28, SEC ID nº: 29, SEC ID nº: 30, SEC ID nº: 31, SEC ID nº: 32, SEC ID nº: 54, SEC ID nº: 55, SEC ID nº: 56 o SEC ID nº: 57.
5. Proteína quimérica según la reivindicación 4, que comprende la secuencia de aminoácidos de SEC ID nº: 57. 15
6. Proteína quimérica según la reivindicación 1, en la que la parte de la proteína PilA de NTHi comprende los residuos 40-149 de SEC ID nº: 2.
7. Proteína quimérica según la reivindicación 6, en la que el epítopo de células B de LB1 está insertado antes del residuo 40 de SEC ID nº: 2.
8. Proteína quimérica según cualquiera de las reivindicaciones 1, 2, 6 ó 7, en la que el epítopo de células B 20 de LB1 comprende SEC ID nº: 5.
9. Polinucleótido que codifica para la proteína quimérica según cualquiera de las reivindicaciones 1 a 8.
10. Vector que comprende un polinucleótido según la reivindicación 9.
11. Composición que comprende una proteína quimérica según cualquiera de las reivindicaciones 1 a 8 y un vehículo farmacéuticamente aceptable. 25
12. Composición según la reivindicación 11, en la que la composición está formulada para una vía de administración seleccionada de entre el grupo constituido por administración parenteral, intravenosa, oral, bucal, nasal, pulmonar, rectal, intranasal, transdérmica, subcutánea, intramuscular o vaginal.
13. Utilización de una o más proteínas quiméricas según cualquiera de las reivindicaciones 1 a 8, para la preparación de un medicamento en un paciente en riesgo de padecer una infección por bacterias NTHi para provocar 30 una respuesta inmunitaria a las bacterias NTHi.
14. Utilización según la reivindicación 13, en la que la infección por NTHi es en el oído medio, la nasofaringe o las vías respiratorias inferiores.
15. Utilización según cualquiera de las reivindicaciones 13 ó 14, en la que el medicamento está formulado para una vía de administración seleccionada entre el grupo constituido por administración parenteral, intravenosa, oral, 35 bucal, nasal, pulmonar, rectal, intranasal, transdérmica, subcutánea, intramuscular o vaginal.
16. Utilización según la reivindicación 13 ó 14, en la que la infección por bacterias NTHi implica un estado patológico seleccionado de entre el grupo constituido por otitis media, neumonía, sinusitis, septicemia, endocarditis, epiglotitis, artritis séptica, meningitis, sepsis, salpingitis, pericarditis, celulitis, osteomielitis, endocarditis, colecistitis, infecciones intraabdominales, infección de las vías urinarias, mastoiditis, infección de injerto aórtico, conjuntivitis, fiebre 40 purpúrica brasileña, bacteriemia oculta, enfermedad pulmonar obstructiva crónica, bronquitis crónica, bronquiectasia y fibrosis quística.
17. Proteína quimérica según cualquiera de las reivindicaciones 1 a 8, para su utilización en la provocación de una respuesta inmunitaria a las bacterias NTHi en un paciente en riesgo de padecer una infección por bacterias NTHi.
18. Proteína quimérica según la reivindicación 17, en la que la infección por NTHi se encuentra en el oído 45 medio, la nasofaringe o las vías respiratorias inferiores.
19. Proteína quimérica según la reivindicación 17, en la que la infección por bacterias NTHi implica un estado patológico seleccionado de entre el grupo constituido por otitis media, neumonía, sinusitis, septicemia, endocarditis, epiglotitis, artritis séptica, meningitis, sepsis, salpingitis, pericarditis, celulitis, osteomielitis, endocarditis, colecistitis, infecciones intraabdominales, infección de las vías urinarias, mastoiditis, infección de injerto aórtico, conjuntivitis, fiebre 50
purpúrica brasileña, bacteriemia oculta, enfermedad pulmonar obstructiva crónica ,bronquitis crónica, bronquiectasia y fibrosis quística.
20. Proteína quimérica según cualquiera de las reivindicaciones 1 a 8, para su utilización en el tratamiento o la prevención de la infección por bacterias NTHi en un paciente que lo necesite.
21. Proteína quimérica según la reivindicación 20, en la que la infección por NTHi se encuentra en el oído 5 medio, la nasofaringe o las vías respiratorias inferiores.
Patentes similares o relacionadas:
Métodos y composiciones para la producción mejorada de ácidos grasos y derivados de los mismos, del 27 de Mayo de 2020, de Genomatica, Inc: Un método para producir un ácido graso o derivado del mismo, que comprende; (a) proporcionar una célula hospedadora bacteriana modificada por ingeniería genética que comprende […]
Composiciones de flagelina y usos, del 6 de Mayo de 2020, de Genome Protection, Inc: Una composición relacionada con la flagelina, comprendiendo la composición una secuencia de aminoácidos que tiene al menos un 95 % de identidad de […]
Composiciones para administración por vía oral que comprende una variante de una proteína de pliegue OB, del 29 de Abril de 2020, de AFFILOGIC: Composición para la administración por vía oral para un uso terapéutico o diagnóstico, que comprende una variante de una proteína salvaje de pliegue OB, presentando […]
Células huésped modificadas y oligosacáridos híbridos para su uso en producción de bioconjugados, del 1 de Abril de 2020, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Un bioconjugado que comprende una proteína de vehículo unida a un oligosacárido o polisacárido híbrido que tiene una estructura (B)n-A→ […]
Proteínas que tienen actividad nucleasa, proteínas de fusión y usos de estas, del 18 de Marzo de 2020, de HELMHOLTZ ZENTRUM MUNCHEN DEUTSCHES FORSCHUNGSZENTRUM FUR GESUNDHEIT UND UMWELT (GMBH): Una molécula de ácido nucleico que codifica (I) un polipéptido que tiene la actividad de una endonucleasa, que es (a) una molécula de ácido nucleico que […]
Procedimiento escalable industrialmente para recuperar proteínas transportadoras recombinantes biológicamente activas, del 18 de Marzo de 2020, de Biological E Limited: Procedimiento para la preparación de proteínas transportadoras seleccionadas de toxoide tetánico (TT), toxoide diftérico (DT), material de reacción […]
Monocinas y métodos de uso, del 19 de Febrero de 2020, de Pylum Biosciences, Inc: Una molécula de ácido nucleico aislada que codifica una monocina, en donde la molécula de ácido nucleico comprende un primer polinucleótido que codifica las […]
Transformación de plantas mediada por Ochrobactrum, del 18 de Diciembre de 2019, de PIONEER HI-BRED INTERNATIONAL, INC.: Una Ochrobactrum haywardense HI aislada, en donde dicha Ochrobactrum se deposita bajo el NRRL B-67078.