VACUNA DE LA GRIPE.
Una composición de vacuna de la gripe monovalente que comprende un componente de virus de la gripe que es una baja dosis de antígeno de virus de la gripe de una cepa de virus de la gripe que está asociada con un brote pandémico o que tiene el potencial de asociarse con un brote pandémico,
en combinación con un adyuvante adecuado, en la que dicha baja dosis de antígeno es de menos de 15 μg de hemaglutinina por dosis o no más de 15 μg por dosis combinada de vacuna, y en la que dicho adyuvante es un vehículo de emulsión de aceite en agua que comprende escualeno, alfa tocoferol y Tween 80
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E05077465.
Solicitante: GlaxoSmithKline Biologicals S.A.
GlaxoSmithKline Biologicals, Niederlassung der SmithKline Beecham Pharma GmbH & Co. KG.
Nacionalidad solicitante: Bélgica.
Dirección: RUE DE L'INSTITUT, 89 1330 RIXENSART BELGICA.
Inventor/es: D\'Hondt,Erik, Hehme,Norbert.
Fecha de Publicación: .
Fecha Solicitud PCT: 27 de Septiembre de 2000.
Clasificación Internacional de Patentes:
- A61K39/145 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Orthomyxoviridae, p. ej. virus de la influenza.
- C07K14/11 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Orthomyxoviridae, p. ej. virus de la influenza.
- C12N7/02 C […] › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 7/00 Virus, p. ej. bacteriófagos; Composiciones que los contienen; Su preparación o purificación (preparaciones de uso médico que contienen virus A61K 35/76; preparación de composiciones de uso médico que contienen antígenos o anticuerpos virales, p. ej. vacunas virales, A61K 39/00). › Aislamiento o purificación.
Clasificación PCT:
- A61K39/145 A61K 39/00 […] › Orthomyxoviridae, p. ej. virus de la influenza.
- A61P31/12 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Antivirales.
Clasificación antigua:
- A61K39/145 A61K 39/00 […] › Orthomyxoviridae, p. ej. virus de la influenza.
- A61P31/12 A61P 31/00 […] › Antivirales.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Finlandia, Chipre.
PDF original: ES-2359982_T3.pdf
Fragmento de la descripción:
La presente invención se refiere a nuevas formulaciones de vacuna, a procedimientos para prepararlas y a su uso en la profilaxis o terapia. En particular, la presente invención se refiere a vacunas para su administración durante pandemias.
El virus de la gripe es uno de los virus más ubicuos presentes en el mundo, que afecta tanto a seres humanos como al ganado, que sigue un patrón aún impredecible de epidemias regulares y pandemias irregulares.
Aunque con frecuencia se considera una enfermedad trivial, la gripe puede tener un impacto devastador. Se han registrado brotes a lo largo de la historia. Se sabe que han sucedido más de 30 epidemias o pandemias mundiales desde 1580, cuatro de ellas en el presente siglo.
Los síntomas habituales de la gripe incluyen tos, fiebre, cefalea y dolores musculares. Muchos de los que la padecen desarrollan complicaciones o infecciones bacterianas secundarias que pueden ser muy graves e incluso mortales.
Durante los periodos interpandémicos, circulan virus de la gripe que están relacionados con los de la epidemia precedente. Los virus se propagan entre personas con niveles variables de inmunidad de infecciones anteriores en su vida. Dicha circulación, durante un periodo de habitualmente 2-3 años, promueve la selección de nuevas cepas que han cambiado los suficiente para causar una epidemia de nuevo entre la población general; este procedimiento se denomina “deriva antigénica”. Las "variantes por deriva” pueden tener diferentes impactos en diferentes comunidades, regiones, países o continentes en un año cualquiera, aunque durante varios años su impacto global es con frecuencia similar.
Las epidemias de gripe típicas causan aumentos en la incidencia de neumonía y enfermedad respiratoria inferior como atestiguan los índices aumentados de hospitalización o mortalidad. Las personas de edad avanzada o los que tienen enfermedades crónicas subyacentes tienen más probabilidades de experimentar tales complicaciones, pero los lactantes de corta edad también pueden padecer una enfermedad grave.
A intervalos impredecibles, emergen nuevos virus de la gripe con un antígeno de superficie clave, la hemaglutinina, de un subtipo totalmente diferente de las cepas que circulaban la temporada anterior. Este fenómeno se denomina “deriva antigénica”. Se cree que al menos en el pasado las pandemias se han producido cuando un virus de la gripe de una especie diferente, tal como un virus de la gripe porcina o aviar, ha cruzado la barrera de especie. Si tales virus tienen el potencial de propagarse de persona a persona, pueden propagarse a nivel mundial en un periodo de pocos meses a un año, dando como resultado una pandemia.
Las características de una cepa de virus de la gripe que le proporcionan el potencial de causar un brote pandémico son: contiene una nueva hemaglutinina en comparación con la hemaglutinina en las cepas actualmente en circulación; es capaz de transmitirse horizontalmente en la población humana y es patógeno para seres humanos. Una nueva hemaglutinina puede ser una que no ha sido evidente en la población humana durante un periodo prolongado de tiempo, probablemente varias décadas, tal como H2. O puede ser una hemaglutinina que no ha estado circulando en la población humana anteriormente, por ejemplo H5, H9 o H6, que se encuentran en aves. En cualquier caso, la mayoría, o al menos una gran proporción de, o incluso toda la población no se ha encontrado previamente con el antígeno y, desde el punto de vista inmunológico, no ha tenido exposición previa al mismo.
Los virus de la gripe H2N2 circularon entre 1957 y 1968, cuando fueron desplazados por el subtipo H3N2, que causó la última pandemia del último siglo. En la actualidad, las personas que han estado expuestas previamente al H2N2 tienen probablemente más de treinta años de edad. Se ha sugerido que un virus que contenga H2 podría causar una nueva pandemia, ya que es de esperar que una porción creciente de la población mundial que nació después de 1968 no haya tenido, desde el punto de vista inmunológico, exposición previa al mismo. Para investigar si esta dicotomía teórica de la población con respecto a la inmunidad frente a H2 es un hecho real, se realizó un estudio seroepidemiológico en 400 individuos y se midieron los anticuerpos contra H2.
Este estudio se realizó en Alemania y los ensayos de anticuerpos se llevaron a cabo en Sächsische Serumwerk (Dresden, Alemania), usando un Ensayo de Inhibición de la Hemaglutinación (EIH) específico para el antígeno H2. Los títulos son la inversa de la mayor dilución de suero que inhibe la hemaglutinación. Los resultados confirman el estado inmunológicamente sin exposición previa de los menores de 30 años de edad, puesto que solamente 7 de los 200 sujetos tenían un título de anticuerpos medible en el intervalo bajo de 10 a 20.
Los datos muestran adicionalmente que una proporción significativa de los de más de 30 años de edad aún son seropositivos para H2, 30 años o más después de la infección. El número de seropositivos (EIH 10) es del 90%. En algunas de las muestras de suero, los títulos anti-H2 (EIH) son tan altos como de 640 y la media geométrica del título (MGT) para todos los participantes en el estudio seropositivos de más de 30 años de edad fue de 65. Una EIH 40 se considera protectora.
Estas observaciones confirman la posibilidad de que un virus H2 podría propagarse en la población de menos de 30 años. Teniendo en cuenta la demografía actual y el hecho de que las personas menores de 30 años representan una gran parte de la población mundial, es posible que un virus H2 pudiera causar de nuevo una pandemia. Esta dicotomía en la población mundial evolucionará adicionalmente durante los próximos años, aumentando el conjunto de personas susceptibles.
Hace dos años, se aisló gripe con H5 (H5N1), que es un virus de la gripe aviar, de seres humanos en Hong Kong. Sin embargo el virus, no se transmitía de persona a persona y, por lo tanto, no tenía la capacidad de causar una pandemia.
Ciertos grupos tienen generalmente un riesgo aumentado de infectarse con gripe en una situación de pandemia. Las personas mayores, los enfermos crónicos y los niños pequeños son particularmente susceptibles, pero muchas personas jóvenes y aparentemente sanas también están en riesgo. Para la gripe H2, la parte de la población nacida después de 1968 presenta un riesgo aumentado. Es importante que estos grupos se protejan eficazmente tan pronto como sea posible y de una manera sencilla.
Otro grupo de personas que presentan un riesgo aumentado son los viajeros. La gente viaja en la actualidad más que nunca antes y las regiones en las que surgen la mayoría de los nuevos virus, China y el sudeste asiático, se han convertido en destinos de viaje populares en los últimos años. Este cambio en los patrones de viaje permite que nuevos virus se extiendan alrededor del globo en cuestión de semanas en lugar de meses o años.
Por lo tanto, para estos grupos de gente existe una necesidad particular de vacunación para protegerse contra la gripe en una situación de pandemia o una situación de pandemia potencial.
Se están realizando grandes esfuerzos para elaborar una estrategia internacional eficaz para reaccionar ante una situación de pandemia y la Organización Mundial de la Salud contribuye decisivamente a esto. Una medida clave es el desarrollo de una estrategia de vacunación pandémica y hasta ahora esto no se ha conseguido en la escala necesaria para abordar una pandemia de gripe.
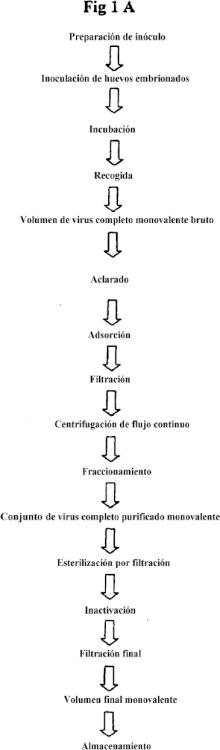
Se ha descubierto ahora de forma sorprendente que las vacunas que serán útiles en una situación de pandemia pueden formularse rápidamente y de una manera específica. En particular, se ha descubierto que una vacuna de virus de la gripe de baja dosis que contiene virus purificado usando como adyuvante un vehículo tradicional y/o formulada de una manera clásica, que puede producirse de forma suficientemente rápida y económica para permitir la vacunación de poblaciones a gran escala, es eficaz en seres humanos.
En el pasado, se han usado en el mercado preparaciones en bruto de vacuna de la gripe inactivada completa derivada de huevo usando sales de aluminio como adyuvante. Sin embargo, el producto estaba escasamente purificado y era bastante reactogénico, y el enfoque se abandonó a finales de los años 70.
Más recientemente, se han combinado vacunas de la gripe divididas mejor caracterizadas y mucho más... [Seguir leyendo]
Reivindicaciones:
1. Una composición de vacuna de la gripe monovalente que comprende un componente de virus de la gripe que es una baja dosis de antígeno de virus de la gripe de una cepa de virus de la gripe que está asociada con un brote pandémico o que tiene el potencial de asociarse con un brote pandémico, en combinación con un adyuvante adecuado, en la que dicha baja dosis de antígeno es de menos de 15 g de hemaglutinina por dosis o no más de 15 g por dosis combinada de vacuna, y en la que dicho adyuvante es un vehículo de emulsión de aceite en agua que comprende escualeno, alfa tocoferol y Tween 80.
2. Una composición de vacuna de la gripe monovalente de acuerdo con la reivindicación 1 están en una relación que es igual a o menor que 1.
3. Una composición de vacuna de acuerdo con cualquiera de las reivindicaciones 1 a 2, en la que el antígeno de virus de la gripe está en forma de virus de la gripe completo purificado o en forma de virus de la gripe dividido.
4. Una composición de vacuna de acuerdo con cualquiera de las reivindicaciones 1 a 3, en la que dicha emulsión de aceite en agua comprende escualeno del 2 al 10%, alfa tocoferol del 2 al 10% y Tween 80 del 0,3 al 3%.
5. Una composición de vacuna de acuerdo con cualquiera de las reivindicaciones 1 a 4, en la que dicha emulsión de aceite en agua comprende además monofosforil lípido A des-O-acilado (3D-MPL) o QS21.
6. Una composición de vacuna de acuerdo con la reivindicación 5, en la que 3D-MPL y QS-21 están presentes en un intervalo de 1 g-100 g, preferentemente 10 g-50 g por dosis.
7. Una composición de vacuna de acuerdo con la reivindicación 5 o reivindicación 6, en la que está presente tanto 3D-M PL como QS-21, y en la que la relación de 3D-MPL:QS21 es de 2,5:1 a 1:1.
8. Una composición de vacuna de acuerdo con una cualquiera de las reivindicaciones 1 a 7, en la que la baja dosis de antígeno es menor de 10 g de hemaglutinina por dosis o por dosis combinada de vacuna.
9. Una composición de vacuna de acuerdo con la reivindicación 8, en la que la dosis de antígeno está entre 0,1 y 7,5 g, o entre 1 y 5 g de hemaglutinina por dosis o por dosis combinada de vacuna.
10. Una composición de vacuna de acuerdo con cualquiera de las reivindicaciones 1 a 9 derivada de huevo o derivada de cultivo celular.
11. Una composición de vacuna de acuerdo con una cualquiera de las reivindicaciones 1 a 10, en la que el antígeno de virus de la gripe está sustancialmente sin contaminación de la célula huésped.
12. Una composición de vacuna de acuerdo con una cualquiera de las reivindicaciones 1 a 11, en la que el componente de virus de la gripe se purifica por un procedimiento que incluye una etapa de incubación con proteasa para digerir las proteínas de virus distintos del de la gripe.
13. Un kit que comprende:
(i) una baja dosis de antígeno de virus de la gripe formulado con un adyuvante como se define en cualquiera de las reivindicaciones 1 a 7 para administración parenteral; y
(ii) una baja dosis de antígeno de virus de la gripe para administración en la mucosa, en un dispositivo de administración en la mucosa tal como un dispositivo de pulverización intranasal.
en el que el componente de virus de la gripe es un antígeno de virus de la gripe de una cepa de virus de la gripe que está asociada con un brote pandémico o que tiene el potencial de asociarse con un brote pandémico, y en el que la baja dosis de antígeno es menor de 15 g de hemaglutinina por dosis o no más de 15 g por dosis combinada de vacuna.
14. El kit de acuerdo con la reivindicación 13, en el que la dosis de antígeno combinada es menor de 10 g de hemaglutinina.
15. El kit de acuerdo con la reivindicación 13 o reivindicación 14, en el que el antígeno de gripe en (i) es virus completo inactivado y el antígeno de la gripe en (ii) es virus dividido.
16. Un procedimiento para la producción de una vacuna de la gripe para una situación de pandemia, comprendiendo dicho procedimiento mezclar un antígeno de virus de la gripe de una sola cepa de virus de la gripe que está asociada con un brote pandémico o que tiene el potencial de asociarse con un brote pandémico, con un adyuvante como se ha definido en cualquiera de las reivindicaciones 1 a 7, y proporcionar lotes de vacuna o kits de vacuna que contienen menos de 10 g de antígeno de hemaglutinina de la gripe por dosis o no más de 15 g de hemaglutinina por dosis combinada.
17. Un procedimiento de acuerdo con la reivindicación 16, en el que el antígeno está altamente purificado.
18. Un procedimiento de acuerdo con la reivindicación 16 o reivindicación 17, en el que el antígeno de virus de la gripe está en forma de partículas de virus de la gripe completas o divididas.
19. La composición de vacuna de acuerdo con una cualquiera de las reivindicaciones 1 a 12, en la que el antígeno de la gripe se selecciona de un antígeno H2 tal como H2N2 y un antígeno H5 tal como H5N1.
5 20. El kit de acuerdo con una cualquiera de las reivindicaciones 13 a 15, en el que el antígeno de la gripe se selecciona de un antígeno H2 tal como H2N2 y un antígeno H5 tal como H5N1.
21.El procedimiento de acuerdo con una cualquiera de las reivindicaciones 16 a 18, en el que el antígeno de la gripe se selecciona de un antígeno H2 tal como H2N2 y un antígeno H5 tal como H5N1.
22. El uso de menos de 10 g, o de menos de 8 g, o de 1-7,5 g o de 1-5 g de antígeno de hemaglutinina de virus de la gripe derivado de huevo de una sola cepa de gripe asociada con un brote pandémico o que tiene el potencial de asociarse con un brote pandémico, en combinación con un adyuvante como se ha definido en cualquiera de las reivindicaciones 1 a 7, en la fabricación de un lote de vacuna o un kit de vacuna para la protección frente a la infección por virus de la gripe.
23. El uso de acuerdo con la reivindicación 22, para su administración como dosis única o en más de una dosis, tal 15 como dos dosis.
24. El uso de no más de 15 g, o de menos de 10 g, o menos de 8 g, o de 1-7,5 g o de 1-5 g de antígeno de hemaglutinina de virus de la gripe derivado de huevo de una sola cepa de gripe asociada con un brote pandémico o que tiene el potencial de asociarse con un brote pandémico, en la fabricación de una vacuna de dos dosis para administración parenteral y mucosa simultánea, en el que la hemaglutinina para administración parenteral se ha formulado con un adyuvante como se ha definido en cualquiera de las reivindicaciones 1 a 7.
Patentes similares o relacionadas:
Virus recombinantes de la influenza de alto título con replicación mejorada en células Vero, del 29 de Julio de 2020, de WISCONSIN ALUMNI RESEARCH FOUNDATION: Una célula Vero infectada con un virus de la influenza recombinante aislado reordenado que comprende un segmento del gen HA que codifica […]
Producción de partículas similares al virus de la gripe en plantas, del 6 de Mayo de 2020, de MEDICAGO INC.: Un ácido nucleico que comprende una región reguladora activa en una planta y un potenciador de la expresión activo en una planta, la región […]
Secuencias y composiciones de péptidos, del 25 de Marzo de 2020, de PEPTCELL LIMITED: Una composición de vacuna contra la gripe, que comprende uno o más polipéptidos que tienen no más de 100 aminoácidos y opcionalmente un excipiente […]
Partículas de tipo virus que comprenden proteínas diana fusionadas a proteínas de revestimiento de virus vegetales, del 4 de Septiembre de 2019, de FRAUNHOFER, USA, INC.: Una partícula de tipo virus que consiste en una proteína de fusión, en la que la proteína de fusión comprende (a) una proteína que tiene una secuencia […]
Virus influenza modificado para monitorear y mejorar la eficiencia de la vacuna, del 8 de Mayo de 2019, de ST. JUDE CHILDREN'S RESEARCH HOSPITAL: Una molécula de hemaglutinina (HA) de virus influenza A H5 que comprende una sustitución de aminoácido en el sitio de unión a receptores, en donde la molécula de HA sustituida […]
Anticuerpos neutralizantes del virus de la influenza A y usos de los mismos, del 27 de Marzo de 2019, de INSTITUTE FOR RESEARCH IN BIOMEDICINE (100.0%): Anticuerpo aislado, o un fragmento de unión a antígeno del mismo, que neutraliza la infección de un subtipo del grupo 1 y un subtipo del grupo 2 del virus de la influenza […]
Proteínas de hemaglutinina del virus de la gripe y método de uso de las mismas, del 24 de Septiembre de 2018, de Avatar Medical, LLC: Un polipéptido, proteína o complejo de proteínas de hemaglutinina (HA) del virus de la gripe, que comprende un dominio de tallo de la HA que comprende […]
Vacuna de péptido modificado derivada de M2 de influenza, del 24 de Septiembre de 2018, de The Chemo-Sero-Therapeutic Research Institute: Un péptido modificado que se prepara insertando uno o varios residuos de cisteína en un péptido que consiste en una secuencia de aminoácidos de las posiciones Núm. […]