MÉTODO PARA LA PREPARACIÓN DE ÉSTERES DE MAITANSINOIDES.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2006/001885.
Solicitante: IMMUNOGEN, INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 830 WINTER STREET WALTHAM, MA 02451 ESTADOS UNIDOS DE AMERICA.
Inventor/es: CHARI, RAVI, V., J., WIDDISON,Wayne,C. .
Fecha de Publicación: .
Fecha Solicitud PCT: 20 de Enero de 2006.
Clasificación Internacional de Patentes:
- C07D498/18 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 498/00 Compuestos heterocíclicos que contienen en el sistema condensado al menos un heterociclo que tienen átomos de nitrógeno y oxígeno como únicos heteroátomos del ciclo (4-oxa-1-azabiciclo [3.2.0] heptanos, p. ej. oxapenicilinas C07D 503/00; 5-oxa-1-azabiciclo [4.2.0] octanos, p. ej. oxacefalosporinas C07D 505/00; aquéllos de sus análogos que tienen el átomo de oxígeno del ciclo en otra posición C07D 507/00). › Sistemas puenteados.
Clasificación PCT:
- C07D491/12 C07D […] › C07D 491/00 Compuestos heterocíclicos que contienen en el sistema cíclico condensado, a la vez uno o más ciclos que tienen átomos de oxígeno como únicos heteroátomos del ciclo, y uno o más ciclos que tienen átomos de nitrógeno como únicos heteroátomos del ciclo, no previstos en los grupos C07D 451/00 - C07D 459/00, C07D 463/00, C07D 477/00 ó C07D 489/00. › en los que el sistema condensado contiene tres heterociclos.
- C07D498/06 C07D 498/00 […] › Sistemas peri-condensados.
- C07D498/18 C07D 498/00 […] › Sistemas puenteados.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
Método para la preparación de ésteres de maitansinoides.
Campo de la invención
La presente invención se refiere a un método para preparar maitansinoides que son diastereómeros sustancialmente individuales. Más específicamente, la invención se refiere a un método para preparar ésteres de maitansinoides que contienen tiol o disulfuro, que existen sustancialmente en forma de un diastereómero individual con la estereoquímica L en la cadena lateral en la posición C-3. Estos ésteres de maitansinoides son agentes citotóxicos que pueden usarse como agentes terapéuticos uniéndolos a un agente de unión celular, a través del grupo tiol, y después suministrándolos a una población celular específica de un modo dirigido.
Antecedentes de la invención
Los maitansinoides son fármacos altamente citotóxicos. La maitansina se aisló por primera vez por Kupchan et al. del arbusto del este de África Maytenus serrata y demostró ser de 100 a 1000 veces más citotóxica que agentes quimioterapéuticos contra el cáncer convencionales como el metotrexato, la daunorrubicina, y la vincristina (patente de Estados Unidos Nº 3.896.111). Posteriormente se descubrió que algunos microbios también producen maitansinoides, tales como el maitansinol y ésteres C-3 de maitansinol (patente de Estados Unidos Nº 4.151.042). También se ha informado de ésteres C-3 sintéticos de maitansinol y análogos de maitansinol (Kupchan et al., 21 J. Med. Chem. 31-37 (1978); Higashide et al., 270 Nature 721-722 (1977); Kawai et al., 32 Chem. Pharm. Bull. 3441-3451 (1984)). Ejemplos de análogos de maitansinol de los que se han preparado ésteres C-3 incluyen maitansinol con modificaciones en el anillo aromático (por ejemplo, descloro) o en el C-9, C-14 (por ejemplo, grupo metilo hidroxilado), C-15, C-18, C-20 y C-4,5.
Los ésteres C-3 de origen natural y sintético pueden clasificarse en dos grupos:
Se descubrió que los ésteres del grupo (b) son mucho más citotóxicos que los ésteres del grupo (a). Como los maitansinoides son altamente citotóxicos, se esperaba que fueran útiles en el tratamiento de muchas enfermedades, tales como el cáncer. Esta esperanza aún tiene que hacerse realidad. Los ensayos clínicos con maitansina no fueron favorables debido a varios efectos secundarios (Issel et al., 5 Can. Trtmnt. Rev. 199-207 (1978)). Los efectos adversos sobre el sistema nervioso central y los síntomas gastrointestinales fueron responsables de que algunos pacientes rechazan terapia adicional (Issel en 204), y parecía que la maitansina estaba asociada con neuropatía periférica que puede ser cumulativa (Issel en 207).
Sin embargo, se han descrito formas de maitansinoides que son altamente citotóxicas, que aún pueden usarse de forma eficaz en el tratamiento de muchas enfermedades (patentes de Estados Unidos Nº 5.208.020 y 5.416.064; Chari et al., 52 Cancer Res. 127-131 (1992); Liu et al., 93 Proc. Natl. Acad Sci. 8618-8623 (1996)).
Las patentes de Estados Unidos Nº 5.208.020, 5.416.064 y 6.333.410 describen que un maitansinoide que contiene tiol puede producirse convirtiendo primero un maitansinoide que alberga un grupo éster en maitansinol, después esterificando el maitansinol resultante con una acil N-metil-L-alanina que contiene disulfuro para producir maitansinoides que contienen disulfuro. La reducción del grupo disulfuro con ditiotreitol dio los maitansinoides que contienen tiol. Sin embargo, este proceso implica varias etapas ineficaces que son engorrosos y producen un rendimiento solamente moderado.
Más específicamente, el maitansinol se obtiene primero de la maitansina u otros ésteres de maitansinol por escisión reductora, tal como con hidruro de litio y aluminio. (Kupchan, S.M. et al., 21 J. Med. Chem. 31-37 (1978); patente de Estados Unidos Nº 4.360.462). También es posible aislar el maitansinol del microorganismo Nocardia (véase Higashide et al., patente de Estados Unidos Nº 4.151.042). En un ejemplo específico, se describe la conversión de Ansamitocina P-3 en maitansinol por hidrólisis reductora con hidruro de litio y aluminio en tetrahidrofurano a -5ºC (patente de Estados Unidos Nº 4.162.940).
La siguiente etapa en el proceso es la conversión de maitansinol en diferentes derivados de éster usando derivados de N-metil-L-alanina, y agentes adecuados tales como diciclohexilcarbodiimida (DCC) y cantidades catalíticas de cloruro zinc (véanse las patentes de Estados Unidos Nº 4.137.230, 4.260.609, 5.208.020, 5.416.064 y 6.333.410; Kawai et al., 32 Chem. Pharm. Bull. 3441-3951 (1984)). En todos los casos, se producen dos productos diastereoméricos que contienen las cadenas laterales de D y L-aminoacilo, así como una pequeña parte de maitansinol sin reaccionar. En los procesos descritos previamente (Kupchan, S. M., 21 J. Med. Chem. 31-37 (1978); patente de Estados Unidos Nº 4.360.462; patente de Estados Unidos Nº 6.333.410), el L-aminoacil éster deseado se obtiene después de la purificación sobre dos columnas de gel de sílice o una combinación de columnas de gel de sílice y columnas de HPLC. Además, a causa de la racemización completa, el rendimiento aislado del isómero L-aminoacilo deseado es solamente de aproximadamente el 30%. Por tanto, los procesos descritos hasta ahora son engorrosos, poco rentables y poco tratables para usarse a una escala industrial.
Por consiguiente, se necesita enormemente un proceso mejorado para la preparación y purificación de maitansinoides que contienen tiol, que provoque predominantemente la síntesis de los diastereómeros deseados.
Sumario de la invención
La presente invención abarca un proceso para preparar un éster de maitansinoide que comprende formar un anión de maitansinol u otros maitansinoides que albergan un resto de hidroxilo C-3 libre y haciendo reaccionar el anión con un compuesto de carboxilo activado para producir de este modo el éster de maitansinoide.
El anión de maitansinol puede producirse por reacción de maitansinol con una base.
El compuesto de carboxilo activado, usado para producir un éster de maitansinoide, puede definirse en líneas generales por la fórmula RCOX, donde X es -OCOR' para dar un anhídrido o un anhídrido mixto, o donde X es un haluro, un grupo alcoxi, un grupo ariloxi, o un imidazol y R y R' son iguales o diferentes y se seleccionan entre un alquilo o alquenilo lineal, ramificado o cíclico que tiene de 1 a 10 átomos de carbono, o un resto aminoacídico sustituido, tal como un resto de N-metil-L-alanilo.
Dicho compuesto de carboxilo activado generalmente abarca, aunque sin limitación, anhídridos ácidos, anhídridos mixtos, anhídridos cíclicos, haluros de ácidos, imidazolidas, ésteres o una mezcla de los mismos.
Descripción detallada de la invención
La presente invención proporciona un proceso mejorado para la preparación y purificación de ésteres de maitansinoides, especialmente ésteres de maitansinoides que contienen tiol y disulfuro, que son sustancialmente un diastereómero.
El término "sustancialmente" como se usa en este documento se refiere a un diastereómero de maitansinoide deseado que es aproximadamente o más de aproximadamente el 75%, preferiblemente, el 75-80%, más preferiblemente, el 80-85%, e incluso más preferiblemente, el 85-100% diasteroméricamente puro.
En un aspecto, el proceso de la presente invención comprende formar un anión de maitansinol u otros maitansinoides que albergan un resto de hidroxilo C-3 libre y hacer reaccionar el anión con un compuesto de carboxilo activado para producir de este modo el éster de maitansinoide.
El material de partida para el método es maitansinol o cualquier maitansinoide de origen natural o sintético que alberga un resto de hidroxilo C-3 libre.
Los ejemplos específicos de maitansinoides adecuados incluyen, aunque sin limitación:
Reivindicaciones:
1. Un proceso para preparar un éster de maitansinoide que comprende formar un anión de maitansinol o un maitansinoide que alberga un resto de hidroxilo C-3 libre y hacer reaccionar el anión con un compuesto de carboxilo activado para producir de este modo el éster de maitansinoide.
2. El proceso de la reivindicación 1, en el que el anión se forma haciendo reaccionar el maitansinol o el maitansinoide que alberga un resto de hidroxilo C-3 libre con una base no acuosa.
3. El proceso de la reivindicación 2, en el que la base no acuosa es una hexametildisilazida metálica, un alquilmetal, un arilmetal, un hidruro metálico, sodamida, o amida potásica.
4. El proceso de la reivindicación 3, en el que la hexametildisilazida metálica es hexametildisilazida de zinc, hexametildisilazida sódica, hexametildisilazida de litio, o hexametildisilazida potásica.
5. El proceso de la reivindicación 3, en el que el alquilmetal o arilmetal es metillitio, n-butillitio, terc-butillitio, fenillitio, di-isopropilamida de litio (LDA), pentilsodio, o 2-fenilisopropil-potasio.
6. El proceso de la reivindicación 3, en el que el hidruro metálico es hidruro sódico o hidruro potásico.
7. El proceso de la reivindicación 1, en el que el compuesto de carboxilo activado es al menos un miembro seleccionado entre el grupo compuesto por un anhídrido ácido, un anhídrido mixto, un anhídrido cíclico, un haluro de ácido, una acilimidazolida, una imidazolida sustituida con acilo, y un éster de carboxilo.
8. El proceso de la reivindicación 7, en el que el anhídrido ácido se selecciona entre anhídrido acético, anhídrido isobutírico, o un anhídrido de un derivado de aminoácido.
9. El proceso de la reivindicación 7, en el que el anhídrido mixto se selecciona entre el grupo compuesto por anhídridos mixtos entre un fosfato o sulfato con el resto ácido de ácido acético, ácido propiónico, ácido butírico o un derivado de aminoácido.
10. El proceso de la reivindicación 7, en el que el anhídrido cíclico se selecciona entre el grupo compuesto por un N-carboxianhídrido de N-metil-L-alanina y un N-carboxianhídrido de N-metil-D-alanina.
11. El proceso de la reivindicación 7, en el que el haluro de ácido es un fluoruro de ácido, un cloruro de ácido, un bromuro de ácido o un yoduro de ácido.
12. El proceso de la reivindicación 7, en el que el éster de carboxilo es un éster de N-hidroxisuccinimida, un éster de para-nitrofenilo, un éster de orto-nitrofenilo, un éster de dinitrofenilo, o un éster de pentafluorofenilo.
13. El proceso de la reivindicación 1, en el que el compuesto de carboxilo activado es un compuesto de fórmula RCOX, donde X es un haluro, un grupo alcoxi, un grupo ariloxi, un imidazol o -OY, donde Y es succinimida, ftalimida, arilo o arilo sustituido, y R es un alquilo o alquenilo lineal, ramificado o cíclico que tiene de 1 a 10 átomos de carbono o un resto aminoacídico sustituido.
14. El proceso de la reivindicación 13, en el que el resto aminoacídico sustituido es el resto N-metil-L-alanilo.
15. El proceso de la reivindicación 13, en el que X es fluoruro, cloruro, bromuro o yoduro, piridilo, imidazolilo o imidazolilo sustituido, o -OY, donde Y es succinimida, ftalimida, arilo o arilo sustituido.
16. El proceso de la reivindicación 13, en el que el arilo sustituido es al menos un miembro seleccionado entre el grupo compuesto por para-nitrofenilo, orto-nitrofenilo, dinitrofenilo y pentafluorofenilo.
17. El proceso de la reivindicación 1, en el que el compuesto de carboxilo activado es un ácido anhídrido de fórmula RCOOCOR', donde R y R' son iguales o diferentes y son un alquilo o alquenilo lineal, ramificado o cíclico que tiene de 1 a 10 átomos de carbono o un resto aminoacídico sustituido.
18. El proceso de la reivindicación 17, en el que el resto aminoacídico sustituido es el resto N-metil-L-alanilo.
19. El proceso de la reivindicación 1, en el que el compuesto de carboxilo activado es un compuesto que contiene aminoácido activado por carboxilo.
20. El proceso de la reivindicación 19, en el que el compuesto que contiene aminoácido activado por carboxilo es un compuesto de fórmula (Ia), (Ib), (Ic) o (Id):
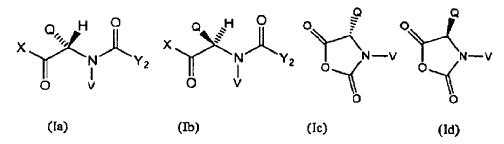
donde:
X representa un haluro, un grupo alcoxi, un grupo ariloxi, un imidazol, o -OY, donde Y es succinimida, ftalimida, arilo o arilo sustituido, un anhídrido o anhídrido mixto; Q representa H o un grupo alquilo ramificado o lineal; V representa H, o un grupo alquilo ramificado o lineal; e Y2 representa (CR7R8)l(CR5R6)m(CR3R4)nCR1R2(SZ2)P, donde:
R1 y R2 son cada uno independientemente H, alquilo o alquenilo lineal, ramificado o cíclico que tiene de 1 a 10 átomos de carbono, fenilo o fenilo sustituido, y además R2 puede ser H;
R3, R4, R5, R6, R7 y R8 son cada uno independientemente H, alquilo o alquenilo lineal, ramificado o cíclico que tiene de 1 a 10 átomos de carbono, fenilo o fenilo sustituido;
l, m y n son cada uno independientemente 0 o un entero de 1 a 5;
Z2 es R9, SR9 o COR9, donde R9 es alquilo lineal, alquilo ramificado o alquilo cíclico que tiene de 1 a 10 átomos de carbono, o arilo simple o sustituido o heterociclilo;
p es 0 ó 1.
21. El proceso de la reivindicación 20, en el que X es fluoruro, cloruro, bromuro, yoduro, piridilo, imidazolilo, imidazolilo sustituido, o -OY, donde Y es succinimida, ftalimida, arilo o arilo sustituido.
22. El proceso de la reivindicación 20, en el que X es -OCOR9, donde R9 es alquilo lineal, alquilo ramificado o alquilo cíclico que tiene de 1 a 10 átomos de carbono, o arilo simple o sustituido o heterociclilo.
23. El proceso de la reivindicación 20, en el que X es un sustituyente que da un anhídrido simétrico de fórmula (Ia) o (Ib).
24. El proceso de la reivindicación 1, 12 ó 20, en el que el anión se forma haciendo reaccionar el maitansinol o un maitansinoide que alberga un resto de hidroxilo C-3 libre con hexametildisilazida de zinc.
25. El proceso de la reivindicación 1, 12 ó 20, en el que el grupo carboxilo activado es un fluoruro de ácido.
26. El proceso de la reivindicación 1, 12 ó 20, en el que el éster de maitansinoide es sustancialmente un diastereómero individual.
27. El proceso de la reivindicación 26, en el que el diastereómero es un L-aminoacil éster.
Patentes similares o relacionadas:
Macrocíclico y composición que comprende el mismo, del 8 de Julio de 2020, de Shenzhen TargetRx, Inc: Un compuesto macrocíclico sustituido, que es un compuesto macrocíclico representado por la fórmula (I), o una forma cristalina, una sal farmacéuticamente […]
Macrociclo de diarilo quiral y uso del mismo en el tratamiento del cáncer, del 24 de Junio de 2020, de Turning Point Therapeutics, Inc: Un compuesto (7S,13R)-11-fluoro-7,13-dimetil-6,7,13,14-tetrahidro-1,15-etenopirazolo[4,3- f][1,4,8,10]benzoxatriazacidotridecin-4(5H)-ona, que tiene la fórmula **(Ver fórmula)** […]
Composición farmacéutica para administración oral que comprende un modulador de P2X7, del 18 de Diciembre de 2019, de JANSSEN PHARMACEUTICA NV: Una composición farmacéutica que comprende: (i) una cantidad terapéuticamente eficaz de un compuesto seleccionado del grupo que consiste de: 11-{[2-Cloro-3-(trifluorometil)fenil]carbonil}-3-pirimidin-2-il-5,6,7,8,9,10-hexahidro-6,10- […]
Derivado de rapamicina para tratar cáncer de páncreas, del 21 de Agosto de 2019, de NOVARTIS PHARMA AG: 40-O-(2-hidroxietil)-rapamicina para su uso como único principio activo en el tratamiento de un tumor sólido, en el que el tumor sólido es un tumor de páncreas […]
Procesos para la preparación de everolimús y productos intermedios del mismo, del 7 de Agosto de 2019, de BIOCON LIMITED: Proceso para obtener everolimús, donde dicho proceso comprende las acciones de: a) añadir anhídrido trifilico a una mezcla de sirulimús, 2-(t-butildimetilsilil) […]
Compuestos de carbamoil-piridona policíclicos y su uso farmacéutico, del 7 de Agosto de 2019, de GILEAD SCIENCES, INC.: Un compuesto que tiene una de las siguientes estructuras:**Fórmula** o una sal farmacéuticamente aceptable del mismo.
Métodos mejorados para la acilación de maitansinol, del 13 de Junio de 2019, de IMMUNOGEN, INC.: Un metodo para preparar un compuesto representado por la siguiente formula:**Fórmula** en donde R1 es metilo; y R2 es metilo, metodo que […]
Derivado de rapamicina para el tratamiento de un tumor sólido asociado con angiogénesis desregulada, del 22 de Mayo de 2019, de NOVARTIS PHARMA AG: 40-O-(2-hidroxietil) -rapamicina para uso en combinación con un inhibidor de la aromatasa para el tratamiento de tumores de mama con receptores hormonales positivos.