USO DE AMINAS, AMINOACIDOS O ESTERES DE AMINOACIDOS COMO MODIFICADORES DE FASE MOVIL EN CROMATOGRAFIA.
Un procedimiento para purificar un lipopéptido usando un modificador de fase móvil en un sistema de cromatografía en fase normal para mejorar la selectividad y/o la productividad de la purificación,
en el que el modificador de fase móvil está seleccionado de un grupo constituido por una amina, un aminoácido o un éster de aminoácido, el sistema de cromatografía en fase normal incluye una fase móvil y una fase estacionaria, la fase móvil es un sistema disolvente que comprende uno o más disolventes, la fase estacionaria está seleccionada de gel de sílice y alúmina, y la amina está seleccionada del grupo constituido por: metilamina, etilamina, diisopropilamina, dietilamina, etilmetilamina, trietilamina, propilamina, anilina y dimetilanilina
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2003/033978.
Solicitante: MERCK & CO., INC..
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 126 EAST LINCOLN AVENUE,RAHWAY, NEW JERSEY 07065-0907.
Inventor/es: GOKLEN,KENT,E, NTI-GYABAAH,JOSEPH, ANTIA,FIROZ,D, DAHLGREN,MARY,ELLEN.
Fecha de Publicación: .
Fecha Concesión Europea: 17 de Febrero de 2010.
Clasificación Internacional de Patentes:
- B01D15/16T
- B01D15/42 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B01 PROCEDIMIENTOS O APARATOS FISICOS O QUIMICOS EN GENERAL. › B01D SEPARACION (separación de sólidos por vía húmeda B03B, B03D, mesas o cribas neumáticas B03B, por vía seca B07; separación magnética o electrostática de materiales sólidos a partir de materiales sólidos o de fluidos, separación mediante campos eléctricos de alta tensión B03C; aparatos centrifugadores B04B; aparato de vórtice B04C; prensas en sí para exprimir los líquidos de las sustancias que los contienen B30B 9/02). › B01D 15/00 Procedimientos de separación que implican el tratamientos de líquidos con absorbentes sólidos; Aparatos para ello. › caracterizado por el modo de desarrollo, p.ej. por desplazamiento o por elución.
- B01J20/283 B01 […] › B01J PROCEDIMIENTOS QUÍMICOS O FÍSICOS, p. ej. CATÁLISIS O QUÍMICA DE LOS COLOIDES; APARATOS ADECUADOS. › B01J 20/00 Composiciones absorbentes o adsorbentes sólidas o composiciones que facilitan la filtración; Absorbentes o adsorbentes para cromatografía; Procedimientos para su preparación, regeneración o reactivación. › a base de sílice.
- B01J20/284 B01J 20/00 […] › a base de alúmina.
- C07K1/16 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › por cromatografía.
- C07K14/37 C07K […] › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › de hongos.
- C07K4/06 C07K […] › C07K 4/00 Péptidos con hasta 20 aminoácidos en una secuencia indeterminada o sólo parcialmente determinada; Sus derivados. › de hongos.
- C07K7/16 C07K […] › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › Oxitocinas; Vasopresinas; Péptidos semejantes.
- C07K7/18 C07K 7/00 […] › Kalidinas; Bradiquininas; Péptidos semejantes.
Clasificación PCT:
- B01D15/00 B01D […] › Procedimientos de separación que implican el tratamientos de líquidos con absorbentes sólidos; Aparatos para ello.
- B01D15/08 B01D 15/00 […] › Adsorción selectiva, p. ej. cromatografía.
- C07K1/16 C07K 1/00 […] › por cromatografía.
- C07K14/00 C07K […] › Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
Clasificación antigua:
- B01D15/00 B01D […] › Procedimientos de separación que implican el tratamientos de líquidos con absorbentes sólidos; Aparatos para ello.
- B01D15/08 B01D 15/00 […] › Adsorción selectiva, p. ej. cromatografía.
- C07K14/00 C07K […] › Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
Fragmento de la descripción:
Uso de aminas, aminoácidos o ésteres de aminoácidos como modificadores de fase móvil en cromatografía.
Referencia cruzada a solicitudes relacionadas
La presente solicitud reivindica el beneficio de la Solicitud Provisional de los Estados Unidos N.º: 60/422.356, presentada el 30 de octubre de 2002.
Campo de la presente invención
La presente invención se refiere al uso de amidas, aminoácidos o ésteres de aminoácidos como modificadores de fase móvil en cromatografía de fase normal de compuestos de lipopéptidos.
Antecedentes de la presente invención
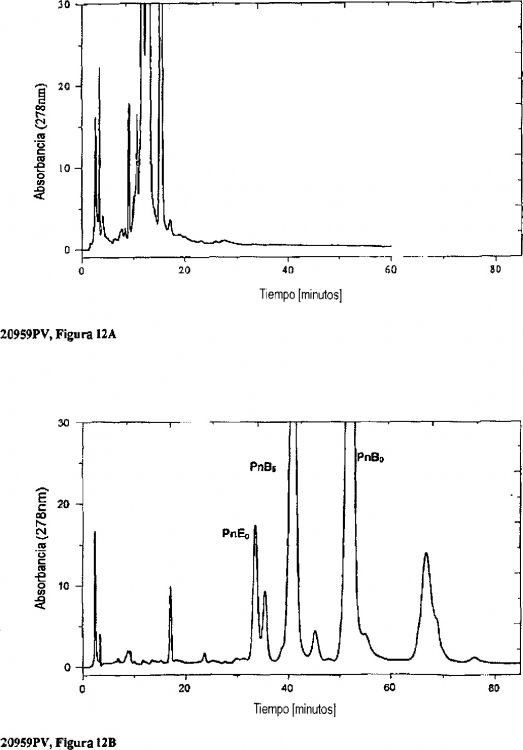
En el pasado, la resolución de impurezas clave tales como Pneumocandinas B5 y E0 a partir de Pneumocandina B0 en la purificación de HPLC en gel de sílice era pobre. Algunos análogos resolvieron sólo parcialmente a partir del producto principal picos según las condiciones de preparación. Para lograr la pureza del producto deseada, la resolución limitada requería que la etapa de purificación se hiciera funcionar a baja carga de columna, lo que limitaba la productividad.
Los lipopéptidos, tales como Pneumocandina B0, son a menudo el producto de un procedimiento de fermentación. Durante un procedimiento de fermentación tal, se producen análogos muy cercanamente seleccionados junto con el producto deseado. Los sistemas de cromatografía en fase normal se usan frecuentemente para purificar el producto de fermentación en bruto. Un sistema de cromatografía en fase normal consiste usualmente en una fase estacionaria y una fase móvil. Para purificación de un péptido o lipopéptido, la fase estacionaria puede ser sílice o alúmina, y la fase móvil puede ser un disolvente individual o una mezcla de disolventes, que incluye los disolventes orgánicos y el agua.
La cromatografía en gel de sílice y otros tipos de la cromatografía en fase normal son útiles para separar estos análogos. Sin embargo, en la práctica, la resolución de ciertos análogos cercanos a partir del producto deseado es a menudo pobre y no satisfactoria, debido a que la resolución no es grande y a menudo hay solapamiento. Lograr la pureza deseada del producto principal a un rendimiento razonable requiere restringir la cantidad de material (a menudo referida como alimento o carga de columna) cargado sobre la columna por ejecución, lo que limita la productividad de la operación.
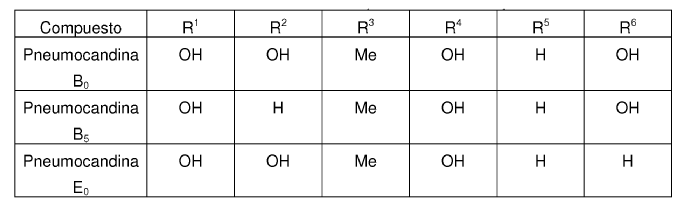
La purificación de Pneumocandina B0 cae dentro de esta categoría. La cromatografía utiliza una fase móvil constituida por una mezcla de disolventes, específicamente acetato de etilo (EtOAc), metanol (MeOH) y agua, en una columna de gel de sílice. La Pneumocandina B0, con un peso molecular de 1065 daltons, es un producto natural y sirve como un intermedio en la producción de acetato de Caspofungina (Cancidas@). La Pneumocandina B0 se produce como un metabolito secundario por fermentación del hongo Glarea lozoyensis. Véanse Patentes de los Estados Unidos N.os 5,194,377 y 5,202,309. Las estructuras de Pneumocandina B0 y dos de las impurezas análogas clave, todas compren- didas en un hexapéptido cíclico acoplado con cadena lateral de dimetilmiristato, se muestran en Fórmula I y Tabla 1.
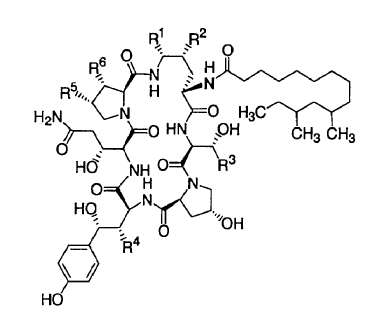
Fórmula I
La cromatografía en gel de sílice explota las variaciones sutiles en afinidad de unión del núcleo de hexapéptido cíclico rico en hidroxi del producto deseado y de las impurezas de análogos, incluyendo Pneumocandinas B5 y E0, para llevar a cabo una separación. En la purificación de HPLC en gel de sílice, las Pneumocandinas B5 y E0, dos de las impurezas clave coproducidas en la fermentación de Pneumocandina B0, eluyen muy cerca de Pneumocandina B0. Por lo tanto, para encontrar los niveles de impureza objetivo en el material purificado para éstos y compuestos análogos similares, la cantidad de Pneumocandina B0 en bruto que se puede cargar en la columna es limitada. Como un resultado, se han hecho esfuerzos significativos para mejorar la resolución de las impurezas clave. Por ejemplo, la fase móvil de acetato de etilo-metanol-agua ternaria se ha equilibrado para optimizar la resolución entre Pneumocandina B0 e impurezas análogas clave. D.J. Roush, F.D. Antia, K.E. Goklen J. Chromatography A, 827 (1998) 373-389. T. Yoshida y T. Okada, J. Chromatography A, 840 (1999) 1-9, describen efectos de fase móvil en separaciones peptídicas usando cromatografía en fase líquida. Se revelan efectos similares en el documento JP 11-023558.
Sumario de la presente invención
La presente invención divulga el uso de modificadores de fase móvil, incluyendo aminoácidos, ésteres de aminoácidos o aminas, durante la purificación de HPLC de un lipopéptido. Los modificadores de fase móvil se unen a la fase estacionaria y modifican las características de unión de la fase estacionaria mejorando la solución y o purificación del lipopéptido deseado a partir de las impurezas relacionadas.
La presente invención es útil en cromatografía analítica e incluso más valiosa para cromatografía preparativa (es decir, usar cromatografía como una técnica de purificación a gran escala). Específicamente, aminoácidos, ésteres de aminoácidos o aminas se pueden usar como modificadores de fase móvil en la purificación cromatográfica de lipopéptidos, por ejemplo la purificación de Pneumocandina B0, que es el material de partida de producto natural (un producto de fermentación) usado para preparar acetato de Capsofungina (Cancidas®). La presente invención podría ser también útil en purificar el precursor de producto de fermentación para otros lipopéptidos, tales como Micafungina, Anidulafungina, Cilofungina y Daptimicina.
Breve descripción de los dibujos
Figura 1
Cromatograma de HPLC preparativa de cromatografía en gel de sílice de Pneumocandina B0 en bruto, donde la alimentación de la columna contiene una pequeña cantidad de prolina. Figura 1A. Primera ejecución de la columna. Figura 1B. Ejecución decimoctavo de la columna. Se ve resolución mejorada de impurezas análogas en la última ejecución debido a la adsorción de prolina a partir de la solución de alimentación en la columna.
Figura 2
Figura 2A. Representación del tiempo de retención de Pneumocandina B0 después de inyectar solución que contiene prolina sobre la columna, mostrando tiempo de retención incrementada, que vuelve al tiempo de retención original, según la prolina se desadsorbe lentamente a partir de la columna. Figura 2B y 2C. Cromatograma de una ejecución típica justo antes (2B) y después (2C)) de inyectar prolina sobre la columna. (Escala analítica columna de sílice de YMC 5 µ usando acetato de etilo/metanol/agua 87/9/7 v/v/v).
Figura 3
Cromatogramas de HPLC en gel de sílice para Pneumocandina B0 en bruto eluidos con la fase móvil: (3A) sin L-prolina, (3B) con L-prolina 0,26 mM añadida, y (3C) con L-prolina 0,65 mM añadida. Muestran tiempo de retención incrementado de Pneumocandina B0 e incrementó solución a partir de niveles análogos de prolina añadidos. (El tiempo de retención de Pneumocandina B0 es 22 minutos con L-prolina 0,65 mM).
Figura 4
Cromatograma de HPLC para Pneumocandina B0 en bruto eluido usando acetato de etilo al 20% y acetato de etilo/metanol/agua 87/9/7 v/v/v al 80% como la fase móvil. Esta mezcla de fase móvil da como resultado tiempo de retención incrementado de Pneumocandina B0 pero sin la resolución incrementada de sus análogos observados cuando se añade prolina a la fase móvil (véase Figura 3). (El tiempo de retención de Pneumocandina B0 es de 23 minutos).
Figuras 5 a 11
Cromatogramas de HPLC en gel de sílice para Pneumocandina B0 en bruto eluidos (A) sin modificador de fase móvil (control) y (B) con la adición de diversos aminoácidos a la fase móvil. Muestran que la adición de todos los aminoácidos tiene un efecto en retención de Pneumocandina B0 y/o en su resolución de sus análogos. (Escala analítica columna de sílice de YMC 5 µ usando acetato...
Reivindicaciones:
1. Un procedimiento para purificar un lipopéptido usando un modificador de fase móvil en un sistema de cromatografía en fase normal para mejorar la selectividad y/o la productividad de la purificación, en el que el modificador de fase móvil está seleccionado de un grupo constituido por una amina, un aminoácido o un éster de aminoácido, el sistema de cromatografía en fase normal incluye una fase móvil y una fase estacionaria, la fase móvil es un sistema disolvente que comprende uno o más disolventes, la fase estacionaria está seleccionada de gel de sílice y alúmina, y la amina está seleccionada del grupo constituido por: metilamina, etilamina, diisopropilamina, dietilamina, etilmetilamina, trietilamina, propilamina, anilina y dimetilanilina.
2. El procedimiento según se expone en la reivindicación 1, en el que el lipopéptido es un precursor de producto de fermentación de caspofungina, micafungina, cilofungina, andulifungina y daptomicina.
3. El procedimiento según se expone en la reivindicación 2, en el que el lipopéptido es Pneumocandina B0.
4. El procedimiento según se expone en cualquiera de las reivindicaciones 1-3, en el que la fase móvil está seleccionada del grupo constituido por: metilamina, etilamina, diisopropilamina, dietilamina, dimetilamina, etilmetilamina, trietilamina, propilamina, anilina y dimetilanilina.
5. El procedimiento según se expone en cualquiera de las reivindicaciones 1-3, en el que el modificador de fase móvil es un aminoácido o un éster de aminoácido.
6. El procedimiento según se expone en la reivindicación 5, en el que el modificador de fase móvil aminoácido o éster de aminoácido está seleccionado del grupo constituido por: L-aminoácidos, D-aminoácidos, ésteres de L-aminoácidos y ésteres de D-aminoácidos.
7. El procedimiento según se expone en la reivindicación 6, en el que el modificador de fase móvil aminoácido o éster de aminoácido está seleccionado de: L-prolina, D-prolina, trans-4-hidroxi-L-prolina, trans-4-hidroxi-D-prolina, glicina, L-treonina, D-treonina, L-lisina, D-lisina, L-metionina, D-metionina, D-valina, L-valina y ésteres de los aminoácidos L- y D- mencionados anteriormente.
8. El procedimiento según se expone en la reivindicación 7, en el que el modificador de fase móvil aminoácido está seleccionado de: L-prolina y D-prolina.
9. El procedimiento según la reivindicación 3, en el que la fase estacionaria es gel de sílice.
10. El procedimiento según se expone en la reivindicación 3, en el que la fase móvil es un sistema disolvente que comprende agua, metanol y acetato de etilo.
Patentes similares o relacionadas:
 Purificación de proteínas, del 29 de Julio de 2020, de UCB Biopharma SRL: Un proceso para la purificación de una proteína de interés a partir de una mezcla que comprende las etapas de
a) en un ciclo de cromatografía operativo, […]
Purificación de proteínas, del 29 de Julio de 2020, de UCB Biopharma SRL: Un proceso para la purificación de una proteína de interés a partir de una mezcla que comprende las etapas de
a) en un ciclo de cromatografía operativo, […]
Composición a base de hidroxiapatita en polvo para el tratamiento del linfoma B o T, del 1 de Julio de 2020, de URODELIA: Composición para uso como autovacuna antitumoral para el tratamiento de linfomas B o T en un sujeto, que comprende un polvo de hidroxiapatita y/o de […]
Eliminación de agregados de proteína de preparaciones biofarmacéuticas en un modo de flujo continuo, del 27 de Mayo de 2020, de MERCK PATENT GMBH: Un método de cromatografía de flujo continuo para separar una proteína monomérica de interés de agregados de proteína en una muestra, comprendiendo […]
Un procedimiento de cromatografía de reparto débil, del 6 de Mayo de 2020, de WYETH LLC: Un procedimiento de recuperación de un producto purificado de un fluido de carga que incluye una o más impurezas, que comprende las etapas de: hacer pasar el fluido […]
Nuevo método de purificación eficiente de albumina sérica humana, del 12 de Febrero de 2020, de Shilpa Medicare Limited: Un método para la purificación de la albúmina humana recombinante, comprendiendo el método las etapas de: a. separar la pluralidad de células […]
Purificación de inmunoglobulina con el uso de etapas de limpieza previa, del 12 de Febrero de 2020, de RICHTER GEDEON NYRT: El procedimiento de purificación de una inmunoglobulina de una muestra que comprende la inmunoglobulina y al menos una impureza, el procedimiento […]
Método de purificación de proteína, del 25 de Diciembre de 2019, de Kyowa Kirin Co., Ltd: Método para purificar una proteína, en el que la proteína se separa de las impurezas utilizando un carbón activado para obtener la proteína con un bajo contenido de impurezas, […]
Método para purificar antitrombina, del 25 de Diciembre de 2019, de Kyowa Kirin Co., Ltd: Método para purificar antitrombina, que comprende las etapas de: (a) adsorber la antitrombina sobre el portador de intercambio aniónico, (b) lavar […]