PROCEDIMIENTOS BASADOS EN RMN PARA DETECTAR LIGANDOS, EN LOS QUE EL LIGANDO O DIANA ESTAN HIPERPOLARIZADOS Y EL ESPECTRO DE RMN DE COMPARA CON UN ESPECTRO DE REFERENCIA DE LIGANDO O DIANA.
Procedimiento basado en RMN para identificar ligandos que se unen a una diana que es una biomolécula,
comprendiendo dicho procedimiento a) hiperpolarizar al menos un ligando o una diana, en el que dicho ligando o dicha diana se enriquecen isotópicamente de forma selectiva con núcleos activos en RMN 13 C y/o 15 N; b) formar una mezcla por contacto del al menos un ligando hiperpolarizado con una diana, o con una diana y al menos un ligando adicional, o poner en contacto la diana hiperpolarizada con al menos un ligando, c) generar un espectro de RMN de la mezcla y d) comparar dicho espectro de RMN con un espectro de referencia del al menos un ligando hiperpolarizado o de la diana hiperpolarizada, respectivamente
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/NO2003/000396.
Solicitante: GE HEALTHCARE AS.
Nacionalidad solicitante: Noruega.
Dirección: NYCOVEIEN 2 0485 OSLO NORUEGA.
Inventor/es: THANING, MIKKEL, HOWARD, MARK, GOLMAN, KLAES, ARDENKJAER-LARSEN, JAN, HENRIK, SERVIN, ROLF, BAUMANN,HERBERT, COTTON,GRAHAM JOHN, WOLBER,JAN, LERCHE,MATHILDE H.
Fecha de Publicación: .
Fecha Solicitud PCT: 27 de Noviembre de 2003.
Fecha Concesión Europea: 11 de Agosto de 2010.
Clasificación Internacional de Patentes:
- G01N24/08 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 24/00 Investigación o análisis de materiales por utilización de la resonancia magnética nuclear, de la resonancia paramagnética electrónica o de otros efectos de spin. › utilizando la resonancia magnética nuclear (G01N 24/12 tiene prioridad).
- G01R33/28A
- G01R33/465 G01 […] › G01R MEDIDA DE VARIABLES ELECTRICAS; MEDIDA DE VARIABLES MAGNETICAS (indicación de la sintonización de circuitos resonantes H03J 3/12). › G01R 33/00 Dispositivos o aparatos para la medida de valores magnéticos. › aplicado a material biológico, p. ej. ensayos in vitro.
Clasificación PCT:
Clasificación antigua:
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
Fragmento de la descripción:
La invención se refiere a procedimientos basados en RMN que comprenden ligandos o dianas hiperpolarizados para su uso en ensayos basados en RMN.
Los diversos proyectos de secuenciación de genoma actualmente en marcha están generando datos a una velocidad muy grande. Las biomoléculas codificadas por las secuencias génicas pertinentes sirven como moléculas diana (= dianas) para identificación o el diseño de compuestos que se unan a las mismas (= ligandos), por ejemplo, como ligandos naturales, como agonistas o antagonistas de un ligando natural, como un inhibidor, un sustrato
o un vector diana. Como tal, la identificación de ligandos es una de las primeras etapas en el descubrimiento de fármacos. El descubrimiento de fármacos comprende tanto la identificación de compuestos candidato, es decir, compuestos que presentan altas afinidades de unión a la diana seleccionada, como un procedimiento de optimización en el que se estudia en detalle la relación estructura-actividad entre la diana y el compuesto candidato identificado. Para acelerar el descubrimiento de fármacos, se emplean bibliotecas de supuestos ligandos naturales o sintéticos en un procedimiento de exploración de alto rendimiento y el parámetro de exploración inicial es habitualmente una alta actividad de unión del ligando hacia la diana. El procedimiento de optimización se centra también en otros parámetros importantes del ligando para que sea adecuado como compuesto farmacológico futuro, tal como estabilidad química y metabólica, no toxicidad y propiedades ADME óptimas (administración, distribución, metabolismo y excreción).
La RMN es una de las herramientas más versátiles en el descubrimiento de fármacos a día de hoy. La RMN no sólo puede contribuir a la identificación de compuestos candidato, sino que también facilita el procedimiento de optimización de compuestos candidato proporcionando información acerca de la estructura molecular e información específica acerca de la unión del ligando a la diana. Existen dos formas diferentes de recoger la información necesaria: el control de las señales de RMN derivadas de la diana o las que surjan del ligando.
Chen y col., J. Am. Chem. Soc. 120 (1998), 10258-10259 describen la denominada “técnica de bombeo de EON” que depende de EON para transferir la señal desde la diana hasta un ligando unido. Se crea una magnetización no en equilibrio por saturación de las moléculas de ligando. Las señales de los ligandos que no se unen a la diana se suprimen por uso de un filtro de difusión (fuerza de gradiente y tiempo de retardo de difusión). Puesto que el filtro de difusión destruye las señales de los ligandos antes de que se aplique una secuencia de EON, sólo la transferencia de polarización desde la diana hasta un ligando unido puede proporcionar polarización a dicho ligando. Cuando el ligando se disocia de la diana, la polarización transferida permanece en el ligando libre. La desventaja del procedimiento descrito es que debido a una relajación rápida (especialmente relajación T2) de la diana la intensidad de señal es reducida, lo que reduce la sensibilidad del procedimiento. Además, el filtro de difusión aplicado requiere un intercambio entre el ligando y la diana. Por lo tanto, la ventana de afinidad en la que pueden controlarse las interacciones está limitada y hace que el procedimiento no sea adecuado para ligandos con una afinidad muy elevada o muy escasa.
Se ha sugerido también una forma diferente de realizar el mismo experimento por A. Chen y col., J. Am. Chem. Soc. 122 (2000), 414-415. Aquí, el mecanismo se invierte en comparación con la técnica de bombeo de EON, en concreto para detectar señales transferidas de un ligando unido a la molécula diana. Se usa un filtro T2 para suprimir las señales diana mientras se mantienen las señales de los ligandos. El resultado es que la intensidad de señal de los ligandos no unidos disminuye debido a la relajación y al bombeo de EON. Para detectar esta diferencia en la pérdida de intensidad de señal, es necesario un espectro de referencia en el que se registre la pérdida de intensidad de señal debido a la relajación. El uso de un filtro T2 limita este procedimiento a sistemas con diferencias relativamente grandes en la relajación T2 entre la diana y el ligando. Esto a su vez requiere que los ligandos estén en equilibrio rápido entre el estado libre y unido. Esto limita el intervalo de afinidades medibles con este procedimiento.
Mayer y col., Angew. Chem. Int. Ed. Engl. 38 (1999), 1784-1788 describen un procedimiento en el que se satura selectivamente una resonancia de diana resuelta. Esto a su vez da como resultado la saturación de la molécula diana completa y cualquier ligando unido a la misma debido a mecanismos de difusión de espín eficaces. Por consiguiente, se aplica un filtro de relajación que permite la observación única de las señales de los ligandos afectados. Se registra un espectro de referencia con irradiación fuera de resonancia y se resta para poner de manifiesto las señales del ligando unido. Puesto que las intensidades del ligando unido pueden traducirse en distancias, el sitio de unión puede cartografiarse. La desventaja de este procedimiento es que mezclas más complejas sólo pueden examinarse usando espectros de RMN 2D. Si sólo están disponibles cantidades pequeñas de diana y/o ligando, el procedimiento requiere mucho tiempo. Además, no pueden medirse ligandos de alta afinidad, debido al filtro de relajación aplicado. Shuker y col., Science 274 (1996), 1531-1534 describen el denominado procedimiento de REA por RMN (REA = relación estructura-actividad) en el que se controlan los cambios de desplazamiento químico en una molécula diana marcada con 15N como una diferencia entre la molécula diana libre y una molécula diana con un ligando unido a la misma. Estos cambios de desplazamiento químico se cartografían sobre la estructura de la diana y los sitios de unión se caracterizan. Los ligandos identificados individualmente con afinidad hacia sitios de unión diferentes en la diana pueden unirse químicamente para dar como resultado un ligando de alta afinidad optimizado. El procedimiento se limita a moléculas diana marcadas con 15N. Además, debe conocerse la asignación espectral de la diana.
El documento WO-A1-97/18471 desvela un procedimiento para explorar supuestos ligandos que se basa en la generación de un primer espectro de correlación de RMN 15N/1H 2D de una proteína enriquecida isotópicamente con 15N y un segundo espectro de correlación de
15115
RMN N/H 2D del complejo de ligando/proteína enriquecido isotópicamente con N. Los cambios del espectro proteico se usan después para identificar el sitio de unión del ligando. De nuevo, este procedimiento se limita a las dianas proteicas enriquecidas isotópicamente con 15N.
El documento WO-A1-00/62074 desvela un procedimiento similar que se basa en y limitado a moléculas diana enriquecidas isotópicamente con 13C.
El documento WO-A1-02/33406 desvela un procedimiento para identificar una molécula de unión usando proteínas marcadas con 13C/15N, en el que los aminoácidos marcados al menos una vez aparecen en las inmediaciones directas de la proteína, generando un primer espectro de RMN tipo HNCO de la diana marcada y un segundo espectro de RMN tipo HNCO del complejo de ligando/diana marcada. Los cambios en el desplazamiento químico se usan después para identificar supuestas moléculas de unión. La desventaja del procedimiento se debe a su limitación a moléculas diana proteicas marcadas de forma especial.
Las desventajas encontradas por los procedimientos de la técnica anterior descritos anteriormente se deben a interferencias de fondo y/o limitaciones de la sensibilidad. Para suprimir las señales de fondo, esos procedimientos implican el uso de los denominados filtros de RMN que, por ejemplo, pueden usarse para suprimir selectivamente señales de la diana y del ligando, respectivamente. Dichos filtros ponen restricciones a los tamaños moleculares y ventanas de afinidad de unión y, por lo tanto, limitan los procedimientos de la técnica anterior. Las limitaciones de sensibilidad pueden ser problemáticas por varias razones: para aliviar dichas limitaciones, son necesarias grandes cantidades de diana o ligando. Las grandes cantidades de ligando necesarias para los procedimientos descritos anteriormente pueden generar demandas de solubilidad rigurosas en los ligandos ensayados y de este modo hacer aún más difícil diseñar bibliotecas de ligando. Además, la reacción puede tener lugar por lo tanto en condiciones que difieran de las condiciones...
Reivindicaciones:
1. Procedimiento basado en RMN para identificar ligandos que se unen a una diana que
es una biomolécula, comprendiendo dicho procedimiento a) hiperpolarizar al menos un ligando o una diana, en el que dicho ligando o dicha diana se enriquecen isotópicamente de forma selectiva con núcleos activos en RMN 13C y/o 15N; b) formar una mezcla por contacto del al menos un ligando hiperpolarizado con una diana, o con una diana y al menos un ligando adicional, o poner en contacto la diana hiperpolarizada con al menos un ligando, c) generar un espectro de RMN de la mezcla y d) comparar dicho espectro de RMN con un espectro de referencia del al menos un ligando hiperpolarizado o de la diana hiperpolarizada, respectivamente.
2. Procedimiento de acuerdo con la reivindicación 1, en el que el ligando se selecciona del grupo que consiste en proteínas, glicoproteínas, lipoproteínas, polipéptidos, glicopolipéptidos, lipopolipéptidos, péptidos, carbohidratos, ácidos nucleicos y moléculas orgánicas pequeñas.
3. Procedimiento de acuerdo con las reivindicaciones 1 a 2, en el que el ligando es una molécula orgánica pequeña de menos de 2000 Da.
4. Procedimiento de acuerdo con las reivindicaciones 1 a 3, en el que se usa más de un ligando hiperpolarizado.
5. Procedimiento de acuerdo con las reivindicaciones 1 a 4, en el que la diana se selecciona del grupo que consiste en proteínas, glicoproteínas, lipoproteínas, ácidos nucleicos, polipéptidos, glicopolipéptidos, lipopolipéptidos y péptidos.
6. Procedimiento de acuerdo con las reivindicaciones 1 a 5, en el que el enriquecimiento es un enriquecimiento con 13C.
7. Procedimiento de acuerdo con las reivindicaciones 1 a 6, en el que el espectro de RMN generado es un espectro de RMN unidimensional.
8. Procedimiento de acuerdo con las reivindicaciones 1 a 7, en el que el espectro de RMN
22 generado se genera usando ángulos de rotación reducidos.
9. Procedimiento de acuerdo con las reivindicaciones 1 a 8, en el que la comparación con el espectro de referencia muestra una diferencia de desplazamiento químico, una diferencia de tiempo de relajación o una diferencia de efecto EON.
Patentes similares o relacionadas:
Método para extraer información codificada en un resultado de una medición de RMN, del 29 de Abril de 2020, de numares AG: Método para extraer información de un espectro de RMN, que comprende las siguientes etapas: a) proporcionar un primer espectro de RMN de una muestra que contiene al menos […]
Método para analizar un espectro de RMN de una muestra que contiene lipoproteína, del 16 de Octubre de 2019, de numares AG: Método para analizar un espectro de RMN de una muestra que contiene lipoproteína, que comprende las siguientes etapas: a) definir un intervalo […]
Dispositivo de espectroscopía de resonancia magnética nuclear (RMN), del 21 de Agosto de 2019, de Wageningen Universiteit: Un dispositivo de espectroscopía de resonancia magnética nuclear (RMN) para realizar mediciones de espectroscopía heteronucleares unidimensionales […]
Método para la caracterización de lipoproteínas, del 13 de Noviembre de 2018, de INSTITUT D'INVESTIGACIÓ SANITÀRIA PERE VIRGILI: Un método in vitro para la caracterización de las lipoproteínas en una muestra, que comprende las siguientes etapas: - obtener un espectro 1H NMR de difusión ordenada en […]
Proceso para la determinación de lipoproteínas en fluidos corporales, del 19 de Noviembre de 2014, de numares AG: Proceso para determinar concentraciones de subclases de lipoproteína k ≥ 1...N en un fluido corporal, estando cada subclase caracterizada por una […]
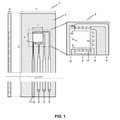 MICROCAMARA Y DISPOSITIVO DE CULTIVO CELULAR MONITORIZABLES POR RESONANCIA MAGNETICA NUCLEAR, del 9 de Agosto de 2012, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención hace referencia a una microcámara y a un dispositivo de cultivo celular, monitorizables por resonancia magnética nuclear y otras técnicas de imagen, […]
MICROCAMARA Y DISPOSITIVO DE CULTIVO CELULAR MONITORIZABLES POR RESONANCIA MAGNETICA NUCLEAR, del 9 de Agosto de 2012, de CONSEJO SUPERIOR DE INVESTIGACIONES CIENTIFICAS (CSIC): La presente invención hace referencia a una microcámara y a un dispositivo de cultivo celular, monitorizables por resonancia magnética nuclear y otras técnicas de imagen, […]
Procedimiento para investigar el destino de un compuesto de ensayo con estrectroscopia de RMN, del 14 de Marzo de 2012, de GE HEALTHCARE LIMITED: Un procedimiento para investigar el destino de un compuesto de ensayo que contiene al menos un núcleo activo de RMN, en el que dicho núcleo activo […]
Formación de imagenes de 13C-RM o de espectroscopia de muerte celular, del 14 de Marzo de 2012, de GE HEALTHCARE AS: Un procedimiento de resonancia magnética para detectar muerte celular, comprendiendo el procedimiento (a) administrar o añadir un medio de formación […]