PROCEDIMIENTO MEJORADO DE PRODUCCION DE LICOPENO MEDIANTE LA FERMENTACION DE CEPAS SELECCIONADAS DE BLAKESLEA TRISPORA.
El procedimiento de fermentación con cepas seleccionadas de B.
Trispora expuesto en la presente invención permite alcanzar unos niveles de producción de licopeno superiores a los actualmente descritos. Los métodos de aislamiento, purificación y formulación son aplicables a cualquier fuente natural de licopeno, especialmente a cultivos sumergidos de hongos mucorales de los géneros Blakeslea, Choanephora, Phycomyces o Mucor. El procedimiento de extracción permite una simplificación en el proceso de recuperación y un incremento de pureza del producto con respecto a los procedimientos anteriormente descritos. Los procedimientos de formulación proporcionan un alto valor añadido, ya que permiten obtener preparaciones estabilizadas de licopeno de aplicación directa en los campos alimentario y farmacéutico
Tipo: Resumen de patente/invención. Número de Solicitud: W0200610ES.
Solicitante: VITATENE, S.A..
Nacionalidad solicitante: España.
Provincia: LEÓN.
Inventor/es: CABRI, WALTER, MUÑOZ RUIZ,ANGEL, ESTRELLA DE CASTRO, ANTONIO, DIEZ GARCIA, BRUNO, COSTA PEREZ, JAVIER, PEIRO CEZON, ENRIQUE, FRAILE YECORA,NIEVES, LOPEZ ORTIZ,JUAN FRANCISCO, MARCOS RODRIGUEZ, ANA TERESA, DE LA FUENTE MORENO,JUAN LUIS, RODRIGUEZ SAIZ,MARTA, BARREDO FUENTE,JOSE LUIS, OLIVER RUIZ,MANUEL ANTONIO.
Fecha de Publicación: .
Fecha Concesión Europea: 4 de Noviembre de 2009.
Clasificación Internacional de Patentes:
- A23L1/275B2
- A23L1/302
- A23L1/30B
- A61K9/107D
- C12P5/02 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12P PROCESOS DE FERMENTACION O PROCESOS QUE UTILIZAN ENZIMAS PARA LA SINTESIS DE UN COMPUESTO QUIMICO DADO O DE UNA COMPOSICION DADA, O PARA LA SEPARACION DE ISOMEROS OPTICOS A PARTIR DE UNA MEZCLA RACEMICA. › C12P 5/00 Preparación de hidrocarburos. › acíclicos.
- C12R1/645 C12 […] › C12R SISTEMA DE INDEXACION ASOCIADO A LAS SUBCLASES C12C - C12Q, RELATIVO A LOS MICROORGANISMOS. › C12R 1/00 Microorganismos. › Hongos.
Clasificación PCT:
- A61K9/14 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 9/00 Preparaciones medicinales caracterizadas por un aspecto particular. › en estado especial, p. ej. polvos (microcápsulas A61K 9/50).
- C09B61/00 C […] › C09 COLORANTES; PINTURAS; PULIMENTOS; RESINAS NATURALES; ADHESIVOS; COMPOSICIONES NO PREVISTAS EN OTRO LUGAR; APLICACIONES DE LOS MATERIALES NO PREVISTAS EN OTRO LUGAR. › C09B COLORANTES ORGANICOS O COMPUESTOS ESTRECHAMENTE RELACIONADOS PARA PRODUCIR COLORANTES; MORDIENTES; LACAS (procesos de fermentación o procesos que utilizan enzimas para la síntesis de un compuesto dado C12P). › Colorantes de origen natural preparados a partir de fuentes naturales.
- C12P23/00 C12P […] › Preparación de compuestos que contienen un ciclo ciclohexeno con una cadena lateral insaturada de al menos diez átomos de carbono unidos por enlaces dobles conjugados, p. ej. carotenos (que contienen heterociclos C12P 17/00).
Clasificación antigua:
- A61K9/14 A61K 9/00 […] › en estado especial, p. ej. polvos (microcápsulas A61K 9/50).
- C09B61/00 C09B […] › Colorantes de origen natural preparados a partir de fuentes naturales.
- C12P23/00 C12P […] › Preparación de compuestos que contienen un ciclo ciclohexeno con una cadena lateral insaturada de al menos diez átomos de carbono unidos por enlaces dobles conjugados, p. ej. carotenos (que contienen heterociclos C12P 17/00).
Fragmento de la descripción:
Procedimiento mejorado de producción de licopeno mediante la fermentación de cepas seleccionadas de Blakeslea trispora.
Campo de la invención
El procedimiento de fermentación con cepas seleccionadas de B. trispora expuesto en la presente invención permite alcanzar unos niveles de producción de licopeno superiores a los actualmente descritos. Los métodos de aislamiento, purificación y formulación son aplicables a cualquier fuente natural de licopeno, especialmente a cultivos sumergidos de hongos mucorales de los géneros Blakeslea, Choanephora, Phycomyces o Mucor. El procedimiento de extracción permite una simplificación en el proceso de recuperación y un incremento de pureza del producto con respecto a los procedimientos anteriormente descritos. Los procedimientos de formulación proporcionan un alto valor añadido, ya que permiten obtener preparaciones estabilizadas de licopeno de aplicación directa en los campos alimentario y farmacéutico.
Estado de la técnica
Los carotenoides están ampliamente distribuidos en la naturaleza, confiriendo su característico color, desde amarillo hasta rojo profundo, a numerosas sustancias naturales como zanahorias, pimientos, tomates, flores o determinados microorganismos entre los que se encuentran ciertas bacterias, hongos y organismos fotosintéticos. Los carotenoides pueden clasificarse en dos tipos: (i) hidrocarburos puros denominados carotenos, entre los que se encuentran compuestos como ß-caroteno, a-caroteno, ?-caroteno o licopeno y (ii) moléculas denominadas xantofilas, las cuales contienen oxígeno en diferentes formas (grupos hidroxi, epoxi, etc.), entre las que se encuentran astaxantina, zeaxantina, capsantina, cantaxantina, luteína, etc. Ambos grupos de compuestos presentan un comportamiento diferente en cuanto a sus propiedades físico-químicas y solubilidad en disolventes orgánicos. Todos estos compuestos juegan un papel importante en la dieta humana habiéndose estudiado ampliamente sus propiedades como antioxidantes para la prevención del cáncer y otras enfermedades humanas y como precursores de la vitamina A. Recientemente se ha demostrado en ratas que el licopeno inhibe el efecto dañino del nitriloacetato férrico sobre el ADN y previene la necrosis del hígado [Matos H.R. et al. (2001) Arch. Biochem. Biophys. vol. 396]. Adicionalmente, debido a sus coloraciones desde amarilla hasta roja, los carotenoides poseen una gran importancia comercial como colorantes y aditivos alimentarios debido a sus efectos beneficiosos para la salud y a sus atractivos colores [Ninet L. y Renaut J. (1979) En: Peppler HJ., Perlman D. (eds). Microbial Technology, 2nd. Edn, vol. 1 Academic Press, NY, pp. 529-544].
El licopeno (C40H56) es un intermediario de la ruta biosintética de ß-caroteno y las xantofilas. Posee un peso molecular de 536,85 y la siguiente fórmula molecular:
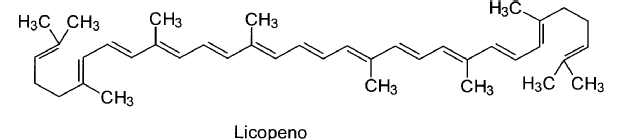
El licopeno, además de actuar como antioxidante, previene enfermedades cardiovasculares y algunos tipos de cáncer y actúa en el control del crecimiento [Giovannucci et al (1995) J Nat. Cancer Inst. 87: 1767-1776; Stahl W. y Sies, H. (1996) Arch. Biochem. Biophys. 336: 1-9; Clinton, SK. (1998) Nutr. Rev. 56: 35-51]. Esto ha dado lugar a un incremento de la demanda por parte de los consumidores. La obtención de licopeno como compuesto de alta pureza ha estado ligada en el pasado a la síntesis química [US 5208381; US 5166445; US 4105855; US 2842599]. No obstante, actualmente existen vías alternativas basadas en fuentes de licopeno de origen natural y procesos de extracción específicos.
La producción de carotenoides mediante biosíntesis microbiana es un ejemplo clásico de competencia entre los procesos químicos y los biológicos. Las preparaciones de licopeno de origen biológico se obtienen a partir de tomate [PCT WO 97/48287, EP 608027] o mediante la fermentación de hongos mucorales de los géneros Phycomyces, Blakeslea y Choanephora [GB 1008469, US 3097146, US 3369974, JP 73016189, JP 73016190, RU 2102416, WO 00/77234]. Para conseguir una máxima producción de carotenoides con B. trispora es preciso fermentar conjuntamente las cepas (+) y (-) [Ciegler, A. (1965) Advances in Applied Microbiology 7: 1-34; Plempel, M. (1965) Planta 65: 225-231; Sutter, RP. y Rafelson, ME. (1968) J. Bacteriology 95: 426-432]. El incremento de producción de carotenoides en cultivos mixtos está correlacionado con la producción de una familia de compuestos ácidos denominados factor ß o ácidos trispóricos [WO 00/77234, Caglioti L. et al. (1966) Tetrahedron Supplement 7: 175-187]. Para biosintetizar ácidos trispóricos, el ß-caroteno producido por las cepas (+) y (-) es metabolizado por ambas a retinal y posteriormente a 4-dihidrotrisporol. La cepa (+) utiliza el 4-dihidrotrisporol como sustrato para formar ácido dihidrotrispórico y su éster metílico (metil-4-dihidrotrisporato). Por su parte, la cepa(-) metaboliza el 4-dihidrotrisporol a trisporol. Finalmente, el metil-4-dihidrotrisporato es convertido en ácido trispórico por la cepa (-) y el trisporol es convertido en ácido trispórico por la cepa (+). Esta descripción de la biosíntesis de los ácidos trispóricos es una simplificación, ya que durante el proceso se generan muchos co-metabolitos, algunos de los cuales son comunes a ambas cepas (+) y (-), pero otros son específicos de una de ellas. Las cantidades relativas de dichos co-metabolitos varían en función de las cepas.
La ruta biosintética de ß-caroteno (ver esquema 1) ha sido descrita en hongos filogenéticamente relacionados con B. trispora como Phycomyces blakesleeanus y Mucor circinelloides [Arrach N. et al. (2001) Proceedings of the National Academic of Sciences USA 98: 1687-1692; Velayos A. et al. (2000) European Journal of Biochemistry 267: 5509-5519]. Para dicha biosíntesis son necesarias al menos tres actividades enzimáticas: (i) fitoeno sintasa, la cual une dos moléculas de geranilgeranil pirofosfato para formar fitoeno, (ii) fitoeno deshidrogenasa, la cual introduce cuatro dobles enlaces en la molécula de fitoeno para sintetizar licopeno, y (iii) licopeno ciclasa, la cual, utilizando licopeno como sustrato, se encarga de formar los anillos situados en ambos extremos de la molécula de ß-caroteno. El análisis de mutantes de B. trispora ha permitido concluir que la ruta biosintética de ß-caroteno en este hongo es similar a la descrita para P. blakesleeanus [Metha B.J. y Cerdá-Olmedo E. (1995) Applied Microbiology and Biotechnology 42: 836-838]. En el caso de P. blakesleeanus, el color amarillo de su micelio puede ser modificado mediante mutación dando lugar a cepas con micelio de color rojo, blanco o varias gradaciones de amarillo. Los mutantes rojos acumulan licopeno, mientras que los blancos carecen de producción de carotenoides o acumulan fitoeno. Para la producción de licopeno es preciso disponer de cepas de B. trispora carentes de actividad licopeno ciclasa o alternativamente adicionar al medio de fermentación compuestos químicos inhibidores de la citada actividad enzimática.
Esquema 1
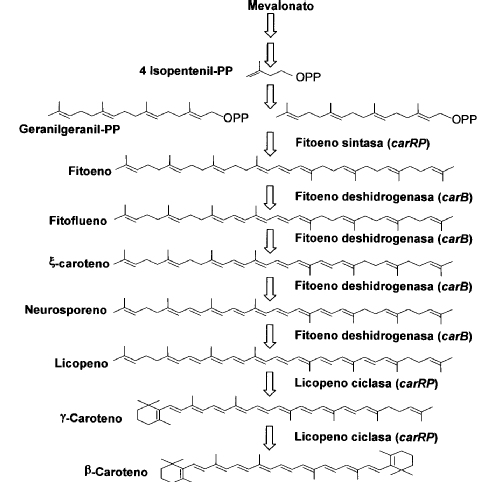
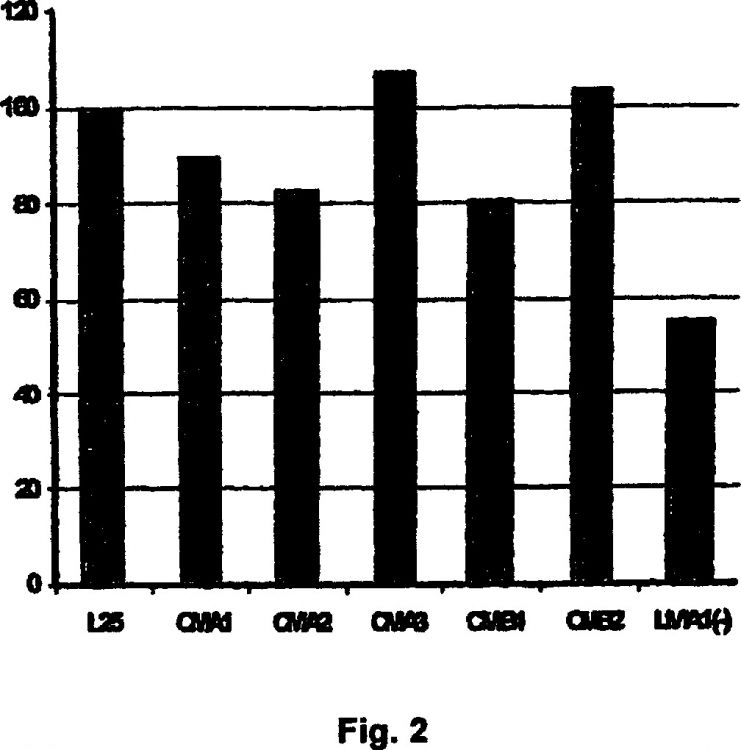
En las patentes GB 1008469, US 3097146, US 3369974, JP 73016189, JP 73016190, RU 2102416 y WO 00/77234 se describe la obtención de licopeno mediante la fermentación de hongos mucorales como Phycomyces, Blakeslea y Choanephora. Las patentes GB 1008469 y US 3097146 describen métodos de fermentación de B. trispora basados en el control del pH entre valores de 7,0 y 9,5, obteniendo producciones de 99,7 mg/l de licopeno tras 7 días de fermentación. Las patentes JP 73016189 Y JP 73016190 describen métodos de producción de licopeno con hongos mucorales basados en la adición aminas terciarias. La patente RU 2102416 describe la adición de aminometilpiridinas y restos de tabaco para inducir la acumulación de licopeno. Además de las sustancias descritas en dichas patentes, se ha publicado el uso de otras bases nitrogenadas heterocíclicas para bloquear la síntesis de carotenoides a nivel de licopeno: nicotina [JP 09313167], imidazol, piridina, morfolina, quinolina y algunos derivados sustituidos [US 3369974; Ninet L., Renaut J. (1979) En: Peppler HJ, Perlman D (eds). Microbial Technology, 2nd. Edn, vol. 1 Academic Press, NY, pp. 529-544]. Asimismo, se han descrito mutantes de B. trispora que acumulan licopeno sin la necesidad de...
Reivindicaciones:
1. Proceso de producción de formulaciones de licopeno a partir de fuentes biosintéticas, que comprende las siguientes etapas en sucesión:
- a. Mezclar, en un medio de cultivo para la producción de licopeno, cepas de superproducción de licopeno (+) y (-) de Blakeslea trispora que consisten, en cepas CPA 1(+) y LMA 1(-) respectivamente, donde LMA 1 (-) se obtiene por mutación de la cepa VKPM F-744 (-) con etilmetano sulfonato (EMS) y N-metil-N'-nitro-N-nitrosoguanidina (NTG) en sucesión, además de la adición de ácidos trispóricos a los mutantes obtenidos y selección de las colonias de color rojo; y CPA 1 (+) se obtiene por mutación de VKPM F-816 (+) con etilmetano sulfonato (EMS) y selección de mutantes cultivándolos en medio sólido complementado con imidazol, transferencia a una placa en la que se ha sembrado previamente B. trispora (-) y selección mediante la intensidad de la coloración de la colonia en la zona de intersección de la colonia de la cepa (+) con la de la cepa (-).
- b. Tratamiento de la biomasa del medio de cultivo de la etapa a) con un alcohol seleccionado entre: metanol, etanol, propanol o isopropanol y separación de una biomasa húmeda purificada.
- c. Acondicionamiento de biomasa húmeda purificada mediante secado y disgregación o ruptura.
- d. Extracción en sólido-líquido del licopeno contenido en la biomasa purificada con un disolvente orgánico de calidad alimentaria.
- e. Concentración del extracto de licopeno enriquecido.
- f. Precipitación/cristalización del licopeno a partir del extracto concentrado mediante la adición de un alcohol, seleccionado entre: metanol, etanol, propanol o isopropanol.
- g. Filtración de los cristales de las aguas de cristalización y secado, dando lugar a cristales de licopeno.
- h. Formulación de licopeno.
2. Proceso, según la reivindicación 1, caracterizado por que la etapa b) se realiza separando previamente la biomasa del medio de cultivo y resuspendiendo de nuevo dicha biomasa en el alcohol, con una proporción de alcohol/biomasa de 1 ml/g a 10 ml/g.
3. Proceso, según la reivindicación 1, caracterizado por que el alcohol utilizado en la etapa b. se usa a una temperatura entre 0ºC y la correspondiente a su punto de ebullición respectivo en dicha etapa b.
4. Proceso, según la reivindicación 3, caracterizado por que el alcohol se usa a una temperatura entre 10ºC y 50ºC.
5. Proceso, según la reivindicación 1, caracterizado por que la etapa b) se realiza directamente mezclando el medio de cultivo de fermentación que contiene la biomasa sin separar previamente, en el alcohol, con una proporción de medio de cultivo/alcohol entre 1/0,5 y 1/5 y a una temperatura entre la temperatura ambiente y el punto de ebullición correspondiente de la mezcla.
6. Proceso, según la reivindicación 5, caracterizado por que la proporción entre medio de cultivo/alcohol está entre 1/1 y 1/3.
7. Proceso, según la reivindicación 5, caracterizado por que la temperatura está entre la temperatura ambiente y 60ºC.
8. Proceso, según la reivindicación 1, caracterizado por que el disolvente usado en la etapa d) es un éster.
9. Proceso, según la reivindicación 8, caracterizado por que el disolvente de tipo éster se selecciona entre: acetato de etilo, acetato de propilo, acetato de isopropilo, acetato de butilo o acetato de isobutilo.
10. Proceso, según la reivindicación 9, caracterizado por que la cantidad de disolvente añadida en la etapa d) varía de 5 a 30 ml por g de la biomasa resultante en la etapa c.
11. Proceso, según la reivindicación 1, caracterizado por que la precipitación/cristalización del licopeno se realiza añadiendo un alcohol en el que la solubilidad del licopeno es muy baja, y que garantiza que las sustancias de carácter lipófilo adjuntas al licopeno permanezcan disueltas, tal como metanol, etanol, propanol o isopropanol.
12. Proceso, según la reivindicación 1, en el que la etapa de formulación h) comprende la preparación de licopeno dispersable en agua fría (CWD), por medio de un proceso que comprende las siguientes etapas:
- i) Se disuelven cristales de licopeno de la etapa g) en disolventes orgánicos, junto con un antioxidante, ajustando la relación temperatura/tiempo con el fin de controlar el porcentaje de licopeno cis en la formulación de licopeno CWD final.
- ii) La disolución del licopeno de la etapa i) se emulsiona o micro-encapsula en una solución acuosa de almidones modificados.
- iii) Los disolventes y parte del agua se eliminan por evaporación, obteniendo la formulación líquida.
- iv) Secado y terminación.
13. Proceso, según la reivindicación 12, caracterizado por que cuando el disolvente empleado en la etapa i) es cloruro de metileno, la temperatura varía entre 20-35ºC durante un tiempo comprendido entre 1 y 15 minutos.
14. Proceso, según la reivindicación 12, caracterizado por que cuando el disolvente empleado en la etapa i) es acetato de isobutilo, la temperatura utilizada es de 114ºC durante un tiempo de 5 minutos.
15. Proceso, según la reivindicación 12, caracterizado por que uno o una mezcla de antioxidantes son usados en la etapa i), en una proporción entre el 1-30% con respecto al peso del licopeno.
16. Proceso, según la reivindicación 15, caracterizado por que el antioxidante usado es de tipo tocoferol o palmitato de ascorbilo.
17. Proceso, según la reivindicación 12, caracterizado por que un aceite vegetal puede ser también añadido en la etapa i).
18. Proceso, según la reivindicación 12, caracterizado por que los almidones modificados usados en la etapa ii) están en forma de ésteres.
19. Proceso, según la reivindicación 18, caracterizado por que los almidones modificados usados en la etapa ii) están en forma de ésteres de octenil succinato.
20. Proceso, según la reivindicación 12, caracterizado por que el secado de la formulación líquida realizado en la etapa iv) se somete a un proceso seleccionado entre: atomización mediante pulverización a alta temperatura, granulación mediante pulverización sobre un lecho fluidizado a temperatura relativamente baja o secado mediante congelación.
21. Proceso, según la reivindicación 20, caracterizado por que el proceso de atomización mediante pulverización a alta temperatura comprende además una etapa de aglomeración mediante pulverización de una solución de uno de los almidones modificados usados en la formulación, o la propia suspensión de licopeno microencapsulado, dentro de un lecho fluidizado de dicho producto atomizado con el fin de aumentar el tamaño de las partículas, reducir el área disponible y aumentar la resistencia a oxidación del producto.
22. Proceso, según la reivindicación 20, caracterizado por que el proceso de granulación mediante pulverización sobre un lecho fluidizado comprende pulverizar una suspensión de licopeno microencapsulado sobre un material de siembra.
23. Proceso, según la reivindicación 22, caracterizado por que el material de siembra es un material inerte.
24. Proceso, según la reivindicación 22, caracterizado por que el material de siembra son partículas de azúcar o polvo fino de material granulado previamente.
25. Proceso, según la reivindicación 12, caracterizado por que la terminación realizada en la etapa iv) consiste en revestir las partículas con soluciones acuosas de azúcares o almidones modificados en una proporción del 0,5-10%.
26. Proceso según cualquiera de las reivindicaciones 1 a 11 en el que la etapa de formulación h. consiste en la formación de una suspensión micro-cristalina de licopeno premezclando cristales de licopeno obtenidos en la etapa g. con antioxidantes y aceites vegetales en proporciones adecuadas, seguido de molienda.
27. Proceso según la reivindicación 26, en el que el aceite usado es de origen vegetal, preferiblemente seleccionado entre aceite de girasol, oliva, maíz, semilla de algodón o soja.
28. Proceso según las reivindicaciones 26 a 27, caracterizado por que se usan antioxidantes liposolubles, preferiblemente tocoferoles naturales, en una proporción del 0,2 al 15%, preferiblemente del 0,5-5% con respecto al peso del licopeno en la mezcla.
Patentes similares o relacionadas:
Preparación de aceite microbiano que contiene ácidos grasos poliinsaturados, del 10 de Junio de 2020, de DSM IP ASSETS B.V.: Un aceite microbiano que comprende al menos el 50% de ácido araquidónico (ARA) basado en el aceite y que tiene un contenido en triglicéridos de al menos el 90%.
Polipéptido degradador de carbohidratos y sus usos, del 13 de Mayo de 2020, de DSM IP ASSETS B.V.: Un polipéptido que tiene actividad como hemicelulasa que comprende la secuencia de aminoácidos indicada en SEQ ID NO: 32 o una secuencia de aminoácidos […]
Extracto de fermento de Eupenicillium crustaceum y uso cosmético del mismo, del 19 de Febrero de 2020, de LUBRIZOL ADVANCED MATERIALS, INC.: Un extracto de fermento de una cepa de la especie Eupenicillium crustaceum, en el que el extracto de fermento comprende del 31 al 79 % en peso de péptidos, del 1 al 8 […]
Proceso para la hidrólisis enzimática de material lignocelulósico y fermentación de azúcares, del 4 de Diciembre de 2019, de DSM IP ASSETS B.V.: Un proceso integrado para la producción de alcohol a partir de material lignocelulósico, en donde el proceso comprende: - pretratamiento […]
Proceso de preparación de un compuesto vinilfenólico a partir de un ácido hidroxicinámico precursor derivado de una torta de semillas oleaginosas, del 4 de Diciembre de 2019, de Institut national de recherche pour l'agriculture, l'alimentation et l'environnement: Procedimiento de preparación de un compuesto vinilfenólico a partir de un ácido hidroxicinámico precursor, caracterizado porque comprende una etapa de biotransformación […]
Variante de levadura oleaginosa, método para obtener la misma y uso de la misma para la producción de lípidos, del 28 de Agosto de 2019, de ENI S.P.A.: Variante de levadura oleaginosa Rhodosporidium azoricum DSM 29495, caracterizada por una alta acumulación de lípidos intracelulares.
Transformante y procedimiento para la producción del mismo, y procedimiento para la producción de ácido láctico, del 28 de Agosto de 2019, de JMTC Enzyme Corporation: Transformante de Schizosaccharomyces pombe que comprende 3 copias de un gen de lactato deshidrogenasa humano, en el que las 3 copias del gen de lactato deshidrogenasa humano […]
SOLUBILIZADOR BIOLÓGICO DE FÓSFORO, del 22 de Agosto de 2019, de BIO INSUMOS NATIVA SpA: La presente invención se refiere a un solubilizador biológico de fósforo (SBF), amigable con el medio ambiente, que comprende una micropartícula acarreadora […]