PROCEDIMIENTO PARA PREPARAR ALDESLEUKINA PARA USO FARMACEUTICO.
Un procedimiento para preparar aldesleukina para uso farmacéutico,
que comprende las etapas de (a) añadir SDS a una composición que comprende aldesleukina, para dar una concentración final de SDS alta; (b) reducir los niveles de SDS para dar una composición con una concentración de SDS baja. La adición y a continuación eliminación parcial de SDS da microagregados de aldesleukina y SDS que son adecuados para uso farmacéutico
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200500241.
Solicitante: CHIRON CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 4560 HORTON STREET,EMERYVILLE, CALIFORNIA 94608.
Inventor/es: HORA,MANINDER.
Fecha de Solicitud: 7 de Febrero de 2005.
Fecha de Publicación: .
Fecha de Concesión: 4 de Marzo de 2010.
Clasificación Internacional de Patentes:
- A61K38/20B
- A61K47/12 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 47/00 Preparaciones medicinales caracterizadas por los ingredientes no activos utilizados, p. ej. portadores o aditivos inertes; Agentes de direccionamiento o agentes modificadores enlazados químicamente al ingrediente activo. › Acidos carboxílicos; Sus sales o anhídridos.
- A61K9/00M5
- A61K9/107D
Clasificación PCT:
- A61K38/20 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Interleuquinas.
- A61K47/12 A61K 47/00 […] › Acidos carboxílicos; Sus sales o anhídridos.
- A61P35/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Agentes antineoplásicos.
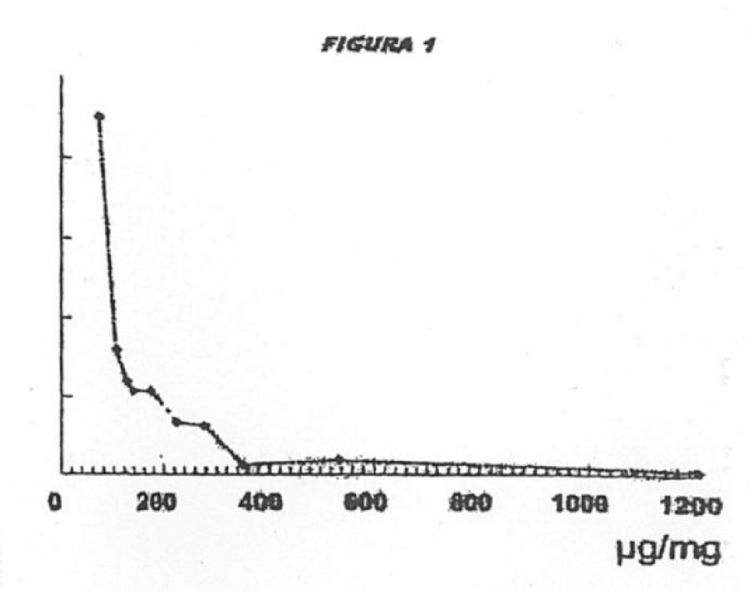
Fragmento de la descripción:
Procedimiento para preparar aldesleukina para uso farmacéutico.
Toda los documentos e información en línea citados en la presente memoria se incorporan en su totalidad como referencia.
Campo técnico
Esta invención es en el campo de la preparación y formulación de interleucina-2 para uso farmacéutico.
Antecedentes de la técnica
La interleucina-2 (IL-2) es una citoquina que fomenta el crecimiento y diferenciación de las células T in vivo y también mejora la citotoxicidad de las células T CD8+ y las células asesinas naturales. La administración a pacientes produce múltiples efectos inmunológicos de una manera dependiente de la dosis, que incluyen activación de la inmunidad celular con linfocitosis profunda, eosinofilia, trombopenia, y la producción de citoquinas que incluye TNF, IL-1 e interferón-?. Detalles adicionales de la IL-2 se pueden encontrar en su "GeneCard" bajo el número de acceso GC04M123831.
La IL-2 se ha aprobado para uso farmacéutico humano en varios países. El nombre común internacional recomendado es ALDESLEUKINA, y se comercializa una formulación de Chiron Corporation bajo la denominación comercial PROLEUKINTM. La FDA de Estados Unidos ha aprobado la IL-2 PROLEUKINTM para uso en el tratamiento de adultos con carcinoma de células renales metastásico (RCC metastásico) o melanoma metastásico.
Como se estipula en su información de prescripciones de EE.UU., la PROLEUKINTM existe como microagregados no covalentemente unidos biológicamente activos con un tamaño medio de 27 moléculas de IL-2 recombinantes. Se suministra como una torta liofilizada estéril de color blanco a blanquecino en viales de un solo uso previstos para administración intravenosa (IV). Cuando se reconstituye con 1,2 ml de agua estéril para inyección, cada mililitro contiene 18 millones de UI (1,1 mg) de IL-2 PROLEUKINTM, 50 mg de manitol, y 0,18 mg de dodecil sulfato de sodio (SDS), tamponado con aproximadamente 0,17 mg de fosfato sódico monobásico y 0,89 mg de fosfato sódico dibásico a pH 7,5. Sin embargo, la mezcla simple de estos ingredientes no da la misma forma microagregada de IL-2 que la encontrada en el producto PROLEUKINTM.
La microagregación de IL-2 en el producto PROLEUKINTM es importante para la eficacia in vivo. Las propiedades farmacocinéticas y farmacodinámicas de la IL-2 no agregada (monomérica libre) son muy diferentes de las de la IL-2 microagregada, y las dos formas tienen índices terapéuticos diferentes: los agregados que son demasiado pequeños son depurados por el cuerpo demasiado rápidamente; los agregados que son demasiado grandes pueden ser insolubles y menos activos. La microagregación es así una característica clave del producto PROLEUKINTM
El procedimiento por el cual se forman los microagregados biológicamente activos de PROLEUKINTM no se ha hecho previamente disponible al público, aunque varios procedimientos para preparar formulaciones farmacéuticas de IL-2 se han descrito en la técnica anterior [por ejemplo véanse las referencias 1 a 30]. La referencia 9 en particular pretende describir el procedimiento de fabricación para la PROLEUKINTM, que incluye detalles de expresión, recuperación, purificación, formulación y terminación, pero esta descripción es incompleta en varios aspectos.
Saber como conseguir la misma forma activa de microagregados de IL-2 que la encontrada en el producto PROLEUKINTM sería útil para cualquiera que quiera hacer un producto de IL-2 similar a PROLEUKINTM. Es por lo tanto un objeto de la invención proporcionar un procedimiento para preparar IL-2 en forma de microagregados coma los encontrados en el producto PROLEUKINTM, y también proporcionar tal IL-2 microagregada. Es un objeto adicional de la invención proporcionar un procedimiento para preparar IL-2 para complementar la descripción de la referencia 9.
Descripción de la invención
El procedimiento por el cual se prepara el producto PROLEUKINTM incluye las etapas clave siguientes: (i) purificación de la IL-2 expresada a partir del cultivo celular; (ii) solubilización de la IL-2 utilizando detergente SDS; (iii) reducción de la IL-2 a forma monomérica; (iv) purificación, oxidación y precipitación de la IL-2; (v) re-solubilización de la IL-2 utilizando un nivel alto de detergente SDS; (vi) purificación para quitar la IL-2 oligomérica; (vii) diafiltración para reducir los niveles de detergente SDS, sin eliminación completa, hasta un intervalo óptimo para obtener una preparación de IL-2 apropiadamente microagregada; (viii) formulación con manitol y tampón; y (ix) liofilización y envasado.
Las etapas (i), (iv), (vi), (viii) y (ix) de este procedimiento se describen en la referencia 9, pero las etapas (ii), (iii), (v) y (vii) no se describen, aunque se describe el uso de un detergente no especificado para re-solubilizar la IL-2 antes de la etapa (vi). Además, la referencia 9 sugiere que se añade SDS a la IL-2 después de la purificación en la etapa (vi), cuando de hecho se elimina.
De las nueve etapas, las más críticas para que se formen los microagregados son la (v) y la (vii). Ninguna de las dos etapas posteriores (viii) o (ix) tienen efecto significativo alguno sobre la microagregación, y los procedimientos de purificación en las etapas (i), (ii), (iii), (iv) y (vi) también tienen poco efecto. Sin embargo, una vez que se añade el SDS en la etapa (v), se disuelve la IL-2, y es la posterior reducción de los niveles de SDS en la etapa (vii) la que causa la formación de los microagregados presentes en el producto final PROLEUKINTM. Se tiene que añadir suficiente SDS para resolubilizar la IL-2 precipitada sustancialmente en una forma soluble monomérica, y a continuación se debe eliminar (pero no completamente) para dar los microagregados deseados.
La invención por lo tanto proporciona un procedimiento para prepara interleucina-2 para uso farmacéutico, que comprende las etapas de: (a) añadir dodecil sulfato de sodio (SDS) a una composición que comprende interleucina-2, para dar una concentración final de SDS de por lo menos 500 µg de SDS por mg de IL-2; (b) eliminar algo del SDS pero no todo de la composición, para dar una composición que contiene entre 95-250 µg de SDS por mg de interleucina-2. Este procedimiento de adición de SDS y después eliminación parcial rinde condiciones óptimas para la interacción íntima de moléculas de IL-2 y SDS para formar microagregados de IL-2 y SDS como los encontrados en el producto PROLEUKINTM y, para una relación IL-2/SDS dada, da lugar a un producto diferente del que se obtiene por simple mezcla de SDS e IL-2.
La composición acuosa que surge del procedimiento se puede liofilizar para distribución, y el producto liofilizado se puede eventualmente reconstituir con un vehículo acuoso para al administración a los pacientes. Después de la reconstitución, la composición preferentemente tiene una turbidez específica (t) menor de 1,1 cm2/g y/o contiene agregados de SDS/IL-2 con un diámetro hidrodinámico medio de entre 8 nm y 20 nm. Así el procedimiento puede además comprender las etapas de liofilizar la composición y a continuación, opcionalmente, reconstituir la composición con un medio acuoso. La composición puede también tener estas 2 y/o características hidrodinámicas antes de la etapa de liofilización.
La invención proporciona una composición que comprende interleucina-2 y dodecil sulfato de sodio, en la que la interleucina-2 y el dodecil sulfato de sodio están presentes en forma de agregados, y en la que los agregados son obtenibles por los procedimientos de la invención. Estas composiciones son adecuadas para uso farmacéutico, como se muestra mediante el producto PROLEUKINTM.
La invención también proporciona una composición que comprende interleucina-2 y dodecil sulfato de sodio, en la que la interleucina-2 y el dodecil sulfato de sodio están presentes en forma de agregados, y en la que la composición tiene una turbidez específica (t) menor de 1,1 cm2/g. Estas composiciones son adecuadas para uso farmacéutico, como se muestra mediante el producto PROLEUKINTM.
La invención también proporciona una composición que comprende interleucina-2 y dodecil sulfato de sodio, en la que la interleucina-2 y el dodecil sulfato de sodio están presentes en forma de agregados, y en la que los agregados tienen un diámetro hidrodinámico medio de entre 8 nm y 20 nm....
Reivindicaciones:
1. Un procedimiento para preparar interleucina-2 para uso farmacéutico, que comprende las etapas de: (a) añadir dodecil sulfato de sodio (SDS) a una composición que comprende interleucina-2 con puentes disulfuro intramoleculares, para dar una concentración final de SDS de por lo menos 500 µg de SDS por mg de IL-2; (b) eliminar cualquier multímero covalente de IL-2 precipitado mediante cromatografía de filtración en gel; (c) reducir la concentración de SDS para eliminar algo del SDS, pero no todo, de la composición para dar una composición que contiene entre 95-250 µg de SDS por mg de interleucina-2.
2. El procedimiento de la reivindicación 1, que comprende las etapas de: purificar la IL-2 mediante RP-HPLC; precipitar la IL-2; añadir dodecil sulfato de sodio (SDS) a la IL-2 precipitada, para dar una concentración final de SDS de al menos 500 µg de SDS por mg de IL-2; eliminar cualquier multímero covalente de IL-2 precipitado mediante cromatografía de filtración en gel; y reducir la concentración de SDS para eliminar algo del SDS, pero no todo, de la composición para dar una composición que contiene entre 95-250 µg de SDS por mg de IL-2.
3. El procedimiento de cualquier reivindicación precedente, en el que la concentración final de SDS en la etapa (a) es por lo menos 900 µg/mg.
4. El procedimiento de cualquier reivindicación precedente, en el que el producto de la etapa (c) tiene una concentración de SDS entre 135-180 µg/mg.
5. El procedimiento de cualquiera de las reivindicaciones precedentes, en el que la concentración de SDS se reduce por diafiltración.
6. El procedimiento de cualquiera de las reivindicaciones precedentes, que además comprende una etapa de: adición de manitol.
7. El procedimiento de cualquiera de las reivindicaciones precedentes, que además comprende una etapa de: liofilización.
8. Una composición que comprende interleucina-2 y dodecil sulfato de sodio, en la que la interleucina-2 y el dodecil sulfato de sodio están presentes en forma de agregados, y en la que los agregados son obtenibles mediante el proceso de una cualquiera de las reivindicaciones precedentes.
9. Una composición que comprende interleucina-2 y dodecil sulfato de sodio, en la que la interleucina-2 y el dodecil sulfato de sodio están presentes en forma de agregados, y en la que la composición tiene una o más de las características siguientes:
- (i) la composición tiene una turbidez específica (t) menor de 1,1 cm2/g; 39
- (ii) la composición contiene agregados de SDS/IL-2 con un diámetro hidrodinámico medio de entre 8 nm y 20 nm; y/o
- (iii) la composición contiene entre 95-250 µg de SDS por mg de interleucina-2.
10. Una composición liofilizada que comprende interleucina-2 y dodecil sulfato de sodio, composición que se puede reconstituir con un medio acuoso para dar la composición de la reivindicación 9.
11. La composición de cualquiera de las reivindicaciones 8-10 precedentes, que tiene una turbidez específica menor de 0,7 cm2/g.
12. La composición de la reivindicación 11, que tiene una turbidez específica entre 0,3 cm2/g y 0,6 cm2/g.
13. La composición de cualquiera de las reivindicaciones 8-12 precedentes, que comprende microagregados de SDS/IL-2 con un diámetro hidrodinámico medio entre 11 nm y 13 nm.
14. El procedimiento de cualquiera de las reivindicaciones 1-7 precedentes, en el que se añade manitol a una concentración final de entre 40 y 50 mg de manitol por mg de IL-2.
15. El procedimiento de cualquiera de las reivindicaciones 1-7 precedentes, en el que la IL-2 es una IL-2 humana.
16. El procedimiento de cualquiera de las reivindicaciones 1-7 precedentes, en el que la IL-2 es una des-alanil-1 IL-2.
17. El procedimiento de cualquiera de las reivindicaciones 1-7 precedentes, en el que la IL-2 es una serina-125 IL-2.
18. El procedimiento de cualquiera de las reivindicaciones 1-7 precedentes, en el que la IL-2 es des-alanil-1, serina-125 IL-2.
19. El procedimiento de cualquiera de las reivindicaciones 1-7 precedentes, en el que la IL-2 tiene la secuencia de aminoácidos SEQ ID NO: 1.
20. El procedimiento de cualquiera de las reivindicaciones 1-7 precedentes, en el que la IL-2 es no glicosilada.
21. La composición de cualquiera de las reivindicaciones 8-13 precedentes, que incluye manitol a una concentración entre 40 y 50 mg de manitol por mg de IL-2.
22. La composición de una cualquiera de las reivindicaciones 8-13 precedentes, en la que la IL-2 es una IL-2 humana.
23. La composición de una cualquiera de las reivindicaciones 8-13 precedentes, en la que la IL-2 es una des-alanil-1 IL-2.
24. La composición de una cualquiera de las reivindicaciones 8-13 precedentes, en la que la IL-2 es una serina-125 IL-2.
25. La composición de una cualquiera de las reivindicaciones 8-13 precedentes, en la que la IL-2 es des-alanil-1, serina-125 IL-2.
26. La composición de una cualquiera de las reivindicaciones 8-13 precedentes, en la que la IL-2 tiene la secuencia de aminoácidos SEQ ID NO: 1.
27. La composición de una cualquiera de las reivindicaciones 8-13 precedentes, en la que la IL-2 es no glicosilada.
28. El procedimiento de cualquiera de las reivindicaciones 1-7 ó 14-20 precedentes, en el que la IL-2 se purifica después de la expresión en un anfitrión procariótico recombinante.
29. La composición de una cualquiera de las reivindicaciones 8-13 6 21-27, que tiene una concentración de IL-2 de 1,1 mg/ml.
30. Una composición farmacéutica liofilizada que, cuando se reconstituye con 1,2 ml de agua estéril para inyección, contiene en cada mililitro: 1,1 mg de desalanil-1, serina-125 IL-2 humana no glicosilada; 50 mg de manitol; 0,18 mg de dodecil sulfato de sodio (SDS); 0,17 mg de fosfato sódico monobásico; y 0,89 mg de fosfato sódico dibásico a pH 7,5, en la que la IL-2 y el SDS están en forma de agregados tales que la composición reconstituida tiene una turbidez específica (t) menor de 1,1 cm2/g.
31. Una composición farmacéutica acuosa, obtenible reconstituyendo la composición liofilizada de la reivindicación 30 con 1,2 ml de agua estéril para inyección.
32. La composición de una cualquiera de las reivindicaciones 8-13, 21-27, 29-31, y un segundo agente farmacéutico, como una preparación combinada para la puesta en práctica de un método terapéutico mediante administración secuencial o separada simultánea.
33. Un kit que comprende (a) la composición de una cualquiera de las reivindicaciones 8-13, 21-27, 29-32; y (b) un segundo agente farmacéutico.
34. La composición de una cualquiera de las reivindicaciones 8-13, 21-27, 29-32, para uso en medicina.
35. El uso de microagregados de (a) interleucina-2 y (b) dodecil sulfato de sodio, en el que los microagregados tienen un diámetro hidrodinámico medio de entre 8 nm y 29 nm, en la fabricación de un medicamento para la administración a un paciente.
36. El uso de una composición que comprende interleucina-2 y dodecil sulfato de sodio, en el que la interleucina-2 y el dodecil sulfato de sodio están presentes en forma de agregados, y en el que la composición tiene una o más de las características siguientes:
- (i) la composición tiene una turbidez específica (t) menor de 1,1 cm2/g;
- (ii) la composición contiene agregados de SDS/IL-2 con un diámetro hidrodinámico medio de entre 8 nm y 20 nm; y/o
- (iii) la composición contiene entre 95-250 µg de SDS por mg de interleucina-2,
en la fabricación de un medicamento para la administración a un paciente.
37. El uso de la reivindicación 35 ó 36, en el que el medicamento es para tratar el cáncer.
38. El uso de la reivindicación 37, en el que el cáncer es carcinoma de células renales.
39. El uso de la reivindicación 37, en el que el cáncer es melanoma.
40. El uso de (a) microagregados de interleucina-2 y dodecil sulfato de sodio, y (b) un segundo agente farmacéutico, en el que los microagregados tienen un diámetro hidrodinámico medio de entre 8 nm y 20 nm, en la fabricación de un medicamento combinado.
41. La composición de la reivindicación 32, en la que el segundo agente farmacéutico es un anticuerpo monoclonal.
42. La composición de la reivindicación 32, en la que el segundo agente farmacéutico es un anticuerpo que proporciona ADCC.
43. La composición de la reivindicación 32, en la que el segundo agente: farmacéutico se selecciona del grupo que consiste en: un anticuerpo anti-CD20; un anticuerpo anti-CD40; un anticuerpo anti-Her2; un anticuerpo anti-EGFR; un anticuerpo anti-VEGF; un anticuerpo anti-CD52; un anticuerpo anti-CD33; un agonista del receptor H2; Bacilo de Calmette-Guerin; talidomida; Lenalidomida; un inhibidor de proteasoma; una combinación de ciclofosfamida, vincristina y prednisona; una combinación de ciclofosfamida, hidroxidoxorubicina, vincristina y prednisona; una citoquina interferón a; interferón ?; 5-fluorouracilo; un compuesto anti-retrovírico; un inhibidor de tirosina quinasa; y Decitabina.
44. La composición de la reivindicación 43, en la que el agonista del receptor de H2 es histamina o una sal farmacéuticamente aceptable de histamina, tal como el dihidrocloruro de histamina.
45. El kit de la reivindicación 33, en el que el segundo agente farmacéutico es un anticuerpo monoclonal.
46. El kit de la reivindicación 33, en el que el segundo agente farmacéutico es un anticuerpo que proporciona ADCC.
47. El kit de la reivindicación 33, en el que el segundo agente farmacéutico se selecciona del grupo que consiste en: un anticuerpo anti-CD20; un anticuerpo anti-CD40; un anticuerpo anti-Her2; un anticuerpo anti-EGFR; un anticuerpo anti-VEGF; un anticuerpo anti-CD52; un anticuerpo anti-CD33; un agonista del receptor H2; Bacilo de Calmette-Guerin; talidomida; Lenalidomida; un inhibidor de proteasoma; una combinación d e ciclofosfamida, vincristina y prednisona; una combinación de ciclofosfamida, hidroxidoxorubicina, vincristina y prednisona; una citoquina; interferón a; interferón ?; 5-fluorouracilo; un compuesto anti-retrovirico; un inhibidor de tirosina quinasa; y Decitabina.
48. El kit de la reivindicación 47, en el que el agonista del receptor de H2 es histamina o una sal farmacéuticamente aceptable de histamina, tal como el dihidrocloruro de histamina.
49. El uso de la reivindicación 40, en el que el segundo agente farmacéutico es un anticuerpo monoclonal.
50. El uso de la reivindicación 40, en el que el segundo agente farmacéutico es un anticuerpo que proporciona ADCC.
51. El uso de la reivindicación 40, en el que el segundo agente farmacéutico se selecciona del grupo que consiste en: un anticuerpo anti-CD20; un anticuerpo anti-CD40; un anticuerpo anti-Her2; un anticuerpo anti-EGFR; un anticuerpo anti-VEGF; un anticuerpo anti-CD52; un anticuerpo anti-CD33; un agonista del receptor H2; Bacilo de Calmette-Guerin; talidomida; Lenalidomida; un inhibidor de proteasoma; una combinación de ciclofosfamida, vincristina y prednisona; una combinación de ciclofosfamida, hidroxidoxorubicina, vincristina y prednisona; una citoquina; interferón a; interferón ?; 5-fluorouracilo; un compuesto anti-retrovírico; un inhibidor de tirosina quinasa; y Decitabina.
52. El uso de la reivindicación 51, en el que el agonista del receptor de H2 es histamina o una sal farmacéuticamente aceptable de histamina, tal como el dihidrocloruro de histamina.
Patentes similares o relacionadas:
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Preparación externa líquida, del 29 de Julio de 2020, de HISAMITSU PHARMACEUTICAL CO. INC.: Una preparación tópica líquida, que comprende: agua; oxibutinina o una sal farmacéuticamente aceptable de la misma; y un éster de ácido dicarboxílico, […]
Método de tratamiento del cáncer, del 22 de Julio de 2020, de Intensity Therapeutics, Inc: Una composición que comprende una cantidad terapéuticamente efectiva de un agente terapéutico y un agente mejorador de la permeación intracelular para uso en el tratamiento […]
Preparaciones ácidas de insulina con estabilidad mejorada, del 15 de Julio de 2020, de SANOFI-AVENTIS DEUTSCHLAND GMBH: Formulación farmacéutica que contiene insulina humana Gly(A21),Arg(B31),Arg(B32) y un tensioactivo, elegido de un grupo que contiene Tween 20® y Tween 80®; siendo […]
Métodos para el tratamiento de la enfermedad ocular en sujetos humanos, del 10 de Junio de 2020, de Clearside Biomedical, Inc: Una formulación farmacéutica que comprende un fármaco para su uso en un método de tratamiento de un trastorno ocular posterior en un sujeto humano que […]
Preparación liofilizada de dipéptidos citotóxicos, del 3 de Junio de 2020, de ONCOPEPTIDES AB: Una preparación farmacéutica liofilizada que comprende (i) melfalán flufenamida, o una sal farmacéuticamente aceptable de la misma; y (ii) al menos un […]
Método y composiciones para el tratamiento de la psoriasis, del 29 de Abril de 2020, de Anaplasi Pharmaceuticals LLC: Una composición tópica en forma de aerosol, espuma o mousse, para el uso en el tratamiento de la psoriasis, en donde la composición comprende: a) del 30 % en […]
Formulación farmacéutica acuosa de tapentadol para administración por vía oral, del 22 de Abril de 2020, de GRUNENTHAL GMBH: Una composición farmacéutica acuosa que contiene tapentadol o una sal fisiológicamente aceptable del mismo y que está adaptada para administración […]