PROCEDIMIENTO PARA OBTENER RESPUESTAS INMUNITARIAS CELULARES DE PROTEINAS.
Una composición inmunógena que comprende un primer antígeno seleccionado y un excipiente farmacéuticamente aceptable,
en la que dicho primer antígeno seleccionado es una partícula de proteína que es diferente estructuralmente de una partícula similar a virus y generalmente de forma esférica, producida mediante un procedimeinto que comprende las etapas de:
(a) proporcionar una solución acuosa de una proteína;
(b) añadir un agente de precipitación a la solución acuosa de la proteína y agitar la mezcla resultante para formar la partícula de proteína;
(c) estabilizar dicha partícula de proteína mediante un tratamiento de estabilización; y
(d) recuperar las partículas de proteína de la solución acuosa
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US00/28040.
Solicitante: CHIRON CORPORATION.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 4560 HORTON STREET,EMERYVILLE, CALIFORNIA 9460.
Inventor/es: SINGH, MANMOHAN, O\'HAGAN, DEREK.
Fecha de Publicación: .
Fecha Concesión Europea: 13 de Enero de 2010.
Clasificación Internacional de Patentes:
- A61K39/21 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Retroviridae, p. ej. virus de la anemia infecciosa equina.
- A61K39/245 A61K 39/00 […] › Herpetoviridae, p. ej. virus del herpes simple.
Clasificación PCT:
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- A61K39/21 A61K 39/00 […] › Retroviridae, p. ej. virus de la anemia infecciosa equina.
- A61K39/245 A61K 39/00 […] › Herpetoviridae, p. ej. virus del herpes simple.
- A61K39/29 A61K 39/00 […] › Virus de la hepatitis.
- A61P31/12 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › A61P 31/00 Antiinfecciosos, es decir antibióticos, antisépticos, quimioterápicos. › Antivirales.
Clasificación antigua:
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
Fragmento de la descripción:
Procedimiento para obtener respuestas inmunitarias celulares de proteínas.
Campo técnico
La presente invención se refiere en general a agentes inmunógenos y a agentes que mejoran la respuesta inmunitaria a un antígeno seleccionado. En particular, la invención se refiere al uso de proteínas como antígenos para obtener respuestas inmunitarias celulares.
Antecedentes
Se han desarrollado numerosas formulaciones de vacunas que incluyen patógenos atenuados o antígenos de subunidades proteicas. Las composiciones de vacuna convencionales a menudo incluyen adyuvantes inmunológicos para mejorar las respuestas inmunitarias mediadas por células y humorales. Por ejemplo, frecuentemente se utilizan adyuvantes de depósito que adsorben y/o precipitan los antígenos administrados y que pueden retener el antígeno en el sitio de inyección. Entre los adyuvantes de depósito típicos se incluyen los compuestos de aluminio y las emulsiones de agua en aceite. Sin embargo, los adyuvantes de depósito, aunque aumentan la antigenicidad, frecuentemente provocan reacciones locales persistentes y severas, como granulomas, abscesos y cicatrices, al ser inyectados subcutánea o intramuscularmente. Otros adyuvantes, como los lipopolisacáridos, pueden provocar respuestas pirógenas al ser inyectados y/o síntomas de Reiter (síntomas similares a la gripe, molestia generalizada en las articulaciones y, en ocasiones, uveítis anterior, artritis y uretritis). Se han utilizado también saponinas, como Quillaja saponaria, como adyuvantes inmunológicos en composiciones de vacuna contra una variedad de enfermedades.
Más en particular, el adyuvante completo de Freund (ACF) es un potente agente inmunoestimulante que ha sido utilizado con éxito con muchos antígenos en base experimental. El ACF incluye tres componentes: un aceite mineral, un agente emulsionante y micobacterias inactivadas, como Mycobacteríum tuberculosis. Aunque efectivo como adyuvante, el ACF presenta severos efectos secundarias principalmente debido a la presencia del componente micobacteriano, incluidos dolor, formación de abscesos y fiebre. Por lo tanto, no se utiliza el ACF en vacunas humanas y veterinarias.
El adyuvante incompleto de Freund (AIF) es similar al ACF pero no incluye el componente bacteriano. El AIF, aunque no está aprobado para uso en los Estados Unidos, ha sido utilizado en otras partes en vacunas humanas contra la gripe y la polio, y en vacunas veterinarias contra la rabia, el moquillo y la fiebre aftosa. Sin embargo, hay pruebas de que tanto el aceite como el emulsionante utilizados en el IFA pueden causar tumores en los ratones.
A pesar de la presencia de dichos adyuvantes, las vacunas convencionales muchas veces no consiguen proporcionar la protección adecuada contra el patógeno diana. A este respecto, hay un cúmulo de indicios que sugieren que la vacunación contra patógenos intracelulares, como una serie de virus, debería dirigirse tanto al brazo celular como humoral del sistema inmunitario. Más en particular, los linfocitos T citotóxicos (LTC) tienen un papel importante en la defensa inmunitaria mediada por célula contra patógenos intracelulares como virus y antígenos específicos tumorales producidos por células malignas. Los LCT median la citotoxicidad de las células infectadas viralmente mediante el reconocimiento de determinantes virales en conjunción con moléculas de CPH de clase I que se observan en las células infectadas. La expresión citoplásmica de proteínas es un prerrequisito para el procesamiento del CPH de clase I y la presentación de péptidos antigénicos a los CTC. Sin embargo, la inmunización con virus inactivados o atenuados frecuentemente no consigue producir los LCT necesarios para frenar la infección intracelular. Además, las técnicas de vacunación convencionales contra virus que exhiben una marcada heterogeneidad genética y/o tasas de mutación rápidas que facilitan la selección de variantes de escape inmunitario, como VIH o gripe, son problemáticas. Por consiguiente, se han desarrollado técnicas de vacunación alternativas.
Se han utilizado portadores particulados con antígenos adsorbidos o inmovilizados en un intento por sortear estos problemas y obtener las respuestas inmunitarias adecuadas. Dichos portadores presentan múltiples copias de un antígeno seleccionado al sistema inmunitario y promueven la inmovilización y la retención de antígenos en los ganglios linfáticos. Las partículas pueden ser fagocitadas por macrófagos y pueden aumentar la presentación de antígenos por medio de la liberación de citocinas. Los ejemplos de portadores particulados incluyen los derivados de polímeros de metacrilato de polimetilo, así como también partículas de polímero derivadas de poli(láctidas) y poli(lactida-co-glicólidos), conocidos como PLG. Aunque ofrecen ventajas significativas con relación a otros sistemas más tóxicos, las partículas de PLG que contienen antígeno presentan algunos inconvenientes. Por ejemplo, la producción a gran escala y la fabricación de portadores particulados pueden resultar problemáticas debido al alto costo de los polímeros utilizados en la fabricación de los portadores particulados.
Se han empleado también liposomas en un intento por superar estos problemas. Los liposomas son vesículas microscópicas formadas a partir de constituyentes lípidos como fosfolípidos que se utilizan para inmovilizar agentes farmacéuticos. Aunque el uso de liposomas como un sistema de administración de fármacos mitiga algunos de los problemas, según se describe anteriormente, los liposomas exhiben una baja estabilidad durante el uso y el almacenamiento, y su producción y fabricación a gran escala resulta problemática.
La publicación internacional N.º WO 98/50071 describe el uso de partículas similares a virus (PSV) como adyuvantes para mejorar las respuestas inmunitarias de los antígenos administrados con las PSV. St. Clair et al. describe el uso de los cristales de proteínas para mejorar las respuestas celulares y humorales. (St. Clair, N. et al., Proc. Natl. Acad. Sci. 96:9469-9474, 1999). Diminsky et al. (Vaccine, 15:637-647, 1997) se refiere a las partículas de antígeno de superficie de la hepatitis B (HBsAg) derivadas del mamífero o de levadura, y a su uso en ratones.
Wade-Evans et al. (J. Gen. Virol., 78: 1611-1616, 1997) describe cristales de la proteína nuclear externa mayor (VP7) del virus de la peste equina (VPE), que se cristaliza espontáneamente en el curso de la purificación viral, y su uso como vacuna en ratones.
Raz et al. (Vaccine, 14:207-211, 1996) trata la vacunación de niños con una dosis reducida de una formulación de vacuna contra la hepatitis B recombinante derivada de células de mamíferos (Bio-Hep-B). La vacuna contenía partículas que albergaban proteínas de superficie del VHB.
El documento US 5,955,342 se refiere a composiciones inmunógenas adecuadas para uso como vacunas, que comprenden partículas similares a retrovirus no infecciosos.
El documento EP-A-0339668 se refiere al antígeno del virus de la hepatitis A (VHA) eficaz para la preparación de vacunas compuestas por partículas inmaduras vacías libres del ARN de virus.
Raychaudhuri et al. (Nature Biotechnology, 16: 1025-1031, 1998) examina los sistemas de administración de vacunas y menciona que las preparaciones de proteínas particuladas (como PSV) son capaces de promover los linfocitos T citotóxicos (LTC).
Speidel et al. (Eur. J. Immunol. 27:2391-1399, 1997) se refieren a la promoción de respuestas de los LTC in vivo por medio del uso de antígenos de proteínas agregadas mediante calor.
Sumario de la invención
Los presentes inventores han descubierto que sorprendentemente las partículas de proteína son agentes inmunógenos autónomos que producen respuestas inmunitarias celulares. En particular, el ingrediente activo es también el sistema de administración, es decir, las partículas de proteína actúan como el antígeno y el sistema de administración. Además, los inventores han descubierto que las partículas de proteína presentan varias ventajas (i) son fáciles de fabricar, (ii) su fabricación es más rentable que la de los agentes existentes, (iii) proporcionan respuestas inmunitarias superiores, y (iv) presentan una toxicidad reducida y eliminan los efectos colaterales indeseados observados con otras formulaciones de vacuna. Por consiguiente, la invención se dirige principalmente al uso de dichas partículas de proteína como antígenos.
La invención proporciona una...
Reivindicaciones:
1. Una composición inmunógena que comprende un primer antígeno seleccionado y un excipiente farmacéuticamente aceptable, en la que dicho primer antígeno seleccionado es una partícula de proteína que es diferente estructuralmente de una partícula similar a virus y generalmente de forma esférica, producida mediante un procedimeinto que comprende las etapas de:
2. La composición inmunógena de la reivindicación 1 en la que la solución acuosa en la etapa (a) comprende además un ácido.
3. La composición inmunógena de la reivindicación 2 en la que el ácido es ácido acético, ácido glicólico, ácido hidroxibutírico, ácido clorhídrico o ácido láctico.
4. La composición inmunógena de la reivindicación 1 en la que el agente de precipitación comprende un aceite, un hidrocarburo o un agente de coacervación.
5. La composición inmunógena de la reivindicación 1 en la que el tratamiento de estabilización comprende tratamiento térmico o tratamiento con un agente químico de reticulación.
6. La composición inmunógena de la reivindicación 5 en la que el tratamiento de estabilización es tratamiento térmico.
7. La composición inmunógena de cualquiera de las reivindicaciones precedentes en la que la partícula de proteína es capaz de producir una respuesta inmunitaria celular.
8. La composición inmunógena de la reivindicación 7 en la que la respuesta inmunitaria celular es un respuesta a linfocitos T citotóxicos.
9. La composición inmunógena de la reivindicación 7 en la que la partícula de proteína se forma a partir de una proteína seleccionada del grupo constituído por una proteína viral, fúngica, bacteriana, aviaria y mamífera.
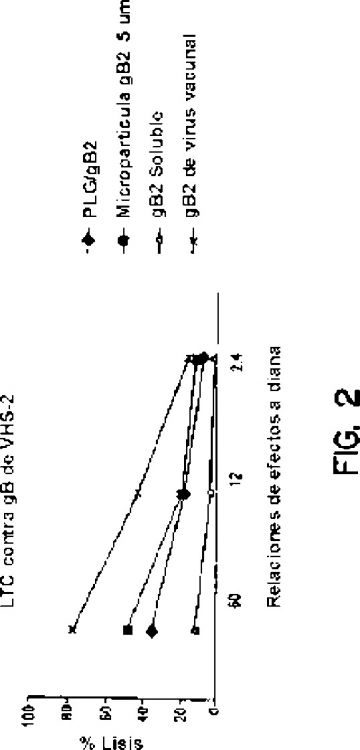
10. La composición inmunógena de la reivindicación 9 en la que la proteína es la glicoproteína B del virus herpes simple de tipo 2 (gB2 de VHS), una proteína del virus de la hepatitis C (VHC) o una proteína del virus de inmunodeficiencia humana (VIH).
11. La composición inmunógena de la reivindicación 10, en la que la proteína del VHC es la proteína nuclear del VHC, E1, E2, NS3, NS4 ó NS5.
12. La composición inmunógena de la reivindicación 10 en la que la proteína del VIH es gp120, gp160, gp41, p24gag o p55gag.
13. La composición inmunógena de la reivindicación 7 que comprende también un adyuvante.
14. La composición inmunógena de la reivindicación 13 en la que dicho adyuvante comprende MF59, LT-K63 o LT-R72.
15. La composición inmunógena de la reivindicación 13 en la que el adyuvante se encuentra encapsulado dentro de la partícula de proteína.
16. La composición inmunógena de la reivindicación 13 en la que el adyuvante es adsorbido o conjugado en la partícula de proteína.
17. La composición inmunógena de la reivindicación 7 que comprende además un segundo antígeno, siendo dicho segundo antígeno distinto de dicha partícula de proteína.
18. La composición inmunógena de la reivindicación 17 en la que dicho segundo antígeno está adsorbido en un portador o encapsulado en éste, estando seleccionadoe dicho portador del grupo compuesto por proteínas, polisacáridos, ácidos polilácticos, ácidos poliglicólicos, aminoácidos poliméricos, copolímeros de aminoácidos, agregados de lípidos, partículas poliméricas y partículas de virus inactivos.
19. La composición inmunógena de la reivindicación 19 en la que dicha partícula polimérica comprende un polímero seleccionado del grupo compuesto pot un poli(a-hidroxi ácido), un ácido polihidroxi butírico, una policaprolactona, un poliortoéster y un polianhídrido.
20. La composición inmunógena de la reivindicación 18 en la que dicho segundo antígeno está conjugado en dicha partícula de proteína.
21. La composición inmunógena de cualquiera de las reivindicaciones precedentes en la que la partícula de proteína es de: (i) entre alrededor de 150 nm y alrededor de 10 µm, (ii) entre alrededor de 200 nm y alrededor de 4 µm o (iii) entre alrededor de 250 nm y alrededor de 3 µm.
22. La composición inmunógena de la reivindicación 1 en la que la partícula de proteína tiene un diámetro: (i) de alrededor de 200 nm a alrededor de 10 µm, (ii) de alrededor de 500 nm a alrededor de 5 µm o (iii) de alrededor de 1 µm a alrededor de 3 µm.
23. La composición inmunógena de cualquier reivindicación precedente para uso en la producción de una respuesta a linfocitos T citotóxicos (LTC) en un individuo vertebrado.
24. Un procedimiento para preparar una composición inmunógena que comprende proporcionar un primer antígeno seleccionado y combinar dicho primer antígeno con un excipiente farmacéuticamente aceptable, siendo dicho primer antígeno una partícula de proteína que es estructuralmente diferente de una partícula similar a virus y generalmente de forma esférica, producida mediante un procedimiento que comprende las etapas de:
25. El procedimiento de la reivindicación 24, que comprende además combinar dicha composición inmunógena con un segundo antígeno, siendo dicho antígeno distinto de dicha partícula de proteína.
26. El uso de un primer antígeno seleccionado y un excipiente farmacéuticamente aceptable, en el que dicho primer antígeno seleccionado es una partícula de proteína que es diferente estructuralmente de una partícula similar a virus y generalmente de forma esférica, y producida mediante un procedimiento que comprende las etapas de:
27. El uso de la reivindicación 26, en el que el medicamento presenta las características de la composición inmunógena de cualquiera de las reivindicaciones 2 a 22.
28. El uso de la reivindicación 26, en el que dicho medicamento puede administrarse con un adyuvante.
29. El uso de la reivindicación 26, en el que dicho medicamento puede administrarse con un segundo antígeno, siendo dicho segundo antígeno diferente de dicho primer antígeno.
30. El uso de la reivindicación 29, en el que dicho medicamento puede administrarse a dicho sujeto vertebrado antes de dicho segundo antígeno.
31. El uso de la reivindicación 29, en el que dicho medicamento puede administrarse a dicho sujeto vertebrado después de dicho segundo antígeno.
32. El uso de la reivindicación 29, en el que dicha partícula de proteína se administra a dicho sujeto vertebrado en forma concurrente con la administración de dicho segundo antígeno.
Patentes similares o relacionadas:
Régimen de glicosidasa para el tratamiento de enfermedades infecciosas, del 15 de Abril de 2020, de Kline, Ellis: Una composición de glicosidasa de señalización inmunológica para uso en el tratamiento de un paciente que tiene una infección viral crónica, en donde un régimen […]
 Inmunógenos de anticuerpos ampliamente neutralizantes del VIH-1, métodos de generación y usos de los mismos, del 25 de Marzo de 2020, de INTERNATIONAL AIDS VACCINE INITIATIVE: Un inmunógeno 10E8 que consiste en la secuencia de aminoácidos:
**(Ver fórmula)**
Inmunógenos de anticuerpos ampliamente neutralizantes del VIH-1, métodos de generación y usos de los mismos, del 25 de Marzo de 2020, de INTERNATIONAL AIDS VACCINE INITIATIVE: Un inmunógeno 10E8 que consiste en la secuencia de aminoácidos:
**(Ver fórmula)**
Vacuna de trímero de Env VIH-1 bioquímicamente estabilizado, del 25 de Diciembre de 2019, de CHILDREN'S MEDICAL CENTER CORPORATION: Un trímero de gp140 de VIH que comprende un polipéptido gp140 de VIH que comprende una secuencia de aminoácidos al menos 95% idéntica a la secuencia: **(Ver secuencia)** […]
Tratamiento de trastornos inflamatorios, autoinmunitarios y neurodegenerativos con polipéptidos derivados de Tat inmunosupresores, del 4 de Septiembre de 2019, de PIN Pharma, Inc: Un polipéptido derivado del trans-activador de la transcripción (Tat) inmunosupresor, comprendiendo el polipéptido derivado de Tat una secuencia de aminoácidos que […]
Vectores víricos Isfahan recombinantes, del 10 de Julio de 2019, de THE BOARD OF REGENTS OF THE UNIVERSITY OF TEXAS SYSTEM: Un virus Isfahan competente en replicación, recombinante que comprende un gen de proteína N que codifica una proteína N que tiene una secuencia de aminoácidos […]
Procedimiento novedoso y composiciones, del 12 de Junio de 2019, de GLAXOSMITHKLINE BIOLOGICALS S.A.: Uno o más primeros polipéptidos inmunógenos para su uso en un procedimiento de generación de una respuesta inmunológica frente a Mycobacterium spp., en los […]
Vectores y construcciones de liberación de antígenos de virus de la gripe, del 8 de Mayo de 2019, de ALTIMMUNE UK LIMITED: Una construcción de vector fluorocarbonado-antígeno de estructura CmFN--CyHx-(Sp)-R, donde m = 3 a 30, n <= 2m + 1, y = 0 a 15, x <= 2y, […]
Vectores de transferencia de gen lentivírico y sus aplicaciones medicinales, del 11 de Abril de 2019, de INSTITUT PASTEUR: Una combinación de compuestos para su uso en el tratamiento terapéutico o profiláctico de una infección por un Virus de la Inmunodeficiencia en donde los […]