PROCEDIMIENTO PARA POTENCIAR O INHIBIR EL FACTOR DE CRECIMIENTO I SIMILAR A LA INSULINA.
Un compuesto de Fórmula II:
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/015957.
Solicitante: THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: OFFICE OF TECHNOLOGY DEVELOPMENT, CAMPUS BOX 4105, 308 BYNUM HALL,CHAPEL HILL, NC 27599-4105.
Inventor/es: CLEMMONS,DAVID,R, MAILE,LAURA,A.
Fecha de Publicación: .
Fecha Concesión Europea: 24 de Marzo de 2010.
Clasificación Internacional de Patentes:
- C07K14/78 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 14/00 Péptidos con más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados. › Péptidos del tejido conectivo, p. ej. colágeno, elastina, laminina, fibronectina, vitronectina, globulina insoluble en frío (CIG).
- C07K16/28B14
- G01N33/50D2B
Clasificación PCT:
- A61K39/00 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
- C07K14/78 C07K 14/00 […] › Péptidos del tejido conectivo, p. ej. colágeno, elastina, laminina, fibronectina, vitronectina, globulina insoluble en frío (CIG).
- G01N33/50 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › Análisis químico de material biológico, p. ej. de sangre o de orina; Ensayos mediante métodos en los que interviene la formación de uniones bioespecíficas con grupos coordinadores; Ensayos inmunológicos (procedimientos de medida o ensayos diferentes de los procedimientos inmunológicos en los que intervienen enzimas o microorganismos, composiciones o papeles reactivos a este efecto, procedimientos para preparar estas composiciones, procedimientos de control sensibles a las condiciones del medio en los procedimientos microbiológicos o enzimáticos C12Q).
Clasificación antigua:
- A61K39/00 A61K […] › Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53).
Fragmento de la descripción:
Procedimiento para potenciar o inhibir el factor de crecimiento I similar a la insulina.
Campo de la invención
La presente invención describe procedimientos para inhibir o potenciar la acción del factor de crecimiento I similar a la insulina (IGF-I).
Antecedentes de la invención
El IGF-I es una hormona polipeptídica pequeña que estimula el crecimiento de todo tipo de células. Debido a que el IGF-I tiene un espectro amplio de acción y estimula el crecimiento equilibrado de tejidos, se ha visto implicado en el desarrollo de varios cánceres humanos importantes y también en la ateroesclerosis. El IGF-I actúa principalmente sobre células dependientes de anclaje que están incluidas en estos tejidos. Estas células poseen también una clase de receptores denominados receptores de integrina, que son responsables de su unión a moléculas de la matriz extracelular. Para que las células se dividan normalmente, la célula, en respuesta a estímulos extracelulares, tiene que sentir que sus receptores de integrina están unidos a moléculas de la matriz extracelular. Por lo tanto, la manipulación de la ocupación del ligando de receptores de integrina puede alterar procesos que son importantes en el desarrollo de enfermedades tales como la división y la migración celular.
Los estudios de los inventores han determinado que el IGF-I estimula la división de las células endoteliales y las del músculo liso. Han determinado, además, que estas células utilizan el receptor de integrina aVß3 para comunicar al núcleo celular que están adheridas adecuadamente a la matriz extracelular con el fin de dividirse. La abundancia de una integrina específica (la integrina aVß3) está relativamente restringida en tejidos humanos y se expresa principalmente en células en crecimiento y, en particular, en células implicadas en el mantenimiento del sistema vascular, tales como las células del músculo liso y las endoteliales. Nuestros estudios han mostrado que la ocupación de este receptor de integrina con sus ligandos naturales tales como osteopontina, vitronectina y trombospondina es necesaria para que estas células respondan al IGF-I con un aumento de la síntesis de ADN y de la migración celular. La ocupación de un ligando bloqueante de esta integrina con antagonistas de desintegrina provoca la inhibición del crecimiento y de la migración celular. Nuestros estudios han mostrado que esta interacción cooperativa entre aVß3 y el receptor de IGF-I está mediada por regulación de la traslocación de dos moléculas señalizadores específicas. Estas moléculas son 1) una proteína tirosina fosfatasa denominada SHP-2 y 2) una proteína señalizadora denominada Shc. En circunstancias normales la SHP-2 se localiza en el citoesqueleto y en compartimentos citosólicos de la célula. Tras la ocupación del ligando de aVß3, el dominio citoplásmico de la integrina ß3 experimenta la fosforilación de tirosina. La SHP-2 se transfiere a la membrana celular uniéndose a proteínas que se unen a los restos de tirosina fosforilados en ß3. Esta transferencia es necesaria para restringir la SHP-2 a la membrana donde capta otras moléculas señalizadores importantes tales como Shc. La colocalización de SHP-2 con Shc y/o desfosforilación de moléculas señalizadoras dentro de la vía de señalización del IGF-I es necesaria para su activación y para la transmisión subsecuente de señales desde el receptor de IGF-I al núcleo. La activación de las dos vías principales de señalización intracelular que son necesarias para la activación del IGF-I (por ejemplo, las vías de la quinasa PI-3 y de la quinasa MAP) pueden inhibirse inhibiendo la transferencia de bien SHP-2 o bien Shc a la membrana. El sitio de restricción de SHP-2 y Shc es una proteína de membrana denominada SHPS-1. La SHPS-1 se fosforila en respuesta al IGF-I. Esta fosforilación es necesaria para la transferencia de SHP-2 y de Shc. La Shc se fosforila después de la transferencia a SHPS-1. La ocupación del ligando aVß3 bloqueante bloquea la transferencia de SHP-2 y Shc, inhibiendo así el crecimiento celular estimulado por el IGF-I.
Aunque se han descrito anteriormente procedimientos para inhibir la ocupación del ligando de la integrina aVß3, todos ellos usan una tecnología que inhibe la unión a un sitio de unión específico en el heterodímero aVß3 que se une a la secuencia arginina, glicina, aspargina (RGD) dentro de los ligandos de la MEC. La unión de antagonistas de aVß3 a este sitio está asociada a toxicidad y efectos secundarios farmacológicos. En consecuencia, existe la necesidad de nuevas vías para inhibir, o activar, la acción de IGF-I, que no utilicen el sitio de unión de aVß3 que se une a la secuencia RGD.
El documento WO9207871 describe oligopéptidos útiles para inhibir la replicación del VIH en individuos infectados víricamente. Vogel y col.; J. Cell Biol.) describen una especificidad de las integrinas novedosa.
Sumario de la invención
En la presente invención, los inventores han determinado que existe un segundo sitio de unión en aVß3 que se une a varias proteínas de la matriz extracelular. De modo más importante, hemos determinado que la potenciación de la ocupación del ligando de este dominio aumenta la ocupación del ligando de inhibición y señalización del IGF-I de este dominio específico e inhibe la acción de IGF-I. De modo importante, la ocupación del ligando de este segundo sitio de unión no estimula los eventos bioquímicos específicos que están estimulados por péptidos que se unen al sitio de unión RGD.
Un primer aspecto de la presente invención es un antagonista del sitio de unión de la proteína de la matriz extracelular de integrina aVß3 (o dominio de un bucle de cisteína incluido en los aminoácidos 177-184 de la subunidad ß3) (por ejemplo, un péptido antagonista o análogo del mismo o anticuerpo que se une al dominio del bucle de cisteína).
Una realización particular de lo anterior es un anticuerpo que se une específicamente al sitio de unión de la proteína de la matriz extracelular de integrina aVß3 (o dominio de bucle de cisteína) (por ejemplo, se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 humana; opcionalmente, pero preferentemente, no se une específicamente al sitio de unión RGD de una integrina ß3 humana; y opcionalmente, pero preferentemente, se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 porcina.
Un segundo aspecto de la presente invención es un agonista del sitio de unión de proteína de la matriz extracelular de integrina aVß3 (o dominio de bucle de cisteína) (por ejemplo, un péptido agonista o análogo del mismo).
Un aspecto adicional de la presente invención es una formulación farmacéutica que comprende un agente activo tal como se describe en el presente documento en un vehículo farmacéuticamente aceptable.
Un aspecto adicional de la presente invención son composiciones y medicamentos para inhibir la acción del IGF-1 en un sujeto con necesidad de ello, comprendiendo dicho sujeto un antagonista del sitio de unión de proteína de la matriz extracelular de integrina aVß3 (o dominio de bucle de cisteína). Por ejemplo, el sujeto puede estar afectado por un tumor (por ejemplo, tumores de cáncer de mama, tumores de cáncer de colon, tumores de cáncer de pulmón y tumores de cáncer de próstata) y el agonista se administra en una cantidad eficaz para tratar el tumor. En algunas realizaciones, el tumor o los vasos sanguíneos que alimentan el tumor expresan receptores de aVß3.
En otro ejemplo, el sujeto está afectado por ateroesclerosis (por ejemplo, ateroesclerosis coronaria), y el antagonista se administra en una cantidad eficaz para tratar la ateroesclerosis. En algunas realizaciones, la ateroesclerosis está caracterizada por células con lesión ateroesclerótica que expresan receptores de aVß3. En otro ejemplo, el sujeto está afectado por osteoporosis, y el antagonista se administra en una cantidad eficaz para tratar la osteoporosis.
En otro ejemplo, el sujeto está afectado por angiogénesis patológica (por ejemplo, vascularización de un tumor, incluidos tumores que expresan niveles de integrina aVß3 detectables por inmunohistoquímica y tumores que no expresan niveles de integrina aVß3 detectables por inmunohistoquímica), y el antagonista se administra en una cantidad eficaz para tratar la angiogénesis patológica.
En otro ejemplo, el sujeto está afectado por diabetes (por ejemplo, diabetes tipo I, diabetes tipo II, retinopatía diabética, nefropatía diabética),...
Reivindicaciones:
1. Un compuesto de Fórmula II:
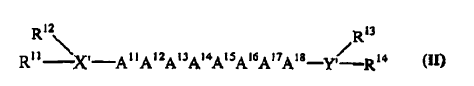
en la que:
A11 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A12 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A13 es cualquier aminoácido;
A14 es cualquier aminoácido;
A15 es un aminoácido aromático seleccionado del grupo constituido por F, Y, W y H;
A16 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A17 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A18 es un aminoácido hidrófobo seleccionado del grupo constituido por I, L y V o un aminoácido neutro seleccionado del grupo constituido por M, F, W, C y A;
X' es una cadena de 0 a 5 aminoácidos, en la que el extremo N de uno de los mismos está unido opcionalmente a R11 y R12;
Y' es una cadena de 0 a 4 aminoácidos, en la que el extremo C de uno de los mismos PUEDE ser fosfoserina o ESTÁ opcionalmente unido a R13 y R14;
R11, R12, R13 y R14 están presentes o ausentes y están seleccionados, cada uno independientemente, del grupo constituido por H, alquilo C1-C12, arilo C6-C18, acilo C1-C12, aralquilo C7-C18 y alcarilo C7-C18;
o una sal farmacéuticamente aceptable del mismo
para la inhibición de la acción del IGF-1 en un sujeto.
2. Uso de un compuesto de Fórmula II:
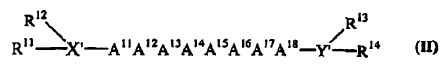
en la que:
A11 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A12 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A13 es cualquier aminoácido;
A14 es cualquier aminoácido;
A15 es un aminoácido aromático seleccionado del grupo constituido por F, Y, W y H;
A16 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A17 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A18 es un aminoácido hidrófobo seleccionado del grupo constituido por I, L y V o un aminoácido neutro seleccionado del grupo constituido por M, F, W, C y A;
X' es una cadena de 0 a 5 aminoácidos, en la que el extremo N de uno de los mismos está unido opcionalmente a R11 y R12;
Y' es una cadena de 0 a 4 aminoácidos, en la que el extremo C de uno de los mismos PUEDE ser fosfoserina o ESTÁ opcionalmente unido a R13 y R14;
R11, R12, R13 y R14 están presentes o ausentes y están seleccionados, cada uno independientemente, del grupo constituido por H, alquilo C1-C12, arilo C6-C18, acilo C1-C12, aralquilo C7-C18 y alcarilo C7-C18;
o una sal farmacéuticamente aceptable del mismo
para la fabricación de un medicamento para inhibir la acción del IGF-I en un sujeto.
3. El compuesto o uso de la reivindicación 2, en el que dicho sujeto está afectado por un tumor seleccionado del grupo constituido por tumores de cáncer de mama, tumores de cáncer de colon, tumores de cáncer de pulmón y tumores de cáncer de próstata.
4. El compuesto o uso de la reivindicación 3, en el que dicho tumor o los vasos sanguíneos que alimentan el tumor expresa los receptores de aVß3.
5. El compuesto o uso de la reivindicación 1 ó 2, en el que dicho sujeto está afectado por ateroesclerosis, y administrándose dicho antagonista en una cantidad eficaz para tratar dicha ateroesclerosis.
6. El compuesto o uso de la reivindicación 5, en el que dicha ateroesclerosis es ateroesclerosis coronaria, carótida o femoral.
7. El compuesto o uso de la reivindicación 5, en el que dicha ateroesclerosis está caracterizada por células con lesión ateroesclerótica que expresan receptores de aVß3.
8. El compuesto o uso de la reivindicación 1 ó 2, en el que dicho sujeto está afectado por osteoporosis, y administrándose dicho antagonista en una cantidad eficaz para tratar dicha osteoporosis.
9. El compuesto o uso de la reivindicación 1 ó 2, en el que dicho sujeto está afectado por angiogénesis patológica, retinopatía o nefropatía, y administrándose dicho antagonista en una cantidad eficaz para tratar dicha angiogénesis patológica, retinopatía o nefrepatía.
10. El compuesto o uso de la reivindicación 9, comprendiendo dicha angiogénesis patológica la vascularización de un tumor.
11. Un compuesto de la Fórmula I:
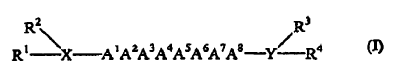
en la que:
A1 es un aminoácido básico seleccionado del grupo constituido por R, K y H o una serina fosforilada;
A2 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A3 es cualquier aminoácido;
A4 es cualquier aminoácido;
A5 es un aminoácido aromático seleccionado del grupo constituido por F, Y, W y H;
A6 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A7 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A8 es un aminoácido básico seleccionado del grupo constituido por R, K y H o una serina fosforilada;
X es una cadena de 0 a 5 aminoácidos, en la que el extremo N de uno de los mismos está opcionalmente unido a R1 y R2;
Y es una cadena de 0 a 4 aminoácidos, en la que el extremo C de uno de los mismos está opcionalmente unido a R3 y R4; y
R1, R2, R3 y R4 están presentes o ausentes y están seleccionados, cada uno independientemente, del grupo constituido por H, alquilo C1-C12, arilo C6-C18, acilo C1-C12, aralquilo C7-C18 y alcarilo C7-C18;
o una sal farmacéuticamente aceptable del mismo
para potenciar la acción de IGF-I en un sujeto.
12. Uso de un compuesto de Fórmula I:
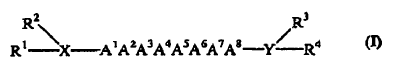
en la que:
A1 es un aminoácido básico seleccionado del grupo constituido por R, K y H o una serina fosforilada;
A2 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A3 es cualquier aminoácido;
A4 es cualquier aminoácido;
A5 es un aminoácido aromático seleccionado del grupo constituido por F, Y, W y H;
A6 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A7 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A8 es un aminoácido básico seleccionado del grupo constituido por R, K y H o una serina fosforilada;
X es una cadena de 0 a 5 aminoácidos, en la que el extremo N de uno de los mismos está opcionalmente unido a R1 y R2;
Y es una cadena de 0 a 4 aminoácidos, en la que el extremo C de uno de los mismos está opcionalmente unido a R3 y R4; y
R1, R2, R3 y R4 están presentes o ausentes y están seleccionados, cada uno independientemente, del grupo constituido por H, alquilo C1-C12, arilo C6-C18, acilo C1-C12, aralquilo C7-C18 y alcarilo C7-C18;
o una sal farmacéuticamente aceptable del mismo
para la fabricación de un medicamento para potenciar la acción del IGF-I en un sujeto.
13. El compuesto o uso de las reivindicaciones 11 ó 12, en el que dicho sujeto está afectado por crecimiento deficiente, y administrándose dicho agonista una cantidad eficaz para potenciar el crecimiento de dicho sujeto.
14. El compuesto o uso de la reivindicación 13, en el que dicho sujeto es un lactante, niño o adolescente.
15. El compuesto o uso de la reivindicación 13, en el que dicho sujeto está afectado por vascularización retinal defectuosa, y administrándose dicho agonista en una cantidad eficaz para tratar dicha vascularización retinal defectuosa.
16. El compuesto o uso de la reivindicación 15, en el que dicho sujeto es un lactante.
17. El compuesto o uso de las reivindicaciones 11 ó 12, en el que dicho sujeto está afectado por una lesión isquémica, y administrándose dicho agonista en una cantidad eficaz para tratar dicha lesión isquémica.
18. El compuesto o uso de la reivindicación 17, en el que dicha lesión isquémica comprende enfermedad vascular periférica con claudicación.
19. El compuesto o uso de las reivindicaciones 11 ó 12, en el que dicho sujeto está afectado por atrofia neuronal o insuficiencia en el desarrollo de procesos neuronales, y administrándose dicho agonista en una cantidad eficaz para tratar dicha atrofia neuronal o facilitar el desarrollo de procesos neurales.
20. El compuesto o uso de las reivindicaciones 11 ó 12, en el que dicho sujeto está afectado por una fractura de cadera y administrándose dicho agonista en una cantidad eficaz para tratar dicha fractura de cadera.
21. El compuesto o uso de la reivindicación 20, en el que dicho sujeto es un adulto o anciano.
22. El compuesto o uso de las reivindicaciones 11 ó 12, en el que dicho sujeto está afectado por una úlcera isquémica diabética, y administrándose dicho agonista en una cantidad eficaz para tratar dicha úlcera isquémica diabética.
23. Un anticuerpo que: (a) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 humana, (b) no se une específicamente al sitio de unión RGD de una integrina ß3 humana; y (c) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 porcina para su uso en la inhibición de la acción del IGF-I en un sujeto.
24. El uso de un anticuerpo que: (a) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 humana, (b) no se une específicamente al sitio de unión RGD de una integrina ß3 humana; y (c) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 porcina en la fabricación de un medicamento para la inhibición de la acción del IGF-I en un sujeto.
25. El compuesto o uso de las reivindicaciones 1 ó 2, 23 ó 24, en el que dicho sujeto está afectado por retinopatía o nefropatía diabética con necesidad de tratamiento, administrándose dicho antagonista del dominio de bucle de cisteína de la integrina aVß3 en una cantidad eficaz de tratamiento.
26. Un compuesto seleccionado del grupo constituido por las SEQ ID Nº: 8-37 y 39-44.
27. Una formulación farmacéutica que comprende un compuesto de la reivindicación 26 en un vehículo farmacéuticamente aceptable.
28. Un compuesto de Fórmula II:
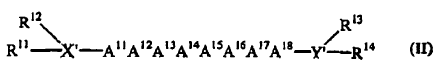
en la que:
A11 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A12 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A13 es cualquier aminoácido;
A14 es cualquier aminoácido;
A15 es un aminoácido aromático seleccionado del grupo constituido por F, Y, W y H;
A16 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A17 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A18 es un aminoácido hidrófobo seleccionado del grupo constituido por I, L y V o un aminoácido neutro seleccionado del grupo constituido por M, F, W, C y A;
X' es una cadena de 0 a 5 aminoácidos, en la que el extremo N de uno de los mismos está unido opcionalmente a R11 y R12;
Y' es una cadena de 0 a 4 aminoácidos, en la que el extremo C de uno de los mismos puede ser fosfoserina o está opcionalmente unido a R13 y R14;
R11, R12, R13 y R14 están presentes o ausentes y están seleccionados, cada uno independientemente, del grupo constituido por H, alquilo C1-C12, arilo C6-C18, acilo C1-C12, aralquilo C7-C18 y alcarilo C7-C18;
o una sal farmacéuticamente aceptable del mismo.
29. Una formulación farmacéutica que comprende un compuesto de la reivindicación 28 en un vehículo farmacéuticamente aceptable.
30. Un implante que tiene un compuesto de la reivindicación 28 acoplado al mismo.
31. El implante de la reivindicación 30, en el que dicho implante es una endoprótesis vascular o un implante oftálmico.
32. Un anticuerpo que: (a) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 humana, (b) no se une específicamente al sitio de unión RGD de una integrina ß3 humana; y (c) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 porcina.
33. Un anticuerpo de la reivindicación 32 acoplado a un grupo detectable.
34. El anticuerpo de la reivindicación 32 acoplado a un grupo terapéutico.
35. Una formulación farmacéutica que comprende un anticuerpo de la reivindicación 32 en un vehículo farmacéuticamente aceptable.
36. Un implante que tiene un anticuerpo de la reivindicación 32 acoplado al mismo.
37. El implante de la reivindicación 36, en el que dicho implante es una endoprótesis vascular o un implante oftálmico.
38. Un procedimiento para seleccionar compuestos por su actividad en la activación de la modulación celular por IGF-I, que comprende las etapas de:
(a) poner en contacto un compuesto de ensayo con un dominio de bucle de cisteína; después
(b) determinar si dicho compuesto de ensayo se une al dominio de bucle de cisteína en los aminoácidos 177 a 184 de dicha integrina ß3
(c) identificar dicho compuesto de ensayo como activo en la activación de la activación celular por IGF-1 si dicho compuesto se une al dominio de bucle de cisteína.
39. El procedimiento de la reivindicación 38, en el que dicho sistema comprende una integrina aVß3.
40. El procedimiento de la reivindicación 38, en el que dicha etapa de puesta en contacto se realiza in vitro.
41. El procedimiento de la reivindicación 38, en el que dicha etapa de determinación se realiza determinando si dicho compuesto de ensayo inhibe o no la unión de una anticuerpo que se une específicamente a dicho dominio de bucle de cisteína.
42. El procedimiento de la reivindicación 38, en el que dicha integrina ß3 es una integrina ß3 de mamífero.
43. El procedimiento de la reivindicación 38, en el que dicha integrina ß3 es una integrina ß3 de mamífero seleccionada del grupo constituido por integrina ß3 humana y porcina.
44. Un procedimiento para seleccionar compuestos por su actividad en la modulación de la activación celular por IGF-I, que comprende las etapas de:
(a) poner en contacto un compuesto de ensayo con un dominio de bucle de cisteína; después
(b) determinar si dicho compuesto de ensayo se une al dominio de bucle de cisteína en los aminoácidos 177 a 184 de dicha integrina ß3;
(c) identificar dicho compuesto de ensayo como activo en la activación de la activación celular por IGF-1 si dicho compuesto se une al dominio de bucle de cisteína.
45. El procedimiento de la reivindicación 44, en el que dicho dominio de bucle de cisteína está inmovilizado en un soporte sólido.
46. El procedimiento de la reivindicación 44, en el que dicha etapa de puesta en contacto se realiza in vitro.
47. El procedimiento de la reivindicación 44, en el que dicha etapa de determinación se realiza determinando si dicho compuesto de ensayo inhibe la unión de una anticuerpo que se une específicamente a dicho dominio de bucle de cisteína o no.
48. El procedimiento de la reivindicación 44, en el que dicha integrina ß3 es una integrina ß3 de mamífero.
49. El procedimiento de la reivindicación 44, en el que dicha integrina ß3 es una integrina ß3 de mamífero seleccionada del grupo constituido por integrina ß3 humana y porcina.
50. Un dominio de bucle de cisteína inmovilizado que comprende un péptido acoplado a un soporte sólido, comprendiendo dicho péptido los aminoácidos 177 a 184 de una integrina ß3.
51. El dominio de bucle de cisteína inmovilizado de la reivindicación 50, en el que dicha integrina ß3 es una integrina ß3 humana o porcina.
52. El dominio de bucle de cisteína inmovilizado de la reivindicación 50, en el que dicho soporte es un soporte polimérico.
53. El dominio de bucle de cisteína inmovilizado de la reivindicación 50, en el que dicho péptido está construido por no más de 15 aminoácidos.
54. Un compuesto de Fórmula II:
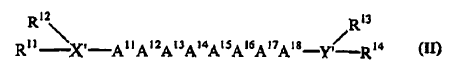
en la que:
A11 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A12 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A13 es cualquier aminoácido;
A14 es cualquier aminoácido;
A15 es un aminoácido aromático seleccionado del grupo constituido por F, Y, W y H;
A16 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A17 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A18 es un aminoácido hidrófobo seleccionado del grupo constituido por I, L y V o un aminoácido neutro seleccionado del grupo constituido por M, F, W, C y A;
X' es una cadena de 0 a 5 aminoácidos, en la que el extremo N de uno de los mismos está unido opcionalmente a R11 y R12;
Y' es una cadena de 0 a 4 aminoácidos, en la que el extremo C de uno de los mismos PUEDE ser fosfoserina o ESTÁ opcionalmente unido a R13 y R14;
R11, R12, R13 y R14 están presentes o ausentes y están seleccionados, cada uno independientemente, del grupo constituido por H, alquilo C1-C12, arilo C6-C18, acilo C1-C12, aralquilo C7-C18 y alcarilo C7-C18;
o una sal farmacéuticamente aceptable del mismo
para su uso en la inhibición de la acción del IGF-I en un sujeto en tratamiento con un compuesto antineoplástico o radioterapia.
55. Uso de un compuesto de Fórmula II:
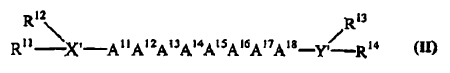
en la que:
A11 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A12 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A13 es cualquier aminoácido;
A14 es cualquier aminoácido;
A15 es un aminoácido aromático seleccionado del grupo constituido por F, Y, W y H;
A16 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A17 es un aminoácido básico seleccionado del grupo constituido por R, K y H;
A18 es un aminoácido hidrófobo seleccionado del grupo constituido por I, L y V o un aminoácido neutro seleccionado del grupo constituido por M, F, W, C y A;
X' es una cadena de 0 a 5 aminoácidos, en la que el extremo N de uno de los mismos está unido opcionalmente a R11 y R12;
Y' es una cadena de 0 a 4 aminoácidos, en la que el extremo C de uno de los mismos PUEDE ser fosfoserina o ESTÁ opcionalmente unido a R13 y R14;
R11, R12, R13 y R14 están presentes o ausentes y están seleccionados, cada uno independientemente, del grupo constituido por H, alquilo C1-C12, arilo C6-C18, acilo C1-C12, aralquilo C7-C18 y alcarilo C7-C18;
o una sal farmacéuticamente aceptable del mismo
para la fabricación de un medicamento para la inhibición de la acción del IGF-I en un sujeto en tratamiento con un compuesto antineoplástico o radioterapia.
56. Un anticuerpo que: (a) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 humana, (b)no se une específicamente al sitio de unión RGD de una integrina ß3 humana; y (c) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 porcina para su uso en la inhibición de la acción del IGF-I en un sujeto en tratamiento con un compuesto antineoplástico o radioterapia.
57. Uso de un anticuerpo que: (a) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 humana, (b) no se une específicamente la sitio de unión RGD de una integrina ß3 humana; y (c) se une específicamente al dominio de bucle de cisteína en los aminoácidos 177 a 184 de una integrina ß3 porcina para la fabricación de un medicamento para la inhibición de la acción del IGF-I en un sujeto en tratamiento con un compuesto antineoplástico o radioterapia.
58. El compuesto o uso de las reivindicaciones 54-57, seleccionándose dicho tumor del grupo constituido por tumores de cáncer de mama, tumores de cáncer de colon, tumores de cáncer de pulmón y tumores de cáncer de próstata.
59. El compuesto o uso de la reivindicación 58, expresando dicho tumor un receptor aVß3.
Patentes similares o relacionadas:
Péptido basado en colágeno tipo II alfa-1 útil para el tratamiento de una enfermedad de la superficie ocular, del 15 de Julio de 2020, de EYEBIO KOREA: Un péptido que consiste en una secuencia de aminoácidos representada por SEQ ID NO: 1.
Matrices de soporte derivadas de TN3 específicas para CD40L y sus métodos de empleo, del 1 de Julio de 2020, de Viela Bio, Inc: Una matriz de soporte de Tenascina 3 (Tn3) que comprende dos subunidades monoméricas específicas para CD40L, conectadas en tándem, donde la subunidad […]
Moléculas de armazón a base de fibronectina de unión a glipicano-3, del 17 de Junio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un polipéptido que comprende un décimo dominio de fibronectina humana de tipo III (10Fn3) que comprende los bucles BC, DE y FG, en donde el polipéptido se une […]
Métodos de replegado de proteínas basados en filtración de flujo tangencial, del 10 de Junio de 2020, de BRISTOL-MYERS SQUIBB COMPANY: Un método para el replegado de una proteína desnaturalizada, que comprende combinar la proteína desnaturalizada con un tampón de solubilización […]
Material biofabricado que contiene fibrillas de colágeno, del 29 de Abril de 2020, de Modern Meadow, Inc: Un material biofabricado (i) que comprende una red de fibrillas de colágeno no humano, en donde menos del 10 % en peso de las fibrillas de colágeno en […]
COMPOSICIÓN A BASE DE BIOPOLÍMEROS RECOMBINANTES Y USOS DE LA MISMA COMO BIOTINTA, del 23 de Abril de 2020, de UNIVERSIDAD DE VALLADOLID: La presente invención se refiere a composiciones que comprenden biopoiímeros recombinantes formados por combinaciones de monómeros de tipo "Recombinámeros […]
Procedimiento para fabricar un material biofabricado que contiene fibrillas de colágeno, del 22 de Abril de 2020, de Modern Meadow, Inc: Un procedimiento para fabricar: (i) un material que comprende una red de fibrillas de colágeno no humano, en donde menos del 10 % en peso de las fibrillas […]
Material compuesto biofabricado, del 22 de Abril de 2020, de Modern Meadow, Inc: Un material compuesto que comprende: (i) al menos un componente secundario poroso, permeable o absorbente, y al menos un material biofabricado […]