INHIBIDORES DEL VIRUS DE LA HEPATITIS C.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/US2005/034777.
Solicitante: THE ADMINISTRATORS OF THE TULANE EDUCATIONAL FUND
THE ROCKEFELLER UNIVERSITY.
Nacionalidad solicitante: Estados Unidos de América.
Dirección: 1430 TULANE AVENUE, TB-32 NEW ORLEANS, LA 70112-2699 ESTADOS UNIDOS DE AMERICA.
Inventor/es: GARRY, ROBERT, F., MCKEATING,JANE A.
Fecha de Publicación: .
Fecha Solicitud PCT: 26 de Septiembre de 2005.
Fecha Concesión Europea: 21 de Julio de 2010.
Clasificación Internacional de Patentes:
- A61K39/29 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 39/00 Preparaciones medicinales que contienen antígenos o anticuerpos (materiales para ensayos inmunológicos G01N 33/53). › Virus de la hepatitis.
- C07K14/18F4
Clasificación PCT:
- A61K38/00 A61K […] › Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00).
- A61K38/02 A61K […] › A61K 38/00 Preparaciones medicinales que contienen péptidos (péptidos que contienen ciclos beta-lactama A61K 31/00; dipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina 2,5-dionas, A61K 31/00; péptidos basados en la ergolina A61K 31/48; que contienen compuestos macromoleculares que tienen unidades aminoácido repartidas estadísticamente A61K 31/74; preparaciones medicinales que contienen antígenos o anticuerpos A61K 39/00; preparaciones medicinales caracterizadas por los ingredientes no activos, p. ej. péptidos como soportes de fármacos, A61K 47/00). › Péptidos de número indeterminado de aminoácidos; Sus derivados.
- A61K38/16 A61K 38/00 […] › Péptidos que tienen más de 20 aminoácidos; Gastrinas; Somatostatinas; Melanotropinas; Sus derivados.
- C07K1/00 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › Procedimientos generales de preparación de péptidos.
- C07K1/107 C07K […] › C07K 1/00 Procedimientos generales de preparación de péptidos. › por modificación química de los péptidos precursores.
- C07K1/14 C07K 1/00 […] › Extracción; Separación; Purificación.
- C07K2/00 C07K […] › Péptidos con un número indeterminado de aminoácidos; Sus derivados.
- C07K7/08 C07K […] › C07K 7/00 Péptidos con 5 a 20 aminoácidos en una secuencia totalmente determinada; Sus derivados. › con 12 a 20 aminoácidos.
Países PCT: Austria, Bélgica, Suiza, Alemania, Dinamarca, España, Francia, Reino Unido, Grecia, Italia, Liechtensein, Luxemburgo, Países Bajos, Suecia, Mónaco, Portugal, Irlanda, Eslovenia, Finlandia, Rumania, Chipre, Lituania, Letonia, Ex República Yugoslava de Macedonia, Albania.
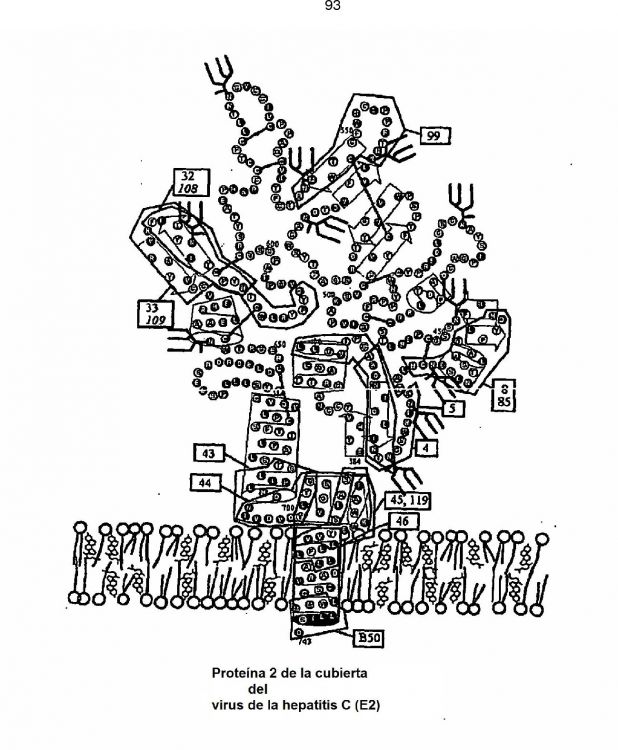
Fragmento de la descripción:
CAMPO DE LA INVENCIÓN
La presente invención se refiere a péptidos y usos de los mismos en el tratamiento o prevención de la infección por el virus de la hepatitis C (VHC).
ANTECEDENTES DE LA INVENCIÓN
Los virus deben infectar las células huésped para replicarse, producir una infección que se disemine y causar enfermedad. La infección por virus con cubierta requiere la unión del virión a una o más estructuras sobre la superficie de la célula (Flint y McKeating, 2000). La etapa inicial puede ser una unión inespecífica de baja afinidad (Barth y col., 2003). Posteriormente, el virus se une a los receptores primarios con alta afinidad y, después, en algunos casos, a los receptores secundarios o co-receptores (Bartosch y coI., 2003; Hsu y col., 2003; Roccasecca y coI., 2003; Cormier y coI., 2003; Pohlmann y coI., 2003; Zhang y coI., 2004). Las etapas de unión a la superficie celular se pueden asociar con una variedad de reorganizaciones estructurales sobre las proteínas de superficie del virión y cambios en las interacciones proteína-proteína entre las proteínas de la superficie viral (Jardetsky y Lamb, 2004; Modis y coI., 2004; Bressanelli y coI., 2004; Gibbons y col., 2004). Las últimas etapas pueden exponer el péptido de fusión, un dominio hidrófobo de una glicoproteína viral que es capaz de interaccionar con las membranas celulares (Flint y coI., 1999; Allison y coI., 2001). En algunos casos, la unión del virus a los receptores de la superficie celular desencadena la captación del virus por vías endocítica o vesicular similar (Garry y Dash, 2003; Jardetsky y Lamb, 2004). La exposición a condiciones más ácidas en las vesículas puede desencadenar cambios conformacionales en las proteínas de la superficie viral, incluidas las que exponen el péptido de fusión (Kuhn y coI., 2002; Lescar y col., 2001). Para la mayoría de los virus, la unión al receptor celular es, principalmente, la función de una proteína de la superficie viral, mientras que la fusión de las membranas celular y viral es, principalmente, la función de otra proteína de la superficie viral. Un ejemplo de un virus con proteínas distintas de unión al receptor y de fusión es el VIH. La proteína de unión al receptor del VIH es la glicoproteína de superficie (SU; gp120) y la proteína de fusión es la glicoproteína transmembrana (TM; gp41) (Kwong y coI., 1998; Gallaher y coI., 1987; 1989). La mayoría de los virus con proteínas de fusión de clase I en las que el péptido de fusión se localiza en, o cerca de, el extremo amino, por ejemplo retrovirus, ortomixovirus, paramixovirus, arenavirus y coronavirus, usan una proteína para la unión al receptor y otra para la fusión (Wilson y coI., 1981; Gallaher y col., 1996; 2001). Los alfavirus, que tienen una proteína de fusión de clase II con un péptido de fusión interno, también usan una proteína principalmente para la unión al receptor y otra para la fusión de las membranas viral y celular (Straus y Straus, 1994). La proteína de la cubierta (E) codificada por los miembros del género flavivirus de Flaviviridae, tiene un péptido de fusión interno pero sirve tanto la función de unión al receptor y de fusión (Allison y col., 2001).
El virus de la hepatitis C codifica dos glicoproteínas de cubierta, E1 (gp35) y E2 (gp70), ambas con dominios de anclaje transmembrana (Flint y McKeating, 2000). La E2 interacciona con varias proteínas de superficie celular (CD81, SR-BI y L-SIGN), lo que sugiere que es la proteína de union al receptor del VHC (McKeating, 2004). La función de la E1 está menos clara y puede actuar para acompañar a la E2 (Flint y coI., 1999; Garry y Dash, 2003). Los péptidos sintéticos correspondientes a la E2 del virus de la hepatitis C pueden bloquear la infección mediada por el virus de la hepatitis C. Las determinaciones estructurales de la E2 del virus de la hepatitis C permiten la identificación de varias características hasta ahora desconocidas de la E2 del virus de la hepatitis C para el desarrollo de fármacos y de vacunas.
La familia de Flavivirus incluye una variedad de patógenos humanos y animales importantes. El virus de la hepatitis C (VHC) es la principal causa viral de hepatitis crónica, cirrosis, insuficiencia hepática y carcinoma hepatocelular (Poynard y coI., 2003). Solo en Estados Unidos, aproximadamente 4 millones de personas están infectadas con el VHC. Esto es aproximadamente cuatro veces el número de infectados por el VIH. En EE.UU. cada año se producen 30-50.000 nuevas infecciones con el VHC y aproximadamente 15-20.000 personas mueren. Además, cabe esperar que estas cifras aumenten espectacularmente dado que una porción considerable de individuos infectados por el VIH muestran poca o ninguna respuesta a las únicas terapéuticas aprobadas actualmente (es decir, tratamiento con interferones y/o con ribavirina). La infección por VHC se transmite principalmente al compartir aguja los usuarios de drogas, aunque hay algún riesgo derivado de las punciones accidentales con agujas, productos hemoderivados antes de 1992, diálisis sanguínea crónica y contactos sexuales frecuentes. Los tratamientos actuales para el VHC usando ribavirina e interferón cuestan 8.000-20.000 $ al año y solo son parcialmente satisfactorios en aproximadamente la mitad de los pacientes tratados. En general, aproximadamente un 80% de los portadores del VHC sufren inflamación hepática crónica y cirrosis, de éstos el 25% desarrollará hepatopatía terminal o carcinoma hepatocelular (CHC) (Colombo, 2000). La enfermedad terminal por VHC es la indicación más frecuente para transplantes de hígado y esto cuesta de 250.000 $ a 300.000 $. Es urgente encontrar mejores fármacos para tratar la infección por VIH y una vacuna eficaz para prevenir la infección por el VHC.
SUMARIO DE LA INVENCIÓN
La presente invención se refiere a las composiciones tal como se han definido en las reivindicaciones, que comprenden péptidos o derivados peptídicos y usos de estas composiciones para tratar o prevenir la infección por el virus de la hepatitis C (VHC). La presente invención se hace posible por el descubrimiento de los inventores de que la glicoproteína E2 codificada por el VHC (y análogo(s) de virus relacionados) tiene dominios no descritos anteriormente que son importantes para la(s) interacción(es) y reorganización(es) de E2 con E2 y/o E1. Para interacciones de alta afinidad con receptores celulares o para interacciones proteína-proteína de E2 y E2-E1 que se producen antes de la fusión virión:membrana celular. Por tanto, la presente invención proporciona péptidos y procedimientos para el tratamiento y profilaxis de enfermedades inducidas por el VHC y virus relacionados.
La presente invención enseña que la glicoproteína E2 de la cubierta del VHC tiene varios dominios que pueden ser el objetivo de péptidos sintéticos para bloquear la infección y la patogenia. Las regiones de la E2 del VHC son importantes para la unión del VHC a sus receptores celulares de alta o baja afinidad, para reorganizaciones de E2 o para interacciones proteína-proteína de E2 que se producen antes de la fusión virión:membrana celular. La presente invención también instruye y proporciona péptidos sintéticos tal como se definen en las reivindicaciones que pueden inhibir la unión al receptor y otras etapas pre-fusión mediadas por la E2 del VHC.
Las características de la glicoproteína 2 de la cubierta del virus de la hepatitis C identificada en la presente memoria descriptiva proporcionan sorprendentes guías para el desarrollo de vacunas y/o fármacos para prevenir o tratar infecciones por el virus de la hepatitis
C. A diana para los péptidos es la E2, la proteína de unión al receptor del VHC. Aunque se ha desarrollado proteínas, tales como CD4 solubles, quimioquinas y anticuerpos, que bloquean la infección apuntando a las interacciones de unión al receptor del virión, no se han descrito mímicos peptídicos de las proteínas de la superficie viral que bloquean esta u otras etapas prefusión. Antes de la disponibilidad de datos estructurales de rayos X (Qureshi y coI., 1990; Wild, y coI., 1993; 1994), se desarrollaron varios potentes inhibidores del VIH-1 sobre la base del modelo de proteína de fusión de Gallaher HIV-1 TM (Gallaher y coI., 1989). Uno de estos inhibidores, en estudios clínicos se ha demostrado que el péptido FUZEON@ (también conocido como enfuvirtida, OP178; T20) reduce considerablemente la carga del VIH-1 en pacientes con SIDA (Lalezari, y coI., 2003). Los fármacos peptídicos, que son el objeto de la presenta invención, también se desarrollaron sin los beneficios de los datos estructurales...
Reivindicaciones:
1. Una composición farmacéutica que comprende uno o más péptidos seleccionados del grupo que consiste en un péptido que consiste en por la secuencia de una cualquiera de las SEC ID Nº 1 a SEC ID Nº: 42.
2. Una composición farmacéutica que comprende al menos un péptido seleccionado de uno o más de los siguientes: a) Un péptido que consiste en por la secuencia de aminoácidos de una cualquiera de las SEC ID Nº 1 a SEC ID Nº 42, en el que el resto N terminal es un grupo amino y el resto C-termina es un grupo carboxilo;
b) un péptido que consiste en por la secuencia de una cualquiera de las SEC ID Nº 1 a SEC ID Nº 42, en el que el resto grupo amino N-terminal es sustituido por un resto N-terminal seleccionado del grupo consiste en r: un grupo acetilo, un grupo hidrófobo, un grupo carbobenzoxilo, un grupo dansilo, un grupo tbutoxicarbonilo o un grupo transportador macromolecular, seleccionado de entre un conjugado lipídico, polietilenglicol o un hidrato de carbono y/o en los que el grupo carboxilo en C terminal está sustituido por un resto en C-terminal seleccionado del grupo consiste en por un grupo amido, un grupo hidrófobo, un grupo t-butiloxicarbonilo o un grupo macromolecular seleccionado de entre un conjugado lipídico, polietilenglicol o un hidrato de carbono;
c) un péptido consiste en por la secuencia de una cualquiera de las SEC ID Nº 1 a SEC ID Nº 42, en el que al menos uno de los enlaces que une residuos de aminoácidos adyacentes es un enlace no peptídico;
d) un péptido constituido por la secuencia de una cualquiera de SEC ID Nº a SEC ID Nº 42, a excepción de que al menos un residuo de aminoácido está en la configuración de D-isómero.
3. La composición de la reivindicación 2, en la que el resto terminal en el aminoácido N-terminal es un grupo acetilo, un grupo hidrófobo, un grupo carbobenzoxilo, un grupo dansilo, un grupo t-butiloxicarbonilo o un grupo transportador macromolecular, seleccionado de un conjugado lipídico, polietilenglicol o un hidrato de carbono; y/o el resto terminal en el aminoácido C-terminal es un grupo hidrófobo, un grupo t
butiloxicarbonilo o un grupo macromolecular seleccionado de un conjugado lipídico, polietilenglicol o un hidrato de carbono.
4. La composición de la reivindicación 2, en la que la composición incluye un péptido consiste en por la secuencia de una cualquiera de SEC ID Nº 1 a SEC ID Nº 42, en la que el resto terminal del aminoácido N-terminal es un grupo transportador macromolecular seleccionado de un conjugado lipídico, polietilenglicol o un hidrato de carbono; y/o el resto terminal en el aminoácido C-terminal es un grupo transportador macromolecular seleccionado de un conjugado lipídico, polietilenglicol o un hidrato de carbono.
5. La composición de la reivindicación 2, en la que al menos un enlace es un enlace no peptídico seleccionado del grupo consiste en por un enlace imido, un enlace éster, un enlace hidracina, un enlace semicarbazoide y un enlace azo.
6. La composición de la reivindicación 2, en la que al menos un aminoácido es un aminoácido D-isómero.
7. La composición de la reivindicación 2, en la que el resto terminal del grupo aminoácido N-terminal es un grupo amino y el resto terminal en el aminoácido C-terminal es un grupo carboxilo.
8. La composición de la reivindicación 1, en la que al menos un péptido se selecciona del grupo de péptidos que consistente en una secuencia seleccionada de las secuencias de SECIDNº 7a42.
9. Un medicamento para su uso en el tratamiento o prevención de la infección por virus de la hepatitis C en un paciente, en el que el medicamento comprende una composición farmacéutica de acuerdo con cualquiera de las reivindicaciones 1 a 8.
10. Uso de una composición farmacéutica de acuerdo con cualquiera de las reivindicaciones 1 a 8 para la preparación de un medicamento para tratar o prevenir la infección por el virus de la hepatitis C en un paciente.
11. Un anticuerpo sustancialmente purificado usando como inmunógeno un péptido tal como se describe en cualquiera de las reivindicaciones 1 a 8.
12. Un medicamento para su uso en el tratamiento o la prevención de la infección por el
5 virus de la hepatitis C en un paciente, en el que el medicamento comprende uno o más péptidos tal como se define en cualquiera de las reivindicaciones 1 a 8 y/o un anticuerpo de acuerdo con la reivindicación 11 y que además comprende uno o más péptidos y/o uno o más anticuerpos dirigidos a la inhibición de la etapa de fusión con la membrana mediada por la proteína 1 de la cubierta del virus de la hepatitis C.
10
13. Un anticuerpo de acuerdo con la reivindicación 11 para usar en el tratamiento o la prevención de la infección por el virus de la hepatitis C en un paciente.
14. Uso de una composición farmacéutica de acuerdo con cualquiera de las
15 reivindicaciones 1 a 8 y/o un anticuerpo de la reivindicación 11 para la preparación de un medicamento para tratar o prevenir la infección por el virus de la hepatitis C en un paciente.
15. Un péptido constituido por la secuencia de una cualquiera de SEC ID Nº 1 a 6. 20
16. Un péptido constituido por la secuencia de una cualquiera de SEC ID Nº 7 a 42.
Patentes similares o relacionadas:
Vectores de CMVH y CMVRh recombinantes que codifican un antígeno heterólogo aislado de un virus Paramyxoviridae y usos de los mismos, del 1 de Julio de 2020, de Oregon Health & Science University: Un vector de CMVRh o CMVH recombinante que comprende una secuencia de ácido nucleico que codifica un antígeno heterólogo, en el que el antígeno […]
Vectores de CMVH y CMVRh recombinantes que codifican un antígeno heterólogo aislado del virus de la hepatitis B y usos de los mismos, del 5 de Febrero de 2020, de Oregon Health & Science University: Un vector de CMVRh o CMVH recombinante que comprende una secuencia de ácido nucleico que codifica un antígeno heterólogo, en el que el antígeno heterólogo es un […]
Compuestos de polímero de polialquileno y usos de los mismos, del 20 de Noviembre de 2019, de Biogen MA Inc: Una composición farmacéutica que comprende un conjugado y un vehículo, adyuvante, diluyente, conservante y/o solubilizante farmacéuticamente […]
Formulaciones secas de vacunas que son estables a la temperatura ambiente, del 21 de Agosto de 2019, de INTERVET INTERNATIONAL B.V: Una formulación seca de una vacuna que comprende un virus vivo atenuado, entre un 30 % y un 80 % (p/p) de un oligosacárido no reductor, entre un 5 % […]
Vacuna para inducir una reacción inmune mejorada, del 10 de Octubre de 2018, de Eyegene, Inc: Una composición de vacuna farmacéutica para uso en vacunación contra un virus de influenza, que comprende: (a) antígeno del virus de la […]
Vacunación tumoral que involucra una respuesta inmunitaria contra la proteína propia CLDN18.2, del 9 de Mayo de 2018, de Biontech Protein Therapeutics GmbH: Una proteína que comprende la secuencia de aminoácidos expuesta en la sec. con núm. de ident.: 37.
Vacuna de ADN, del 4 de Abril de 2018, de OSAKA UNIVERSITY: Un vector de expresión que codifica un polipéptido del antígeno de la nucleocápsida del virus de la hepatitis B quimérico insertado con una secuencia de aminoácidos que comprende […]
Composiciones inmunoterapéuticas para el tratamiento o prevención de infección por virus de hepatitis delta, del 21 de Marzo de 2018, de GLOBEIMMUNE, INC: Una composición inmunoterapéutica que comprende: a) un vehículo de levadura; y b) una proteína de fusión que comprende antígenos de VHD, en la que el antígeno […]