PROCEDIMIENTO PARA EL AISLAMIENTO DE LA MASA CELULAR INTERNA EN BLASTOCISTOS DE MAMIFEROS NO HUMANOS.
Procedimiento para el aislamiento de la masa celular interna (MCI) en blastocistos de mamíferos no humanos que incluye el cultivo directo en placa de dichos blastocistos y la posterior ablación mediante láser del trofoectodermo de dichos blastocistos.
El procedimiento de la invención permite una mejora de la eficiencia del aislamiento de la masa celular interna de blastocistos y el aprovechamiento de blastocistos de poca calidad no aptos para la separación de su masa celular interna mediante los procedimientos mencionados en los documentos del estado de la técnica
Tipo: Patente de Invención. Resumen de patente/invención. Número de Solicitud: P200701625.
Solicitante: FUNDACION PROGRESO Y SALUD.
Nacionalidad solicitante: España.
Provincia: SEVILLA.
Inventor/es: MENENDEZ BUJAN,PABLO, CORTES ROMERO,JOSE LUIS, COBO MARTINEZ,FERNANDO.
Fecha de Solicitud: 1 de Junio de 2007.
Fecha de Publicación: .
Fecha de Concesión: 23 de Junio de 2010.
Clasificación Internacional de Patentes:
- A61B17/435 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61B DIAGNOSTICO; CIRUGIA; IDENTIFICACION (análisis de material biológico G01N, p.ej. G01N 33/48). › A61B 17/00 Instrumentos, dispositivos o procedimientos quirúrgicos, p. ej. torniquetes (A61B 18/00 tiene prioridad; dispositivos anticonceptivos, pesarios, dispositivos para su introducción A61F 6/00; cirugía ocular A61F 9/007; cirugía otorrina A61F 11/00). › para el trasplante de embriones.
- B23K26/00F2
- C12N13/00 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › Tratamiento de microorganismos o enzimas por energía eléctrica u ondulatoria, p. ej. por magnetismo, por ondas sonoras.
- C12N5/06B2P
Clasificación PCT:
- A61B17/435 A61B 17/00 […] › para el trasplante de embriones.
- B23K26/00 TECNICAS INDUSTRIALES DIVERSAS; TRANSPORTES. › B23 MAQUINAS-HERRAMIENTAS; TRABAJO DE METALES NO PREVISTO EN OTRO LUGAR. › B23K SOLDADURA SIN FUSION O DESOLDEO; SOLDADURA; REVESTIMIENTO O CHAPADO POR SOLDADURA O SOLDADURA SIN FUSION; CORTE POR CALENTAMIENTO LOCALIZADO, p. ej. CORTE CON SOPLETE; TRABAJO POR RAYOS LASER (fabricación de productos revestidos de metal por extrusión de metales B21C 23/22; realización de guarniciones o recubrimientos por moldeo B22D 19/08; moldeo por inmersión B22D 23/04; fabricación de capas compuestas por sinterización de polvos metálicos B22F 7/00; disposiciones sobre las máquinas para copiar o controlar B23Q; recubrimiento de metales o recubrimiento de materiales con metales, no previsto en otro lugar C23C; quemadores F23D). › Trabajo por rayos láser, p. ej. soldadura, corte o taladrado.
- C12N13/00 C12N […] › Tratamiento de microorganismos o enzimas por energía eléctrica u ondulatoria, p. ej. por magnetismo, por ondas sonoras.
- C12N5/0735 C12N […] › C12N 5/00 Células no diferenciadas humanas, animales o vegetales, p. ej. líneas celulares; Tejidos; Su cultivo o conservación; Medios de cultivo para este fin (reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00). › Células madre embrionarias; Células germinales embrionarias.
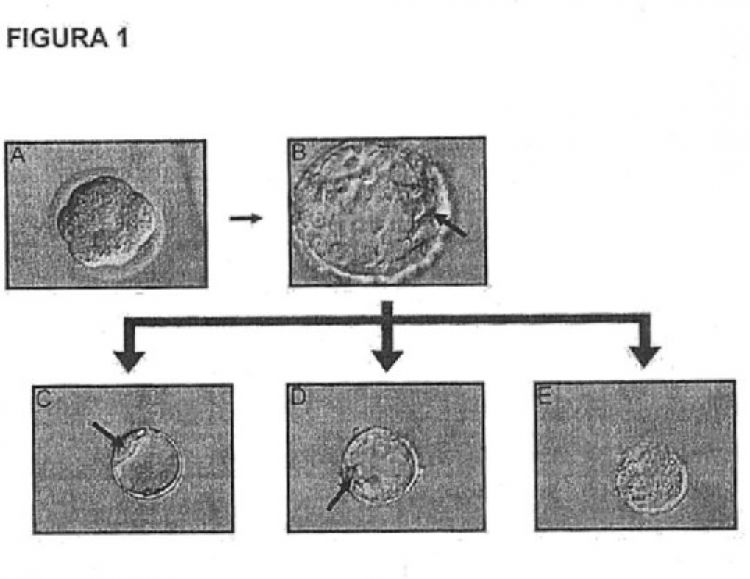
Fragmento de la descripción:
Procedimiento para el aislamiento de la masa celular interna en blastocistos de mamíferos no humanos.
Objeto de la invención
El objeto de la presente invención es un procedimiento para el aislamiento de la masa celular interna (MCI) en blastocistos de mamíferos no humanos que incluye el cultivo directo en placa de dichos blastocistos y la posterior ablación mediante láser del trofoectodermo de dichos blastocistos. El procedimiento de la invención permite una mejora de la eficiencia del aislamiento de la masa celular interna de blastocistos y el aprovechamiento de blastocistos de poca calidad no aptos para la separación de su masa celular interna mediante los procedimientos mencionados en los documentos del estado de la técnica.
Estado de la técnica
En 1981 se obtuvieron por primera vez células troncales embrionarias a partir de blastocistos de ratón (Evans MJ, Kaufman MH. Establishment in culture of pluripotential cells from mouse embryos. Nature 1981; 292:154-56). Estas células están dotadas de dos propiedades únicas que las distinguen de todas las células troncales órgano-específicas identificadas hasta el momento:
Primero, que se auto-renuevan continuamente en cultivo y que pueden ser conservadas y multiplicadas durante prolongados periodos de tiempo, manteniéndose en status de "no-diferenciación".
Segundo, que son pluripotentes, capaces de diferenciarse en cualquier tipo de célula en el cuerpo (Keller G. Embryonic stem cell differentiation: emergence of a new era in biology and medicine. Genes Dev. 2005; 19:1129-55).
Las primeras líneas de células troncales embrionarias humanas se derivaron en 1998 de la MCI de embriones no transferidos donados y congelados (Thomson JA, Itskovitz-Eldor J, Shapiro SS, Waknitz MA, Swiergiel JJ, Marshall VS, Jones JM. Embryonic stem cell lines derived from human blastocysts. Science 1998; 282:1145-7). Dichas líneas celulares mostraban las dos referidas propiedades de auto-renovación y pluripotencialidad. A partir de esa fecha, numerosos laboratorios han comunicado la derivación de líneas celulares troncales embrionarias humanas, a partir de embriones no transferidos, utilizando bien células alimentadoras humanas o de ratón.
Debe tenerse en cuenta que la calidad de los blastocistos y el método de aislamiento de la MCI usado, son los dos factores principales que conducen al éxito o al fracaso del proceso de derivación de líneas de células troncales embrionarias humanas. Respecto a la calidad de los blastocistos, los humanos son de calidad más pobre que los de ratón. Ello es debido, al menos en parte, al hecho de que los blastocistos humanos están congelados cuando se intenta la derivación de líneas celulares troncales embrionarias humanas, debido a restricciones éticas, mientras que los blastocistos de ratón se utilizan normalmente en fresco. Ello explica no solo el extremadamente bajo grado de éxito de los procesos de derivación de líneas celulares troncales embrionarias humanas, sino que implica también el que embriones humanos de pobre calidad se descarten directamente, e incluso ni se descongelen ni se usen para este propósito.
Por otro lado, los procedimientos actuales para el aislamiento de MCI son objeto de controversia. La MCI es aislada usualmente de los blastocistos expandidos usando una amplia variedad de técnicas que incluyen la inmunocirugía (Solter D., Knowles BB. 1975. Immunosurgery of mouse blastocysts; Proc. Natl. Acad. Sci. U S A 72:5099-5102), procedimientos mecánicos (Bongso A, Fong CY, Ng SC, Ratnam S. 1994. Isolation and culture of inner cell mass cells from human blastocysts. Hum. Reprod. 9:2110-2117), y procedimientos de cultivo de blastocisto completo (Kim HS, Oh SK, Park YB, Anh HJ, Sung KC, Kang MJ, Lee LA, Suh CS, Kim SH, Kim DW, Moon SY. 2005. Methods for derivation of human embryonic stem cells. Stem Cells 23:1228-1233). Recientemente, se ha obtenido MCI a partir de blastómeros obtenidos de embriones en fase célula (Chung Y, Klimanskaya I, Becker S, Marh J, Lu SJ, Johnson J, Meisner L, Lanza R. 2006. Embryonic and extraembryonic stem cell lines derived from single mouse blastomeres. Nature 439:216-219).
Todos estos procedimientos de aislamiento de MCI presentan dos inconvenientes relevantes: cambios en el cariotipo tras cultivo prolongado y la utilización de xeno-componentes que podrían comprometer el uso de estas líneas celulares troncales embrionarias humanas o los derivados de las mismas en potenciales aplicaciones terapéuticas. Estas células troncales embrionarias y derivados de las mismas obtenidas por los métodos indicados y cultivadas durante periodos largos, han estado asociadas con inestabilidad genética a largo plazo, aunque queda por dilucidar si ello es debido al propio proceso de derivación, o a los procesos mecánicos y/o enzimáticos utilizados para el mantenimiento rutinario de los cultivos de células troncales embrionarias.
Existe claramente una demanda urgente de estudios sobre calidad de blastocistos, métodos de aislamiento de MCI y subsiguiente derivación de células troncales embrionarias, para poder dar cumplimiento a las expectativas generadas por la investigación con células troncales embrionarias humanas. La tecnología láser se usa habitualmente en reproducción asistida (Antinori S, Selman HA, Caff B, Panci C, Dani GL, Versaci C. 1996. Zona opening of human embryos using non-contact UV laser for assisted hatching in patients with poor prognosis of pregnancy. Hum. Reprod. 11:2488-2492), porque facilita la transferencia nuclear, acelerando el proceso de enucleación de forma que se desarrolle en segundos, evitando al mismo tiempo cualquier daño al óvulo (Chen S., Chao K., Chang C., Hsieh F., Ho H., Yang Y. 2004. Technical Aspects of the piezo, laser-assisted, and conventional methods for nuclear transfer of mouse oocytes and their efficiency and efficacy: Piezo minimizes damage of the ooplasmic membrane at injection. J Exp. Zool. 301:344-351).
Muy recientemente, se ha utilizado la tecnología de ablación con láser para destruir el trofoectodermo de blastocistos de ratón de buena calidad, permitiendo separar con éxito la MCI y la subsiguiente derivación de líneas de células troncales embrionarias de ratón (Cortes JL, Cobo F, Catalina P, Nieto A, Cabrera C, Montes R, Concha A, Menendez P. "Evaluation of the laser technique method to isolate the inner cell mass of murine blastocysts". Biotechnol. Appl. Biochem. 2007; 46:205:209 y solicitud de patente WO03/018783). Es importante, sin embargo, señalar que el uso de la tecnología de ablación con láser para destruir las células del trofoectodermo permitiendo el aislamiento de la MCI, requiere que se usen blastocistos expandidos de muy buena calidad con una MCI claramente distinguible, ya que si no es así, el embriólogo no puede ver con precisión y distinguir la MCI de las células del trofoectodermo, convirtiendo los disparos con el láser en poco precisos y aleatorios.
El procedimiento objeto de la presente invención permite superar estos inconvenientes, a través de la combinación de una etapa de cultivo de los blastocistos completos seguida de la destrucción del trofoectodermo mediante ablación con láser para mejorar la eficacia del aislamiento de la MCI y de la derivación de células troncales embrionarias a partir de embriones de ratón. Se utiliza este modelo animal, previo a su uso en humanos, para estudiar la efectividad de esta novedosa tecnología, debido a la escasez de embriones humanos disponibles para investigación, y la baja tasa de derivación de células troncales embrionarias humanas experimentada hasta ahora con otras técnicas.
Explicación de la invención
Constituye el objeto de la presente invención un procedimiento para el aislamiento de la MCI en blastocistos de mamíferos no humanos que incluye una etapa de ablación mediante láser del trofoectodermo de dichos blastocistos. Para hacer más efectivo el aislamiento de la MCI, los blastocistos se someten, previamente a dicha etapa de ablación mediante láser, a cultivo directo en placa durante un periodo de tiempo de al menos 72 horas. En un modo preferente de realización de la invención, los blastocistos son de ratón.
El cultivo directo previo a la ablación mediante láser incluye las siguientes subetapas:
a) cultivo de los blastocistos recuperados de los oviductos en medio estándar, particularmente medio de cultivo G2 V.III (Vitrolife, Sweden) a 37ºC y con 6% de CO2 durante un periodo de tiempo comprendido entre 24 y 48 horas.
b) tratamiento de los blastocistos cultivados en la subetapa anterior para conseguir una completa eliminación...
Reivindicaciones:
1. Procedimiento para el aislamiento de la masa celular interna en blastocistos de mamíferos no humanos que incluye una etapa de ablación mediante láser del trofoectodermo de dichos blastocistos y caracterizado porque previamente a dicha etapa de ablación mediante láser los blastocistos se someten a cultivo directo en placa durante un periodo de tiempo de al menos 72 horas.
2. Procedimiento para el aislamiento de la masa celular interna en blastocistos de mamíferos, según las reivindicación 1, caracterizado porque los blastocistos son de ratón.
3. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según las reivindicaciones 1-2, caracterizado porque el cultivo directo previo a la ablación mediante láser incluye las siguientes subetapas:
a) cultivo de los blastocistos recuperados de los oviductos en medio estándar, particularmente medio de cultivo G2 V.III (Vitrolife, Sweden) a 37ºC y con 6% de CO2 durante un periodo de tiempo comprendido entre 24 y 48 horas.
b) tratamiento de los blastocistos cultivados en la subetapa anterior para conseguir una completa eliminación de la zona pelúcida.
c) colocación de los blastocistos tratados en la etapa anterior sobre una superficie de cultivo y posterior adhesión del trofoectodermo y la masa celular interna de los blastocistos a dicha superficie.
d) mantenimiento de los blastocistos sobre dicha superficie y en un medio estándar de cultivo durante un periodo de tiempo comprendido entre 24 y 48 horas.
e) refresco del medio de cultivo y mantenimiento de los blastocistos en el mismo durante un nuevo periodo de tiempo comprendido entre 24 y 48 horas.
4. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según las reivindicaciones 1-3, caracterizado porque la eliminación de la zona pelúcida se lleva acabo mediante tratamiento con ácido Tyrode o enzima pronasa durante un periodo de tiempo comprendido entre 30 y 60 segundos.
5. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según las reivindicaciones 1-3, caracterizado porque la eliminación de la zona pelúcida se lleva a cabo por eclosión espontánea del blastocisto.
6. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según las reivindicaciones 1-5, caracterizado porque la superficie de cultivo sobre la cual se colocan los blastocistos tras la eliminación de la zona pelúcida es una placa recubierta con MEFs (Mouse embryonic fibroblasts).
7. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según las reivindicaciones 1-5, caracterizado porque la superficie de cultivo sobre la cual se colocan los blastocistos tras la eliminación de la zona pelúcida es una placa recubierta de gelatina.
8. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según las reivindicaciones 1-7, caracterizado porque el medio en el cual se mantienen los blastocistos sobre la superficie de cultivo es medio DMEM (Dubelcco's Modified Eagle's Médium) suplementado con suero fetal bovino al 20%, L-glutamina al 1%, aminoácidos no esenciales al 0,1 mM, 2000 IU/ml de factor inhibidor de leucemia de ratón, ß-mercaptoetanol 0,1 mM, 50 U/ml de penicilina y 50 µg/ml de estreptomicina.
9. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según las reivindicaciones 1 y 2, caracterizado porque la etapa de ablación mediante láser del trofoectodermo de los blastocistos, a realizar inmediatamente tras la etapa de cultivo previo, se lleva a cabo con un dispositivo de diodo láser de emisión en infrarrojo a una frecuencia óptica (longitud de onda) de 1,48 µm.
10. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según la reivindicación 9, caracterizado porque para la ablación mediante láser del trofoectodermo de los blastocistos se realizan entre 20 y 100 disparos.
11. Procedimiento para el aislamiento de masa celular interna en blastocistos de mamíferos según la reivindicación 10, caracterizado porque tras la ablación con láser del trofoectodermo de los blastocistos, se produce el establecimiento de las líneas celulares embrionarias de ratón a partir de la masa celular interna aislada de los blastocistos sometidos al procedimiento.
Patentes similares o relacionadas:
METODO PARA INCREMENTAR LA PRODUCCION DE BIOMASA Y DE LIPIDOS EN CHLORELLA VULGARIS, del 18 de Junio de 2020, de CENTRO DE INVESTIGACIÓN CIENTÍFICA Y DE EDUCACIÓN SUPERIOR DE ENSENADA, BAJA CALIFORNIA (CICESE): Un método para incrementar la producción de biomasa y de ácidos grasos en el alga Chlorella vulgaris Beyerinck y obtener una biomasa […]
Canalrodopsinas para el control óptico de células, del 1 de Abril de 2020, de MASSACHUSETTS INSTITUTE OF TECHNOLOGY: Polipéptido de canal iónico activado por luz aislado que comprende una secuencia de aminoácidos de un polipéptido de canal de Stigeoclonium […]
Dispositivo para la desintegración eléctrica de grupos de células, del 9 de Octubre de 2019, de HUGO VOGELSANG MASCHINENBAU GMBH: Dispositivo para la desintegración eléctrica de grupos de células con: - una unidad de electrodo que presenta una cabeza de electrodo […]
Métodos y dispositivos para preparación de muestra eléctrica, del 4 de Septiembre de 2019, de Qvella Corporation: Un método de procesamiento eléctrico de un líquido dentro de un dispositivo microfluídico, el líquido conteniendo uno o más microorganismos; el dispositivo […]
Dispositivo y método para la transfección de grandes volúmenes, del 17 de Julio de 2019, de Lonza Cologne GmbH: Dispositivo para aplicar un campo eléctrico a una suspensión de células, derivados celulares, orgánulos, partículas subcelulares y/o vesículas, comprendiendo al menos […]
Construcciones de moléculas MHC y sus usos para el diagnóstico y terapia, del 29 de Mayo de 2019, de DAKO DENMARK A/S: Una construcción de moléculas MHC en forma soluble en un medio de solubilización o inmovilizada en un soporte sólido o semi-sólido, comprendiendo dicha construcción de moléculas […]
Dispositivos de modulación de la actividad celular utilizando ultrasonido, del 15 de Mayo de 2019, de Arizona Board Of Regents For And On Behalf Of Arizona State University: Un dispositivo generador de ondas ultrasónicas para modular la actividad de las células neuronales de un sujeto, que comprende al menos un componente […]
Sistema de electroporación de aguja única de densidad de corriente variable, del 17 de Abril de 2019, de Inovio Pharmaceuticals, Inc: Un sistema de electroporación para suministrar una molécula en células de un mamífero, que comprende: a) un electrodo de anillo plano geométrico […]