DETECCION DE LITIO EN MUESTRAS BIOLOGICAS LIQUIDAS Y LOS REACTIVOS PARA DICHO FIN.
Un método para detector litio soluble en una muestra biológica líquida que comprende la combinación de:
(a) una cantidad de la muestra biológica;
(b) 2,3,7,8,12,13,17,18-octabromo-5,10,15,20-tetrakis(4-sulfonatofenil) porfirina;
(c) álcali;
(d) detergente;
(e) agente de quelación; y
(f) opcionalmente un solvente adecuado; para producir una muestra de prueba que tiene un pH de al menos 10; detectar un cambio de absorbancia de la muestra de prueba con relación a una muestra estándar deficiente en litio a una longitud de onda entre 475 nm y 485 nm, entre 515 nm y 525 nm o simultáneamente entre 475 nm y 485 nm y entre 515 nm y 525 nm, en donde el cambio de absorbancia indica la presencia de litio soluble en la muestra biológica
Tipo: Resumen de patente/invención. Número de Solicitud: W0100603AU.
Solicitante: SEBA DIAGNOSTICS PTY. LTD.
Nacionalidad solicitante: Australia.
Dirección: 26 MADDEN GROVE,BURNLEY, VIC 3121.
Inventor/es: BALAZS, NICHOLAS, DENNIS, HENRY, SECOMBE, JOHN, WILLIAM.
Fecha de Publicación: .
Fecha Concesión Europea: 26 de Agosto de 2009.
Clasificación Internacional de Patentes:
- G01N33/84 FISICA. › G01 METROLOGIA; ENSAYOS. › G01N INVESTIGACION O ANALISIS DE MATERIALES POR DETERMINACION DE SUS PROPIEDADES QUIMICAS O FISICAS (procedimientos de medida, de investigación o de análisis diferentes de los ensayos inmunológicos, en los que intervienen enzimas o microorganismos C12M, C12Q). › G01N 33/00 Investigación o análisis de materiales por métodos específicos no cubiertos por los grupos G01N 1/00 - G01N 31/00. › en los que intervienen compuestos inorgánicos o el pH.
Clasificación PCT:
- G01N21/78 G01N […] › G01N 21/00 Investigación o análisis de los materiales por la utilización de medios ópticos, es decir, utilizando rayos infrarrojos, visibles o ultravioletas (G01N 3/00 - G01N 19/00 tienen prioridad). › produciendo un cambio de color.
- G01N33/52 G01N 33/00 […] › Utilización de compuestos o de composiciones para investigaciones colorimétricas, espectrofotométricas o fluorométricas, p. ej. utilización de cintas de papel indicador.
- G01N33/84 G01N 33/00 […] › en los que intervienen compuestos inorgánicos o el pH.
Clasificación antigua:
Fragmento de la descripción:
Detección de litio en muestras biológicas líquidas y los reactivos para dicho fin.
Campo de la invención
La presente invención se relaciona con métodos para detectar litio en muestras biológicas líquidas, con métodos para medir cuantitativamente el litio en muestras biológicas líquidas y con los reactivos que pueden ser utilizados en tales métodos.
Antecedentes de la invención
La terapia con litio ha sido adoptada durante muchos años para el tratamiento de pacientes que sufren de trastornos de manía bipolar y de otras enfermedades siquiátricas. El mantenimiento de la concentración de iones de litio en la sangre en el rango de concentración terapéutica entre 0,5 y 1,0 mmol/L en pacientes siquiátricos, generalmente por medio de la administración de iones de litio en la forma de carbonato de litio, se ha encontrado que es particularmente efectiva para controlar el humor en tales pacientes. Sin embargo, surge una dificultad ya que la exposición de los pacientes a niveles elevados de iones de litio (aproximadamente por encima de 1,5 mmol/L) durante un período prolongado contribuye a nefrotoxicidad y toxicidad para la glándula tiroides. Una elevación aguda de niveles fisiológicos de litio representa una emergencia médica debida a nefrotoxicidad. Desde luego no es poco común que los pacientes siquiátricos, o bien no obedezcan su medicación de litio o que accidental o intencionalmente se mediquen más de la cuenta. Por estas razones, y con el propósito de ayudar a los médicos a monitorear la efectividad de la terapia de litio en los pacientes, existe la necesidad de métodos efectivos sencillos pero costosos por medio de los cuales se pueda detectar el litio y/o para cuantificar los niveles de litio en muestras biológicas líquidas.
Históricamente, se han medido los niveles de litio en suero por medio de técnicas de fotometría de emisión de llama. En el uso de la fotometría de emisión de llama para las mediciones de sodio y de potasio, se adopta el litio como estándar interno. Tales técnicas se modifican para las mediciones de litio siendo remplazado el estándar interno de litio por cesio. Infortunadamente, los aparatos para fotometría de emisión llama que utiliza cesio como estándar interno son costosos de adquirir y de mantener y pueden ser molestos de operar.
Más recientemente, las mediciones de concentración de litio en muestras biológicas han sido llevadas a cabo por medio de la utilización de técnicas de electrodo de ión selectivo (ISE), que involucran éteres en corona que tienen un núcleo que acomoda al ion Li+. Aunque las primeras técnicas de ISE eran propensas a interferencia provocadas por sodio y otros iones presentes en la muestra de prueba, los analizadores más recientes de ISE son capaces de una medición más exacta y precisa del litio. Aunque los analizadores de ISE son menos costos y más fáciles de operar y de mantener que el equipo fotómetro de llama, son deseables otras técnicas alternativas y de bajo costo para medición de litio.
Se han identificado recientemente una cantidad de compuestos de porfirina que muestran alta selectividad por iones metálicos, como se reporta por ejemplo en Richards y colaboradores (1) y Tabata y colaboradores (2). Infortunadamente, se han encontrado algunas dificultades en la utilización de los compuestos de porfirina identificados en los trabajos de Richards y colaboradores y Tabata y colaboradores en métodos simples y eficientes para determinar la presencia de y/o la cuantificación de los niveles de litio en muestras líquidas biológicas. En particular, Tabata y colaboradores advierten que la proteína reacciona con la porfirina y reduce la absorbancia, y que como resultado, el suero sometido al método para determinación de litio requieren de la remoción de la proteína por medio del uso de ácido tricloroacético. Después se requiere eliminar al ácido tricloroacético por medio de extracción con éter dietílico. Estas etapas de remoción de la proteína incrementan la complejidad y el costo de las técnicas espectrofotométricas de medición de litio con base en porfirina, evitando efectivamente el uso del método de Tabata y colaboradores en analizadores químicos automatizados.
Haiping Sun, Masaaki Tabata, "Separation and transport of lithium of 10-5 M in the presence of sodium chloride higher than 0.1 M by 2,3,7,8,12,13,17,18-octabromo-5,10,15-20-tetrakis(4-sulfonatophenyl)porphyrin", Talanta Vol. 49, No. 3, 1999, páginas 603 - 610, se relaciona con una porfirina soluble en agua (2,3,7,8,12,13,17,18-octabromo-5,10,15-20-tetrakis(4-sulfonatofenil) porfirina (H2(obtpps)4-, H2P4-) que fue sintetizada y aplicada a un método de extracción con solvente y un transporte de litio en líquido a través de membrana tan bajo como 10-5.
M (M= mol dm-3) en presencia de cloruro de sodio superior a 0,1 M. Se extrajo exitosamente porfirina de litio con cinco cargas negativas en cloroformo con ion tetrabutilamonio (But4 N+) a un pH de 12,7. Se transportó el litio a una fase acuosa a pH 7 a través de una membrana líquida de cloroformo que contenía [(But4N)5HP]. Se separó el litio en una muestra de suero o de agua de mar y se determinó su concentración espectrofotométricamente por medio del método anterior sin ninguna interferencia de cloruro de sodio. La interferencia de iones metálicos pesados y de transición estaba enmascarada por Mg-EDTA. Una curva de calibración era lineal sobre un rango de 2 x 10-6 a 2 x 10-5 M con una precisión de 1,51% (RSD).
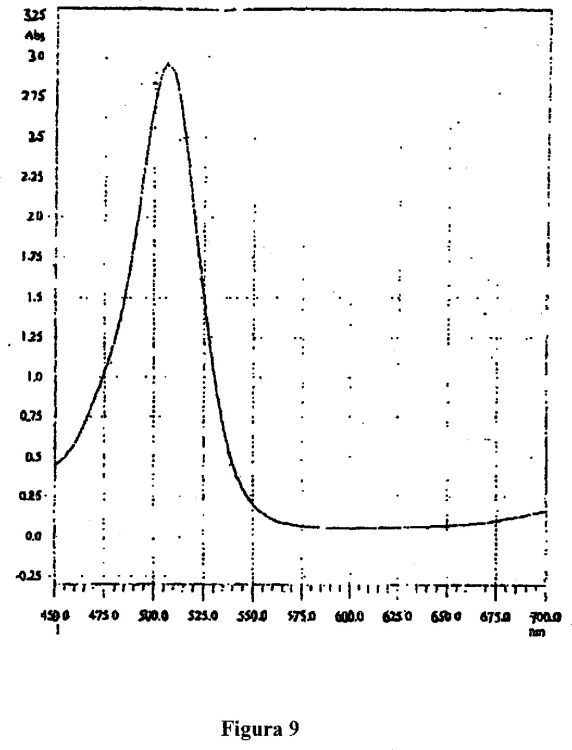
Tabata M. y colaboradores, "Spectrophotometric determination of lithium ion using a water-soluble octabromoporphyrin in aqueous solution", Talanta Vol. 46, No. 4, 1998, páginas 703 - 709, que se relaciona con porfirina soluble en agua, (2,3,7,8,12,13,17,18-octabromo-5,10,15,20-tetrakis(4-sulfonatofenil) porfirina; H2Obtpps4) fue sintetizada y desarrollada para la determinación de ion litio en solución acuosa. Los grupos octabromo disminuyeron la basicidad de la porfirina por medio de su efecto de retirada de electrones, y permiten que la porfirina reaccione con el ion litio en solución alcalina para formar el complejo de litio junto con un cambio de absorción máximo: ? max/nm (log e/mol-1 dm3 cm-1) de la porfirina de litio son 490,5 nm (5,31) y 734 nm (4,36). El ion litio en un nivel menor a ppm fue determinado espectrofotométricamente en solución acuosa. Se aplicó el método propuesto a la determinación de litio en muestras en suero humano y agua de mar. Se aplicó el método propuesto a la determinación de litio en muestras de suero humano y de agua de mar.
Con la descripción anterior en mente, un objetivo de la presente invención es el de proporcionar un método para detectar y/o medir niveles de litio dentro de muestras líquidas biológicas que supera algunos o todos los problemas anteriormente identificados con las técnicas del estado del arte. También es un objetivo de la invención proporcionar un reactivo que pueda ser utilizado fácilmente en tales técnicas. Otros objetivos de la presente invención se harán evidentes a partir de la siguiente descripción detallada de la misma.
Resumen de la invención
De acuerdo con una modalidad de la presente invención se proporciona un método para detectar iones solubles de litio en una muestra biológica líquida que comprende la combinación de:
Reivindicaciones:
1. Un método para detector litio soluble en una muestra biológica líquida que comprende la combinación de:
2. Un método para medir cuantitativamente litio soluble en una muestra biológica líquida que comprende la combinación de:
3. El método de acuerdo a la reivindicación 1 o a la reivindicación 2 en donde el cambio de absorbancia se detecta aproximadamente a 480 nm, aproximadamente a 520 nm o simultáneamente a 480 nm y aproximadamente 520 nm.
4. El método de acuerdo a cualquier reivindicación precedente en donde la muestra biológica líquida es plasma, suero, linfa, proteína, orina, saliva, lágrimas, leche o en donde la muestra biológica líquida se deriva de uno de los anteriores.
5. El método de acuerdo a cualquier reivindicación precedente en donde el pH de la muestra de prueba es aproximadamente 13.
6. El método de acuerdo a cualquier reivindicación precedente en donde el álcali es hidróxido de sodio o carbonato de potasio.
7. El método de acuerdo a cualquier reivindicación precedente en donde el detergente es un detergente catiónico, aniónico o no iónico.
8. El método de acuerdo a cualquiera de las reivindicaciones 1 a 6 en donde el detergente es un sulfato de alquilo, un éter de polioxietileno, un alcanosulfonato o un alquilbencenosulfonato.
9. El método de acuerdo a la reivindicación 8 en donde el detergente es polioxietileno 23 lauril éter.
10. El método de acuerdo a cualquier reivindicación precedente en donde el agente de quelación es etilén diamina, piridina, propilén diamina, dietilén triamina, trietilén tetramina, 2,2'-bipiridina, 1,10-fenantrolina, ácido etilendiaminotetraacético (EDTA), dimetilglioximato, glicinato o acetilacetonato.
11. El método de acuerdo a la reivindicación 10 en donde el agente de quelación es EDTA.
12. El método de acuerdo a cualquier reivindicación precedente en donde el solvente es agua destilada, etanol, metanol, acetona, dimetilformamida o dimetilsulfóxido.
13. El método de acuerdo a cualquier reivindicación precedente en donde el estándar deficiente en litio incluye cada uno de los componentes (b) hasta (e) y (f) si están presentes en la muestra de prueba, con un solvente adecuado presente en lugar del componente (a).
14. El método de acuerdo a la reivindicación 1 en donde el litio está indicado por medio de un cambio negativo de absorbancia aproximadamente a 520 nm.
15. El método de acuerdo a la reivindicación 1 en donde el litio está indicado por medio de un cambio positivo de absorbancia aproximadamente a 480 nm.
16. Un reactivo para uso en un método para detección de litio en una muestra biológica líquida que comprende:
17. El reactivo de acuerdo a la reivindicación 16 en donde el componente (i) está presente en una concentración entre 5 mg/L y 200 mg/L.
18. El reactivo de acuerdo a la reivindicación 16 o a la reivindicación 17 n donde el álcali es hidróxido de sodio o carbonato de potasio.
19. El reactivo de acuerdo a la reivindicación 18 en donde el álcali está presente en una concentración entre 0,001 M y 0,5 M.
20. El reactivo de acuerdo a cualquiera de las reivindicaciones 16 a 19 en donde en detergente es polioxietileno 23 lauril éter (aproximadamente solución al 30% (v/v)).
21. El reactivo de acuerdo a la reivindicación 20 en donde el polioxietileno 23 lauril éter está presente en una concentración aproximadamente entre 0,001% hasta aproximadamente 4,0% en volumen del volumen total del reactivo.
22. Un reactivo de acuerdo a cualquiera de las reivindicaciones 16 a 21 en donde el agente de quelación es ácido etilendiaminotetraacético (EDTA).
23. El reactivo de acuerdo a la reivindicación 22 en donde el EDTA es EDTA tetrasódico presente en una concentración entre 1,0 µM hasta 1000 µM.
24. El reactivo de acuerdo a cualquiera de las reivindicaciones 16 a 23 que comprende además un fungicida y/o un bactericida.
25. Un reactivo de acuerdo a la reivindicación 24 en donde el fungicida/bactericida es azida de sodio.
26. El reactivo de acuerdo a la reivindicación 25 en donde la azida de sodio está presenta en una concentración entre 0,1 g/L y 10 g/L.
27. El reactivo de acuerdo a la reivindicación 16 que comprende:
28. Un reactivo de acuerdo a la reivindicación 27 que comprende además aproximadamente 1,0 g/L de azida de sodio.
Patentes similares o relacionadas:
Dispositivo de indicación, del 25 de Marzo de 2020, de Aristotech Holding GmbH: Dispositivo de indicación para indicar al menos un valor químico de un líquido, en particular de un líquido corporal, que comprende al menos un primer […]
Indicador terapéutico atómico, del 25 de Marzo de 2020, de Atomic Oncology Pty Ltd: Un procedimiento para determinar la radio-sensibilidad de un cáncer, comprendiendo el procedimiento cuantificar el nivel de manganeso en una […]
Sistemas y procedimientos para determinar la osmolaridad de una muestra, del 8 de Enero de 2020, de LacriSciences LLC: Un sistema que comprende: (i) un sensor que comprende una superficie de detección que comprende una región revestida, en el que el sensor comprende una pluralidad […]
Composición de reactivo de litio, y método y dispositivo para cuantificar iones de litio usando la misma, del 1 de Enero de 2020, de Metallogenics Co., Ltd: Composición de reactivo para detectar y medir litio, caracterizada porque está en forma de una disolución acuosa que comprende los siguientes […]
Aparato de control de amoniaco y método de control de amoniaco, del 20 de Noviembre de 2019, de AJINOMOTO CO., INC.: Método de control de amoniaco para fermentación, que es para controlar la concentración de amoniaco de un medio de cultivo contenido en un tanque […]
Control del ph en soluciones acuosas que contienen urea utilizando composiciones que contienen aminoácidos, del 6 de Noviembre de 2019, de SIEMENS HEALTHCARE DIAGNOSTICS INC.: Una composición que comprende un reactivo de control de calidad o calibración acuoso dispuesto en un sistema cerrado, comprendiendo la composición: urea […]
Método de adquisición de datos para determinar la probabilidad de que un quiste endometriósico ovárico sea canceroso, y dispositivo de diagnóstico para el mismo, del 8 de Octubre de 2019, de CELLSPECT CO., LTD: Método para adquirir datos para determinar la probabilidad de cancerización del quiste ovárico endometriósico, que incluye una etapa de medir la concentración de hierro […]
Métodos para tratar trastornos del ciclo de la urea con el fin de prevenir crisis hiperamonémicas controlando los niveles de amoniaco en sangre, del 10 de Julio de 2019, de Immedica Pharma AB: Fenilbutirato de glicerol (GPB) para su uso en un método de prevención de una crisis hiperamonémica (CHA) en un sujeto con un trastorno del ciclo de la urea (TCU) […]