CICLIZACION DE PEPTIDOS SOBRE RESINA.
Método de síntesis de péptidos, que comprende las etapas de:
a.
sintetizar un péptido enlazado a una fase sólida cuyo péptido comprende al menos un residuo de cisteína, homo- o nor-cisteína, cuya cisteína es protegida en su cadena lateral por un grupo S-terc-butilsulfenilo; y
b. ya sea acoplar N-terminalmente otro aminoácido que tiene un radical 3-[(2-carboxietilo)ditio]propionilo en su Na u, o desproteger el Na del aminoácido N-terminal y reaccionar el Na libre con 3,3''-ditiopropionimida para proporcionar la correspondiente Na-3-[(2-carboxietil)ditio]propionamida, o desproteger el Na del aminoácido N-terminal y reaccionar el Na libre con un compuesto de fórmula IV
IVR7-S-S-[CH2]2-COOH
en donde R7 es arilo-, incluyendo heteroarilo-, o es aralquilo-, alquilarilo- o alquilo- que puede estar además sustituido con halógeno, amido, éster y/o éter; y
c. reaccionar el péptido con un reactivo separador del grupo protector S-terc-butilsulfenilo, y
d. ciclizar el péptido sobre resina por medio de la formación de un enlace disulfuro, con preferencia ciclizar el péptido en presencia de aire y/u oxígeno
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2005/011182.
Solicitante: LONZA AG.
Nacionalidad solicitante: Suiza.
Dirección: MUNCHENSTEINERSTRASSE 38,4052 BASEL.
Inventor/es: WERBITZKY, OLEG, VARRAY,STEPHANE, ZEITER,THOMAS.
Fecha de Publicación: .
Fecha Concesión Europea: 13 de Enero de 2010.
Clasificación Internacional de Patentes:
- C07K1/04 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07K PEPTIDOS (péptidos que contienen β -anillos lactamas C07D; ipéptidos cíclicos que no tienen en su molécula ningún otro enlace peptídico más que los que forman su ciclo, p. ej. piperazina diones-2,5, C07D; alcaloides del cornezuelo del centeno de tipo péptido cíclico C07D 519/02; proteínas monocelulares, enzimas C12N; procedimientos de obtención de péptidos por ingeniería genética C12N 15/00). › C07K 1/00 Procedimientos generales de preparación de péptidos. › sobre soportes.
- C07K1/06 C07K 1/00 […] › utilizando grupos protectores o agentes de activación.
- C07K7/06A
Clasificación PCT:
Fragmento de la descripción:
Ciclización de péptidos sobre resina.
La presente invención se refiere a un método de formación de enlaces disulfuro en la síntesis de péptidos en fase sólida (SPPS).
Se puede emplear una amplia variedad de grupos protectores para la protección de residuos de cisteína, por ejemplo, tritilo, acetamidometilo, t-butilo, trimetilacetamidometilo, 2,4,6-trimetoxibencilo, metoxitritilo, t-butilsul- fenilo.
Como es muy usual, el grupo tritilo se emplea para la protección convencional de la cadena lateral de cisteína durante la síntesis de péptidos. Para la protección de cisteínas que posteriormente son ciclizadas a cistina, en su amplia mayoría se ha utilizado el grupo protector acetamidometilo (acm) junto con oxidación con yodo (Kamber et al., 1980, Helv. Chim. Acta 63, 899-915; Rietman et al., 1994, Int. J. Peptide Protein Res. 44, 199-206).
Se ha descrito una multitud de agentes oxidantes distintos del yodo al objeto de permitir la formación de cistina en la ciclización en fase sólida (ejemplos derivados de Albericio et al., en: Chan and White, eds., 'FMOC Solid-phase Peptide Synthesis',Oxford university Press 2000, p. 91 a 114: glutationa en tampón acuoso, DMSO, ferricianuro potásico, reactivo de Ellman, 5,5'-ditiobis-(ácido 2-nitrobenzoico), yodo, trifluoracetato de talio (III), alquiltriclorosilano-sulfóxido, oxidación mediada por trifluormetanosulfonato de plata-DMSO en un medio fuertemente ácido.
Normalmente, todos esos métodos dan lugar a múltiples productos secundarios indeseables y requieren largos tiempos de reacción del orden de 10-20 horas para lograr un rendimiento óptimo.
Volkmer-Engert et al. (J. Peptide Res. 51, 1998, 365-369) describen la formación oxidativa de enlaces disulfuro catalizada con carbón vegetal mediante el uso de oxígeno disuelto en el disolvente acuoso. Se ha dicho que el uso de controles cuidadosos prueban que el depósito de oxígeno físicamente disuelto en el medio acuoso era necesario y suficiente para cargar el carbón vegetal con oxígeno para la oxidación. El uso de carbón vegetal, en comparación con la pulverización tradicional de aire en ausencia de catalizador, aceleraba la velocidad de reacción de forma drástica.
El uso de carbón vegetal requiere inevitablemente llevar a cabo dicha reacción en solución homogénea pero no sobre resina; además, las posteriores etapas de reacción de desprotección no tolerarían la presencia continua de carbón vegetal el cual es imposible de eliminar de la fase sólida de péptido-resina.
La WO 03/093302 describe la ciclización de un péptido que contiene triptófano en solución después de su liberación desde una fase sólida. El péptido tiene una cisteinilcarboxamida C-terminal cuya función tiol de la cadena lateral está sin proteger y cuyo péptido experimenta además una derivación N-terminal con una mitad mercaptopropionamida o 3-[(2-carboxietil)ditio]propionamida. La protección y/o desprotección de la cadena lateral amídica de cisteína llega a ser superflua por la presencia de la cadena lateral que efectúa el anclaje del péptido sobre la resina por vía del enlace de tioéster de dicha cadena lateral de cisteína. La derivación N-terminal con ditiopropionato tiene lugar antes de escindirse de la resina. La ciclización tiene lugar después de la escisión desde la resina, por tanto en solución, por medio de una formación de puente disulfuro entre cisteína y la mitad tiopropionamida. La escisión respecto del soporte sólido y la desprotección global, excepto para la función tiopropionilo, antes de la ciclización, es un hecho obligado en este esquema.
Como un inconveniente, debe tenerse un cuidado sumo a la hora de preservar la mitad tiopropionamida durante la escisión y desprotección global. Atherton et al. (1985, J. Chem. Perkin Trans. I., 2065) indicaron que el uso popular de tioanisol que tiene la doble función de barredor y de promotor de la acidólisis, para efectuar la escisión respecto de la resina, también dio lugar a una desprotección parcial prematura de cisteínas protegidas con acm, terc-butilo y terc-butilsulfenilo. La vía de síntesis general es intrincada, ya que las muchas etapas involucradas afectan de manera negativa a los rendimientos que pueden obtenerse por esta vía. La ciclización ha de realizarse en solución altamente diluida para prevenir la dimerización. En realidad, en la descripción de esta referencia no se indica de forma explícita los rendimientos obtenidos.
Un objeto de la presente invención consiste en trazar otro método u otro método mejorado más simple y directo para sintetizar péptidos cíclicos enlazados por disulfuro por medio de la síntesis en fase sólida. Este objeto es conseguido, de acuerdo con la presente invención, a través de un método de síntesis de péptidos que comprende las etapas de:
El péptido de acuerdo con la presente invención puede ser cualquier péptido que comprenda aminoácidos naturales o no naturales tales como, por ejemplo, homocisteína, homoarginina, D-ciclohexilalanina, penicilamina (Pen) u ornitina (Orn). Los términos espina dorsal o cadena principal del péptido, cadena lateral y los prefijos "nor-" y "homo-" están considerados en el presente contexto de acuerdo con las definiciones de IUPAC-IUB (Joint IUPAC-IUB Commission on Biochemical Nomenclature, "Nomenclature and symbolism for amino acids and Peptides", Pure Appl. Chem., 56, 595-624 (1984). En su significado más estrecho, preferido, representa la presencia de solo un grupo de puente metileno extra en la porción de la cadena lateral.
Debe prestarse una atención especial a una protección adicional de la cadena lateral, en particular cuando se hace referencia a otros residuos de cisteína, homo- o nor-cisteína incluidos en la secuencia péptida y que se desea que permanezcan protegidos durante la reacción de ciclización y no participen en esta última. Con preferencia, dichos otros residuos que comprenden una mitad sulfhidrilo son protegidos por grupos protectores no sensibles a trialquilfosfina, más preferentemente, dicho grupo protector no sensible a sulfhidrilo se elige del grupo consistente en grupos protectores tritilo, terc-butilo, acetatamidometilo, acetamidometilo alquilado y tritilo alquilado. A nivel general, se pueden emplear grupos protectores de la cadena lateral como los normalmente utilizados en la técnica (véase, por ejemplo, Bodansky, M. Principles of Peptide Syntesis, ver a continuación) para proteger cadenas laterales susceptibles que de otro modo podrían ser modificados en los ciclos de acoplamiento y desprotección. Ejemplos de aminoácidos con cadenas laterales susceptibles son Cys, Asp, Glu, Ser, Arg, Homo-Arg (Har), Tyr, Thr, Lys, Om, Pen, Trp, Asn y Gln. Alternativamente, se puede efectuar una modificación química posterior en la síntesis en fase sólida de la amida péptida para proporcionar una cadena lateral deseada. Por ejemplo, como se indica ampliamente en diferentes referencias (EP-301 850; Yajima et al., 1978, J. Chem. Soc Chem. Commun., p.482; Nishimura et al., 1976, Chem. Pharm. Bull. 24: 1568), se puede preparar homoarginina por guanidación de un residuo...
Reivindicaciones:
1. Método de síntesis de péptidos, que comprende las etapas de:
2. Método según la reivindicación 1, caracterizado porque dicha cisteína se encuentra a por lo menos 3, más preferentemente por lo menos 5 residuos de aminoácidos separada del residuo de aminoácido N-terminal de dicho péptido.
3. Método según la reivindicación 1, caracterizado porque la resina de fase sólida se elige entre 2-clorotritilo (CTC) o una resina productora de amida.
4. Método según la reivindicación 1, caracterizado porque el péptido tiene al menos otro grupo protector de la cadena lateral que incluye otros residuos de cisteína, homo- o nor-cisteína protegidos de manera diferente.
5. Método según la reivindicación 1, caracterizado porque la cisteína es el último residuo C-terminal.
6. Método según la reivindicación 1 o 6, caracterizado porque la separación de al menos el grupo S-terc-butilsulfenilo se lleva a cabo por reacción del péptido con una trialquilfosfina.
7. Método según la reivindicación 1, caracterizado porque la péptido es ciclizado en presencia de una base débil en un disolvente aprótico polar.
8. Método según la reivindicación 1 o 7, caracterizado porque el enlace del péptido a la fase sólida es lábil a los ácidos, preferentemente lábil en 60% de TFA en diclorometano a temperatura ambiente.
9. Método según la reivindicación 5, caracterizado porque la resina es una resina Sieber.
10. Método según la reivindicación 1, caracterizado porque en una etapa posterior, el péptido se escinde de la resina, preferentemente bajo condiciones de desprotección global.
11. Péptido de fórmula I
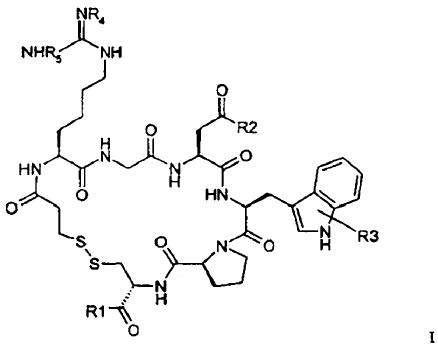
en donde R4, R5 son H o un grupo protector de Arg, R2 es un grupo protector de ácido carboxílico y R3 es un grupo protector de Trp y R1 es una fase sólida en una unión con enlace tioéster, éster o amida a la espina dorsal del péptido.
12. Péptido según la reivindicación 11, caracterizado porque R4 y R5 son H y R3 es N- benciloxicarbonilo y R2 es terc-butilo.
13. Péptido según la reivindicación 12, caracterizado porque la fase sólida es una resina Sieber que consecuentemente está enlazada mediante un enlace amida a la espina dorsal del péptido.
14. Péptido, preferentemente un péptido que comprende al menos un grupo protector de la cadena lateral de aminoácido, en donde el péptido está unido a una fase sólida por vía del residuo C-terminal o por vía de una cadena lateral de aminoácido, caracterizado porque el péptido es un péptido cíclico que comprende una mitad de fórmula II
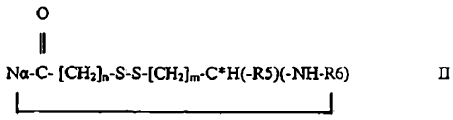
en donde n y m se eligen de manera independiente en el intervalo de 1 a 10, preferentemente n es 2 y m es 1 (proporcionando una mitad cisteinilo), Na es el nitrógeno N-terminal de la espina dorsal del péptido y C* es el Ca de un residuo de aminoácido de la espina dorsal del péptido, siendo R6 la mitad cíclica N-terminal de la espina dorsal del péptido que termina con dicho Na, y siendo R5 la mitad C- terminal de la espina dorsal del péptido que está unida a la fase sólida, con la condición de que N no es Na, y en donde preferentemente R6 comprende al menos 3, más preferentemente al menos 4 residuos de aminoácido intervinientes.
15. Péptido, preferentemente un péptido que comprende al menos un grupo protector de la cadena lateral de aminoácido distinto de un grupo S-terc-butilsulfenilo en un residuo de cisteína, homo- o nor-cisteína, cuyo péptido está enlazado a una fase sólida por vía del residuo C-terminal, caracterizado porque el péptido comprende al menos un residuo de cisteína, homo- o nor-cisteína que está protegido en su cadena lateral por un grupo S-terc-butilsulfenilo y que está sustituido en el terminal N en su Na para constituir una mitad amida de fórmula III
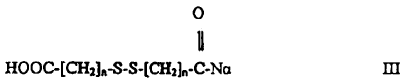
en donde n es 1 a 10, preferentemente n es 2.
16. Péptido, preferentemente un péptido que comprende al menos un grupo protector de la cadena lateral de aminoácido distinto de un grupo S-terc-butilsulfenilo en un residuo de cisteína, homo- o nor-cisteína, cuyo péptido está enlazado a una fase sólida por vía del residuo C-terminal, caracterizado porque el péptido comprende al menos un residuo de cisteína, homo- o nor-cisteína que tiene un grupo tiol libre en su cadena lateral y que está sustituido en el N-terminal en su Na para constituir la mitad amida de fórmula III
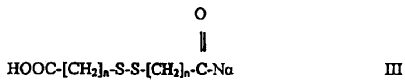
en donde n es 1 a 10, preferentemente n es 2.
Patentes similares o relacionadas:
Método de síntesis de linaclotida, del 27 de Mayo de 2020, de Hybio Pharmaceutical Co., Ltd: Método de síntesis de linaclotida, que comprende las siguientes etapas: 1) preparar una resina precursora de linaclotida haciendo reaccionar […]
Método para preparar semaglutida, del 13 de Mayo de 2020, de Hybio Pharmaceutical Co., Ltd: Método de preparación de semaglutida, que comprende las etapas de: etapa 1: acoplar Gly a una resina mediante síntesis en fase sólida para obtener Gly-resina; y […]
Procedimientos para la preparación de análogos de oxitocina, del 18 de Febrero de 2019, de F. HOFFMANN-LA ROCHE AG: Procedimiento para la preparación de análogos de oxitocina de fórmula I **Fórmula** en la que R1 es hidrógeno o alquilo C1-7 y R2 es hidrógeno […]
Método para preparar exenatida, del 29 de Octubre de 2018, de Hybio Pharmaceutical Co., Ltd: Un método para la preparación de exenatida, que se caracteriza por comprender las siguientes etapas: Etapa 1: se obtiene serina-resina mediante un primer […]
Péptido antibiótico y método de su preparación, y aplicación del mismo, del 3 de Enero de 2018, de Jiangsu Protelight Pharmaceutical & Biotechnology Co., Ltd: Un peptido antimicrobiano con secuencia de aminoacidos de Ac-F-K-K-L-K-K-L-F-S-K-L-W-N-W-K-NH2 (SEQ ID NO: 1).
Método para la síntesis en fase sólida de liraglutida, del 27 de Julio de 2016, de Hybio Pharmaceutical Co., Ltd: Un método para la síntesis en fase sólida de liraglutida, que se caracteriza por que el método comprende las siguientes etapas: A) en […]
Derivados de ácido aspártico, del 8 de Junio de 2016, de MERCK PATENT GMBH: Compuestos de las fórmulas Ia y/o Ib**Fórmula** en las que R1, R2, R3 representan, independientemente uno de otro, una cadena de hidrocarburo […]
Híbridos de monómero-dímero quiméricos de inmunoglobulina, del 4 de Mayo de 2016, de Biogen Hemophilia Inc: Una proteína quimérica que comprende una molécula biológicamente activa y dos regiones constantes de inmunoglobulina o partes de las mismas que son […]