Vector que comprende promotor de manosa y promotor de manosa.
Vector que se puede expresar en una célula anfitriona procariótica que comprende un promotor inducible por manosa del operón de manosa de Bacillus subtilis ligado en forma funcional a una unidad transcripcional que comprende una secuencia de ácidos nucleicos heteróloga que codifica un polipéptido,
en donde el promotor inducible por manosa se selecciona del promotor manP y promotor manR.
Tipo: Patente Europea. Resumen de patente/invención. Número de Solicitud: E09010283.
Solicitante: LONZA AG.
Nacionalidad solicitante: Suiza.
Dirección: Rottenstrasse 6/E3 3930 Visp VS SUIZA.
Inventor/es: ALTENBUCHNER, JOSEF, KIZIAK,CHRISTOPH, SUN,TIANQI.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- C12N15/63 QUIMICA; METALURGIA. › C12 BIOQUIMICA; CERVEZA; BEBIDAS ALCOHOLICAS; VINO; VINAGRE; MICROBIOLOGIA; ENZIMOLOGIA; TECNICAS DE MUTACION O DE GENETICA. › C12N MICROORGANISMOS O ENZIMAS; COMPOSICIONES QUE LOS CONTIENEN; PROPAGACION, CULTIVO O CONSERVACION DE MICROORGANISMOS; TECNICAS DE MUTACION O DE INGENIERIA GENETICA; MEDIOS DE CULTIVO (medios para ensayos microbiológicos C12Q 1/00). › C12N 15/00 Técnicas de mutación o de ingeniería genética; ADN o ARN relacionado con la ingeniería genética, vectores, p. ej. plásmidos, o su aislamiento, su preparación o su purificación; Utilización de huéspedes para ello (mutantes o microorganismos modificados por ingeniería genética C12N 1/00, C12N 5/00, C12N 7/00; nuevas plantas en sí A01H; reproducción de plantas por técnicas de cultivo de tejidos A01H 4/00; nuevas razas animales en sí A01K 67/00; utilización de preparaciones medicinales que contienen material genético que es introducido en células del cuerpo humano para tratar enfermedades genéticas, terapia génica A61K 48/00; péptidos en general C07K). › Introducción de material genético extraño utilizando vectores; Vectores; Utilización de huéspedes para ello; Regulación de la expresión.
- C12N15/70 C12N 15/00 […] › Vectores o sistemas de expresión especialmente adaptados a E. coli.
- C12N15/75 C12N 15/00 […] › para Bacillus.
PDF original: ES-2394668_T3.pdf
Fragmento de la descripción:
Vector que comprende promotor de manosa y promotor de manosa La presente invención se relaciona con vectores que se pueden expresar en células anfitrionas procarióticas que comprenden un promotor inducible por manosa para la expresión heteróloga de ácidos nucleicos que codifican, por ejemplo, polipéptidos tales como proteínas recombinantes.
En particular, la presente invención se relaciona con nuevos vectores para la expresión heteróloga en un anfitrión que comprende una región promotora del operón de manosa ligado en forma funcional a una unidad transcripcional que comprende una secuencia de ácidos nucleicos que es heteróloga a dicho anfitrión, mientras la expresión de dicha secuencia de ácidos nucleicos se controla por dicha región promotora del operón de manosa. Adicionalmente, la presente invención se relaciona con el uso de estos vectores para la expresión heteróloga de ácidos nucleicos que codifican por ejemplo polipéptidos tales como proteínas recombinantes.
Se han descrito muchos sistemas para la expresión heteróloga de ácidos nucleicos que codifican, por ejemplo, polipéptidos (genes estructurales) en sistemas procarióticos. Para esto, el anfitrión se transforma con un vector que comprende la secuencia de ácidos nucleicos del gen estructural de interés ligado en forma funcional a un promotor que es una secuencia de ácidos nucleicos que permite que el gen estructural sea transcrito. Mediante la inducción adecuada el promotor se activa y permite la transcripción del gen estructural. La inducción puede ser bajo control positivo o negativo.
En la inducción de control negativo un represor se une al promotor y evita la transcripción del gen estructural. Si está presente un inductor adecuado, se desactiva el represor y se permite la transcripción.
En la inducción de control positivo el promotor se activa luego de unión de un activador, en donde la unión del activador al promotor se media por un inductor adecuado.
Los inductores típicos pueden ser sustratos cuyos anfitriones procarióticos requieren metabolismo, por ejemplo, diferentes tipos de azúcares.
La presente invención se relaciona con sistemas positivamente inducibles, en donde en la presencia de un sustrato adecuado, es decir el inductor, un activador se une al promotor que inicia la transcripción de los genes ligados en forma funcional a dicho promotor.
Hasta ahora, la mayoría de sistemas de expresión de gen heterólogo en los sistemas de anfitrión procarióticos se han basado exclusivamente sobre un conjunto limitado de promotores bacterianos. Por consiguiente, también se limita el número de sustratos, que se pueden utilizar como inductores.
Adicionalmente, la producción de un sistema de expresión heteróloga depende del número de anfitriones procarióticos transformados disponibles. Por lo tanto, se requieren sistemas de anfitrión procarióticos que sean capaces de crecer a una alta densidad celular, es decir, permite la proliferación rápida sin perder el vector en la división celular.
El documento US 2007/0259004 A1 describe la expresión de una secuencia de ácidos nucleicos que utiliza un sistema de expresión en Bacillus que comprende un promotor gsiB como un promotor inducible, en donde se puede inducir el promotor por una medida seleccionada de reducción en pH, aumento en la temperatura, adición de alcohol, agotamiento de nutrientes, y limitación de oxígeno.
El documento WO 2004/033633 A2 se relaciona con un vector lanzadera recombinante que comprende un primer origen de replicación o región de integración (OR/RI) funcional en bacterias Gram positivas con bajo contenido de GC, un segundo OR/RI funcional en un primer tipo bacteriano, un tercer OR/RI funcional en un segundo tipo bacteriano, por lo menos un sitio cos; y por lo menos un marcador de selección de anticuerpo. El vector es inducible a replicación con alto número de copias. El vector es funcional en Bacillus subtilis, B. lichenifomis, B.cereus, B.pumilus, B.anthracis, Glostridium acetobutylicum, Lactobacillus lactis, L.plantarum, o Enterococcus feacalis.
En el documento DE 102 25 380 A1 se describe un plásmido recombinante que comprende:
(a) un vector lanzadera de E. coli y Bacillus, que incluye un sitio de clonación múltiple;
(b) un promotor inducible o constitutivo (P) ; y
(c) bajo control de P (promotor xylA) , un gen glicosiltransferasa.
Los promotores adecuados adicionales son los promotores Bacillus megaterium GlucDH, spolV, bgaM, y el promotor Bacillus subtiles Pspac.
En el documento WO 2006/133210 A2 se describe la expresión de polipéptido recombinante en células de Pseudomonas fluorescens en donde la célula se transfecta con ácido nucleico que codifica el polipéptido ligado a un promotor inducible de fuente de carbono seleccionado de promotores inducibles de manitol, glucitol, y arabitol.
Resumen de la invención De acuerdo con la presente invención estos y otros objetivos serán evidentes a partir de la siguiente descripción, que se han alcanzado al proporcionar nuevos vectores que comprenden una región promotora del operón de manosa ligados en forma funcional a una unidad transcripcional que comprende una secuencia de ácidos nucleicos que es heteróloga a dicho anfitrión, mientras que la expresión de dicha secuencia de ácidos nucleicos se controla por dicha región promotora del operón de manosa.
También se proporcionan el uso de dicho nuevo vector para la expresión heteróloga regulada de una secuencia de ácidos nucleicos en un anfitrión procariótico; una secuencia de ácidos nucleicos que se puede expresar aislada y purificada en un anfitrión que comprende una región promotora del operón de manosa; un anfitrión procariótico transformado con dicho vector o dicha secuencia de ácidos nucleicos aislada y purificada; un método para producir un polipéptido en un anfitrión que utiliza dicho vector o dicha secuencia de ácidos nucleicos aislada y purificada; así como también el uso de un anfitrión procariótico transformado con dicho vector o dicha secuencia de ácidos nucleicos aislada y purificada en fermentación, en particular en fermentación de alta densidad celular.
Otros objetivos y ventajas serán evidentes a aquellos expertos en la técnica a partir de la revisión de la siguiente descripción detallada con referencia a las figuras ilustrativa acompañantes, y las reivindicaciones adjuntas.
Breve descripción de las figuras
Se muestra en La Figura 1 la secuencia de ácidos nucleicos de B.subtilis utilizada en el mapeo del sitio de iniciación de transcripción del promotor manP con el sitio de inicio de transcripción en un nucleótido de adenina que se resalta, las secuencias -35 y -10 deducidas en cursiva, el fin de manR y el inicio del gen lys marcado por flechas y los sitios de restricción BglII, XbaI, AflII y NdeI subrayados;
La Figura 2 la secuencia de ácidos nucleicos de la región promotora que comprende promotor manR con el sitio de inicio de transcripción en un nucleótido de guanina que se resalta, las secuencias -35 y -10 deducidas están en cursiva, el inicio del gen manR que se indica por una flecha y el sitio de restricción HinDIII y la secuencia cre putativa que se subraya;
La Figura 3 la secuencia de ácidos nucleicos obtenida de B.subtiles que comprende la región promotora del promotor manR que está contenida en pSUN291, pSUN384.1 y pSUN385.2, respectivamente, con el inicio de lacZ que se indica por una flecha y los sitios de restricción que se subrayan;
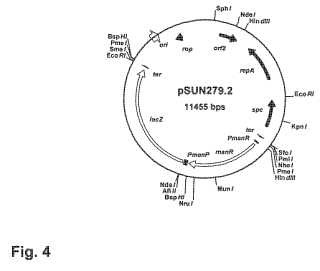
La Figura 4 el mapa de plásmido del vector de expresión pSUN 279.2 de acuerdo con la presente invención;
La Figura 5 las actividades de β-galactosidasa de B.subtiles 3NA que contiene los plásmidos pSUN 279.2, pSUN
284.1 y pSUN 291, respectivamente, de acuerdo con la presente invención;
La Figura 6 la secuencia de ácidos nucleicos obtenida de B.subtiles que comprenden la región promotora del promotor manP de B.subtiles que incluye el extremo de terminal C de manR, la región intergénica entre manR y manP, aquí se reemplaza por gen indicador lacZ, con el sitio de inicio de transcripción, las secuencias -35 y -10 que están en negrita, el fin de manR y el inicio de lacZ que se indica por una flecha y los sitios de restricción que se subrayan;
La Figura 7 las actividades de β-galactosidasa de B.subtiles 3NA que contiene el plásmido pSUN 279.2 así como también de plásmidos adicionales que contienen fragmentos de diferentes longitudes de la secuencia de ácidos nucleicos mostrados en la figura 6;
La Figura 8 las actividades de β-galactosidasa de B.subtilis 3NA que comprende los vectores pSUN291, pSUN384.1 y pSUN345.2 con... [Seguir leyendo]
Reivindicaciones:
1. Vector que se puede expresar en una célula anfitriona procariótica que comprende un promotor inducible por manosa del operón de manosa de Bacillus subtilis ligado en forma funcional a una unidad transcripcional que comprende una secuencia de ácidos nucleicos heteróloga que codifica un polipéptido, en donde el promotor inducible por manosa se selecciona del promotor manP y promotor manR.
2. Vector de acuerdo con la reivindicación 1 en donde el vector comprende la secuencia parcial o completa del gen regulador manR.
3. Vector de acuerdo con cualquiera de las reivindicaciones 1 o 2, en donde el promotor manP comprende una secuencia seleccionada de
y
y una secuencia complementaria las mismas o variantes de estas.
4. Vector de acuerdo con la reivindicación 1, en donde el promotor manR comprende una secuencia seleccionada 15 de y
una secuencia complementaria de las mismas o variantes de estas
5. Vector de acuerdo con una cualquiera de las reivindicaciones precedentes, en donde el vector comprende en dirección 5’ de la secuencia de ácidos nucleicos heteróloga un elemento de respuesta a un catabolito.
6. Vector de acuerdo con una cualquiera de las reivindicaciones precedentes en donde el vector comprende una secuencia de terminación de transcripción ubicada en dirección 3’ de la secuencia de ácidos nucleicos heteróloga.
7. Vector de acuerdo con la reivindicación 6 en donde la secuencia de terminación de transcripción se deriva de la región 3’ del gen tufA de Bacillus subtilis.
8. Vector de acuerdo con una cualquiera de las reivindicaciones precedentes en donde el vector es un vector lanzadera replicable en Escherichia coli y Bacillus subtilis.
9. Vector de acuerdo con cualquiera de las reivindicaciones precedentes en donde el vector comprende el origen de
replicación de plásmido pUC18 y/o el replicón pBS72 o el gen rep junto con el origen de replicación del plásmido 5 pUB110.
10. Vector de acuerdo con una cualquiera de las reivindicaciones precedentes en donde la secuencia de ácidos nucleicos heteróloga codifica un anticuerpo o un fragmento del mismo.
11. Vector de acuerdo con cualquiera de las reivindicaciones precedentes, en donde la región de iniciación de transcripción de gen manP o gen manR se reemplaza por la región de iniciación de transcripción de otro gen.
12. Vector de acuerdo con la reivindicación 11, en donde la región de iniciación de transcripción del gen manP o gen manR se reemplaza por la región de iniciación de transcripción del gen tufA o gen gsiB.
13. Una secuencia de ácidos nucleicos aislada y purificada de la región promotora inducible por manosa del operón de manosa del Bacillus subtilis, secuencia complementaria de esta o variantes de la misma, en donde el promotor inducible por manosa se selecciona del promotor manP y el promotor manR.
14. La secuencia de ácidos nucleicos aislada y purificada de acuerdo con la reivindicación 13, en donde la secuencia comprende cualquiera de y
secuencia complementaria de estas o variantes de las mismas.
15. Célula anfitriona procariótica transformada con el vector de una cualquiera de las reivindicaciones 1 a 12 o con 25 una secuencia de ácidos nucleicos de acuerdo con la reivindicación 13 o 14.
16. Célula anfitriona procariótica de acuerdo con la reivindicación 15, en donde la célula anfitriona procariótica se somete a represión catabólica de carbono y comprende un sistema de fosfortransferasa para fosfoenolpiruvato: carbohidrato.
17. Célula anfitriona procariótica de acuerdo con reivindicaciones 15 o 16, en donde la célula anfitriona procariótica 5 es Gram-positiva.
18. Célula anfitriona procariótica de acuerdo con cualquiera de las reivindicaciones 16 a 17, en donde la célula anfitriona pertenece al phylum Firmicutes.
19. Método para producir un polipéptido en un célula anfitriona procariótica que comprende las etapas de construir un vector de acuerdo con una cualquiera de las reivindicaciones 1 a 12, transformar un célula anfitriona procariótica
con dicho vector, permitir la expresión de dicho polipéptido al hacer crecer la célula anfitriona transformada en un medio de cultivo celular bajo condiciones adecuadas y recuperar el polipéptido de las células o del cultivo celular.
20. Método de acuerdo con la reivindicación 19 en donde las células anfitrionas se hacen crecer primero en la presencia de una fuente de carbono diferente del inductor, y luego, en una segunda etapa, en la presencia del inductor.
21. Uso del vector de una cualquiera de las reivindicaciones 1 a 12 o de una secuencia de ácidos nucleicos aislada y purificada de acuerdo con la reivindicación 13 o 14, para la expresión regulada de una secuencia de ácidos nucleicos heteróloga que codifica un polipéptido en una célula anfitriona procariótica.
concentración de biomasa seca células de subclonación de plásmido [%]
generaciones
prueba de estabilidad de plásmido de pMW 168.01 en B. Subtilis 3NA
Fase de tanda de carga Fase de tanda
duración del cultivo
progreso de crecimiento de serie 1
concentración de biomasa seca Fluorescencia [RFU]
Fase de tanda Fase de tanda de carga inducción de impacto inducción de impacto duración
señal de fluorescencia de serie 1
Fase de tanda Fase de tanda de carga duración del cultivo progreso de crecimiento de serie 2
concentración de biomasa seca Fluorescencia [RFU]
Fase de tanda Fase de tanda de carga
inducción de impacto inicio y fin deCarga de o-Manosa
duración señal de fluorescencia de serie 2
Fase de tanda Fase de tanda de carga
duración progreso de crecimiento de serie 3
Fluorescencia [RFU]
concentración de biomasa seca
Fase de tanda Fase de tanda de carga inducción de impacto inicio y carga ep.
duración
señal de fluorescencia de serie 3
Fase de tanda Fase de tanda de carga
duración progreso de crecimiento de serie 4
Fluorescencia [RFU]
Fluorescencia [RFU]
Fase de tanda Fase de tanda de carga inducción de impacto inicio y carga ep.
duración señal de fluorescencia de serie 4
Fase de tanda Fase de tanda de carga inducción duración progreso de crecimiento de serie 5
Fase de tanda Fase de tanda de carga Fluorescencia [RFU]
duración [1: inicio de carga de glucosa
2: inducción de impacto D-manosa y fin de la carga de glucosa
3: carga constante de D-manosa]
progreso de crecimiento de serie 6
Patentes similares o relacionadas:
 Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Métodos para producir proteínas bicatenarias en bacterias, del 29 de Julio de 2020, de GENENTECH, INC.: Un método para producir un receptor de linfocitos T monoclonal de movilización inmunitaria contra el cáncer (ImmTAC) que comprende una cadena alfa del receptor de linfocitos […]
Anticuerpo biespecífico o mezcla de anticuerpos con cadenas ligeras comunes, del 15 de Julio de 2020, de Jiangsu Alphamab Biopharmaceuticals Co., Ltd: Anticuerpo biespecífico o parte de unión a antígeno del mismo, en el que el anticuerpo biespecífico o la parte de unión a antígeno del mismo tiene una cadena […]
Vacunas y diagnóstico de torque teno virus porcino, del 18 de Junio de 2020, de VIRGINIA TECH INTELLECTUAL PROPERTIES, INC.: Composición inmunogénica que comprende una proteína según SEQ ID NO. 16.
Producción de FDCA catalizada por deshidrogenasa, del 17 de Junio de 2020, de PURAC BIOCHEM B.V.: Proceso para oxidar ácido 5-hidroximetil-2-furancarboxílico (HMFCA) a ácido 5-formil-2-furoico (FFA), donde el proceso comprende la etapa de incubar una […]
Vectores de AAV dirigidos a oligodendrocitos, del 10 de Junio de 2020, de THE UNIVERSITY OF NORTH CAROLINA AT CHAPEL HILL: Un ácido nucleico que codifica una cápside de AAV, comprendiendo el ácido nucleico una secuencia codificante de la cápside de AAV que es al menos el 96 % idéntica […]
Ácido nucleico que comprende o codifica para un tallo-bucle de histona y una secuencia poli(A) o una señal de poliadenilación para aumentar la expresión de un antígeno patogénico codificado, del 3 de Junio de 2020, de CureVac AG: Secuencia de ácido nucleico que comprende o codifica en la dirección 5' → 3' para: i) • una región codificante, que codifica para al menos […]
Microorganismo con productividad de l-lisina aumentada y procedimiento para producir l-lisina utilizando el mismo, del 27 de Mayo de 2020, de CJ CHEILJEDANG CORPORATION: Una subunidad beta prima (subunidad-β') mutante de la ARN polimerasa, en la que la subunidad beta prima (subunidad-β') mutante de la ARN polimerasa tiene […]
Agrupación de genes de biosíntesis de carrimicina, del 27 de Mayo de 2020, de Shenyang Fuyang Pharmaceutical Technology Co., Ltd: Agrupación de genes de biosíntesis de carrimicina, que consiste en 44 genes que comprende: 1) cinco genes de policétido sintasa, incluyendo los residuos […]