Forma polimórfica de rotigotina.
Una forma polimórfica (II) de Rotigotina ((-)-5,6,7,8-tetrahidro-6-[propil[2-(2-tienil)etil]-amino]-1-naftalenol) que tiene por lo menos uno de
un espectro de difracción de rayos X de polvo que comprende picos a los siguientes ángulos 2θ
º (+-0,2): 12,04,13,68, 17,13, 17,72 y 19,01, medidos con irradiación de Cu-Kα (1,54060 Å);
un espectro Raman que comprende por lo menos un pico a los siguientes números de onda (+-3 cm-1): 226,2, 297,0,
363,9, 710,0, 737,3, 743,3, 750,8, 847,3, 1018,7, 1075,6, 1086,2, 1214,3, 1255,1, 1278,2, 1330,7, 1354,3 y 1448,7;
un pico de DSC con una Tinicio a 97ºC+-2ºC medido con una velocidad de calentamiento de 10ºC/min;
un punto de fusión de 97ºC+-2ºC.
Tipo: Patente Internacional (Tratado de Cooperación de Patentes). Resumen de patente/invención. Número de Solicitud: PCT/EP2008/066137.
Solicitante: UCB PHARMA GMBH.
Nacionalidad solicitante: Alemania.
Dirección: ALFRED-NOBEL-STRASSE 10 40789 MONHEIM ALEMANIA.
Inventor/es: WOLFF, HANS-MICHAEL, QUERE,LUC, RIEDNER,JENS.
Fecha de Publicación: .
Clasificación Internacional de Patentes:
- A61K31/381 NECESIDADES CORRIENTES DE LA VIDA. › A61 CIENCIAS MEDICAS O VETERINARIAS; HIGIENE. › A61K PREPARACIONES DE USO MEDICO, DENTAL O PARA EL ASEO (dispositivos o métodos especialmente concebidos para conferir a los productos farmacéuticos una forma física o de administración particular A61J 3/00; aspectos químicos o utilización de substancias químicas para, la desodorización del aire, la desinfección o la esterilización, vendas, apósitos, almohadillas absorbentes o de los artículos para su realización A61L; composiciones a base de jabón C11D). › A61K 31/00 Preparaciones medicinales que contienen ingredientes orgánicos activos. › teniendo ciclos de cinco eslabones.
- A61P25/00 A61 […] › A61P ACTIVIDAD TERAPEUTICA ESPECIFICA DE COMPUESTOS QUIMICOS O DE PREPARACIONES MEDICINALES. › Medicamentos para el tratamiento de trastornos del sistema nervioso.
- C07D333/20 QUIMICA; METALURGIA. › C07 QUIMICA ORGANICA. › C07D COMPUESTOS HETEROCICLICOS (Compuestos macromoleculares C08). › C07D 333/00 Compuestos heterocíclicos que contienen ciclos de cinco miembros que tienen un átomo de azufre como único heteroátomo del ciclo. › por átomos de nitrógeno (radicales nitro, nitroso C07D 333/12).
PDF original: ES-2547231_T3.pdf


Fragmento de la descripción:
Forma polimórfica de rotigotina Campo de la invención La presente invención se refiere a una nueva forma polimórfica (forma II) de Rotigotina y a un procedimiento para su producción, forma que es útil para la fabricación de un medicamento estable para tratar o aliviar síntomas de la enfermedad de Parkinson y otros trastornos relacionados con la dopamina.
Antecedentes técnicos La Rotigotina es el nombre común internacional (INN) del compuesto (-) -5, 6, 7, 8-tetrahidro-6-[propil[2- (2-tienil) etil]amino]-1-naftalenol que tiene la estructura mostrada a continuación
** (Ver fórmula) **
La Rotigotina es un agonista de dopamina D1/D2/D3 no ergolínico que se parece a la dopamina estructuralmente y tiene un perfil de receptor similar pero una mayor afinidad por el receptor.
En contraste con los compuestos ergolínicos, la Rotigotina tiene una muy baja afinidad por receptores 5 HT2B y de este modo un bajo riesgo de inducir fibrosis.
Las acciones de receptores no dopaminérgicos (tales como agonismo de 5-HT1A y antagonismo de A2B) pueden contribuir a otros efectos beneficiosos, tales como actividad antidisquinética, actividad neuroprotectora y efectos antidepresivos.
La Rotigotina se describe como agente activo para tratar pacientes que padecen la enfermedad de Parkinson (descrita en el documento WO 2002/089777) , síndrome de Parkinson plus (descrito en el documento WO 2005/292331) , depresión (descrita en el documento WO 2005/009424) y el síndrome de piernas inquietas (descrito en el documento WO 2003/092677) así como para el tratamiento o prevención de la pérdida de neuronas dopaminérgicas (descrito en el documento WO 2005/063237) .
Las composiciones farmacéuticas conocidas que contienen Rotigotina comprenden un sistema terapéutico transdérmico (TTS) (descrito en el documento WO 99/49852) , una forma de depósito (descrita en el documento WO 02/15903) , un dispositivo iontoforético (descrito en el documento WO 2004/050083) y una formulación intranasal (descrita en el documento WO 2005/063236) .
Cada una de las anteriormente citadas publicaciones se incorpora aquí como referencia en su totalidad.
Ya se conoce una forma cristalina de Rotigotina y de aquí en adelante se designará como forma polimórfica (I) . Se usa, por ejemplo, como material de partida en la preparación de la matriz descrita en el documento WO 2004/058247 para la administración transdérmica de Rotigotina.
Sorprendentemente se ha identificado ahora una forma cristalina adicional de Rotigotina (forma polimórfica (II) ) y se ha encontrado que muestra una estabilidad termodinámica enormemente aumentada y una mejorada vida útil así como una forma cristalina cúbica que representa una ventaja sobre las partículas en forma de aguja de la forma polimórfica (I) con respecto a sus propiedades de manejo tales como propiedades de filtración, fluidez, comportamiento electrostático, etc.
El descubrimiento de un segundo polimorfo cristalino de Rotigotina es especialmente sorprendente ya que la Rotigotina es un fármaco comercial que se conoce desde mediados de los ochenta y ha sido bien investigado durante la pasada década. Además, no se observó ninguna indicación de la presencia de un segundo polimorfo cristalino de Rotigotina en un primer examen de polimorfismo que se efectuó previamente durante el desarrollo de su formulación.
Sumario de la invención La presente invención proporciona una nueva forma polimérica (forma II) de Rotigotina ( (-) -5, 6, 7, 8-tetrahidro-6[propil[2- (2-tienil) etil]-amino]-1-naftalenol) .
La nueva forma polimórfica de Rotigotina según la presente invención tiene por lo menos una de las siguientes características:
un espectro de difracción de rayos X de polvo que comprende un pico por lo menos a uno de los siguientes ángulos 2º (0, 2) : 12, 04, 13, 68, 17, 72 y/o 19, 01, medido con radiación Cu-K (1, 54060 Å) ;
un espectro Raman que comprende por lo menos un pico a los siguientes números de onda (3 cm-1) : 226, 2, 297, 0, 363, 9, 737, 3, 847, 3, 1018, 7 y/o 1354, 3;
un pico de calorimetría diferencial de barrido (DSC) con una Tinicio a 97ºC2ºC medido con una velocidad de calentamiento de 10ºC/min; y/o un punto de fusión de 97ºC2ºC
En una realización la nueva forma polimórfica de Rotigotina se caracteriza por dos, tres o cuatro de los siguientes picos de difracción de rayos X de polvo 2º (0, 2) : 12, 04, 13, 68, 17, 72, 19, 01, medidos con radiación Cu-K (1, 54060 Å) ;
En una realización la nueva forma polimórfica de Rotigotina según la invención se caracteriza por picos en su espectro Raman a los números de onda 297, 0, 847, 3 y 1018, 7 3 cm-1 .
Las temperaturas dadas aquí incluyen variaciones de 2ºC debido a imprecisiones de las medidas, por ejemplo, de un experimento de DSC. Los ángulos 2 dados aquí incluyen variaciones de 0, 2 debido a imprecisiones de la medida de los experimentos de difracción de rayos X de polvo. Finalmente, los números de onda dados aquí incluyen variaciones de 3 cm-1 debido a imprecisiones de los experimentos de Raman.
La presente invención proporciona también una substancia farmacológica de Rotigotina que comprende por lo menos alrededor de 5%, más preferentemente por lo menos alrededor de 10%, de la nueva forma polimórfica de Rotigotina como se define anteriormente.
En una realización preferida la substancia farmacológica de Rotigotina comprende por lo menos alrededor de 50%, más preferentemente por lo menos alrededor de 70%, de la nueva forma polimórfica (II) de Rotigotina como se define anteriormente. Lo más preferentemente sustancialmente toda o toda (100%) la Rotigotina en la substancia farmacológica de Rotigotina está presente en la nueva forma polimórfica (II) . "sustancialmente toda" se desea que se refiera a una substancia farmacológica de Rotigotina que comprende forma II en la que preferentemente por lo menos 80%, más preferentemente por lo menos 90%, aún más preferentemente por lo menos 95% de la Rotigotina está presente como forma (II) .
En el contexto de la presente solicitud todos los porcentajes se dan en peso a menos que se indique lo contrario.
Además, la presente invención proporciona una composición farmacéutica que comprende la nueva forma polimórfica (II) de Rotigotina como se define anteriormente y por lo menos un excipiente farmacéuticamente aceptable.
La presente invención también proporciona un procedimiento para producir la nueva forma polimórfica (II) de Rotigotina como se define anteriormente, que comprende templar Rotigotina sólida de forma polimórfica (I) durante por lo menos 10 días a 40ºC.
En dicho procedimiento de templado la Rotigotina de forma polimórfica (I) puede estar en estado seco o en estado de suspensión. Cuando está en estado de suspensión, la suspensión se prepara preferentemente en ciclohexano o etanol.
En otra realización preferida de la presente invención la nueva forma polimórfica (II) de Rotigotina como se define anteriormente se produce cuantitativamente añadiendo a la Rotigotina de forma polimórfica (I) en estado de suspensión cristales de Rotigotina de forma polimórfica (II) obtenidos del procedimiento de templado o de precipitación etanólica.
En otra realización de la presente invención la nueva forma polimórfica (II) de Rotigotina como se define anteriormente se produce cuantitativamente añadiendo a la Rotigotina de forma polimórfica (I) en estado seco a 40ºC cristales de Rotigotina de forma polimórfica (II) . Los cristales de siembra de la forma (II) usados se pueden obtener de experimentos de suspensión etanólica, precipitación etanólica o de otro procedimiento de templado.
En otro aspecto de la presente invención la nueva forma polimórfica (II) de Rotigotina como se define anteriormente se usa para tratar un paciente que padece una enfermedad sensible al tratamiento con agonistas de receptor D2.
En varias realizaciones de la presente invención la nueva forma polimórfica (II) de Rotigotina como se define anteriormente se usa para tratar un paciente que padece enfermedad de Parkinson, síndrome de Parkinson plus, depresión, fibromialgia o síndrome de piernas inquietas.
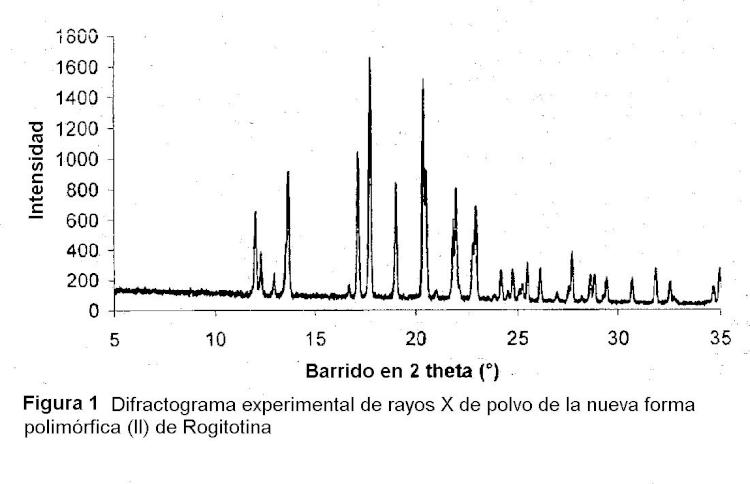
Breve descripción de los dibujos Figura 1. Difractograma experimental de rayos X de polvo de la nueva forma polimórfica (II) de Rotigotina.
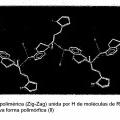
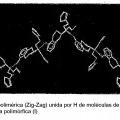
Figura 2. Cadena polimérica (Zig-Zag) unida por H de moléculas de Rotigotina en cristales de nueva forma polimórfica (II) . Figura 3. Cadena polimérica (Zig-Zag) unida por H de moléculas de Rotigotina en cristales de forma polimórfica (I) . Figura 4. Difractograma experimental de rayos X de polvo de la forma polimórfica (I) de Rotigotina. Figura... [Seguir leyendo]
Reivindicaciones:
1. Una forma polimórfica (II) de Rotigotina ( (-) -5, 6, 7, 8-tetrahidro-6-[propil[2- (2-tienil) etil]-amino]-1-naftalenol) que tiene por lo menos uno de un espectro de difracción de rayos X de polvo que comprende picos a los siguientes ángulos 2º (0, 2) : 12, 04, 13, 68, 17, 13, 17, 72 y 19, 01, medidos con irradiación de Cu-K (1, 54060 Å) ;
un espectro Raman que comprende por lo menos un pico a los siguientes números de onda (3 cm-1) : 226, 2, 297, 0, 363, 9, 710, 0, 737, 3, 743, 3, 750, 8, 847, 3, 1018, 7, 1075, 6, 1086, 2, 1214, 3, 1255, 1, 1278, 2, 1330, 7, 1354, 3 y 1448, 7;
un pico de DSC con una Tinicio a 97ºC2ºC medido con una velocidad de calentamiento de 10ºC/min;
un punto de fusión de 97ºC2ºC.
2. Una forma polimórfica de Rotigotina que tiene un espectro de difracción de rayos X de polvo medido con irradiación de Cu-K (1, 54060 Å) substancialmente como se muestra en la Figura 1.
3. Una substancia farmacológica de Rotigotina que comprende por lo menos 5% de una forma polimórfica de Rotigotina como se define en una cualquiera de las reivindicaciones 1-2.
4. Una substancia farmacológica de Rotigotina que comprende por lo menos 50% de una forma polimórfica de Rotigotina como se define en una cualquiera de las reivindicaciones 1-2.
5. Una substancia farmacológica de Rotigotina que comprende por lo menos 90% de una forma polimórfica de Rotigotina como se define en una cualquiera de las reivindicaciones 1-2.
6. Una substancia farmacológica de Rotigotina que comprende por lo menos 95% de una forma polimórfica de Rotigotina como se define en una cualquiera de las reivindicaciones 1-2.
7. Una substancia farmacológica de Rotigotina según cualquiera de las reivindicaciones 3-6 para su uso como substancia activa terapéutica.
8. Un polimorfo cristalino según cualquiera de las reivindicaciones 1 a 2 para su uso como substancia activa terapéutica.
9. El uso de la forma polimórfica de Rotigotina como se define en una cualquiera de las reivindicaciones 1-2 o de la substancia farmacológica de Rotigotina según las reivindicaciones 3-6 y por lo menos un excipiente farmacéuticamente aceptable en un método para la producción de una composición farmacéutica.
10. El uso según la reivindicación 9, en el que la composición farmacéutica está en la forma de un sistema terapéutico transdérmico.
11. El método para la producción de una composición farmacéutica usando la forma polimórfica de Rotigotina como se define en una cualquiera de las reivindicaciones 1-2 o la substancia farmacológica de Rotigotina según las reivindicaciones 3-6 y por lo menos un excipiente farmacéuticamente aceptable.
12. El método según la reivindicación 11, en el que la composición farmacéutica está en la forma de un sistema terapéutico transdérmico.
13. Una forma polimórfica de Rotigotina como se define en cualquiera de las reivindicaciones 1-2 o una substancia farmacológica de Rotigotina según las reivindicaciones 3-6 para su uso en un método para tratar un paciente que padece un trastorno relacionado con la dopamina, en el que tal trastorno se selecciona de enfermedad de Parkinson, síndrome de Parkinson plus, depresión, fibromialgia y/o síndrome de piernas inquietas.
14. El uso de una forma polimórfica de Rotigotina como se define en cualquiera de las reivindicaciones 1-2 o de la substancia farmacológica de Rotigotina según las reivindicaciones 3-6 para la fabricación de un medicamento para el tratamiento de un paciente que padece un trastorno relacionado con la dopamina, en el que el trastorno relacionado con la dopamina se selecciona de enfermedad de Parkinson, síndrome de Parkinson plus, depresión, fibromialgia y/o síndrome de piernas inquietas.
Patentes similares o relacionadas:
Derivados de 8-amino-2-oxo-1,3-diazaespiro-[4.5]-decano, del 29 de Julio de 2020, de GRUNENTHAL GMBH: Un compuesto según la fórmula general (I) **(Ver fórmula) donde R1 y R2 significan independientemente -H; -alquilo C1-C6, lineal o ramificado, […]
Preparación sólida que contiene colorante, del 29 de Julio de 2020, de DAIICHI SANKYO COMPANY, LIMITED: Preparación farmacéutica sólida que comprende monobencenosulfonato de ácido [(1R,5S,6S)-6-(aminometil)-3- etilbiciclo[3.2.0]hept-3-en-6-il]acético […]
Derivados de bencimidazol como inhibidores Nav 1.7 (subunidad alfa del canal de sodio, dependiente del voltaje, tipo IX (SCN9A)) para tratar el dolor, la disuria y la esclerosis múltiple, del 22 de Julio de 2020, de Sumitomo Dainippon Pharma Co., Ltd: Un compuesto de fórmula (I): **(Ver fórmula)** o una sal farmacéuticamente aceptable del mismo, donde R1a, R1b, R1c, y R1d son independientemente hidrógeno, […]
Derivado de 5-etiol-4-metil-pirazol-3-carboxamida que tiene actividad como agonista de TAAR, del 15 de Julio de 2020, de F. HOFFMANN-LA ROCHE AG: Un compuesto de fórmula I: **(Ver fórmula)** que es 5-etil-4-metil-N-[4-[(2S) morfolin-2-il]fenil]-1H-pirazol-3-carboxamida, o una sal de adición de ácido farmacéuticamente […]
Nuevos moduladores de receptores de fosfato de esfingosina, del 15 de Julio de 2020, de THE SCRIPPS RESEARCH INSTITUTE: Una composicion farmaceutica que comprende un compuesto de formula 265: **(Ver fórmula)** o una sal, estereoisomero, hidrato o solvato farmaceuticamente aceptable […]
Composición que comprende cinamaldehído y cinc, del 8 de Julio de 2020, de SOCIETE DES PRODUITS NESTLE S.A.: Composición que comprende cinamaldehído y cinc para la utilización en la mejora de uno o más de rendimiento cognitivo, cognición, humor o memoria en un […]
Derivado de amina cíclica y uso farmacéutico del mismo, del 1 de Julio de 2020, de TORAY INDUSTRIES, INC.: Un derivado de amina cíclica representado por la siguiente fórmula general (I): **(Ver fórmula)** donde R1 representa un grupo alquiloxi que tiene de 1 a 3 átomos […]
Cápsulas blandas entéricas de liberación controlada de ésteres de fumarato, del 1 de Julio de 2020, de Banner Life Sciences LLC: Una composición farmacéutica oral que comprende una cápsula blanda entérica que encapsula fumarato de monometilo suspendido en una matriz líquida […]